Эндотелиальная дисфункция при сердечной недостаточности
Введение
Если вы в последнее время читали о сердечно-сосудистых заболеваниях или недавно разговаривали с врачом о профилактике или лечении сердечно-сосудистых заболеваний, возможно, вы встречали термин «эндотелиальная дисфункция». Концепция эндотелиальной дисфункции стала важной в последние годы для нашего понимания многих сердечно-сосудистых заболеваний, включая ишемическую болезнь сердца (ИБС), артериальную гипертензию, микрососудистую стенокардию (кардиальный синдром Х), диастолическую дисфункцию и другие.
Эндотелиальная дисфункция — это состояние, при котором эндотелиальный слой (внутренняя оболочка) малых артерий не может нормально выполнять все свои важные функции. В результате с тканями, которые снабжаются этими артериями, может случиться несколько неприятных процессов.
Функция эндотелиального слоя
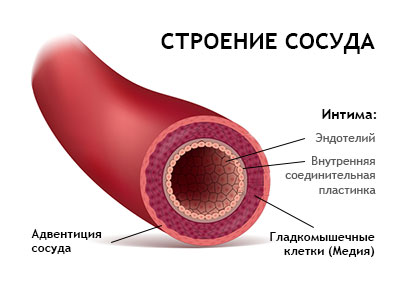
В артериолах организма (небольших артериях, которые точно регулируют поток крови к тканям) эндотелиальный слой (или эндотелий) является внутренней оболочкой клеток, которая выполняет несколько критических функций.

Эндотелий поддерживает правильное расширение и сужение кровеносных сосудов. Эта функция мгновенно определяет, сколько крови поступает в различные ткани организма. Эндотелиальный «тонус» (баланс между дилатацией и сужением) также в значительной степени определяет кровяное давление человека и то, сколько работы сердце должно проделать, чтобы выкачать кровь в организм.
Кроме того, эндотелий также защищает ткани от различных токсических веществ; регулирует механизм свертывания крови; контролирует жидкость, электролиты и многочисленные другие вещества, которые проходят между кровью и тканями; и регулирует воспаление в тканях.
Все это означает, что правильное функционирование эндотелия имеет решающее значение для нормального функционирования тканей и органов организма.
Когда эндотелиальный слой не выполняет все эти функции адекватно — иными словами, при наличии эндотелиальной дисфункции — условие будет благоприятствовать развитию атеросклероза, гипертонии (артериальной гипертензии) и другим сердечно-сосудистым заболеваниям.
Причины эндотелиальной дисфункции
Поскольку эндотелий так важен для многих жизненно важных функций, проводится много исследований, чтобы понять все причины эндотелиальной дисфункции. В этот момент очевидно, что эндотелиальная дисфункция связана со снижением уровня оксида азота (NO) в стенках кровеносных сосудов.
Оксиды азота представляют собой газ, который образуется в результате метаболизма аминокислоты (L-аргинин). Оксиды азота, имеющие очень короткий период полураспада, действуют локально в кровеносных сосудах, помогая модулировать тонус сосудов и другие важные эндотелиальные функции.
Дефицит продукции NO приводит к избыточному сужению кровеносных сосудов (которое может вызвать артериальную гипертензию), способствует активации тромбоцитов (приводит к свертыванию крови), увеличивает стимуляцию воспаления в стенках кровеносных сосудов (что способствует атеросклерозу) и увеличивает проницаемость стенок сосудов для повреждения липопротеинов и различных токсинов.
Подводя итог, можно сказать, что эндотелиальная дисфункция характеризуется снижением уровня оксида азота (NO) в сосудах, что, в свою очередь, приводит к нескольким нарушениям функции кровеносных сосудов. Эти функциональные нарушения способствуют развитию сердечно-сосудистых патологий.
Кроме того, эндотелиальная дисфункция может непосредственно вызывать аномальное сужение мелких артерий, и считается, что она является основным фактором, вызывающим кардиальный синдром Х и, возможно, диастолическую дисфункцию.
Нарушения и расстройства, сопутствующие эндотелиальной дисфункции

Точные причины, по которым у человека развивается эндотелиальная дисфункция, все еще изучаются. Тем не менее, очевидно, что этому способствуют многочисленные медицинские расстройства, привычки и неизбежные жизненные события, в том числе:
- повышенное кровяное давление (артериальная гипертензия);
- сахарный диабет;
- повышенные уровни холестерина и триглицеридов ЛПНП;
- курение;
- сидячий образ жизни;
- эмоциональный стресс (считается, что стрессовая кардиомиопатия, также известная как «синдром разбитого сердца» или кардиомиопатия Такоцубо, возникает в результате острой и тяжелой формы эндотелиальной дисфункции);
- инфекционные заболевания;
- сердечная недостаточность;
- гипотиреоз;
- остеопороз;
- естественное старение;
- химиотерапия и лучевая терапия;
- генетические влияния.
Диагностика
Делать формальный диагноз эндотелиальной дисфункции обычно нет необходимости. Некоторая степень дисфункции эндотелия может быть с уверенностью диагностирована у всех, кто имеет ишемическую болезнь сердца, гипертонию или основные факторы риска сердечно-сосудистых заболеваний (особенно перечисленные выше).
Таким образом, обследование эндотелиальной функции пациента — это не то, чем обычно занимаются врачи. Но если эндотелиальная дисфункция заподозрена у человека без четких причин (например, у человека, предположительно, имеющего кардиальный синдром X), диагноз может быть подтвержден различными диагностическими тестами, которые измеряют способность кровеносных сосудов расширяться (во время катетеризации или с помощью ультразвукового исследования) в ответ на введение ацетилхолина.
Лечение эндотелиальной дисфункции
Функционирование эндотелия может быть улучшено с помощью мер, направленных на снижение риска сердечно-сосудистых заболеваний, включая потерю веса, физические упражнения, прекращение курения, контроль гипертонии и диабета, которые всем нам обычно настоятельно рекомендуются.
Некоторые из этих мер контроля рисков были хорошо зарекомендованы для снижения эндотелиальной дисфункции. К ним относятся:
- применение статинов (фармацевтические препараты, направленные на борьбу с высокими уровнями холестерина в крови человека);
- средиземноморская диета;
- другие пищевые продукты, включая орехи, оливковое масло, темный шоколад, зеленый чай, растительные продукты;
- аэробные упражнения;
- потеря лишнего веса;
- применение ингибиторов АПФ (группа природных и синтетических химических соединений, применяющихся для терапии и профилактики сердечной и почечной недостаточности, для снижения артериального давления).
Кроме того, в настоящее время изучается несколько лекарственных препаратов, специально предназначенных для клинического улучшения эндотелиальной дисфункции. К перспективным агентам относятся нифедипин, эстроген, рунолазин, аспирин, L-аргенин и сильденафил.
Заключение
В последние годы медицинские исследования установили, что эндотелиальная дисфункция является важным фактором, способствующим возникновению многих видов сердечно-сосудистых расстройств. В то время как ведутся активные исследования по поиску путей улучшения лечения эндотелиальной функции и, следовательно, снижения риска сердечно-сосудистых заболеваний, мы уже многое можем сделать сами для решения этой проблемы. В частности, следует уделять большое внимание физическим упражнениям, бросать курить и при наличии таких заболеваний, как гипертония или диабет, работать с докторами.
Источник
В рамках короткого сообщения о новом подходе к лечению ДЭ нет возможности остановиться на всех интенсивно изучаемых в мире вариантах лекарственного воздействия на такой орган-мишень, как эндотелий. Суммируя краткие сведения предыдущей публикации (Атрощенко Е.С, 2002) и известные к настоящему моменту данные хотя бы по частной проблеме – медикаментозной коррекции ДЭ при ХСН, выделим главное.
1. Наличие любой функции (в том числе и множественных функций у эндотелия) подразумевает возможность появления дисфункции. В частном случае – при ХСН – уменьшение активного воздействия ряда вазодилататоров, контролируемых эндотелием, а также потеря последним функции контроля за состоянием ГМК сосудов и их пролиферацией сопровождается усиленным выделением эндотелийзависимых факторов вазоконстрикции. Причем как интрацеллюлярный, так и внутрисосудистый ангиотензин II начинает играть роль одного из основных медиаторов ДЭ.
2. В отличие от экспериментальных моделей, выполненных на животных, т. е. в ситуации, где имеют место 1 или 2 фактора риска (ФР), которые потенциально могут создать условия для повреждения сердечно-сосудистой системы, ДЭ у человека провоцируется многими ФР. Кроме того, патологическое моделирующее воздействие в эксперименте создается на короткий период времени.
Возникновение ДЭ обусловлено генетическими, диетическими, гормональными и метаболическими факторами, а также зависит от привычек и образа жизни человека (курение, малая подвижность и т.д.), материального благополучия (питание и пр.) и состояния окружающей среды. Таким образом, у человека, в отличие от модельных аналогов, ДЭ развивается на протяжении длительного периода времени, из чего следует важный вывод: поскольку возможно влияние на фенотип, существует и потенциальная возможность воздействия на ДЭ.
Известно по меньшей мере 10 основных ФР, способствующих развитию ДЭ. В 1994 году D.S. Celermajer впервые предложил шкалу зависимости ФР, приводящих к ДЭ. Это следующие ФР:
- ИБС;
- дислипопротеинемия;
- снижение активности углеводного обмена;
- курение;
- возраст;
- период постменопаузы у женщин;
- ожирение;
- метаболический синдром;
- синдром X (см.: 3. Am. Coll. Cardiol. – 1994. – Vol. 24. – P. 1468-1474).
Было подчеркнуто, что чем хуже функция эндотелия, тем хуже прогноз течения заболевания.
Исходя из многофакторности поражения эндотелия, выделим те основные звенья, на которые (в отличие, например, от возраста) можно оказывать воздействие.
3. Обратимость ДЭ, в частности при ХСН, может быть достигнута за счет стимуляции выработки и высвобождения N0 и EDHF, например, через брадикининовый механизм, что, как мы отмечали выше, возможно при использовании иАПФ (Kichuk M.R. и соавт., 1997). При ХСН наличие эндотелийзависимой дилатации, вызываемой гиперполяризацией, которая индуцируется брадикинином, доказано еще 10 лет назад у пациентов кардиохирургической клиники (Nakashima М. и соавт., 1993). Отметим важное для клиницистов обстоятельство: в большинстве опубликованных исследований обратимость нарушенной функции эндотелия, в частности эндотелийзависимой дилатации, достигнута, во-первых, у больных с умеренно выраженной ХСН, а во-вторых, при применении иАПФ не менее 3-х месяцев (Jeserich М. и соавт., 1995). Следовательно, эффект воздействия на фенотипичные признаки достигается очень медленно. У некоторых пациентов с ХСН действие иАПФ на ДЭ может быть настолько выраженным, что развивающаяся у них стойкая артериальная вазодилатация может привести к снижению сопротивления резистивных сосудов (Vanhoutte P.M., 1996).
4. Исходя из вышесказанного, не исключено, что положительное воздействие на ДЭ могут оказать и блокаторы рецепторов ангиотензина II (ATI-рецепторов), несмотря на отсутствие у них «накопительного» действия кининов. Не останавливаясь подробно на данном вопросе, отметим следующее: эндотелиальные клетки имеют свои ATI-рецепторы, которые способствуют секреции N0 и вазодилатирующих простагландинов посредством фосфолипазы С (Pueyo М.Е., Michel J.В., 1997). Активация АТ2-рецепторов и рецепторов ангиотензина (1-7) может вызывать ряд полезных эффектов (Атрощенко Е.С, Атрощенко И.Е., 19…,2002), в частности эффект эндотелийзависимой релаксации сосудов (Gohlke Р. и соавт., 1998). То есть, кроме «классического» пути (например, с помощью иАПФ), существует возможность воздействия на ATI-рецепторы эндотелия (а также их ген), что в итоге оказывает благоприятное влияние и на процесс гипертрофии (ремоделирования) и пролиферацию ГМК (подробно см.: Griendling К.К. и соавт., 1997; Harrison D.G., 1997; Gibbons G.H., 1997).
В отношении возможности воздействия на все вышеперечисленные ФР (курение, возраст и т.д.) нет необходимости подробного изложения имеющихся подходов, конечной целью которых является улучшение состояния функции эндотелия. Поэтому мы рассмотрим вопрос об оказании помощи женщинам так называемого «постбальзаковского» возраста. Следует отметить, что информация по этой проблеме запаздывает, а фирмы, получающие большой доход от эксплуатации идеи омолаживания женщин, расходуют финансы на проведение прежде всего экспериментальных исследований.
Еще в 1991 году Е. Barrett-Connor и T.L Bush продемонстрировали стимулирующее действие эстрогенов на синтез NO и проста цикл и нов. В течение последующих 10 лет в мире появились сотни сотен работ не только по вопросу реальной помощи женщинам, находящимся в постменструальном периоде, но и по проблеме профилактики сердечно-сосудистых (т.е. самых дорогостоящих в плане лечения) заболеваний. Не углубляясь в данную проблему хотя бы в рамках статьи о ДЭ у женщин в постменопаузе, тем не менее выделим главное.
На недавно прошедшем (апрель 2002, Москва) IX Конгрессе «Человек и лекарство» проф. Н.А. Грацианский в своем докладе «Гормональная заместительная терапия в постменопаузе и обострении коронарной болезни сердца: предупреждение или провоцирование?» отметил следующее. В прошедшее десятилетие в позиции ряда положений гормональной заместительной терапии (ГЗТ) применимо к проблемам кардиологии произошли существенные изменения. Почему же в столь короткий срок мы наблюдали такую эволюцию: от триумфа самой идеи до ее пессимистического восприятия? Ответ прост: финансовые интересы, в большей мере – консервативность медицины, в данном случае обусловленная запаздыванием объективной информации о реальном положении дел даже на уровне ведущих кардиоцентров, и чисто человеческое желание «панацеи». Хотя и практикам, и теоретикам понятно, что всякий подход к лечению, даже доказанный многочисленными многоцентровыми исследованиями, применим к частностям, оговоренным в протоколах (когда в исследование включается только каждый 5-7-й из рандомизированных пациентов по критериям «включение» и «исключение», т.е. при строго научных и корректных исследованиях), выводы не касаются большинства пациентов, не вошедших в рандомизированный контингент программ, о чем мы ранее подробно сообщали (Атрощенко Е.С, 2001).
В докладе проф. Н.А. Грацианский подчеркнул, что профилактическая эффективность ГЗТ в отношении сердечно-сосудистой патологии была показана только в одном исследовании – MHS («Здоровье медицинских сестер в постменопаузе»: ColditzG.A. и соавт., 1987).
Уже спустя 7 лет в исследовании HERS («Heart and Estrogen progestin Replacement Study»: Hulley S. и соавт., 1998) было установлено следующее. Назначение ГЗТ женщинам, ранее перенесшим инфаркт миокарда (ИМ), ассоциируется с повышением частоты эпизодов нестабильной стенокардии (в 2 раза) и смертности (но за исключением женщин, до ИМ длительно применявших ГЗТ), что подтверждено в ряде других исследований. Так, в до сих пор длящемся в США исследовании WHI (11 тыс. женщин после гистерэктомии и 16 тыс. – с сохраненным органом) замечено существенное увеличение частоты тромбоэмболии легочной артерии.
Какова же возможная причина столь грозных осложнений ГЗТ? По данным трехлетнего исследования WIIS («Здоровье женщин») сделан вывод: ГЗТ, проводимая с помощью прогестина и эстрогена, обладает провоспалительным действием, особенно спустя полгода от начала терапии, что ассоциируется не только с высоким риском осложнений ишемической болезни сердца, но и с повышением риска инсульта (более чем в 2,5 раза). Таким образом, несмотря на возможное положительное действие ГЗТ на функцию эндотелия у здоровых женщин в период постменопаузы, нужно помнить о высоком риске коронарных осложнений в течение первых двух лет лечения. По рекомендации экспертов АСА ГЗТ не применяется у пациенток, перенесших OИМ, если они длительно не получали ее ранее, т.е. до OИМ. Объективности ради отметим, что теоретические и экспериментальные исследования по вопросам ГЗТ не прекращаются до сих пор и именно этой проблеме посвящен февральский номер «Cardiovascular Research» под тематическим названием «Пол и сердечно-сосудистая система» (2001, 2002, т. 53, № 3).
Суммируя мнения ведущих ученых мира, можно привести «Рекомендации для кардиологов Европы по заместительной гормональной терапии для женщин в постменструальном периоде» (Schenck-Gustafsson К., Swahn Е., 2000), основой которых явилось вышеупомянутое исследование HERS (HuLLey S. и соавт., 2000). Определены допустимые и предположительные показания к проведению ГЗТ.
Допустимые показания:
- Такие вегетативные проявления климакса, как покраснение кожи, чувство жара, повышенная потливость.
- Высокий риск остеопороза у женщин (ГЗТ проводится с целью профилактики заболевания).
Предположительные – «сердечные» – показания:
- Гиперлипидемия при невозможности должного контроля положительных и отрицательных эффектов лечения. Отмечается, что наиболее выраженный эффект терапии наблюдается, во-первых, при пероральном приеме гормонов (Darling G.M. и соавт., 1997), во-вторых, у пожилых женщин (Rosano M.C.G. и соавт., 2000). При невозможности добиться нормализации липидного спектра с помощью монотерапии стати нам и или ГЗТ рекомендуется их сочетание (Rosano G.M.C. и соавт., 2000).
- Синдром X, т.е. когда типичная ангинозная боль возникает у лиц с нормальными коронарными артериями, но с патологическими проявлениями на ЭКГ при проведении нагрузочного тестирования, стрессэхокардиографии или сцинтиграфии миокарда с таллием. Эстроген может снижать число болевых эпизодов, но не оказывает эффекта на ишемию (Rosano G.M. и соавт., 1999).
5. Статины и ДЭ. Как мы подробно сообщали ранее (Атрощенко Е.С, 2002), эндотелийзависимая вазодилатация сосудов существенно снижена при гиперхолестеринемии, что было известно еще десятилетие назад (Mugge А. и соавт., 1991). Более того, при гиперхолестеринемии повышается продукция эндотелием супероксиданионов, что в конечном итоге ведет к нарушению эндотелийзависимой вазодилатации (Ohara Y. и соавт., 1993).
Таким образом, с позиции вышеизложенного просматриваются 2 пути коррекции ДЭ:
- тактический (например, использование антиокислителей (антиоксидантов));
- стратегический (к примеру, применение стати нов, улучшающих состояние липидного обмена).
Первый клинический опыт в этом направлении показал, что под влиянием ряда антиоксидантов, например аскорбиновой кислоты (Levine G.N. и соавт., 1996) или пробукола (Anderson T.J. и соавт., 1995), функция эндотелия улучшается, что, по-видимому, можно объяснить более благоприятными условиями для высвобождения N0 клетками эндотелия (NADH/NADPH-оксидаза – это источник супероксиданионов). Кардиологам может показаться любопытным то, что применение популярного лекарства дипиридамола (в РБ – курантила) у больных с гиперхолестеринемией улучшает и вазодилататорную функцию эндотелия (Gould K.L. и соавт., 1994).
Ухудшение барьера для диффузии N0/EDHF происходит также вследствие утолщения интимы атеросклеротически пораженного сосуда. Поэтому применение статинов для улучшения функции эндотелия патогенетически оправдано. По данным Т.С Andrews и соавт. (1997), реальный эффект воздействия стати нов на миокардиальную ишемию достигается только спустя 4 недели от начала их приема, при этом снижение уровня липопротеинов низкой плотности сопровождается улучшением функции эндотелия, поскольку статины влияют на продукцию эндотелиальной NO-синтазы (Laufs U. и соавт., 1998).
В заключение отметим следующее. Поскольку антиоксиданты и статины, во-первых, не могут быть у всех пациентов одинаково эффективны, а во-вторых, обладают разным механизмом действия, рациональным представляется их сочетанное использование. В частности, известно, что длительное (4-месячное) применение витамина Е у больных с высоким уровнем антител к окисленным липопротеинам низкой плотности улучшает функцию эндотелия даже у курильщиков (Heitzer Т. и соавт., 1997). Таким образом можно добиться главного – увеличения синтеза и повышения активности основного регулятора вазодилатации – NO.
=================
Вы читаете тему:
Эндотелиальная дисфункция: длинный путь от патофизиологии до терапии
1. Важность знания эндотелиальной дисфункции для врача.
2. Возможности коррекции дисфункции эндотелия.
3. Медикаментозная коррекция дисфункции эндотелия при хронической сердечной недостаточности.
Атрощенко Е.С. РНПЦ «Кардиология».
Опубликовано: “Медицинская панорама” № 6, сентябрь 2002.
Источник
