Антагонисты ангиотензина в лечении сердечной недостаточности

К этой группе лекарств относятся препараты, эффект которых при ХСН изучается более 10 лет. Однако в сравнительных с иАПФ протоколах не удавалось доказать полной эквивалентности этого альтернативного способа блокады ренин–ангиотензиновой системы. Кроме того, учитывая абсолютные показания к назначению иАПФ всем пациентам с ХСН, невозможно было организовать плацебо–контролируемые исследования с антагонистами рецепторов к АII (АРА) в “эру” иАПФ.
Ситуация поменялась лишь после завершения трех исследований, вошедших в программу CHARM, в которых изучалась эффективность и безопасность применения АРА кандесартана, у пациентов с ХСН и сниженной или сохранной ФВ ЛЖ [109–111]. В программе CHARM было продемонстрировано достоверное снижение смертности и сердечно–сосудистых госпитализаций. Снижение риска смерти составляло 33% после первого, 20% после второго и 12% после третьего года наблюдения, что очень близко к показателям, полученным в исследовании SOLVD с “эталонным” иАПФ эналаприлом (23% через год, 23% через два и 16% через три года терапии). Кроме этого, в исследовании CHARM alternative более 2000 пациентов принимали кандесартан в сравнении с плацебо без иАПФ (которые не могли быть назначены из–за наличия серьезных побочных реакций). И в этих условиях снижение риска достижения комбинированной конечной точки (смерти плюс госпитализации) составило 30% [109]. Следует добавить, что кандесартан был поставлен в более сложные условия, чем иАПФ, которые применялись на фоне комбинации лишь двух препаратов – сердечных гликозидов и мочегонных. Эффект кандесартана доказан для больных ХСН, большинство из которых уже получали и гликозиды, и диуретики, и БАБ, и антагонисты альдостерона, а часть и иАПФ, но не достигли состояния компенсации. Поэтому на сегодня кандесартан может применяться в лечении больных с ХСН и сниженной ФВ наравне с иАПФ (степень доказанности А).
Титрование доз кандесартана проводится по тем же принципам, что и иАПФ. Стартовая доза – 4 мг однократно в сутки, которая при стабильном АД и отсутствии осложнении удваивается каждые 3–5 дней до достижения дозировки 16 мг однократно в сутки. У больных с высоким уровнем АД максимальная дозировка – 32 мг однократно в сутки. При исходной гипотонии (САД менее 100 мм рт. ст.) терапию безопасно начинать с дозы 2 мг в сутки.
В то же время нет убедительных доказательств в способности кандесартана предотвращать развитие ХСН и его эффективности в лечении пациентов с сохраненной систолической функцией ЛЖ. Хотя число госпитализаций больных с сохранной систолической функцией ЛЖ на фоне лечения кандесартаном снижается, достоверного улучшения прогноза не наблюдается.
Очевидно, что кандесартан на сегодня наиболее обоснованный выбор для лечения больных с ХСН, если говорить о всем классе АРА. Из других представителей класса АРА, учитывая отличную переносимость препаратов этой группы при минимуме побочных эффектов, можно с успехом использовать лосартан и валсартан.
Стартовая доза лосартана – 25 мг x 1 р / сут, затем – 50 мг x 1 р / сут и, наконец, 100 мг x 1 р / сут. Порядок повышения дозировок такой же, как для иАПФ.
В исследовании ELITE II лосартан лишь незначительно и недостоверно уступал каптоприлу по влиянию на прогноз пациентов с декомпенсацией и имел лучший профиль переносимости. Кроме того, лосартан может предупреждать развитие ХСН, в том числе у пациентов с диабетом и нефропатией, что выдвигает его в число препаратов для профилактики декомпенсации сердечной деятельности (степень доказанности В).
В крупном исследовании Val–HeFT были продемонстрированы способности сочетания АРА валсартана с иАПФ в уменьшении числа госпитализаций больных с ХСН при отсутствии влияния на прогноз.
Важное значение имеет анализ эффективности валсартана, у больных не получавших иАПФ [241]. В этом случае были впервые продемонстрированы способности АРА не только к уменьшению числа госпитализаций, но и снижению риска смерти больных с ХСН, в сравнении с плацебо. Валсартан на 33% снижал риск смерти и на 44% риск смерти плюс повторных госпитализаций у декомпенсированных больных, даже превосходя по этим показателям кандесартан. Кроме того, применение валсартана сопровождается клиническим улучшением и значительной блокадой процессов ремоделирования сердца. По своей эффективности валсартан не уступает иАПФ и может применяться для лечения ХСН (степень доказанности В).
Кроме того, валсартан является эффективным средством профилактики ХСН у больных с острым коронарным синдромом, не уступая по этому показателю иАПФ каптоприлу.
Дозы валсартана, соответственно – 40 мг x 2 р/д – 80 мг x 2 р/д – 160 мг x 2 р/д. Причем для валсартана показаны положительные эффекты именно высоких доз (степень доказанности В).
Для других АРА пока недостаточно данных для оценки их эффективности и безопасности в лечении ХСН. В таблице 1 представлены сведения о трех наиболее эффективных АРА, применяемых сегодня для лечения и профилактики ХСН.
Таблица 1
Показания к применению и дозировки АРА, рекомендуемых для профилактики и лечения ХСН
| Препарат | Показания | Стартовая доза | Терапевтическая доза | Максимальная доза |
| Кандесартан Валсартан Лосартан | ХСН I–IV ФК, диаст. ХСН ХСН II–IV, после ОИМ Непереносимость ИАПФ, профилактика ХСН | 4 мг x 1 р/д 20 мг x 2 р/д 25 мг x 1 р/д | 16 мг x 1 р/д 80 мг x 2 р/д 50 мг x 1 р/д | 32 мг x 1 р/д 160 мг x 2 р/д 100 мг x 1 р/д |
Исходя из имеющихся сегодня данных, АРА можно назначать дополнительно к иАПФ, хотя предпочтение всегда должно отдаваться сочетанию иАПФ с БАБ. Только при непереносимости БАБ следует переходить к комбинации иАПФ плюс АРА.
Показано, что комбинация иАПФ с АРА и нередко при дополнительном назначении БАБ способна в большей степени блокировать нейрогормоны и процессы ремоделирования, что показано для кандесартана и валсартана. Однако тройная комбинация иАПФ + БАБ + АРА может приводить к чрезмерному снижению уровня АД и реактивации нейрогормональных систем, ответственных за прогрессирование ХСН. Поэтому при хорошей переносимости комбинации иАПФ (АРА) + БАБ в качестве третьего нейро–гормонального модулятора лучше использовать антагонисты альдостерона а не АРА (иАПФ).
Не выявлено половых различий в эффективности АРА при ХСН (Val–HeFT, CHARM, ELITE–II), что выгодно отличает этот класс препаратов от иАПФ.
Хроническая сердечная недостаточность
Рекомендации ВНОК
Опубликовал Константин Моканов
Источник
Несмотря на впечатляющие успехи современной кардиологии, хроническая сердечная недостаточность (ХСН) остается ее «ахиллесовой пятой». Существенное снижение летальности от сердечно-сосудистых заболеваний, достигнутое за последние три десятилетия в большинстве индустриальных стран, не сопровождалось уменьшением летальности от ХСН и частоты госпитализаций по этой причине.
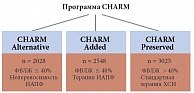
Рис. 1. Общая структура программы CHARM
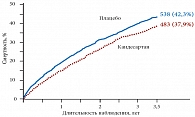
Рис. 2. CHARM-Added: сердечно-сосудистая смертность и госпитализация по поводу ХСН

Рис. 3. CHARM-Added: вторичные конечные точки

Рис. 4. CHARM-Added: сердечно-сосудистая смертность и госпитализация по поводу ХСН в предварительно определенных подгруппах
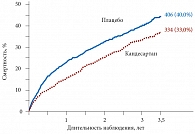
Рис. 5. CHARM-Alternative: сердечно-сосудистая смертность и госпитализация по поводу ХСН

Рис. 6. CHARM-Alternative: вторичные конечные точки

Рис. 7. CHARM-Preserved: первичная и вторичная конечные точки
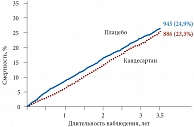
Рис. 8. CHARM-Overall: общая смертность

Рис. 9. CHARM-Overall: конечные точки

Таблица 1. Исходные характеристики пациентов в программе CHARM (M. Pfeffer и соавт., 2003)

Таблица 2. Характеристика базовой терапии пациентов в программе CHARM (M. Pfeffer и соавт., 2003)
Частично этот феномен объясняется увеличением средней продолжительности жизни. По данным Фремингемского исследования, частота ХСН удваивается каждое десятилетие. Повторная декомпенсация ХСН в течение 6 лет наблюдения отмечается у 60–70% пациентов [1]. Таким образом, разработка новых эффективных способов лечения хронической сердечной недостаточности остается актуальной задачей современного здравоохранения.
Обоснование возможности применения антагонистов рецепторов ангиотензина II при ХСН
С момента появления нового класса лекарственных препаратов – антагонистов рецепторов ангиотензина II 1 типа (АРА) – их эффективность изучается при ХСН как в качестве монотерапии (как альтернатива ингибиторам ангиотензин-превращающего фермента (ИАПФ)), так и в комбинации с ИАПФ. Использование АРА обеспечивает дополнительную блокаду действия ангиотензина II (AII), поскольку существуют альтернативные (не связанные с АПФ) пути образования данного вещества. При приеме ИАПФ определенная часть AII продолжает синтезироваться в организме [2].
Применение АРА блокирует эффекты АII вне зависимости от способа его образования. Кроме того, АРА оказывают опосредованное стимулирующее влияние на рецепторы 2 типа к АII, что может вести к дополнительному вазодилатирующему действию [3]. Ряд побочных эффектов ИАПФ, таких как кашель и ангионевротический отек, связаны с повышенным содержанием брадикинина, поскольку ИАПФ также тормозят деградацию кининов [4]. Вместе с тем ряд благоприятных клинических эффектов ИАПФ связан именно с брадикинином [4]. Назначение АРА позволяет нивелировать эти побочные явления без снижения клинической эффективности. При хорошей переносимости ИАПФ наиболее целесообразной стратегией является добавление АРА к ИАПФ, так как при этом уменьшение биораспада брадикинина сохраняется и обеспечивается дополнительная блокада системы «ренин – ангиотензин – альдостерон».
Программа CHARM
Программа CHARM (The Candesartan in Heart Failure –Assessment of Reduction in Mortality and Morbidity) состояла из трех независимых клинических исследований [5]. В исследовании CHARM-Added изучали эффективность кандесартана у пациентов с фракцией выброса левого желудочка (ФВЛЖ) 40% вне зависимости от приема ИАПФ (рис. 1). После завершения проекта был проведен композитный анализ полученных результатов, объединенных в рамках проекта CHARM-Overall. Клинико-демографические показатели пациентов, включенных в исследование, представлены в таблице 1. В таблице 2 приведены особенности базовой терапии больных, принимавших участие в исследовании.
Исследование CHARM-Added
Целью исследования CHARM-Added явилось определение эффективности кандесартана при его добавлении к терапии ИАПФ [6]. Пациенты (n = 2548) были рандомизированы в группы плацебо или кандесартана (целевая доза 32 мг/сут). Критерии включения в исследование: ФВЛЖ
Кроме того, прием кандесартана уменьшал риск возникновения сердечно-сосудистой смерти и госпитализации по поводу ХСН (первичной конечной точки) во всех предварительно определенных подгруппах в зависимости от терапии без доказательств гетерогенности действия. Интересно, что по сравнению с результатами исследования Val-HeFT благотворное действие кандесартана в большей степени выявлялось у пациентов, которые дополнительно получали бета-адреноблокаторы (рис. 4). Таким образом, добавление АРА кандесартана к ИАПФ у пациентов с ХСН и ФВЛЖ
Исследование CHARM-Alternative
В исследовании CHARM-Alternative изучали эффективность кандесартана у пациентов с непереносимостью ИАПФ [7]. В него были включены 2028 пациентов, удовлетворяющих следующим критериям: ФВЛЖ
Кандесартан достоверно уменьшал риск наступления сердечно-сосудистой смерти и госпитализаций по поводу ХСН по сравнению с плацебо (33% и 40% соответственно, отношение шансов 0,77; 95% ДИ 0,67–0,89; р = 0,004). Достоверность различий была достигнута в основном за счет уменьшения госпитализаций по поводу ХСН (р
Исследование CHARM-Preserved
В исследовании CHARM-Preserved изучали эффективность добавления кандесартана к стандартной терапии ХСН у пациентов с сохраненной ФВЛЖ (> 40%) [8]. Критериями включения служили: ФВЛЖ > 40%, II–IV класс ХСН по NYHA, наличие хотя бы одной госпитализации в связи с заболеваниями сердца. В исследовании участвовали 3023 человека. Пациенты были рандомизированы в группы плацебо или кандесартана (целевая доза 32 мг/сут). Средний срок наблюдения составил 36,6 месяца. В каждой из групп ИАПФ получали менее чем 20% пациентов. Первичная конечная точка не различалась по сравнению с другими исследованиями в рамках программы.
По сравнению с результатами проектов CHARM-Added и CHARM-Alternative в исследовании CHARM-Preserved не выявлено достоверных различий по частоте наступления сердечно-сосудистой смерти и госпитализаций по поводу ХСН между группами кандесартана и плацебо (22,0% и 24,3% соответственно, нескорректированное отношение шансов 0,89; 95% ДИ 0,77–1,03; р = 0,12). Тем не менее наблюдалась тенденция к уменьшению частоты госпитализаций в связи с ХСН (р = 0,072). Каких-либо различий по вторичным конечным точкам между группами не выявлено (рис. 7). Отмечено также достоверное снижение новых случаев развития сахарного диабета на фоне использования кандесартана (отношение шансов 0,60; 95% ДИ 0,41–0,86; р = 0,005). Таким образом, у больных с клиническими проявлениями ХСН и ФВЛЖ > 40% применение кандесартана по сравнению с плацебо в умеренной степени снижает частоту госпитализаций по поводу ХСН.
Программа CHARM-Overall
Был проведен комбинированный анализ результатов всех трех исследований [9]. В него были включены данные, полученные у 7601 пациента, принимавшего кандесартан или плацебо. Средний срок наблюдения составил 37,7 месяца. Хотя во всех исследованиях программы использовалась комбинированная конечная точка, состоящая из сердечно-сосудистой смертности и госпитализации по поводу ХСН, первичной конечной точкой в проекте CHARM-Overall являлась общая смертность. Всего за период наблюдения от всех причин умерли 23,3% пациентов в группе кандесартана и 24,9% в группе плацебо (нескорректированное отношение шансов 0,91; 95% ДИ 0,83–1,00; р = 0,055) (рис. 8). Снижение смертности в группе кандесартана было обусловлено уменьшением частоты сердечно-сосудистой смертности (18,2% против 20,3% соответственно, отношение шансов 0,88; 95% ДИ 0,79–0,97; р = 0,012). Это улучшение (как для общей, так и для сердечно-сосудистой смертности) определялось уже в первые 6 месяцев терапии и продолжалось в течение всего периода наблюдения. Снижение смертности было достоверным для пациентов с ФВЛЖ ≤ 40% (р = 0,018 для общей смертности и р = 0,005 для сердечно-сосудистой смертности). Тем не менее показано, что между тремя исследованиями отсутствует какая-либо гетерогенность по показателям общей смертности. Прием кандесартана ассоциировался с достоверным снижением частоты сердечно-сосудистой смертности и госпитализаций в связи с ХСН по результатам всех трех исследований (30,2% против 34,5%, р = 0,0001) (рис. 9).
В исследовании CHARM-Overall также получены доказательства хорошей переносимости кандесартана, хотя количество пациентов, выбывших досрочно, в основных группах было выше по сравнению с плацебо (причины: гипотензия – 132 против 66, повышение уровня креатинина в сыворотке – 234 против 115, гиперкалиемия – 85 против 21). Использование кандесартана приводило к достоверному снижению частоты новых случаев сахарного диабета (отношение шансов 0,78; 95% ДИ 0,64–0,96; р = 0,02). Комбинированный анализ трех исследований в рамках CHARM-Overall показал, что добавление кандесартана к стандартной терапии ИАПФ позволяет значимо снизить показатели сердечно-сосудистой заболеваемости и смертности.
Дополнительный анализ результатов программы CHARM
Для определения влияния кандесартана на функцию крупных артерий проводили изучение параметров неинвазивной гемодинамики у 30 пациентов из группы кандесартана и 34 пациентов из группы плацебо [10]. Используя калиброванную тонометрию и допплеровское исследование аортального кровотока, рассчитывали типовой импеданс (отношение давления в сонной артерии и аортального кровотока в раннюю систолу). Общая артериальная податливость измерялась с использованием метода диастолической площади. Исследование проводили через 6 и 14 месяцев после начала терапии. Показатели сердечного выброса и периферического сопротивления между группами не различались. Снижение центрального пульсового давления в группе кандесартана (57 ± 20 против 67 ± 17 мм рт. ст., р = 0,043) сопровождалось уменьшением типового импеданса (200 ± 78 против 240 ± 74 дин с/см5, р = 0,039) и увеличением общей артериальной податливости (1,87 ± 0,70 против 1,47 ± 0,48 мл/мм рт. ст., р = 0,008). При стратификационном анализе в зависимости от ФВЛЖ ( 40%) были получены аналогичные результаты. Следовательно, терапия кандесартаном улучшает функциональное состояние крупных артерий. При регрессионном анализе после корректировки по возможным причинным факторам (демографические показатели, тяжесть заболевания, курение, особенности сочетанной терапии) показано, что хорошая приверженность к лечению (прием > 80% назначенного врачом препарата) ассоциировалась с достоверно меньшей общей смертностью у всех пациентов, включенных в программу CHARM (отношение шансов 0,65; 95% ДИ 0,57–0,75; р
Итоги программы CHARM
По результатам исследования ELITE II, в которое было включено 3152 пожилых пациента с ХСН, не выявлено преимуществ АРА лозартана по сравнению с ИАПФ каптоприлом по показателю общей смертности [14]. В исследовании OPTIMAAL [15] также проводилось сравнительное изучение лозартана и каптоприла у пациентов после инфаркта миокарда с ХСН или дисфункцией ЛЖ. После среднего срока наблюдения 2,7 лет смертность между двумя группами достоверно не различалась (р = 0,07). Результаты проекта VALIANT, разработанного с целью сравнения эффективности валсартана и каптоприла у пациентов после инфаркта миокарда, осложненного сердечной недостаточностью или дисфункцией ЛЖ, показали, что эффективность этих лекарственных средств не различается (отношение шансов для валсартана составило 0,98; р = 0,62) [16]. Проект Val-HeFT – исследование, наиболее близкое по критериям включения и характеристикам пациентов к CHARM-Added. В нем сравнивалась эффективность добавления АРА валсартана к стандартной терапии у 5010 пациентов с ХСН [17]. Показатель смертности достоверно не изменился, однако использование валсартана позволило достоверно уменьшить частоту госпитализаций по поводу ХСН (р = 0,001). Следует отметить, что этот эффект был наиболее выраженным у пациентов, которые исходно не принимали ИАПФ. Программа CHARM включила в себя максимально возможное количество комбинаций различных факторов, встречающихся у пациентов с ХСН в реальной практике.
Результаты исследования CHARM-Alternative убедительно доказали, что при непереносимости ИАПФ назначение АРА кандесартана приводит к благоприятным долгосрочным клиническим результатам и характеризуется хорошей переносимостью. Наиболее впечатляющие результаты получены в исследовании CHARM-Added. Добавление кандесартана к терапии ИАПФ ведет к дальнейшему снижению не только госпитализаций по причине ХСН, но и показателя сердечно-сосудистой смертности. Таким образом, у пациентов с ХСН и ФВЛЖ
Источник
