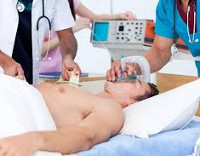
Трансмуральный инфаркт и кардиогенный шок


Трансмуральный инфаркт миокарда — это наиболее тяжелая форма некроза кардиальной мышцы, при которой поражаются все слои сердца. Проявляется выраженным болевым синдромом, беспокойным поведением, лихорадкой. Главный этиологический фактор состояния — атеросклероз. Выявление патологии производится с помощью электрокардиографии, лабораторных анализов крови, ангиографии с контрастом. Лечение включает в себя методы консервативной терапии, но приоритетным, наиболее эффективным является хирургическое вмешательство в виде коронарного стентирования, шунтирования, трансмиокардиальной лазерной реваскуляризации.
Общие сведения
Трансмуральный инфаркт миокарда — одна из самых тяжелых, жизнеугрожающих патологий сердца, уже многие годы остающаяся ведущей причиной смерти больных с сердечно-сосудистыми заболеваниями. Госпитальная смертность достигает 10%, а в некоторых регионах России 15%. В течение года после интенсивной терапии умирает еще около 10%. Половина больных с тяжелой формой кардиального некроза погибает на догоспитальном этапе. Мужчины 40-60 лет болеют чаще женщин, пик заболеваемости отмечается после 50 лет. Основная группа пациентов — люди с сопутствующим сахарным диабетом, гиперлипидемией, отягощенным семейным анамнезом.

Трансмуральный инфаркт миокарда
Причины
Подавляющее большинство случаев инфаркта миокарда является следствием окклюзии главного ствола или ветви коронарной артерии. Процесс сопровождается значительным ухудшением снабжения кровью сердечной мышцы. При увеличении нагрузки на кардиальную мышцу она начинает испытывать гипоксию, ее функции снижаются, что приводит к последующему некрозу. В рамках современной медицины выделяют несколько причин сужения просвета венечных сосудов:
- Атеросклероз. Ведущий фактор развития инфаркта, обнаруживаемый у 95% людей, умерших от крупноочаговых процессов. Частый признак — высокий уровень липидов крови. Перекрытие диаметра артерии более чем на 75% вызывает отмирание тканей.
- Тромбоз. Флотирующие образования в кровотоке могут попадать в коронарные сосуды двумя путями: из левого желудочка, в котором образуются в результате фибрилляции предсердий и клапанных патологий, либо при незакрытом овальном окне.
К факторам риска развития инфаркта относят отягощенную наследственность (сердечно-сосудистые заболевания у ближайших родственников), возраст старше 50 лет, многолетний стаж курения. Провоцировать отложение липидов в стенках сосудов может ожирение, недостаточная физическая активность. Группу риска составляют пациенты с установленной артериальной гипертензией, сахарным диабетом, системными заболеваниями (особенно васкулитами).
Патогенез
Трансмуральный инфаркт развивается вследствие нарушения кровоснабжения сердечной мышцы. Адекватность коронарного кровотока запросам миокарда определяется наполненностью венечных артерий, которое зависит от аортального давления и сосудистого сопротивления, насыщенности кислородом, колеблющейся в зависимости от нагрузки на сердце и частоты его сокращений, а также составом плазмы и форменных элементов, меняющемся при гипогидратации, анемиях, токсических отравлениях. Любое нарушение баланса приводит сначала к ишемии, затем к омертвлению кардиальных клеток.
Крупноочаговый характер патологии практически всегда находит отражение в интенсивном болевом синдроме. Это связано с массивным поражением кардиальной мышцы, активацией большого количества болевых рецепторов, значительным снижением ее функции. Массивный очаг некроза может стать причиной попадания в кровь большого количества продуктов распада (миоглобин, тропонины) с развитием системного воспалительного ответа — резорбционно-некротического синдрома.
Симптомы
Трансмуральный инфаркт миокарда обычно имеет выраженную клиническую картину. Наиболее характерным симптомом является интенсивная боль, способная иррадиировать в левую сторону тела — руку, шею, спину, челюсть. Кардиалгия при данной патологии напоминает хорошо знакомый пациентам с заболеваниями сердечно-сосудистой системы приступ стенокардии, но, в отличие от него, крайне сложно купируется, длится более 20 минут.
Применение нитроглицерина, оправданное в большинстве случаев, не дает должного эффекта даже после трех таблеток. Также малоэффективно изменение положения тела, подача свежего воздуха, холодное питье. Помимо боли пациенты могут ощущать головокружение, тошноту вплоть до рвоты. При выраженной сердечной недостаточности на фоне инфаркта появляется одышка, особенно выраженная у женщин. Поражение массивного участка миокарда приводит к нарушению проведения импульса, тахикардии, экстрасистолии, различным блокадам. К общим признакам относят холодный пот, угнетение сознания или эмоциональное возбуждение, выраженную слабость.
Ретроспективно диагностируется около 50% случаев патологии, особенно у пожилых людей или больных сахарным диабетом на фоне развившейся нейропатии, в состоянии после трансплантации сердца. В подобных случаях инфаркт начинается без боли в грудной клетке, поэтому второстепенные признаки приобретают ведущую роль. Нетипичная манифестация может включать в себя инсульт, острый психоз, расстройства пищеварения, периферические эмболии.
Если к общему состоянию присоединяется резорбционно-некротический синдром, к прочим симптомам добавляется повышение температуры тела до 38-39° С на протяжении более 5-7 дней, лейкоцитоз до 15х109/л с преобладанием нейтрофильной фракции. В анализе крови обнаруживается высокая скорость оседания эритроцитов в течение нескольких недель, анэозинофилия. Больные отмечают озноб, сменяющийся жаром, потливость, выраженную слабость.
Осложнения
Трансмуральный инфаркт миокарда способен привести к целому ряду жизнеугрожающих состояний. Самое частое осложнение — нарушения ритма сердца вплоть до фибрилляции желудочков. Нередко наблюдается сердечная недостаточность, обычно – левожелудочковая, сопровождающаяся хрипами, сердечной астмой, отеком легких. Специфическим именно для массивного некроза сердечной мышцы является кардиогенный шок, для которого характерно критическое уменьшение сердечного выброса, падение давления.
К менее частым последствиям относят эмболии в системе легочной артерии, аневризму и разрыв стенки сердца с тампонадой. При затрагивании инфарктом сосочковых мышц может возникнуть недостаточность митрального клапана с острой кардиальной недостаточностью. Описаны случаи так называемого постинфарктного синдрома, появляющегося через одну или несколько недель после болезни как иммунологическая реакция на некротическую ткань. Протекает как перикардит или плеврит с выраженной эозинофилией.
Диагностика
Физикальное обследование не позволяет выявить каких-то надежных диагностических признаков, подтверждающих либо опровергающих инфаркт миокарда, однако имеет большое значение в процессе оценки тяжести состояния больного. Визуально пациент обычно беспокоен, бледен, кожа покрыта холодным потом. Артериальное давление может повышаться на пике болевого приступа, сочетаться с тахикардией. Нередко нарастают признаки левожелудочковой недостаточности. Из инструментальных методик врачи-кардиологи используют:
- Электрокардиографию. Базовый метод диагностики. Изменения на ЭКГ появляются уже во время стенокардии и проходят ряд характерных стадий. Трансмуральный инфаркт характеризуется глубоким и широким зубцом Q, снижением амплитуды R, сегмент ST поднимается над изолинией. Через несколько дней формируется отрицательный зубец Т, сегмент ST снижается. Локализацию процесса определяют по грудным отведениям.
- Лабораторные методы. Массивный некроз мышечной ткани находит свое отражение в общем анализе крови. У пациентов обнаруживается выраженный лейкоцитоз на фоне лихорадки, лейкоцитарный сдвиг влево, увеличение СОЭ. В биохимическом анализе повышается значение внутриклеточных ферментов (АЛТ, АСТ, ЛДГ), отмечается высокий уровень креатининфосфокиназы, тропонинов.
- Коронарная ангиография. Рентгенологический метод, помогающий установить окклюзию коронарной артерии тромбом, оценить функцию желудочков, риск аневризм или разрыва стенок. Является обязательным компонентом предоперационной подготовки перед аортокоронарным шунтированием, ангиопластикой.
Лечение трансмурального инфаркта миокарда
Все больные с подозрением на данную патологию подлежат скорейшей госпитализации в специализированные отделения — реанимации, неотложной кардиологии, сосудистые центры. Терапию начинают на этапе до госпитализации, особенно при активном вызове скорой медицинской помощи, и продолжают стационарно. Больному прописывается строгий постельный режим, психический и эмоциональный покой, диета.
Консервативная терапия
Важнейшей начальной целью лечения является адекватное обезболивание, предотвращение шоковых состояний, жизнеугрожающих аритмий. Применяют сильные обезболивающие средства (морфин, промедол, трамадол), комбинируемые с атропином, кордароном. Назначают ингаляции кислорода, при угрозе фибрилляции желудочков используют дефибрилляцию либо внутривенное введение лидокаина. При подозрении на тромбоз показаны антикоагулянты прямого действия, преимущественно гепарин или стрептокиназа в больших дозировках.
Хирургическое лечение
Непосредственная цель инвазивных методов — восстановление адекватного кровоснабжения миокарда (реваскуляризация). Своевременно сделанная операция может значительно уменьшить зону некроза, снизить риск осложнений, предупредить рецидивы патологии. В настоящее время хирургическое лечение является приоритетным методом в терапии ишемической болезни сердца и инфаркта миокарда, позволяет добиться тех результатов, которые недоступны при медикаментозном воздействии. Применяются:
- Чрескожная коронаропластика. Расширение просвета сосуда достигается путем введения в него сетчатой металлической трубочки. Манипуляция провидится под рентген-контролем, чаще с доступом из бедренной или подключичной артерии. Результат вмешательства по многом зависит от материала, из которого изготовлен стент. В последующем от пациента требуется долгосрочный прием лекарственных средств (гиполипидемических, антитромбоцитарных).
- Аортокоронарное шунтирование. Суть операции заключается в создании обходного пути для тока крови в обход склерозированного или тромбированного участка сосуда. Это более серьезная манипуляция, приводимая на открытом сердце с использованием аппарата искусственного кровообращения. В качестве шунта может применяться как эндогенный материал (части дистальных артерий), так и искусственные импланты.
- Трансмиокардиальная лазерная реваскуляризация. Перспективный хирургический метод лечения, появившийся в последние годы. С помощью специальной лазерной установки в миокарде проделывается несколько десятков тонких сквозных ходов глубиной плоть до желудочковых полостей. По этим ходам кровь поступает непосредственно из камер к мышечным клеткам, минуя коронарные сосуды.
Прогноз и профилактика
Трансмуральный инфаркт наиболее неблагоприятен по прогнозу вследствие высокой вероятности летального исхода еще до момента оказания медицинской помощи, 20% вероятности гибели в первый месяц после приступа. Полноценная своевременная помощь минимизирует эти риски. Профилактика состояния, главным образом, сводится к предупреждению или коррекции атеросклероза. Важна нормализация массы тела, уровня липидов крови, контроль артериального давления, отказ от вредных привычек. Эти мероприятия особенно необходимы лицам с неблагоприятным семейным анамнезом.
Источник
Кардиогенный шок – это крайняя степень проявления острой сердечной недостаточности, характеризующаяся критическим снижением сократительной способности миокарда и перфузии в тканях. Симптомы шока: падение АД, тахикардия, одышка, признаки централизации кровообращения (бледность, уменьшение кожной температуры, появление застойных пятен), нарушение сознания. Диагноз ставится на основании клинической картины, результатов ЭКГ, тонометрии. Цель лечения – стабилизация гемодинамики, восстановление сердечного ритма. В рамках неотложной терапии используются бета-блокаторы, кардиотоники, наркотические анальгетики, оксигенотерапия.
Общие сведения
Кардиогенный шок (КШ) – острое патологическое состояние, при котором сердечно-сосудистая система оказывается неспособной обеспечить адекватный кровоток. Необходимый уровень перфузии временно достигается за счет истощаемых резервов организма, после чего наступает фаза декомпенсации. Состояние относится к IV классу сердечной недостаточности (наиболее тяжелая форма нарушения сердечной деятельности), летальность достигает 60-100%. Кардиогенный шок чаще регистрируется в странах с высокими показателями кардиоваскулярной патологии, слабо развитой профилактической медициной, отсутствием высокотехнологичной медпомощи.
Причины
В основе развития синдрома лежит резкое понижение сократительной способности ЛЖ и критическое уменьшение минутного выброса, что сопровождается недостаточностью кровообращения. В ткани не поступает достаточного количества крови, развиваются симптомы кислородного голодания, снижается уровень артериального давления, появляется характерная клиническая картина. КШ может отягощать течение следующих коронарных патологий:
- Инфаркт миокарда. Выступает основной причиной кардиогенных осложнений (80% всех случаев). Шок развивается преимущественно при крупноочаговых трансмуральных инфарктах с выходом из сократительного процесса 40-50% массы сердца. Не возникает при инфарктах миокарда с малым объемом пораженных тканей, поскольку оставшиеся неповрежденными кардиомиоциты компенсируют функцию погибших клеток миокарда.
- Миокардит. Шок, влекущий за собой смерть пациента, встречается в 1% случаев тяжелого инфекционного миокардита, вызванного вирусами Коксаки, герпеса, стафилококком, пневмококком. Патогенетический механизм – поражение кардиомиоцитов инфекционными токсинами, образование противокардиальных антител.
- Отравление кардиотоксическими ядами. К числу подобных веществ относится клонидин, резерпин, сердечные гликозиды, инсектициды, фосфорорганические соединения. При передозировке этих препаратов происходит ослабление сердечной деятельности, урежение ЧСС, падение минутного объема до показателей, при которых сердце неспособно обеспечить необходимый уровень кровотока.
- Массивная ТЭЛА. Закупорка крупных ветвей легочной артерии тромбом – тромбоэмболия ЛА – сопровождается нарушением легочного кровотока и острой правожелудочковой недостаточностью. Расстройство гемодинамики, обусловленное чрезмерным наполнением правого желудочка и застоем в нем, приводит к формированию сосудистой недостаточности.
- Тампонада сердца. Тампонада сердца диагностируется при перикардите, гемоперикарде, расслоении аорты, травмах грудной клетки. Скопление жидкости в перикарде затрудняет работу сердца ‒ это становится причиной нарушения кровотока и шоковых явлений.
Реже патология развивается при дисфункции папиллярных мышц, дефектах межжелудочковой перегородки, разрыве миокарда, сердечных аритмиях и блокадах. Факторами, повышающими вероятность сердечно-сосудистых катастроф, являются атеросклероз, пожилой возраст, наличие сахарного диабета, хроническая аритмия, гипертонические кризы, чрезмерные физические нагрузки у пациентов с кардиогенными заболеваниями.
Патогенез
Патогенез обусловлен критическим падением артериального давления и последующим ослаблением кровотока в тканях. Определяющим фактором выступает не гипотония как таковая, а уменьшение объема крови, проходящей по сосудам за определенное время. Ухудшение перфузии становится причиной развития компенсаторно-приспособительных реакций. Резервы организма направляются на обеспечение кровью жизненно-важных органов: сердца и головного мозга. Остальные структуры (кожа, конечности, скелетная мускулатура) испытывают кислородное голодание. Развивается спазм периферических артерий и капилляров.
На фоне описанных процессов происходит активация нейроэндокринных систем, формирование ацидоза, задержка ионов натрия и воды в организме. Диурез снижается до 0,5 мл/кг/час и менее. У больного выявляют олигурию или анурию, нарушается работа печени, возникает полиорганная недостаточность. На поздних стадиях ацидоз и выброс цитокинов провоцируют чрезмерную вазодилатацию.
Классификация
Заболевание классифицируется по патогенетическим механизмам. На догоспитальных этапах определить разновидность КШ не всегда представляется возможным. В условиях стационара этиология болезни играет решающую роль в выборе методов терапии. Ошибочная диагностика в 70-80% случаев оканчивается смертью пациента. Различают следующие варианты шока:
- Рефлекторный – нарушения вызваны сильным болевым приступом. Диагностируется при небольшом объеме поражения, т. к. выраженность болевого синдрома не всегда соответствует размерам некротического очага.
- Истинный кардиогенный – последствие острого ИМ с формированием объемного некротического очага. Сократительная способность сердца снижается, что уменьшает минутный объем. Развивается характерный комплекс симптомов. Смертность превышает 50%.
- Ареактивный – наиболее опасная разновидность. Сходен с истинным КШ, патогенетические факторы выражены сильнее. Плохо поддается терапии. Летальность – 95%.
- Аритмогенный – прогностически благоприятен. Является результатом нарушения ритма и проводимости. Возникает при пароксизмальной тахикардии, АВ блокадах III и II степени, полных поперечных блокадах. После восстановления ритма симптомы исчезают в течение 1-2 часов.
Патологические изменения развиваются ступенчато. Кардиогенный шок имеет 3 стадии:
- Компенсации. Уменьшение минутного объема, умеренная гипотония, ослабление перфузии на периферии. Кровоснабжение поддерживается за счет централизации кровообращения. Пациент обычно в сознании, клинические проявления умеренные. Присутствуют жалобы на головокружение, головную боль в сердце. На первой стадии патология полностью обратима.
- Декомпенсации. Присутствует развернутый симптомокомплекс, перфузия крови в головном мозге и сердце снижена. Уровень АД критически мал. Необратимые изменения отсутствуют, однако до их развития остаются минуты. Больной находится в сопоре или без сознания. За счет ослабления почечного кровотока уменьшается образование мочи.
- Необратимых изменений. Кардиогенный шок переходит в терминальную стадию. Характеризуется усилением имеющейся симптоматики, выраженной коронарной и церебральной ишемией, формированием некрозов во внутренних органах. Развивается синдром диссеминированного внутрисосудистого свертывания, на коже появляется петехиальная сыпь. Возникают внутренние кровотечения.
Симптомы кардиогенного шока
На начальных стадиях выражен кардиогенный болевой синдром. Локализация и характер ощущений сходны с инфарктом. Пациент жалуется на сжимающую боль за грудиной («как будто сердце сжимают в ладони»), распространяющуюся на левую лопатку, руку, бок, челюсть. Иррадиации по правой стороне тела не отмечается.
Дыхательная недостаточность проявляется полной или частичной утратой способности к самостоятельному дыханию (цианоз, частота дыхания менее 12-15 в минуту, беспокойство, страх смерти, включение в процесс дыхания вспомогательной мускулатуры, втягивание крыльев носа). При развитии альвеолярного отека легких изо рта больного выделяется белая или розоватая пена. Человек занимает вынужденное положение сидя, с наклоном вперед и упором руками в стул.
Отмечается снижение систолического АД ниже 80-90 мм рт. ст., пульсового – до 20-25 мм рт. ст. Пульс нитевидный, слабого наполнения и напряжения, тахикардия до 100-110 ударов/минуту. Иногда ЧСС падает до 40-50 уд/мин. Кожа пациента бледная, холодная и влажная на ощупь. Выражена общая слабость. Диурез снижен или полностью отсутствует. На фоне шока происходит нарушение сознания, развивается сопор или кома.
Осложнения
Кардиогенный шок осложняется полиорганной недостаточностью (ПОН). Нарушается работа почек, печени, отмечаются реакции со стороны пищеварительной системы. Системная органная недостаточность является следствием несвоевременного оказания больному медицинской помощи или тяжелого течения болезни, при котором предпринимаемые меры по спасению оказываются малоэффективными. Симптомы ПОН – сосудистые звездочки на коже, рвота «кофейной гущей», запах сырого мяса изо рта, набухание яремных вен, анемия.
Диагностика
Диагностика осуществляется на основании данных физикального, лабораторного и инструментального обследования. При осмотре больного кардиолог или реаниматолог отмечает внешние признаки заболевания (бледность, потливость, мраморность кожи), оценивает состояние сознания. Объективные диагностические мероприятия включают:
- Физикальное обследование. При тонометрии определяется снижение уровня АД ниже 90/50 мм рт. ст., пульсовый показатель менее 20 мм рт. ст. На начальной стадии болезни гипотония может отсутствовать, что обусловлено включением компенсаторных механизмов. Сердечные тоны глухие, в легких выслушиваются влажные мелкопузырчатые хрипы.
- Электрокардиография. ЭКГ в 12 отведениях выявляет характерные признаки инфаркта миокарда: снижение амплитуды зубца R, смещение сегмента S-T, отрицательный зубец T. Могут отмечаться признаки экстрасистолии, атриовентрикулярной блокады.
- Лабораторные исследования. Оценивают концентрацию тропонина, электролитов, креатинина и мочевины, глюкозы, печеночных ферментов. Уровень тропонинов I и T повышается уже в первые часы ОИМ. Признак развивающейся почечной недостаточности – увеличение концентрации натрия, мочевины и креатинина в плазме. Активность ферментов печени увеличивается при реакции гепатобилиарной системы.
При проведении диагностики следует отличать кардиогенный шок от расслаивающей аневризмы аорты, вазовагальных синкопе. При расслоении аорты боль иррадиирует вдоль позвоночника, сохраняется на протяжении нескольких дней, носит волнообразный характер. При синкопе отсутствуют серьезные изменения на ЭКГ, в анамнезе – болевое воздействие или психологический стресс.
Лечение кардиогенного шока
Пациенты с острой сердечной недостаточностью и признаками шокового состояния экстренно госпитализируются в кардиологический стационар. В составе бригады СМП, выезжающей на подобные вызовы, должен присутствовать реаниматолог. На догоспитальном этапе проводится оксигенотерапия, обеспечивается центральный или периферический венозный доступ, по показаниям выполняется тромболизис. В стационаре продолжают лечение, начатое бригадой СМП, которое включает в себя:
- Медикаментозную коррекцию нарушений. Для купирования отека легких вводят петлевые диуретики. Чтобы уменьшить сердечную преднагрузку, используют нитроглицерин. Инфузионная терапия проводится при отсутствии отека легких и ЦВД ниже 5 мм рт. ст. Объем инфузии считается достаточным, когда этот показатель достигает 15 единиц. Назначаются антиаритмические средства (амиодарон), кардиотоники, наркотические анальгетики, стероидные гормоны. Выраженная гипотония является показанием для применения норадреналина через шприц-перфузор. При стойких нарушениях сердечного ритма применяется кардиоверсия, при тяжелой дыхательной недостаточности – ИВЛ.
- Высокотехнологичную помощь. При лечении пациентов с кардиогенным шоком используют такие высокотехнологичные методы, как внутриаортальная баллонная контрапульсация, искусственный желудочек, баллонная ангиопластика. Приемлемый шанс выжить пациент получает при своевременной госпитализации в специализированное отделение кардиологии, где присутствует необходимая для высокотехнологичного лечения аппаратура.
Прогноз и профилактика
Прогноз неблагоприятный. Летальность составляет более 50%. Снизить этот показатель удается в случаях, когда первая помощь пациенту была оказана в течение получаса от начала болезни. Уровень смертности в таком случае не превышает 30-40%. Выживаемость достоверно выше среди пациентов, которым было проведено хирургическое вмешательство, направленное на восстановление проходимости поврежденных коронарных сосудов.
Профилактика заключается в недопущении развития ИМ, тромбоэмболий, тяжелых аритмий, миокардитов и травм сердца. С этой целью важно проходить профилактические курсы лечения, вести здоровый и активный образ жизни, избегать стрессов, соблюдать принципы здорового питания. При возникновении первых признаков сердечной катастрофы требуется вызов бригады скорой помощи.
Источник