Стенокардия нестабильная стенокардия инфаркт миокарда
Нестабильная стенокардия — это период обострения ишемической болезни сердца, сопровождающийся высоким риском развития некротических изменений миокарда и внезапной кардиальной смерти. Пациенты отмечают сильные загрудинные боли, нарушения ритма, одышку и генерализованные отеки. План диагностических мероприятий включает кардиографию, Эхо-КГ, лабораторные методы и ангиографию. Лечение базируется на комплексной медикаментозной терапии. При неэффективности консервативных мероприятий или обширном характере повреждения кардиальной мышцы применяются инвазивные методы (реваскуляризация).
Общие сведения
Нестабильная стенокардия является актуальной проблемой современной кардиологии из-за наличия плохо контролируемых клинических проявлений. Согласно последним рекомендациям, данная патология вместе с мелкоочаговым и крупноочаговым инфарктом миокарда входит в понятие острого коронарного синдрома, соответственно, представляет серьезную угрозу для жизни и здоровья пациента. В 25% наблюдений заболевание завершается некротическим процессом в миокарде, 80% из них — в первые семь дней с начала обострения. Летальность составляет около 15%, наиболее высокий уровень смертности наблюдается у лиц с массивной гибелью кардиомиоцитов, поражающей все кардиальные стенки.

Нестабильная стенокардия
Причины
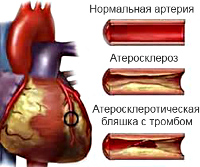
К настоящему времени установлено, что основным этиологическим фактором прогрессирующего течения ишемической болезни в целом и нестабильной стенокардии в частности является постепенное сужение просвета коронарных артерий. Это создает предпосылки для некроза кардиомиоцитов, ухудшает прогноз для пациента. Основной причиной патологического процесса считается атеросклероз. Отложение липидов на эндотелии коронарных сосудов ведет к формированию бляшки, способной значительно снизить объем кровотока по артерии.
Размер образования имеет второстепенное значение, на первый план выходит наличие большого липидного ядра и тонкой покрышки, при разрыве которых начинают формироваться тромбы. Одновременно с этим поврежденные сосуды становятся чрезмерно восприимчивыми к сосудосуживающим веществам, выделяемым тромбоцитами, что влечет за собой дополнительное сужение просвета артерий.
Патогенез
Основные патогенетические механизмы дестабилизации стенокардии связаны с формированием тромбоцитарного агрегата. Развитию тромбоза коронарной артерии предшествует поражение сосудистой стенки атеросклеротическими бляшками с их последующим разрывом. Чаще ему подвергаются липидные образования, которые обладают обширным подвижным растущим ядром, занимающим более половины их объема, и тонкой соединительнотканной оболочкой. В такой бляшке обычно присутствует значительное количество лимфоцитов и макрофагов, способных быстро инициировать воспалительную реакцию.
Надрыву способствует критическая масса бляшки, окисление ее содержимого, высокое артериальное давление и физические нагрузки. Затем начинается процесс тромбообразования с активацией факторов свертывания крови. Сформированный агрегат состоит из фибрина, эритроцитов и лейкоцитов, обычно имеет протяженность около 1 см. Нестабильная стенокардия также может развиваться на фоне коронароспазма, обусловленного нарушением функции эндотелия и повышением его чувствительности к вазоконстриктивным веществам.
Классификация
В практической медицине часто используют классификацию, согласно которой патология делится на три класса в зависимости от скорости формирования болевого синдрома: дебютная (1 класс), развившаяся в течение месяца (2 класс) и за последние 48 часов (3 класс). Однако эта номенклатура не учитывает этиологические и клинические особенности заболевания. Поэтому общепризнанным среди практикующих кардиологов считается выделение следующих форм нестабильной стенокардии:
- Впервые возникшая. Приступы загрудинных болей появились впервые либо после длительного (до нескольких лет) бессимптомного периода. Обычно пациенты ощущают боли на фоне активной физической нагрузки, выявляется тенденция к увеличению частоты и интенсивности пароксизмов.
- Прогрессирующая. За последние 30 дней больной отмечает значительное увеличение частоты приступов (в том числе появление боли в покое), их продолжительности, потребности в нитратах. Обычно он может указать точную дату начала негативных изменений. Патология нередко сочетается с аритмиями и снижением функции левого желудочка.
- Спонтанная. Стенокардия с возникающими единичными приступами, не зависящими от физической активности, продолжительностью более 15 минут. Нитроглицерин недостаточно эффективен, наблюдаются признаки ишемии на ЭКГ, однако некроз не развивается.
- Вариантная (стенокардия Принцметала). Болевой синдром возникает в покое, имеет высокую интенсивность, длится более 10 минут. Особенность данной формы — появление кардиалгии в одно и то же время суток, наличие выраженного подъема сегмента ST на кардиограмме. В межприступный период заболевание себя никак не проявляет, пациент может выполнять любую физическую работу без последствий.
- Постинфарктная. Появление, учащение и усиление приступов через 1-10 дней после перенесенного инфаркта миокарда. Этот вариант болезни представляет опасность из-за возможного расширения зоны некроза, значительного ухудшения работы левого желудочка.
Симптомы нестабильной стенокардии
Клиническая картина включает несколько обязательных признаков. Основной симптом – боль средней или высокой интенсивности сжимающего либо давящего характера длительностью от 10-15 минут, которая локализуется за грудиной, по левому ее краю, отдает в левую руку, плечо, лопатку, левую часть шеи или нижнюю челюсть. Кардиалгия слабо купируется нитроглицерином, часто требует неоднократного приема, имеет тенденцию к прогрессированию — увеличению частоты приступов.
Выделяются провоцирующие боль факторы: физическая активность, эмоциональные потрясения, неблагоприятный тип погоды, обильный прием пищи. Особенностью нестабильной формы патологии является невозможность установления четкой закономерности между интенсивностью воздействий и развитием симптома. Кардиалгия часто наблюдается в покое или при минимальной нагрузке (наклоны тела, ходьба по дому). К другим признакам относят нарушения ритма и проводимости — увеличение частоты кардиальных сокращений, ощущение перебоев в работе сердца. На этом фоне возможно развитие одышки, чувства нехватки воздуха.
Осложнения
Из-за прогрессирующего течения нестабильная стенокардия часто становится причиной развития осложнений. Основными неблагоприятными последствиями являются инфаркт миокарда и увеличение вероятности внезапной сердечной смерти. Возможны кардиальные аритмии: патологическая тахикардия, брадикардия, экстрасистолии, блокады проведения импульса. Постоянный характер процесса сказывается непосредственно на миокарде, что приводит к развитию хронической сердечной недостаточности по обоим кругам кровообращения. В тяжелых случаях исходом ХСН становится отек легких и гибель пациента.
Диагностика
Нестабильная стенокардия имеет достаточно неспецифические признаки, поэтому физикальное обследование дает крайне скудные данные. Помимо боли могут отмечаться симптомы сердечной недостаточности и нарушений гемодинамики: генерализованные отеки, одышка, быстрая утомляемость. Уточняются предрасполагающие факторы риска, семейный анамнез. На первом этапе диагностики основной задачей является исключение инфаркта, затем – внесердечных причин кардиалгий и неишемических патологий сердца. В клинической практике используются следующие методы:
- Электрокардиография. Типичными признаками на ЭКГ являются ишемические изменения – элевация сегмента ST и инверсия зубца Т в двух последовательных отведениях. Важно отслеживание признаков в динамике, сравнение текущей картины с предшествующими записями. Полностью нормальная ЭКГ при наличии симптомов не исключает ОКС и стенокардию, однако вынуждает расширить диагностический поиск.
- Лабораторные методы. В общем анализе крови обнаруживаются признаки воспаления — лейкоцитоз, повышение СОЭ. В биохимическом анализе определяется количество холестерина, липидных фракций, глюкозы. Это необходимо для оценки риска атеросклеротического поражения коронарных сосудов. Важнейшее значение имеет уровень тропонинов, позволяющий с точностью установить наличие инфаркта, глубокого ишемического повреждения кардиомиоцитов.
- Эхокардиография. УЗИ сердца выполняется для уточнения размеров камер, миокардиальной структуры, внутрикардиальной гемодинамики и состояния клапанной системы. Возможно выявление нарушений сократимости. Процедура может проводиться в стресс-режиме с физической нагрузкой для установления функционального класса патологии. Нормальная картина Эхо-КГ не исключает наличия нестабильной стенокардии.
- Коронарография. Это инвазивное рентгенологическое исследование коронарных сосудов дает возможность определить степень сужения артерий и причину данного явления — спазм, наличие атеросклеротических бляшек с оценкой их состояния, тромбы в просвете. На основе полученной информации можно решить вопрос о необходимости оперативного лечения.
Дифференциальная диагностика проводится с некоронарными причинами болезненных ощущений в области сердца, способными имитировать инфаркт миокарда. Чаще всего заболевание дифференцируют с гипертрофической кардиомиопатией, пороками, миокардитом, перикардитом и кардиальной аневризмой. Необходимо исключить сосудистые патологии: тромбоэмболию легочной артерии, расслоение стенки аорты. В последнюю очередь рассматривают внесердечные причины кардиалгии: межреберную невралгию, плеврит и пневмонию.
Лечение нестабильной стенокардии
Диагностированная патология требует скорейшей госпитализации для наблюдения и лечения. Назначается строгий постельный режим, бессолевая диета, проводится весь спектр необходимых клинических исследований. Обязательной является запись ЭКГ в динамике. Основные цели включают предотвращение развития инфаркта, уменьшение симптоматики, улучшение качества жизни и прогноза пациента. При адекватной терапии, благоприятном течении заболевания стабилизация наступает через одну-две недели. Основным методом остается медикаментозное воздействие, которое предполагает использование средств нескольких основных фармакологических групп:
- Антиангинальные препараты. Необходимы для купирования непосредственно стенокардии. Назначаются нитраты, способствующие расширению просвета сосудов и улучшению кровоснабжения сердечной мышцы, уменьшающие преднагрузку. Также используются кардиоселективные бета-блокаторы, антагонисты кальциевых каналов, уменьшающие частоту сердечных сокращений и потребность миокарда в кислороде. В экстренных случаях может применяться нейролептаналгезия путем внутривенного введения сильных обезболивающих средств.
- Тромболитические препараты. Обязательными составляющими лечебной программы являются дезагреганты (аспирин, клопидогрель, тиклопидин) и прямые антикоагулянты (гепарин), которые препятствуют тромбообразованию. При отсутствии явных противопоказаний требуется длительный прием препаратов данных групп.
- Гиполипидемические препараты. В долгосрочной перспективе применяются статины, способствующие нормализации уровня холестерина и назначаемые независимо от его исходного уровня. Постоянный прием достоверно снижает общую смертность, вероятность повторных приступов и осложнений. Обычно используется аторвастатин или симвастатин. Возможна комбинация с никотиновой кислотой.
Сохранение кардиалгии, несмотря на проводимую терапию, наличие обширной зоны ишемии с прогрессирующим характером процесса и поражение крупных коронарных артерий являются показаниями для назначения инвазивных методов воздействия. Выбор способа реваскуляризации зависит от данных коронароангиографии. Осуществляют транслюминарную коронарную ангиопластику, коронарное шунтирование. Эти оперативные вмешательства лишь в незначительной степени улучшают отдаленный прогноз пациента, однако значительно повышают качество его жизни и практически полностью устраняют симптоматику.
Прогноз и профилактика
При своевременной госпитализации, адекватно проведенном лечении и соблюдении врачебных рекомендаций прогноз относительно благоприятный. Эффективной профилактикой является предотвращение ожирения, отказ от вредных привычек (прежде всего – курения), минимизация стрессовых воздействий. Существенную роль играет регулярная физическая активность, степень которой зависит от возможностей больного. Это может быть ходьба, бег, катание на велосипеде или лыжах, плавание. Необходимо контролировать артериальное давление, рационально и сбалансировано питаться.
Источник
Инфаркт миокарда (некроз или гибель сердечной мышцы) является грозным осложнением ИБС, подчас смертельным. По статистическим данным в США острый инфаркт миокарда приводит к смерти в среднем каждого третьего мужчины в возрасте 35-50 лет [9]. Причем больше половины этих смертельных случаев имеют место в течение первых 3-4 часов от начала инфаркта по вине опасной для жизни аритмии (фибрилляции желудочков сердца), которая без лечения всегда приводит к смерти. Можно сказать, что инфаркт миокарда является частным случаем ИБС. Инфаркт миокарда происходит вследствие закупорки (тромбоза) артерии, кровоснабжающей тот или иной участок сердечной мышцы. Как правило, инфаркту предшествует разрыв атеросклеротической бляшки, отложение на поверхности такой измененной бляшки тромбоцитов. Все это способствует тому, что просвет артерии начинает закрываться, а это приводит к острой ишемии миокарда. Инфаркту миокарда, как правило, предшествует повышение вязкости крови. Если в ходе инфаркта миокарда возникает спазм коронарной артерии в месте все той же бляшки, то это вызывает еще большее сужение артерии, вплоть до полной ее закупорки.
Иногда возможно развитие инфаркта миокарда только вследствие длительного спазма атеросклеротически неизменененных коронарных артерий [9], например, в результате вазоспастической стенокардии (см. ниже). В результате инфаркта миокарда происходит гибель участка сердечной мышцы. Со временем этот участок замещается на другую ткань, рубцовую (или так называемую соединительную ткань), не содержащую мышечных волокон. Такое состояние называется постинфарктным кардиосклерозом, в отличие от атеросклеротического кардиосклероза, когда мышечная ткань замещается соединительной без предшествующего инфаркта миокарда. Во время инфаркта миокарда может погибнуть как участок сердечной мышцы целиком, во всю его толщину (трансмуральный инфаркт миокарда), так и только один из ее слоев: внутренний (субэндокардиальный инфаркт), средний (интрамуральный инфаркт) или наружный (субэпикардиальный инфаркт). В том случае, если произошел инфаркт только в одном из слоев сердечной мышцы, то это не исключает того, что в остальных слоях впоследствии не разовьется трансмуральный инфаркт. Прогноз для жизни и сохранности достаточной сократительной функции миокарда в результате случившегося инфаркта миокарда зависит, прежде всего, от площади погибшего миокарда (крупноочаговый или мелкоочаговый инфаркт). А это, в свою очередь, определяется количеством пораженных артерий и месторасположением закупорки в самой артерии. Если закупорка произошла в устье артерии, кровоснабжающей большой по площади участок миокарда, то прогноз может быть самым печальным. Таким образом, чем более удаленный от устья участок артерии поражен, тем безопаснее прогноз. В среднем рубец формируется в сроки до 1,5-2 месяцев, после чего трудоспособность пациента может восстановиться.
Проявления инфаркта миокарда
Заболевание может начинаться по-разному: как на фоне общего благополучия, так и как утяжеление приступов стенокардии. Иногда инфаркт миокарда является первым проявлением ИБС. Больной беспокоен, потлив, бледен, могут отмечаться тошнота и рвота. Болевой приступ значительно тяжелее и продолжительнее обычных приступов стенокардии. Ранее помогавшие лекарства перестают действовать. Боль может быть настолько невыносимой, что может привести к болевому шоку с потерей сознания и резким падением АД. Если болевой приступ не снимается 3 таблетками нитроглицерина, нужно срочно вызывать «скорую медицинскую помощь». Иногда инфаркт миокарда никак себя не проявляет. Именно о таких случаях говорят, что больной перенес инфаркт миокарда «на ногах».
Диагностика инфаркта миокарда
Для диагностики инфаркта миокарда используют те же методы, что и для диагностики ИБС в целом. Пробы с дозированной физической нагрузкой категорически противопоказаны из-за высокого риска развития различных осложнений и смерти больного. В большинстве случаев инфаркта миокарда появляются характерные изменения на ЭКГ. Дополнительным методом диагностики инфаркта миокарда является выявление его биохимических маркеров – биологических субстанций (ферментов), которые появляются или значительно повышаются только при этом заболевании. Биохимическими маркерами инфаркта миокарда являются креатинфосфокиназа (КФК) и ее компоненты (фракции), а также тропонин и некоторые другие. Уже спустя 4 часа от начала заболевания, особенно при нечетких проявлениях заболевания и сомнительной ЭКГ, с помощью маркеров можно разрешить еще остающиеся сомнения.
Лечение инфаркта миокарда
Инфаркт миокарда – абсолютное показание к госпитализации больного в кардиологический стационар для лечения и круглосуточного врачебного наблюдения. Только своевременное медицинское вмешательство может снизить риск тяжелых последствий инфаркта. В больнице обычно проводят лечение, способствующее ограничению зоны инфаркта (внутривенное введение нитроглицерина, -адреноблокаторов, антагонистов ионов кальция), увеличению сердечного выброса (добутамин, допамин, адреналин), снижению вязкости и свертываемости крови (гепарин), нормализации АД, ликвидации аритмии. Обезболивающие средства, в том числе наркотические, обычно вводятся еще врачами бригады «скорой медицинской помощи». При необходимости их введение продолжают и в больнице. Идеальной считается госпитализация в кардиологический стационар, где специалисты владеют методами интервенционной диагностики и лечения. При поступлении больного в такой стационар ему может быть предписана коронароангиография, что позволит с высокой точностью установить, какая именно артерия стала причиной инфаркта. Затем больному может быть выполнены ТЛБАП и/или стентирование этой инфаркт-зависимой артерии с целью восстановления кровотока по ней. При такой последовательности событий можно свести к минимуму последствия даже тяжелого инфаркта миокарда.
Но, к сожалению, отделения интервенционной кардиологии имеются пока далеко не во всех медицинских стационарах нашей страны. В ряде кардиологических стационаров, а в идеальном варианте еще на дому, врачами кардиологической бригады «скорой медицинской помощи» выполняется так называемый системный тромболизис. Этот метод заключается во внутривенном введении препаратов, способных устранить («растворить») тромбы в коронарных артериях. Системный тромболизис более распространен, чем ТЛБАП и стентирование коронарных артерий. В отделениях интервенционной кардиологии, в свою очередь, имеется возможность для выполнения внутрикоронарного тромболизиса, т.е. введения растворяющего тромб препарата (тромболитика) непосредственно в коронарные артерии. Тромболизис является альтернативой ТЛБАП и стентирования коронарных артерий, однако он не устраняет стенозы. Обычно операция коронарного шунтирования во время острого инфаркта миокарда не выполняется, что связано с повышенным операционным риском смерти больного. Как исключение операцию проводят в тех случаях, когда необходимо устранить осложнения инфаркта миокарда, угрожающие его жизни, например, разрыв межжелудочковой перегородки и др. В последнее время предпринимаются попытки, направленные на восстановление количества утраченных в результате инфаркта миокарда мышечных клеток. Для этого в миокард вводят донорские «прародители» мышечных клеток, так называемые стволовые клетки. Эти клетки внедряют либо во время операции на сердце, обкалывая ими рубцовую зону, либо вводят в коронарные артерии при выполнении коронароангиографии. В настоящее время идет накопление такого научного материала.
Осложнения инфаркта миокарда
Как и при любом другом заболевании, в результате инфаркта миокарда наблюдаются осложнения. Развитие осложнений определяется площадью инфаркта и тем, какой именно участок миокарда пострадал. Смертельными осложнениями являются наружные разрывы сердца, то есть разрыв его наружных стенок. Если произошел разрыв одной из внутренних стенок (перегородок) сердца, то это состояние является потенциально опасным для жизни. Многое зависит опять же от размеров образовавшегося дефекта и от того, как сердце справляется с последствиями, обусловленными наличием этого дефекта. Иногда для спасения жизни больного в таких случаях требуется выполнение срочной операции на сердце. Основной метод диагностики разрывов сердца – ЭхоКГ. В результате перенесенного инфаркта могут образовываться аневризмы сердца. Аневризма представляет собой выпуклое образование на поверхности сердца, которое во время сердечных сокращений пассивно выбухает наружу. Аневризмы могут состоять из рубцовой ткани (истинная аневризма) или окружающих сердце тканей (ложная аневризма). Опасность аневризмы состоит в том, что в ее полости могут образовываться тромбы. Фрагменты этих тромбов могут разноситься с током крови, вызывая инфаркты уже других внутренних органов (мозга, почек, печени, легких и т.д.). Такое распространение фрагментов тромбов по организму называется тромбоэмболией. Поэтому всем больным с аневризмой сердца показан прием антикоагулянтов – медикаментов, препятствующих образованию тромбов. Кроме того, зона аневризмы может быть источником устойчивых и опасных для жизни нарушений ритма сердца. Диагностика аневризм сердца осуществляется при помощи ЭКГ, ЭхоКГ и рентгенографии органов грудной клетки. Лечение аневризм сердца только хирургическое. На операции аневризма иссекается, а окружающий ее миокард сшивается между собой. Также может быть выполнена пластика аневризмы: после иссечения аневризмы на ее место подшивается биологическая или синтетическая заплата. Иссечение или пластика аневризм выполняется одновременно с коронарным шунтированием. Еще одним грозным осложнением инфаркта миокарда является кардиогенный шок – состояние, при котором сердце не может справиться со своей насосной (сократительной) функцией. Это состояние возникает, когда в результате инфаркта погибает не менее 50% массы сократительного миокарда. Только в небольшом проценте случаев, по некоторым данным до 20%, можно спасти больному жизнь [9].
Кардиогенный шок – это частный случай постинфарктной сердечной недостаточности, то есть снижения насосной функции сердца вследствие инфаркта миокарда. В результате гибели какого-либо участка миокарда, как говорилось выше, формируется рубец, который в отличие от остального миокарда не может полноценно сокращаться и вносить свой вклад в насосную функцию сердца. Рубец – это как большая заплатка на воздушном шаре: с одной стороны и шар вроде бы цел, а с другой – вовсе необязательно, что этот шар теперь можно полноценно надуть. Создается ситуация, когда миокард, не пострадавший от инфаркта, вынужден взять на себя функцию погибшего миокарда, при этом какая-то зона сердца будет сокращаться более интенсивно, а другая – менее. Со временем и здоровый миокард начнет сдавать свои «сократительные» позиции, особенно при выполнении физической нагрузки. В конечном итоге возникнет и будет постепенно прогрессировать сердечная недостаточность – неспособность сердца в полной мере справляться со своей насосной функцией. Кровь начнет задерживаться в венах легочного (малого), а затем и большого круга кровообращения. В результате появится одышка как следствие застоя крови в сосудах легких, а также отеки, гепатомегалия (увеличение печени, проявляющееся тяжестью в правом подреберье), асцит (увеличение объема живота за счет застоявшейся жидкой части крови). Все эти признаки (симптомы) сердечной недостаточности становятся обычно заметными к вечеру, когда организм максимально «устанет» после всего того, что он проделывал в течение дня. К сожалению, постинфарктная сердечная недостаточность наряду с прогрессированием атеросклероза коронарных артерий и последующими инфарктами миокарда не увеличивает продолжительность жизни больных ИБС.
Несмертельными осложнениями инфаркта миокарда являются различные нарушения проводимости сердечного импульса (блокады), что иногда требует постановки временного электрокардиостимулятора. Иногда, наоборот, после инфаркта миокарда появляются различные аритмии, нуждающиеся в соответствующей антиаритмической терапии (лечении). У больных, перенесших трансмуральный инфаркт миокарда, примерно в 30% случаев [9] отмечается неинфекционное воспаление сердечной сумки или оболочки (перикарда) – перикардит. Проявляется он кратковременными болями в области сердца, обычно при глубоком вдохе. Продолжительность перикардита при инфаркте миокарда обычно составляет 3-5 дней.
Существует еще одно редкое осложнение инфаркта миокарда – так называемый синдром Дресслера. (Синдром – это совокупность симптомов или признаков какого-либо заболевания). Возникает он спустя дни, недели и даже месяцы после перенесенного инфаркта миокарда. Синдром Дресслера – это ответная реакция иммунной системы организма на измененные в результате инфаркта миокарда ткани собственного же сердца. Проявляется это осложнение неинфекционным перикардитом, а также неинфекционным воспалением наружной оболочки легких (плевритом) и других тканей. Лечение синдрома Дресслера – медикаментозное.
Нестабильная стенокардия
Нестабильная стенокардия (синонимы: прогрессирующая, вариантная) – пограничное состояние между обычной (стабильной) стенокардией напряжения и инфарктом миокарда. Оно характеризуется учащением и утяжелением приступов стенокардии. Иногда нестабильную стенокардию также называют предынфарктным состоянием. Приступы стенокардии при этой разновидности ИБС возникают уже при меньших, чем ранее, нагрузках, в покое или ночью. В основе нестабильной стенокардии, как правило, лежит все тот же тромбоз коронарных артерий, что и при инфаркте миокарда, только обратимый. В отличие от инфаркта миокарда, при нестабильной стенокардии в пораженной артерии остается небольшой просвет и кровь через него все-таки поступает дальше места тромбоза. Но этого количества крови все равно недостаточно для кровоснабжаемого данной артерией миокарда, что приводит к учащению и утяжелению болевых приступов. Нестабильная стенокардия обязательно разрешится либо в сторону стабильной стенокардии напряжения, либо в сторону инфаркта миокарда. По данным американских ученых, примерно у трети больных нестабильной стенокардией в течение 3 месяцев от момента ее появления при отсутствии соответствующего лечения разовьется инфаркт миокарда [9]. Именно поэтому нестабильная стенокардия нуждается в активном стационарном лечении, как медикаментозном, так и хирургическом. Диагностика заболевания такая же, как и инфаркта миокарда.
Вазоспастическая стенокардия
Вазоспастическая стенокардия (синонимы: стенокардия Принцметала, спонтанная стенокардия) – состояние, обусловленное непроизвольным сокращением (спазмом), чаще крупных, неизмененных атеросклерозом коронарных артерий. Спазм коронарных артерий приводит к ишемии миокарда, что проявляется стенокардией. Обычно вазоспастической стенокардией страдают люди молодого возраста. Болевой приступ чаще возникает в предутренние часы, иногда он сопровождается нарушениями ритма сердца и обычно проходит после приема нитроглицерина или нифедипина. Вне приступа ЭКГ у таких лиц не отличается от ЭКГ здоровых людей. Помощь в диагностике заболевания может оказать холтеровское мониторирование ЭКГ. Надежно диагностировать данное заболевание можно только при помощи лекарственной провокации (эргоновиновая проба). Для профилактики приступов вазоспастической стенокардии назначают медикаменты, расширяющие коронарные артерии, например, нифедипин. Длительный приступ вазоспастической стенокардии может закончиться инфарктом миокарда. СИНДРОМ Х Синдром Х (икс) – это состояние, проявляющееся стенокардией напряжения. Жалобы больных и результаты инструментальных методов диагностики такие же, как и при типичной стенокардии напряжения. Отличает эти два заболевания то, что при синдроме Х коронароангиография никаких изменений в коронарных артериях не выявляет. Это объясняется тем, что синдром Х обусловлен спазмом мелких, не видимых на коронароангиограмме коронарных артерий. Окончательный диагноз устанавливается методом исключения.
Внезапная кардиогенная смерть
Под этим термином понимают внезапно наступившую смерть, причиной которой послужило заболевание сердца (от греческих слов kardia – «сердце» и genesis – «происхождение, возникновение» [2]). Примерно в 20% случаев внезапная кардиогенная (сердечная) смерть является первым и единственным проявлением ИБС [9]. Обычно погибают больные с тяжелым поражением коронарных артерий и грубым нарушением сердечной деятельности. Непосредственной причиной смерти является внезапная закупорка коронарных артерий, сопровождающаяся жизнеугрожающей аритмией (фибрилляцией желудочков). Как говорилось выше, при отсутствии своевременного лечения фибрилляция желудочков всегда заканчивается смертью. Диагноз ИБС у погибших больных может быть заподозрен по расспросам родственников, а подтвержден в ходе патологоанатомического исследования.
Источник
