Сердце и сосуды после инфаркта
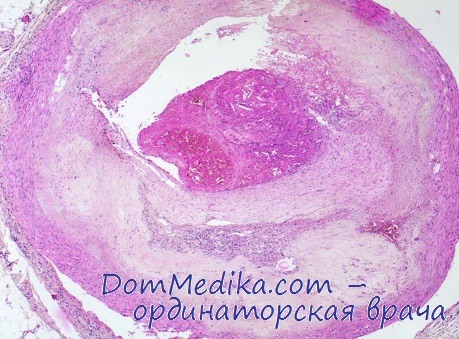
Реактивность сосудов при инфаркте миокарда была изучена в 21 случае на сердце человека. Возраст больных этой группы был от 43 до 83 лет.
В клинической практике течение инфаркта миокарда условно разделяют на несколько стадий, что связано со сменой одних симптомокомплексов другими, а также с эволюцией некротического очага в сердечной мышце. Различают несколько периодов течения инфаркта миокарда. Первый из них — период предвестников (продромальный период) — обусловлен нарастающей ишемией миокарда, предшествующей некрозу. Клинически он проявляется во все возрастающем числе ангинозных приступов, более сильных и продолжительных, чем обычные. Этот период перед возникновением инфаркта может продолжаться от 24 часов до 45 дней.
За ним следует острый период (в большинстве случаев он равняется 8—10 дням), в течение которого некроз и миомаляция сердечной мышцы достигают наивысшего развития. За острым периодом следует подостри и, в течение которого развиваются процессы заживления и рубцевания миокарда; он начинается с 8—10-го дня и заканчивается через 1,5—2 месяца от начала заболевания.
Как выяснилось при исследовании, в 9 случаях из 21 возникновению инфаркта предшествовал период учащения и усиления приступов стенокардии — период предвестников; после возникновения инфаркта в 13 случаях больные умерли в первые часы и дни заболевания — острый период и в 8 случаях смерть наступила через 10—60 дней после возникновения инфаркта — подострыи период.
Возникновению инфаркта миокарда в 14 случаях предшествовал длительный стенокардический анамнез с частыми приступами загрудинных болей; в некоторых из них приступы возникали во время физической нагрузки — в результате стенокардии напряжения. В 13 случаях инфаркт миокарда возник на фоне гипертонической болезни.
Наступление инфаркта миокарда сопровождалось яркой клинической картиной. Одним из первых ее проявлений являлся длительный болевой приступ — status anginosus, обычно не устраняемый нитроглицерином. Он, как правило, длился несколько часов, иногда с явлениями шока, и в большинстве случаев заканчивался смертью.

У всех больных, умерших в первые часы и дни после возникновения инфаркта, клинически наблюдались нарушения со стороны сердечно-сосудистой системы: расширение границы сердца влево, глухие сердечные тоны, частый нитевидный пульс, падение артериального давления и др. В ряде случаев имелась тяжелая картина острого отека легких.
Больные, переживите острый период заболевания, умерли в различные сроки после возникновения инфаркта. При жизни у них наблюдались симптомокомплексы, связанные с возникновением и эволюцией некротического очага в миокарде (повышение температуры тела, лейкоцитоз, ускоренная РОЭ), а также явлениями недостаточности сердечно-сосудистой системы.
Смерть больных как в острых, так и в подострых стадиях развития инфаркта часто наступала при явлениях недостаточности сердечно-сосудистой системы.
В некоторых случаях в течение заболевания наблюдалась эмболия сосудов мозга, легких и нижних конечностей, что вызывало стойкие нарушения функции этих органов. Возникшие осложнения были вызваны заносом в сосудистую систему указанных органов кусочков пристеночного тромба, обнаруживаемого нами у ряда больных в полости аневризмы левого желудочка сердца.
Лечение больных начиналось уже в приемном отделении Института имени Склифосовского и выражалось в срочных мероприятиях, направленных на устранение острой сердечнососудистой недостаточности и нарастающего отека легких. С этой целью давали нитроглицерин, проводили внутривенные инъекции строфантина в 40% растворе глюкозы и подкожные инъекции камфары, кофеина, атропина, лобелина, вдыхание кислорода. В более поздние периоды, кроме нитроглицерина и строфантина, применяли также эуфиллин, диуретин, папаверин, адонис и антикоагулянты — дикумарин и др. Ни в одном случае не были употреблены препараты наперстянки.
Проведенными макро- и микроскопическими обследованиями установлено, что в 7 случаях инфаркт был первичным, а в 15 случаях, кроме инфаркта, приведшего больного к смерти, в сердечной мышце были обнаружены старые рубцовые изменения, указывающие на ранее перенесенный инфаркт миокарда. Наиболее частым местом поражения была передняя стенка левого желудочка; кроме того, имелись случаи одновременного поражения двух, трех и даже четырех его стенок.
Выраженная гипертрофия сердечной мышцы обнаружена в 13 случаях.
Максимальный вес сердца в этой группе больных равнялся 620 г, минимальный — 350 г.
Во всех случаях инфаркта миокарда был отмечен атеросклероз венечных артерий. Степень атеросклеротического процесса в наших наблюдениях была различной: слабо выраженный атеросклероз — в 2 случаях; умеренный — в 4, резко выраженный— в 15. Атеросклоротические бляшки обычно носили многоэтажный характер, в отдельных случаях в них можно было обнаружить свежие и старые кровоизлияния. Мышечный слой сосудистой стенки в расположении крупных бляшек атрофировался. Коропароатеросклсроз, как правило, посил тотальный характер: наблюдалось поражение всех крупных стволов коронарных артерий.
При изолированном поражении изменения чаще обнаруживались к нисходящей ветви левой венечной артерии. Тромбоз венечных артерий был найден в 7 случаях, в 4 — тромб был свежим и в 3 — в состоянии организации, в одном случае просвет сосуда закрывали известковые массы, в другом — разбухшая от кровоизлияния бляшка. Микроскопически в атеросклеротических бляшках обнаружены явления стаза, периваскулярного отека, свежие и старые кровоизлияния в атерому. Отмеченные изменения указывали на функциональное расстройство венечного кровообращения при жизни.
– Вернуться в раздел “Кардиология”
Оглавление темы “Миокард и коронарные сосуды при гипоксии”:
- Микроэлементы при инфаркте миокарда. Роль катехоламинов при инфаркте миокарда
- Гормоны надпочечников при инфаркте миокарда. Белково-жировой обмен при инфаркте миокарда
- Содержание тиамина при инфаркте миокарда. Факторы приводящие к быстрому некрозу миокарда
- Влияние гипоксии на реактивность сердца и сосудов. Гипоксия миокарда
- Последовательность гипоксических изменений миокарда. Метаболизм миокарда при гипоксии
- Миозин под действием гипоксии. Реактивность сосудов сердца на фоне стенокардии
- Примеры ишемии миокарда. Макроскопия и микроскопия сердца при острой ишемии
- Влияние нитроглицерина на стенокардитическое сердце. Влияние эуфиллина на сердце при стенокардии
- Влияние строфантина на стенокардитическое сердце. Влияние адонизида, дигиталиса на сердце при стенокардии
- Сосуды сердца при инфаркте миокарда. Реактивность коронарных сосудов после инфаркта
Источник
Как правило, люди, перенесшие инфаркт, считают, что к полноценной жизни вернуться уже не удастся. Однако медицина не стоит на месте, и в настоящее время такое мнение ошибочно.
Используя передовые методики можно добиться максимального восстановления функций сердечной мышцы (миокарда), а значит, обеспечить нормальное кровообращение в организме. Это, в свою очередь, позволит, не задумываясь, справляться с повседневными нагрузками, работать, отдыхать, вести половую жизнь и справляться с возникающими жизненными стрессами и проблемами. Кроме того, сейчас возможно максимально снизить риск повторного инфаркта, а значит, приобрести уверенность в завтрашнем дне.
Таких результатов позволяет достичь лечение стволовыми клетками, уже доступное в российских клиниках.
Лечение в деталях
Инфаркт миокарда развивается, когда на атеросклеротической бляшке в просвете артерии сердца по какой-либо причине появляется дефект, то есть частичное ее разрушение. Организм реагирует на повреждение формированием кровяного сгустка – тромба. Но в суженном бляшкой просвете артерии тромб не только “латает” дефект, но и перекрывает кровоток.
Постоянно работающая сердечная мышца нуждается в бесперебойном притоке крови, снабжающей ее кислородом. Когда просвет артерии, питающей тот или иной участок миокарда, перекрывается тромбом, этот участок начинает испытывать острое кислородное голодание, приводящее к гибели клеток и возникновению участка мертвой ткани – некроза. Это событие и называется инфарктом миокарда.
После формирования очага некроза погибшие клетки замещаются соединительной тканью, и в сердечной мышце формируется рубец, который, разумеется, не может сокращаться. Это влияет на функции всего сердца – оно не может перекачивать кровь так же эффективно, как до инфаркта.
Для улучшения деятельности неповрежденных участков сердечной мышцы, обеспечивающих работу всего органа, традиционно применяют лекарственные препараты и, в некоторых случаях, операцию на сосудах сердца – шунтирование или стентирование.
И лекарственное, и хирургическое лечение в значительной степени помогают улучшить самочувствие и снизить риск, однако о более или менее полном восстановлении функций сердца при их применении речи не идет. Кроме того, к лекарствам и операциям имеются противопоказания, и лечение может иметь побочные эффекты.
В отличие от традиционных методов, терапия стволовыми клетками базируется на естественных процессах восстановления сердечной мышцы и формирования в ней новых сосудов, обеспечивающих достаточное кровоснабжение.
Перед тем как приступить к такой терапии, перенесшего инфаркт человека всесторонне обследуют: делают развернутый анализ крови, ЭКГ, эхокардиограмму, при необходимости – суточное мониторирование ЭКГ и другие исследование. Это необходимо, чтобы определить, насколько лечение показано конкретному человеку и каких результатов можно ожидать.
После этого у пациента берут небольшое количество костного мозга или жировой ткани и выделяют из него мезенхимальные стволовые клетки. Эти клетки неспециализированны, то есть не имеют признаков какой-либо конкретной ткани, а являются универсальными. Они могут развиться в любой тип клеток, необходимый для восстановления имеющегося дефекта органа или ткани, причем восстановленный участок будет иметь как “рабочие” клетки, так и соединительнотканный каркас, сосуды и нервы.
Еще одной важнейшей особенностью стволовых клеток является их способность самостоятельно распознавать повреждение и начать работу по его восстановлению.
С возрастом число функционирующих стволовых клеток существенно уменьшается: если в костном мозге новорожденного одна стволовая клетка приходится на 10 тысяч кроветворных, то к подростковому возрасту ее удается обнаружить лишь в 100 тысячах клеток, к 50 годам – в 500 тысячах, а к 70 годам – в миллионе. Тем не менее, стволовые клетки есть у человека любого возраста.
Полученные от пациента мезенхимальные клетки помещают в специальный инкубатор, где происходит их размножение до необходимого количества. Как правило, на один курс лечения требуется не менее 200 миллионов клеток, для получения которых нужно около двух недель.
Еще некоторое количество выращивается “про запас”, подвергается криоконсервации в жидком азоте и направляется на бессрочное хранение в банк клеток, имеющийся в клинике. Это делается на тот случай, если понадобится повторный курс лечения – при наличии консервированных клеток их не придется получать повторно. Кроме того, с возрастом качество стволовых клеток организма ухудшается, а клетки из банка останутся “молодыми”.
Когда необходимое количество мезенхимальных стволовых клеток выращено, часть из них подвергают частичной дифференцировке, то есть превращению в клетки-предшественницы необходимой ткани. Для сердца такими клетками являются кардиомиобласты, которые способны развиваться в ткань сердечной мышцы. На их получение уходит еще одна неделя.
Затем смесь мезенхимальных клеток и кардиомиобластов вводят пациенту внутривенно. С током крови они попадают в сердце, обнаруживают очаг повреждения и принимаются за работу. В процессе активного деления их число быстро достигает нескольких триллионов. При этом введенные клетки постоянно выделяют определенные “сигнальные” вещества, которые мобилизуют стволовые клетки в самом организме и “призывают” их также заняться лечением.
Этого более чем достаточно для восстановления поврежденного кислородным голоданием миокарда и формирования в нем разветвленной сети сообщающихся друг с другом коллатеральных сосудов. Эти сосуды обеспечивают адекватное кровоснабжение обновленного миокарда кислородом и “страхуют” друг друга в случае закупорки тромбом – при закрытии одной из артерий кровь пойдет в обход по другим и некроза не произойдет.
Во многих случаях помимо улучшения функций выжившей после инфаркта сердечной мышцы, своей работой компенсирующей отмерший участок, терапия стволовыми клетками позволяет существенно уменьшить размер рубца и укрепить поврежденный участок сердца, что снижает вероятность такого опасного осложнения, как аневризма сердца.
Редакция благодарит Клинику стволовых клеток “Новейшая медицина” за помощь в подготовке материала.
Источник
Help heart, 3 декабря 2019
Последствия и осложнения инфаркта миокарда
Острый инфаркт миокарда — одно из самых опасных сердечно-сосудистых заболеваний. Достижения современной медицины последних десятилетий позволили значительно усовершенствовать его лечение и увеличить вероятность благоприятного исхода. И все же перенесенный однажды инфаркт миокарда (ИМ) может иметь последствия.
Механизм развития острого коронарного синдрома
Инфаркт миокарда, который наряду с эпизодом нестабильной стенокардии входит в понятие острый коронарный синдром, представляет собой обострение ишемической болезни сердца. При инфаркте миокарда развивается некроз сердечной мышцы, обусловленный острым нарушением кровоснабжения.
В большинстве случаев это происходит в результате атеротромбоза, при котором коронарные сосуды частично или полностью блокируются тромбом. Заболевание проявляется внезапно возникающими интенсивными болями за грудиной, тахикардией, «холодным потом», бледностью кожных покровов и рядом других симптомов1.
Цель лечения острого инфаркта — быстрое восстановление кровоснабжения. Однако даже после того, как кровоток налажен, терапию нельзя прекращать, поскольку коронарный атеросклероз, который стал фундаментом для развития острого коронарного синдрома, протекает хронически1,2.
Ранние последствия инфаркта миокарда1
Начиная с первых часов после инфаркта и вплоть до 3-4 дня могут развиваться ранние последствия инфаркта, среди которых:
- острая левожелудочковая недостаточность, которая возникает при снижении сократительной способности сердца. При ее возникновении появляется одышка, тахикардия, кашель;
- кардиогенный шок. Это тяжелое осложнение острого коронарного синдрома, развивающееся в результате значительного ухудшения сократительной способности сердечной мышцы вследствие обширного некроза;
- нарушения ритма и проводимости сердца, отмечаются у 90% больных с острым ИМ.
- Приступы ранней постинфарктной стенокардии (ПСК). ПСК – возникновение или учащение приступов стенокардии через 24 часа и до 8 недель после развития ИМ.1
- перикардит – воспалительный процесс, развивающийся в наружной оболочке сердца-перикарде. Он возникает в первые-третьи сутки заболевания и может проявляться болью в области сердца, которая изменяется при смене положения тела, повышением температуры тела1.
В 15-20% случаев инфаркта происходит истончение и выбухание стенки сердца, чаще всего — левого желудочка. Это состояние называется аневризма сердца. Как правило, она развивается при обширном поражении сердечной мышцы.
К факторам, предрасполагающим к развитию аневризмы сердца, также относят нарушение режима с первых дней заболевания, сопутствующую артериальную гипертензию и некоторые другие1.
Особую группу составляют тромбоэмболические последствия, при которых просвет сосудов полностью или частично перекрывается сгустками крови. Это часто происходит на фоне сопутствующей варикозной болезни, нарушения свертывающей системы крови и длительного постельного режима1.
Из-за нарушения кровоснабжения острый коронарный синдром может осложняться и желудочно-кишечными проблемами, такими как эрозии, острые язвы желудочно-кишечного тракта. Могут возникать и нарушения в психическом состоянии — депрессия, психозы. Им способствуют пожилой возраст, сопутствующие заболевания нервной системы1.
Поздние последствия инфаркта
По окончании острого периода заболевания могут развиваться так называемые поздние последствия.
К ним относятся осложнения, которые появляются через 10 дней после манифестации ИМ и позже4,5 :
- постинфарктный синдром Дресслера, возникает через 2-6 недель после манифестации инфаркта миокарда и проявляется воспалением перикарда, плевры, альвеол, суставов и другими патологическими изменениями;
- тромбоэндокардит с тромбоэмболическим синдромом (возникновение пристеночного тромба в полости сердца, на клапанах сердца);
- поздняя постинфарктная стенокардия, которая характеризуется возникновением или учащением приступов стенокардии. Ее частота колеблется от 20 до 60%4.
Некоторые больные, перенесшие острый инфаркт миокарда, находятся в группе высокого риска по развитию повторных осложнений ишемической болезни сердца и прежде всего — рецидива инфаркта миокарда, нестабильной стенокардии.
Это связано с тем, что у больных с острым коронарным синдромом наряду с наличием атеросклеротической бляшки, которая осложнилась разрывом и перекрыла просвет коронарной артерии, существуют бляшки и в других артериях. Именно они могут служить причиной повторных эпизодов сердечно-сосудистых событий, вероятность которых очень высока 5.
Жизнь после инфаркта миокарда
После стабилизации состояния больного, перенесшего острый инфаркт, усилия врачей направляются прежде всего на уменьшение риска прогрессирования атеросклероза и ИБС.
Для вторичной профилактики используются лекарственные средства, эффективность которых доказана во множестве крупных международных исследований, и одни из них — антитромбоцитарные препараты, или антиагреганты 5.
Антиагреганты уменьшают агрегацию, то есть объединение тромбоцитов, чем препятствуют формированию кровяных сгустков. Один из самых известных антиагрегантов — ацетилсалициловая кислота.
Она уменьшает содержание вещества, активирующего процесс тромбообразования, — тромбоксана А2, необратимо подавляя таким образом агрегацию тромбоцитов, а также незначительно расширяет сосуды. Даже после однократного применения ацетилсалициловой кислоты ее антиагрегантный эффект сохраняется на протяжении до 7 суток6.
В начале 2000-х годов ученые выяснили, что антиагрегантная терапия, направленная на предотвращение риска повторных сердечно-сосудистых событий, может быть гораздо эффективней, если наряду с ацетилсалициловой кислотой назначать антиагрегант с другим механизмом подавления активности тромбоцитов, например, клопидогрел, тикагрелор или прасугрел7.
Такая схема лечения получила название двойной антитромбоцитарной терапии (ДАТТ). Сегодня в составе ДАТТ используются комбинации ацетилсалициловой кислоты с новыми антиагрегантами, например, ингибиторами P2Y12 тромбоцитов8.
В большинстве случаев для снижения риска рецидива инфаркта миокарда ДАТТ назначают на протяжении года после первичного сердечно-сосудистого события. Решение о длительности терапии принимает врач с учетом индивидуальных особенностей пациента.
Эффективность профилактики во многом зависит от дисциплинированности пациента. Известно, что самостоятельная отмена лекарств в течение полугода после эпизода острого коронарного синдрома по сравнению с дальнейшим профилактическим лечением приводит к повышению риска смертности в 2,7 раза.
Если же пациент прекращает принимать ДАТТ в течение 7-12 месяцев после первичного ИМ, риск рецидива возрастает в 2,3 раза9.
Помимо антиагрегантов в индивидуальном порядке пациентам после инфаркта миокарда доктор может назначить: препараты для снижения уровня холестерина, для нормализации артериального давления и частоты сердечных сокращений, средства, предотвращающие ремоделирование сердца1,3-5,10.
Таким образом, в значительной мере люди, перенесшие ИМ, сами влияют на его прогноз. Изменение образа жизни, соблюдение всех рекомендаций врачей и аккуратный прием назначенных препаратов — залог успешного восстановления и полноценной жизни после эпизода острого коронарного синдрома.
Использованная литература
- Якушин С.С.Инфаркт миокарда / С. С. Якушин – Москва, 2010. Вып. ГЭОТАР-Мед– 224c.
- Эрлих А.Д. Двойная антитромбоцитарная терапия: необходимость приверженности к лечению и возможности ее повышения / Эрлих А.Д. // Специализированный медицинский журнал – 2014. – № 2 – С.25–33.
- Шилов А.М. Лечение неосложненного инфаркта миокарда (Общие положения) / Шилов А.М., Мельник М.В., Осия А.О. // Вестник анестезиологии и реаниматологии – 2010. – Т. 7 – № 5 – С.36–42.
- Цеденова Е.А. Выбор метода диагностики для оценки степени риска сердечно-сосудистых осложнений и летальности у больных Q-образующим инфарктом миокарда / Цеденова Е.А., Волов Н.А., Лебедева А.Ю. // Российский кардиологический журнал – 2007. – № 4. –С.83-91.
- Аронов Д.М. Лечение больных после острых коронарных синдромов / Аронов Д.М., Лупанов В.П. // Consilium medicum – 2004. – № 11 –С.823-830.
- Инструкция по медицинскому применению препарата Ацетилсалициловая кислота.Рег.уд. ЛП-004828.
- Yusuf S. Clopidogrel in Unstable Angina to Prevent Recurrent Events Trial Investigators. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation / Yusuf S., Zhao F., Mehta S.R., Chrolavicius S., Tognoni G., Fox K.K. // N Engl J Med. 2001; 345 (7): 494–502.
- Roffi M. et al. ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation of the E / Roffi M. et al. // Eur Heart J 2016; 37: 267–315.
- Zeymer U. Systematic review of the clinical impact of dual antiplatelet therapy discontinuation after acute coronary syndromes / Zeymer U., Becher A., Jennings E., Johansson S., Westergaard M. // European heart journal. Acute cardiovascular care. 2017; 6 (6): 522-531.
- Джаиани Н.А. Вторичная профилактика инфаркта миокарда: фармакотерапевтические аспекты / Джаиани Н.А., Терещенко С.Н. // Справочник поликлинического врача – 2007. – № 2 –С.19-23.
Оригинал статьи: https://helpheart.ru/infarkt/ob-infarkte-miokarda/posledstviya-i-oslozhneniya-infarkta/
Help heart
Информационный портал о профилактике сердечно-сосудистых заболеваний
Источник
