Может ли инсулин привести к инфаркту

Инсулин при инфаркте миокарда и сахарном диабете. Значение глюкозо-инсулиновой смеси при диабете и инфарктеВпоследствии всем больным, которым вводили глюкозо-инсулиновую смесь, назначали подкожно инсулин 4 раза в сутки по крайней мере в течение 3 мес с целью поддержания нормального уровня глюкозы в крови. Три раза в день перед едой вводили инсулин короткого действия, на ночь — инсулин пролонгированного действия (средней продолжительности). Пациентам, вошедшим в контрольную группу, назначали стандартное лечение. Они не получали инсулин, если на то не было чётких клинических показаний. При выписке из больницы 266 больных (87 %) из группы, получавшей глюкозо-инсулиновую смесь с последующим подкожным введением инсулина, продолжали получать инсулин, тогда как только 135 больных (43 %) из контрольной группы получали инъекции инсулина (р < 0,0001). Эти рекомендации не случайно приведены столь подробно, так как ознакомившись с результатами данного исследования, многие врачи могут заинтересоваться использованием глюкозо-инсулиновой смеси для лечения больных сахарным диабетом, у которых развился инфаркт миокарда. В результате введения данной смеси (с последующим назначением инсулина подкожно) достоверно снизилась общая смертность в течение года и в среднем через 3,4 года наблюдения.
Через год от начала наблюдения общая смертность в группе больных, которым вводилась глюкозо-инсулиновая смесь с последующим назначением инсулина подкожно, снизилась на 30 % и составила 19 % (58 умерших) по сравнению с 26 % (82 умерших) в контрольной группе (р = 0,027). За весь период наблюдения общая смертность в группе больных, которым вводили глюкозо-инсулиновою смесь с «следующим назначением инсулина подкожно, снизилась на 28 % (11 % — в абсолютном выражении: 44 % — 33 % = 11 %) и составила соответственно 33 % (102 умерших) по сравнению с 44 % (138 умерших) в контрольной группе (р = 0,011). Эти положительные сдвиги были особенно выражены у больных, отнесённых к благополучной группе (с низким риском неблагоприятного течения заболевания), которые до развития инфаркта не получали инсулин. В “неблагополучную” группу высокого риска вошли больные, у которых отмечали минимум два из перечисленное ниже признаков: возраст старше 70 лет, перенесенный в прошлом инфаркт миокарда, сердечная недостаточность в анамнезе, приём дигоксина перед поступлением в больницу и включением в исследование. Среди больных благополучной группы которые до развития инфаркта миокарда не получали инсулин, больничная смертность снизилась (на фоне введения глюкозо-инсулиновой смеси с последующим назначением инсулина подкожно) на 58 % и составила 5 % по сравнению с 12 % среди пациентов из “благополучной” группы, не получавших такого лечения. Через 3 мес кюлюдения общая смертность снизилась на 52 % и составила соответственно по группам 6,5 и 13,5 % (р = 0,046). Через год наблюдения общая смертность снизилась на те же 52% и составила соответственно по группам 8,6 и 18 % (р = 0,020). За весь период наблюдения общая смертность в группе больных, которым вводили глюкозо-инсулиновую смесь с последующим назначением инсулина подкожно, снизилась на 51 % (15 % — в абсолютном выражении) и составила соответственно 18 % (25 умерших) по сравнению с 33 % (44 умерших) в контрольной группе (р = 0,004). Виновато ли в таких благоприятных сдвигах относительно непродолжительное введение глюкозо-инсулиновой смеси в остром периоде инфаркта миокарда и/или последующее хроническое введение инсулина (возможно, также повлекшее за собой усиленное внимание к этим больным), сказать сложно. Общий результат впечатляет. Дальнейшее изучение этого вопроса имеет большое клиническое значение. – Вернуться в оглавление раздела “Кардиология.” Оглавление темы “Лечение инфаркта миокарда”: |
Источник
Инсулин – это гормон, который регулирует углеводный обмен в организме человека и вырабатывается клетками Лангерганса поджелудочной железы. С его помощью ткани усваивают глюкозу, вещество, служащее источником энергии в организме. При сахарном диабете I типа (инсулинозависимом) собственный инсулин поджелудочной железой не вырабатывается, поэтому жизненно важно вводить его извне. Препараты инсулина содержат синтезированный гормон. Их регулярные инъекции – основа поддерживающей терапии сахарного диабета I типа.
 Источник: depositphotos.com
Источник: depositphotos.com
Инсулин обладает и анаболическим действием, поэтому его используют и в терапии некоторых других заболеваний, также он применяется бодибилдерами для увеличения мышечной массы.
Какое количество инсулина необходимо для передозировки?
Для здорового (т. е. не страдающего диабетом) взрослого человека безопасной дозой инсулина является 2–4 ЕД.
Нередко бодибилдеры, начиная с безопасной, постепенно увеличивают дозу, доводя ее до 20 ЕД.
При сахарном диабете доза инсулина подбирается эндокринологом индивидуально, с учетом концентрации глюкозы в сыворотке крови и наличия сахара в моче. Средняя терапевтическая доза при сахарном диабете находится в диапазоне 20–40 ЕД, в тяжелых случаях или при развитии осложнений (гипергликемическая кома) она может быть увеличена, и значительно.
Основными причинами передозировки инсулина являются:
- неправильно подобранная доза инсулинсодержащего препарата;
- ошибки при проведении инъекции, которые чаще всего наблюдаются при смене препарата или использовании нового типа шприцов;
- внутримышечное (вместо подкожного) введение;
- пропуск приема пищи после инъекции;
- значительные физические нагрузки при недостаточном поступлении углеводов после инъекции.
Некоторые состояния повышают чувствительность организма к действию инсулина. К ним относятся:
- жировая дистрофия печени;
- хроническая почечная недостаточность;
- первый триместр беременности;
- состояние алкогольного опьянения (в т. ч. и легкой степени).
В этих случаях даже введение привычной дозы лекарственного препарата, подобранной врачом, может стать причиной развития симптомов передозировки инсулином.
Признаки передозировки
При передозировке инсулина в крови резко снижается содержание глюкозы. Если этот показатель опускается ниже 3,3 ммоль/л, говорят о развитии гипогликемии.
Если передозировка возникла при применении инсулина короткого действия, ее признаки начинают проявляться уже через несколько минут после инъекции. Если использовался препарат инсулина длительного действия (депо-инсулин), то симптомы гипогликемии появляются позже и нарастают медленнее.
Заподозрить передозировку инсулина можно при наличии следующих симптомов, возникающих спустя некоторое время после инъекции:
- нарастающая общая слабость;
- тахикардия;
- головная боль;
- сильное чувство голода.
Если в этот момент не предпринять необходимых мер, состояние больного начнет быстро ухудшаться, присоединятся и другие симптомы:
- сильная потливость;
- тремор;
- онемение пальцев рук;
- бледность кожных покровов;
- гиперсаливация;
- расширение зрачков;
- нестерпимый голод;
- преходящие нарушения зрительной функции;
- нарушение способности к самостоятельному передвижению;
- нервное возбуждение или, наоборот, заторможенность;
- затуманивание сознания;
- клонико-тонические судороги.
 Источник: depositphotos.com
Источник: depositphotos.com
Самое тяжелое проявление передозировки инсулином – развитие гипогликемической комы, несущей угрозу жизни.
Передозировка инсулином может быть не только острой, но и хронической. Развитие последней связано с проведением длительной гормонозаместительной терапии сахарного диабета. После введения инсулина, даже в правильно подобранной дозировке, у больного на некоторое время снижается уровень глюкозы в крови. Организм стремится компенсировать это увеличением синтеза глюкагона, кортикостероидов и адреналина – гормонов, повышающих концентрацию глюкозы.
Признаки формирования хронической передозировки инсулином:
- постоянно повышенный аппетит;
- повышение массы тела;
- появление в моче ацетона;
- наличие в моче сахара;
- частые случаи развития кетоацидоза;
- резкие скачки уровня глюкозы в крови в течение суток;
- гипогликемия, периодически возникающая в течение дня;
- переход сахарного диабета в тяжелую форму.
Нарушения углеводного обмена, связанные с хронической передозировкой инсулина, приводят к тому, что в утренние часы у пациентов с сахарным диабетом I типа возникает гипергликемия, а в дневные часы уровень глюкозы в крови снижается и развивается гипогликемия.
Первая помощь при передозировке инсулином
При передозировке инсулином, особенно короткого действия, первая помощь должна быть оказана незамедлительно. Она предельно проста: больному следует выпить сладкий чай, съесть конфету, ложку варенья или кусочек сахара. Если его состояние не улучшается в течение 3-5 минут, прием пищи, содержащей быстрые углеводы, следует повторить.
Антидот
Поскольку при передозировке инсулином происходит резкое снижение концентрации глюкозы в крови, в качестве антидота используют гипертонические (20–40%) растворы глюкозы.
Когда необходима медицинская помощь?
Если при передозировке инсулином оказание первой помощи привело к быстрому улучшению состояния, необходимости в экстренной медицинской помощи нет. Однако больному в ближайшее время следует обязательно посетить лечащего врача для коррекции дозы и кратности введения инсулина.
В тех случаях, когда передозировка инсулином протекает тяжело и прием углеводной пищи не выводит пациента из состояния гипогликемии, необходимо срочно вызвать бригаду скорой помощи.
Лечение пациентов с передозировкой инсулином проводится в отделении эндокринологии. При развитии гипогликемической комы – в отделении реанимации и интенсивной терапии.
В стационаре больным в срочном порядке определяют уровень глюкозы в крови и некоторые другие биохимические показатели. Терапию начинают с внутривенного введения 20–40% растворов глюкозы. При необходимости внутримышечно вводят глюкагон.
При развитии комы проводится коррекция нарушенных функций жизненно важных органов.
Возможные осложнения
Незначительная передозировка инсулином не представляет опасности для жизни и здоровья, легкие степени гипогликемии изредка случаются практически у всех больных сахарным диабетом I типа. Однако если гипогликемия возникает регулярно, то следует заподозрить формирование хронической передозировки инсулином, способной утяжелить течение основного заболевания.
Тяжелая передозировка инсулином может привести к развитию выраженных неврологических нарушений:
- менингеальные симптомы;
- отек головного мозга;
- деменция (нарушение умственной деятельности с формированием слабоумия).
Гипогликемия особенно опасна для людей пожилого возраста, а также тех, кто страдает заболеваниями сердечно-сосудистой системы. У пациентов этих категорий она может осложниться инсультом, инфарктом миокарда, кровоизлиянием в сетчатую оболочку глаза.
Видео с YouTube по теме статьи:
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
Источник
Хорошо известно, что гипергликемия на момент поступления больного с инфарктом миокарда (ИМ) увеличивает риск госпитальной смерти независимо от наличия или отсутствия СД, но недавние исследования показали, что гипергликемия также повышает риск смерти во время искусственного кровообращения и что кривая риска неблагоприятных событий зависит от концентрации глюкозы в крови и имеет U-образную форму, т.е. риск увеличивается и при гипогликемии.
Базовый уровень глюкозы в плазме крови и краткосрочные изменения концентрации глюкозы в плазме также исследовали в качестве предикторов поздней смертности. При анализе данных 1469 пациентов с ОИМ было обнаружено, что у больных без СД повышенный уровень глюкозы крови и отсутствие снижения уровня глюкозы после 24 час были значимыми предикторами 30- и 180-суточной летальности.
После инфаркта миокарда (ИМ) уровень глюкозы в крови может увеличиваться пропорционально размеру инфаркта миокарда (ИМ) и выраженности гемодинамических нарушений даже у больных без СД в результате выброса катехоламинов, глюкагона, кортизола и соматотропина. Эти гормоны могут создавать временную ИР с нормализацией уровня глюкозы к моменту выписки из больницы. В некоторых случаях очень высокий уровень глюкозы при поступлении по отношению к размеру ИМ указывает на не диагностированный ранее СД.
Риск событий также повышается у пациентов с предиабетическими состояниями. В исследовании Whitehall Study 17 869 гражданских служащих мужского пола наблюдали в течение 33 лет. Исходы были сопоставлены с начальными показателями уровня глюкозы в крови, измеренными через 2 час после нагрузки глюкозой per os. OP смертности от ИБС увеличивался линейно по мере повышения показателей указанного теста с нагрузкой глюкозой выше 83 мг/дл. В диапазоне от 83 до 200 мг/дл ОР для ИБС с поправкой на возраст составил 3,62 (95% ДИ 2,3-5,6).
«Агрессивный» контроль уровня глюкозы в плазме крови при лечении ишемии миокарда у больных СД может существенно улучшить исходы. В исследовании DIGAMI (Diabetes and Insulin-Glucose Infusion in Acute Myocardial Infarction) 620 пациентов с СД и ОИМ были рандомизированы в группу интенсивной инсулинотерапии (инфузия инсулина с глюкозой в течение 24 час с дальнейшими п/к инъекциями инсулина в течение по крайней мере 3 мес) и группу стандартной стратегии гликемического контроля.
Больные, получавшие интенсивную инсулинотерапию, имели более низкий уровень глюкозы в крови в течение первого часа (9,6 ммоль/л vs 11,7 ммоль/л, р < 0,01) и при выписке (8,2 ммоль/л vs 9,0 ммоль/л, р < 0,01), чем в контрольной группе. В течение первого года наблюдалось значительное снижение смертности в группе интенсивной инсулинотерапии по сравнению с группой обычной терапии (19% vs 26%, р < 0,027).
В группе интенсивной терапии смертность оставалась ниже, чем в группе обычной терапии в течение 3,4 года (33% vs 44%, р < 0,011). Предикторами смертности были возраст, ХСН в анамнезе, продолжительность СД, уровень глюкозы и HbA1c при поступлении. В подгруппе пациентов, у которых до развития ИМ проводили терапию СД с помощью диеты или гипогликемических средств per os, наблюдали наибольшее увеличение выживаемости.
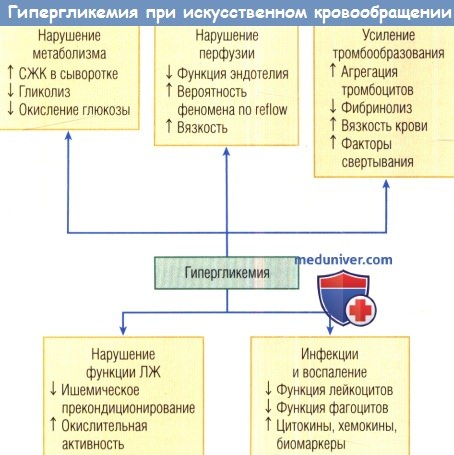
Схематическое представление факторов, которые способствуют повышению риска смерти во время искусственного кровообращения у пациентов с гипергликемией.
ЛЖ — левый желудочек; СЖК — свободные жирные кислоты.
Исследование DIGAMI-2 (продолжение исследования DIGAM1) было проспективным рандомизированным открытым исследованием, в котором сравнивали исходы ОИМ у пациентов с СД-1 и СД-2 после трех видов контроля гликемии в постинфарктном периоде: группа 1 получала инфузию инсулина с глюкозой в острый период с последующим длительным контролем уровня глюкозы (n = 474), группа 2 получала инфузию инсулина и глюкозы с последующим обычным контролем гликемии (n = 473), группа 3 получала обычную терапию (n = 306). Всех пациентов наблюдали в среднем 2,1 года. ОС (первичная конечная точка) не отличалась между группами 1 и 2 и группами 2 и 3.
Не было существенных различий между тремя группами и по повторным нефатальным инфарктом миокарда (ИМ) и мозгового инсульта (МИ). Отсутствие эффекта долгосрочной инсулинотерапии на результаты исследования может быть частично объяснено тем, что 14% пациентов в группе обычного лечения получали инфузию инсулина и глюкозы и нарушение протокола, к тому же 41% назначали дополнительные инъекции глюкозы, В результате уровень глюкозы в крови во всех группах во время лечения существенно не различался.
Значение интенсивного метаболического контроля для улучшения исходов было рассмотрено в двух исследованиях. В исследовании по сравнению периоперационных исходов у пациентов с СД, перенесших КШ, которые получали непрерывную инфузию инсулина или периодические инъекции инсулина п/к, инфузия инсулина значительно уменьшала смертность по сравнению с п/к его введением (2,5% vs 5,3%, р < 0,0001).
Несмотря на отсутствие в исследовании группы плацебо, смертность в группе инфузии инсулина была значительно меньше, чем прогнозировала модель по оценке риска Society of Thoracic Surgeons. В рандомизированном исследовании в отделении интенсивной терапии 1200 пациентов (16,9% больных СД) получали инфузию инсулина для поддержания уровня глюкозы в крови в пределах 80-110 мг/дл или инъекции инсулина, когда глюкоза в плазме крови превышала 215 мг/дл.
Интенсивный контроль гликемии путем инфузии инсулина не снижает смертность, но значительно уменьшает частоту осложнений, предотвращая повреждение почек, уменьшая период механической вентиляции, а также ускоряет выписку из отделения интенсивной терапии.
Инфузию ГИК-смеси, которую начали использовать в 1960-1970-х гг. в качестве поляризующего раствора для поддержания электрической стабильности, вновь стали применять как способ положительного влияния на метаболизм миокарда при лечении ИМ, реваскуляризации КА и КШ. Метаанализ 9 исследований (n = 1932), проводившихся в период 1965-1987 гг., показал, что инфузия ГИК-смеси снижает внутрибольничную смертность с 21 до 16,1%. Однако только 2 из этих исследований были двойными слепыми и никакой информации о больных СД не содержали.
В проспективном рандомизированном открытом исследовании инфузии ГИК-смеси у 940 пациентов, подвергшихся ЧТКА при ОИМ, снижения смертности в группе ГИК-смеси по сравнению с группой плацебо не наблюдалось. В подгруппе СД был отмечен выраженный эффект ГИК-смеси (инфузия снизила смертность с 12,2 до 4%), но из-за небольшого размера подгруппы и небольшого количества летальных исходов этот результат не достиг статистической значимости.
У больных СД, которым выполняли плановое коронарное шунтирование (КШ), инфузия ГИК-смеси благотворно влияла на метаболизм, о чем свидетельствовало устранение миокардиальной экстракции неэстерифицированных ЖК и увеличение потребления миокардом лактата и глюкозы. Также было проведено сравнение исходов КШ у больных СД (n = 141), проспективно рандомизированных в группу введения ГИК-смеси для «агрессивного» контроля гликемии во время операции или в группу, получавшую стандартную терапию (периодические инъекции инсулина).
Пациенты из группы ГИК-смеси имели более низкие уровни глюкозы крови в ближайшем послеоперационном периоде (138 мг/дл vs 260 мг/дл, р < 0,0001), снижение частоты развития фибрилляции предсердий (ФП) (16,6% vs 42%, р = 0,0017) и более короткое послеоперационное пребывание в стационаре (6,5 сут vs 9,2 сут, р = 0,003). Хотя по показателям 30-суточной летальности различий между группами не было, у пациентов, получавших ГИК-смесь, наблюдали значительное улучшение выживаемости в течение 2 лет после операции. Для оценки долгосрочных эффектов инфузии ГИК-смеси у больных СД, получавших терапию по поводу ИМ или ОКС, необходимы новые проспективные исследования.
Для объяснения благоприятных эффектов инфузии ГИК-смеси при лечении ИМ и ОКС был предложен ряд механизмов. Способность ГИК-смеси ослаблять рост концентрации СЖК, наблюдаемый во время ИМ, объясняется переключением окислительного метаболизма миокарда с СЖК на окисление глюкозы — более эффективный метаболический процесс, т.е. производящий больше АТФ на моль О2. Чистым эффектом этих метаболических изменений является ослабление повреждения клеток при ишемии и реперфузии и улучшение функции после ишемии. Справедливость этого заключения в последнее время подвергается сомнению на основании результатов исследований на животных, показавших, что защита от ишемического повреждения миокарда, связанного с повышением уровня глюкозы и инсулина в крови, не связана с изменениями эффективности работы сердца или соотношением окисления глюкозы и гликолиза.
Благоприятный эффект ГИК-смеси в условиях ИМ также может быть результатом прямых эффектов инсулина. Введение как ГИК-смеси, так и одного инсулина оказывает противовоспалительный и профибринолитический эффекты при ИМ, что может служить протективным фактором. Кроме того, инсулин может ограничить повреждение миокарда путем подавления апоптоза, что способствует выживаемости клеток в условиях реперфузии.
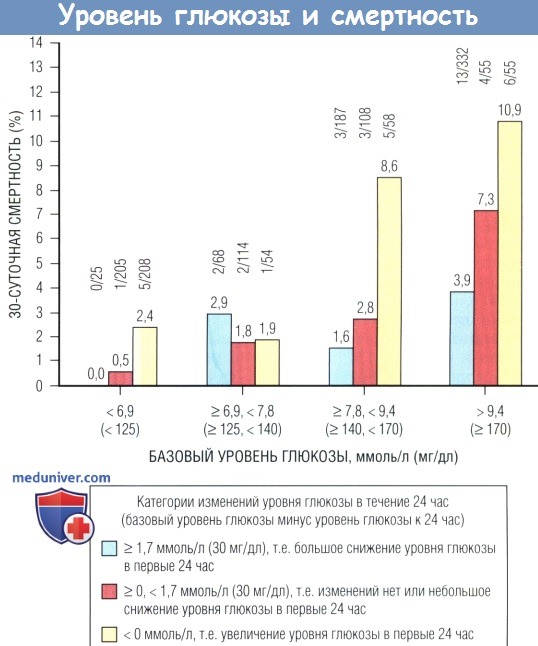
Уровень глюкозы в крови является существенным предиктором смертности у пациентов без сахарного диабета.
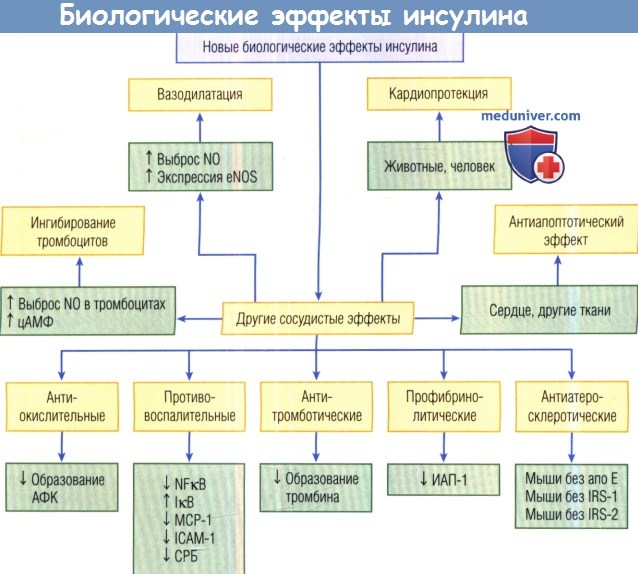
Новый взгляд на биологические эффекты инсулина.
СРБ — С-реактивный белок; eNOS — эндотелиальная синтаза оксида азота; IкВ — ингибитор NFkB;
ICAM-1 — молекула межклеточной адгезии 1; IRS — субстрат рецептора инсулина;
МСР-1 — моноритарный хемоаттрактантный белок 1; NFkB — нуклеарный фактор каппа В;
NO — оксид азота; апо — аполипопротеин; АФК — активные формы кислорода;
ИАП-1 — ингибитор активатора плазминогена 1; цАМФ — циклический аденозинмонофосфат.
– Читать “Влияние сахарного диабета на прогноз хронической сердечной недостаточности (ХСН)”
Оглавление темы “Влияние сахарного диабета на сердце.”:
- Влияние сахарного диабета на прогноз острого коронарного синдрома (ОКС)
- Антитромбоцитарные препараты при сахарном диабете и ОКС
- Абциксимаб, эптифибатид при сахарном диабете и ОКС
- Пиявка (бивалирудин) при сахарном диабете и ОКС
- β-адреноблокаторы при сахарном диабете и ОКС
- Ингибиторы ангиотензинпревращающего фермента (иАПФ) при сахарном диабете и ОКС
- Инсулин при сахарном диабете и инфаркте миокарда
- Влияние сахарного диабета на прогноз хронической сердечной недостаточности (ХСН)
- Причины и механизмы развития диабетической кардиомиопатии
- Влияние сахарного диабета на развитие ХСН
Источник