Инфаркт миокарда осложненный тромбозом
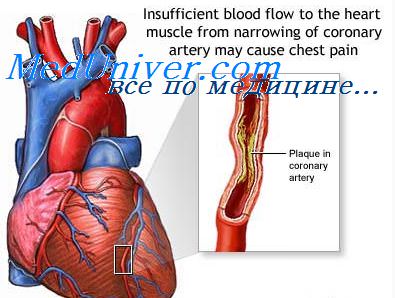
Тромбоэмболические осложнения инфаркта миокарда. Тромбоэмболии при инфаркте миокарда.
Тромбоэмболические осложнения (системные тромбоэмболии) встречаются редко (у 4% больных, чаще с обширным передним ИМ, отягощенным СН), тогда как образование пристеночного тромба в ЛЖ отмечается у 20-50%. На вскрытии у половины больных ИМ находят тромбоэмболии. Следовательно, они часто протекают бессимптомно, обусловливают 15% летальности в первые 7 дней ИМ. Обычно тромбозы возникает в первую неделю ИМ, а большая часть тромбоэмболии — в течение первых 2—3 месяцев. Зона ИМ прямо связана с риском тромбоэмболии.
ФР тромбоэмболии: гиперкоагуляция, наличие пристеночного тромба в зоне ИМ или тромба в ушке левого предсердия, тромбофлебиты ног, длительный постельный режим.
Тромбоэмболические осложнения при ИМ можно разделить на четыре вида:
• периферический венозный тромбоз и ТЭЛА;
• пристеночные (муральные) тромбы в зоне субэндокардиального ИМ (обычно их можно выявить в первые 10 дней, даже уже через 36 ч; возникают у 20—40% больных с передним ИМ и, как правило, хорошо видны на ЭхоКГ) или аневризмы с последующей потенциальной опасностью системной артериальной эмболизации;
• прогрессирование тромбоза коронарных артерий и ИМ (его распространение) или тромбоза сосудов конечностей;
• повторная закупорка коронарной артерии после успешного тромболизиса.

При ИМ эмболии возникают чаще в системе легочной артерии на фоне имеющихся тромбофлебитов ног (с последующими венозными эмболиями) вследствие длительного постельного режима и фоновой ФП. Так, тромбоз глубоких вен голеней отмечается у трети больных ИМ и гораздо чаще у лиц старше 70 лет с наличием ХСН, варикоза ног и гиперкоагуляции. Реже могут возникать ТЭЛА при ИМ ПЖ. Небольшие ТЭЛА отмечаются у 20% больных ИМ на секции. Массивные ТЭЛА ответственны в 10% случаев за летальность при ИМ. Обычно ТЭЛА мелких ветвей в клинике не диагностируется. Иногда на ЭКГ появляются признаки ОЛС, а на рентгенограмме легких — разнообразная инфильтрация и повышение купола диафрагмы на стороне поражения.
Несколько реже (в 5—10% случаев) эмболии из пристеночных тромбов ЛЖ (особенно при переднем ИМ) возникают в системе кровообращения большого круга (по убывающей частоте): почечные артерии -> артерии селезенки -» артерии мозга -> артерии нижних конечностей. Эти тромбоэмболические осложнения обычно возникают в первые 10 дней ИМ, их трудно распознать.
Симптоматика зависит от места тромбоэмболии (тромбоза). Так, при эмболии в сосуды почек появляется триада: сильные, но не иррадиирующие боли в животе или пояснице (несколько часов), повышение АД, мочевой синдром (микрогематурия, лейкоцитурия и белок; могут быть и олигурия, азотемия). Вскоре вслед за болями в пояснице может появиться лихорадка. При тромбоэмболии в мезентериальные сосуды возникают признаки «острого живота»: сильная, разлитая боль неопределенной локализации, резкое вздутие живота, кровавый понос и парез кишечника (симптомы перитонита). Позднее развивается клиническая картина кишечной непроходимости и симптоматика нарастающей интоксикации.
Проявления поражения артерий мозга могут быть различные: от легких неврологических до отека мозга с нарушением сознания и рвотой. При эмболии артерий нижних конечностей возникают: нарастающая сильная боль в ноге, мраморность кожи, похолодание ног, снижение их чувствительности, исчезновение пульса на бедренной артерии. Если кровообращение не восстанавливается, то на коже появляются пузыри, очаги некроза. Позднее развивается гангрена конечности.
Лечение тромбоэмболии. Лечение эмболии сводится к немедленному назначению внутривенно струйно гепарина — 5000—10 000 ЕД, затем внутривенно капельно, постоянно с начальной скоростью 1000 ЕД/ч (до 30 000 ЕД/сут) под контролем АЧТВ, которое должно повыситься в 2 раза по сравнению с исходным уровнем (до 50—65 с). Показания к полной дозе антикоагулянтов при ИМ: наличие ТЭЛА или системных эмболии в анамнезе; активный венозный тромбоз; большие размеры сердца; наличие пристеночных тромбов; ХСН; ФП; ожирение; выраженный варикоз ног. После 5—10 дней внутривенного введения гепарина назначают орально варфарин в течение 3-6 месяцев (больным с видимыми муральными тромбами, особенно если они мобильные, или тем, у кого уже были эпизоды эмболии).
Для профилактики артериальных тромбоэмболии всем больным ИМ назначают аспирин (тиклопидин).
– Также рекомендуем “Венозный тромбоз и ТЭЛА при инфаркте миокарда. Тромбоэндокардит.”
Оглавление темы “Разрыв миокарда. Аневризмы сердца. Постинфарктные тромбоэмболии и перикардиты.”:
1. Лечение разрыва сердца. Разрыв межжелудочковой перегородки.
2. Диагностика разрыва межжелудочковой перегородки. Лечение разрыва межжелудочковой перегородки.
3. Разрывы сосочковых мышц. Диагностика и лечение разрыва сосочковых мышц.
4. Острая дисфункция сосочковых мышц. Митральная регургитация при инфаркте миокарда.
5. Острая аневризма левого желудочка. Клиника аневризмы при инфаркте миокарда.
6. Диагностика аневризмы левого желудочка. Лечение аневризмы левого желудочка.
7. Тромбоэмболические осложнения инфаркта миокарда. Тромбоэмболии при инфаркте миокарда.
8. Венозный тромбоз и ТЭЛА при инфаркте миокарда. Тромбоэндокардит.
9. Перикардит при инфаркте миокарда. Синдром Дресслера.
10. Постинфарктный синдром Дресслера. Диагностика и лечение постинфарктного синдрома Дресслера.
Источник
В возникновении тромбоэмболии при ИМ важную роль играют такие общие факторы, как депрессия противосвертывающей системы организма, повышение содержания коагулянтов в крови, нарушение кровообращения в органах и тканях при недостаточности кровообращения. Большое значение имеют также местные атеросклеротические изменения’ в артериях.
До применения антикоагулянтов и тромболизирующих препаратов тромбоэмболические осложнения наблюдались в 13—30% случаев ИМ [Раевская Г. А., 1960; Wright et al., 1954]. При использовании этих препаратов частота тромбоэмболии снизилась до 5,6% [Лукомский П. Е., Казьмина П. В., 1961] и даже до 2% [Чазов Е. И., 1966], уменьшилась их тяжесть.
Чаще всего наблюдаются тромбоэмболии легочной артерии и ее ветвей. В происхождении их большую роль играют тромбофлебиты ног, малого таза, повышение свертывания крови, а также пристеночный тромбоэндокардит при поражении перегородки и тромбозы правого желудочка и предсердия, образующиеся иногда при недостаточности кровообращения и расширении правых полостей сердца. Замедление кровотока в системе легочной артерии при наличии левожелудочковой недостаточности также может способствовать развитию тромбоза этой области.
Диагностика этого осложнения представляет большие трудности, так как многие признаки тромбоэмболии легочной артерии могут быть объяснены основным заболеванием, особенно если она развивается в первые часы и дни ИМ. Клиническая картина во многом зависит от величины пораженного сосуда. При тромбоэмболии основного ствола легочной артерии наступает мгновенная смерть. Тромбоэмболии мелких ветвей легочной артерии часто остаются нераспознанными, а внезапное ухудшение состояния больного объясняется основным процессом. Для тромбоэмболии крупной ветзи легочной артерии характерно внезапное развитие острой сердечной недостаточности, проявляющейся выраженной одышкой, тахикардией, акроцианозом. В ряде случаев развивается отек легких. Довольно часто наблюдаются нарушения ритма сердца типа мерцательной аритмии, пароксизмальной тахикардии, связанные с острой перегрузкой правых отделов сердца. Примерно в 35—40% случаев появляются боли в груди, усиливающиеся при глубоком вдохе и обусловленные сопутствующим плевритом. Тромбоэмболия обычно приводит к развитию инфаркта легких, одним из частых симптомов которого является кровохарканье. Как правило, к этому присоединяется воспалительный процесс — так называемая инфарктная пневмония, для которой характерны все физикальные и лабораторные симптомы пневмонии.
При тромбоэмболии относительно крупной ветви легочной артерии на ЭКГ могут появиться изменения, характерные для острого легочного сердца: глубокий зубец S в I отведении, зубец Q в III (тип 5i — Qui) и отрицательный зубец Т в III, aVF, Vi_4 отведениях, высокий зубец Р во II и III отведениях (Р pulmonale), смещение сегмента S — Т книзу от изоэлектрической линии в I и II и кверху в III, aVF, Vi_2 отведениях. Эта электрокардиографическая картина напоминает ЭКГ при диафрагмальном инфаркте. Отличием являются высокие зубцы R в III и правых грудных отведениях при остром легочном сердце, тогда как при диафрагмальном инфаркте зубец R в III отведении снижен. В некоторых случаях острого легочного сердца наблюдаются глубокие зубцы S во всех грудных отведениях. Иногда развивается блокада правой ножки предсердно-желудочкового пучка. При тромбоэмболии мелких ветвей легочной артерии изменения на ЭКГ могут отсутствовать. В этих случаях большое диагностическое значение имеет определение активности ферментов в сыворотке крови. В первую очередь характерно резкое повышение активности «легочного» изофермента — ЛДГ3.
Определенную помощь в диагностике может оказать рентгенологическое исследование. При массивной тромбоэмболии на рентгенограммах можно выявить увеличение правого желудочка сердца, выбухание конуса и дуги легочной артерии, повышение прозрачности легочной ткани в зоне разветвления затромбированной артерии, симптом «ампутации» корня с расширением его проксимальнее тромбоза. При развитии инфаркта легких и инфарктной пневмонии рентгенологически определяется характерный участок затемнения легочной ткани в виде треугольника, обращенного основанием к плевре. В случае тромбоэмболии мелких ветвей легочной артерии при рентгенологическом исследовании можно не выявить патологических изменений.
С целью уточнения диагноза и определения локализации тромбоза в ряде случаев прибегают к ангиографическому исследованию.
Тромбоэмболия нижнего отдела брюшной аорты (в области ее бифуркации) приводит к острому симметричному нарушению кровообращения в ногах (синдром Лериша), которое чаще наблюдается у пожилых людей с выраженным атеросклерозом брюшной аорты. Клиническая картина характеризуется острым началом с появлением сильных болей в нижнем отделе живота, отдающих в крестец, промежность и ноги. К болям в ногах присоединяется чувство их онемения.
Отмечается мраморность кожи ног, их бледность с цианотичным оттенком, похолодание, исчезновение пульса на бедренных артериях, снижение (или исчезновение) кожной чувствительности. Нередко возникают парестезии и парезы нижних конечностей [Чазов Е. И., 1966]. Если под влиянием лечебных мероприятий кровообращение не восстанавливается, то трофические нарушения прогрессируют вплоть до развития гангрены ног. При нарастании тромбоза появляются признаки расстройства кровообращения в органах брюшной полости и таза. Как правило, наблюдаются повышение температуры, высокий лейкоцитоз, увеличение СОЭ, симптомы интоксикации организма. Тромбоэмболия бифуркации аорты всегда протекает тяжело и обычно сопровождается развитием шока. Прогноз при этом осложнении очень серьезный, особенно если своевременно не проводится лечение.
При тромбоэмболии артерий нижних конечностей клиническая картина зависит от быстроты развития закупорки и степени развития коллатералей. Характерно острое начало заболевания: появление сильнейших болей в ноге, бледности кожных покровов с цианотичными пятнами, похолодание конечности, исчезновение пульса на артерии. В дальнейшем, если кровообращение не восстанавливается, развивается гангрена. Примерно в половине случаев возникновение тромбоэмболии артерий нижних конечностей сопровождается острой сердечно-сосудистой недостаточностью. Уже к концу 1-х суток отмечаются повышение температуры тела, лейкоцитоз со сдвигом лейкоцитарной формулы влево, увеличение СОЭ.
Для тромбоэмболии почечных артерий характерна триада признаков: боль, мочевой синдром, артериальная гипертония. Боли возникают в поясничной области, в соответствующей половине живота и продолжаются от нескольких часов до 1—2 сут. Часто они сопровождаются тошнотой, рвотой. В отличие от приступов почечной колики они не иррадиируют в паховую область и половые органы. В ряде, случаев бывает положительным симптом Пастернацкого. Нередко наблюдается макрогематурия или же в моче отмечается умеренное количество эритроцитов и белок, что связано в основном с повышением проницаемости стенок мелких сосудов. Часто имеет место олигурия.
Вслед за болевым синдромом повышается температура, появляется нейтрофильный лейкоцитоз, увеличивается СОЭ.
Артериальная гипертония, связанная с острой ишемией почки, является важным, но не постоянным симптомом тромбоэмболии почечных артерий. Повышение АД наблюдается не только во время болевого приступа, оно может сохраняться и в дальнейшем, а в ряде случаев прогрессировать. Диагноз тромбоэмболии почечной артерии подтверждается в дальнейшем при расширении режима с помощью урологических, рентгенологических и радиологических методов исследования.
При тромбоэмболии мелких ветвей почечной артерии развивается инфаркт почки, который в отдельных случаях также может обусловить развитие реноваскулярной гипертонии. Как правило, имеет, место макро- или микрогематурия. Закупорка мелких ветвей почечной артерии обычно не проявляется описанной выше характерной клинической картиной, часто протекает под видом неясных и неинтенсивных болей в поясничной области или в животе и в ряде случаев не диагностируется.
Клиническая картина тромбоэмболии мезентериальных артерий представляет собою острую катастрофу в брюшной полости. Отличительная особенность болей в животе в этих случаях — неопределенность их локализации. Одновременно с появлением болей развивается картина острого живота (парез кишечника и т. п.). Часто наблюдается дегтеобразный стул. У ряда больных тромбоэмболия мезентериальных артерий сопровождается тяжелым коллапсом.
При тромбоэмболии мозговых сосудов клиническая картина зависит как от степени выраженности общемозговых симптомов, связанных с отеком мозга (нарушение сознания, тошнота, рвота),так и от локализации и величины очага поражения. При этом нарушения обычно протекают более тяжело и сохраняются дольше, чем при динамическом расстройстве мозгового кровообращения. В то же время мелкие эмболии в отдельные области, например лобные, могут протекать малосимптомно. Желательно, чтобы вопросы диагностики, дифференциальной диагностики тромбоэмболии мозговых артерий, кровоизлияния в мозг и
динамического нарушения мозгового кровообращения, а также вопросы лечения решались совместно терапевтом и невропатологом.
Тромбоэмболия артерии селезенки встречается редко. При этом осложнении отмечаются боли в левом подреберье, болезненность этой области при пальпации, симптомы раздражения брюшины. Может выслушиваться шум трения брюшины. Обычно наблюдаются температурная реакция и изменения периферической крови. При тромбоэмболии мелких ветвей селезеночной артерии инфаркт селезенки нередко не диагностируется и проходит незамеченным.
Источник
Содержание:
Инфаркт миокарда (ИМ) – самая серьезная клиническая форма ишемии сердца. Это острое, угрожающее жизни, состояние, обусловленное относительным либо абсолютным недостатком кровоснабжения определенной части миокарда вследствие тромбоза коронарной артерии, в результате чего формируется очаг некроза, т.е. область с отмершими клетками – кардиомиоцитами.
Инфаркт сердца – одна из ведущих причин смертности населения планеты. Его развитие напрямую зависит от возраста и пола человека. В связи с более поздним появлением атеросклероза у женщин инфаркты диагностируются у них в 3–5 раз реже, чем у мужчин. В группу риска попадают все представители мужского пола, начиная с 40-летнего возраста. У людей обоих полов, перешедших рубеж 55–65 лет, заболеваемость примерно одинакова. По статистике 30–35% всех случаев острого инфаркта сердечной мышцы заканчиваются летальным исходом. До 20% внезапных смертей вызваны этой патологией.
Причины инфаркта
Главные причины развития ИМ:
- Атеросклероз сосудов сердца, в частности коронарных артерий. В 97% случаев атеросклеротическое поражение стенок сосудов приводит к развитию ишемии миокарда с критическим сужением просвета артерий и длительным нарушением кровоснабжения миокарда.
- Тромбоз сосудов, к примеру, при коронарите различного генеза.Полное прекращение кровоснабжениямышцы происходит вследствиеобтурации (закупорки) артерий или мелких сосудов атеросклеротической бляшкой или тромбом.
- Эмболия венечных артерий, например, при септическом эндокардите, реже заканчивается образованием некротического очага, тем не менее являясь одной из причин формирования острой ишемии миокарда.
Нередко встречается сочетание вышеперечисленных факторов: тромб закупоривает спастически суженный просвет артерии, пораженной атеросклерозом или формируется в области атеросклеротической бляшки, выпяченной из-за произошедшего кровоизлияния в ее основание.
- Пороки сердца. Коронарные артерии могут отходит от аорты вследствие формирования органического поражения сердца.
- Хирургическая обтурация. Механическое вскрытие артерии или ее перевязка во время проведения ангиопластики.
Факторы риска инфаркта миокарда:
- Пол (у мужчин чаще).
- Возраст (после 40–65 лет).
- Стенокардия.
- Порок сердца.
- Ожирение.
- Сильный стресс или физическое перенапряжение при имеющейся ИБС и атеросклерозе.
- Сахарный диабет.
- Дислипопротеинемия, чаще гиперлипопротеинемия.
- Курение и прием алкоголя.
- Гиподинамия.
- Артериальная гипертония.
- Ревмокардит, эндокардит или другие воспалительные поражения сердца.
- Аномалии развития коронарных сосудов.
Механизм развития инфаркта миокарда
Течение болезни делится на 5 периодов:
- Прединфарктный (стенокардия).
- Острейший (острая ишемия сосудов сердца).
- Острый (некробиоз с формированием некротической области).
- Подострый (стадия организации).
- Постинфарктный (образование рубца в месте некроза).
Последовательность патогенетических изменений:
- Нарушение целостности атеросклеротического отложения.
- Тромбоз сосуда.
- Рефлекторный спазм поврежденного сосуда.
При атеросклерозе избыточный холестерин откладывается на стенках сосудов сердца, на которых образуются липидные бляшки. Они сужают просвет пораженного сосуда, замедляя кровоток по нему. Различные провоцирующие факторы, будь то гипертонический криз или эмоциональное перенапряжение, приводят к разрыву атеросклеротического отложения и повреждению сосудистой стенки. Нарушение целостности внутреннего слоя артерии активирует защитный механизм в виде свертывающей системы организма. К месту разрыва прилипают тромбоциты, из которых формируется тромб, закупоривающий просвет сосуда. Тромбоз сопровождается выработкой веществ, приводящих к спазмированию сосуда в области повреждения либо по всей его длине.
Клиническое значение имеет сужение артерии на 70% размера ее диаметра, при этом просвет спазмируется до такой степени, что кровоснабжение не может быть компенсировано. Это возникает вследствие атеросклеротических отложений на стенки сосудов и ангиоспазма. В результате нарушается гемодинамика области мышцы, получающей кровь через поврежденное сосудистое русло. При некробиозе страдают кардиомиоциты, недополучая кислород и питательные вещества. Нарушается метаболизм и функционирование сердечной мышцы, ее клетки начинают отмирать. Период некробиоза длится до 7 часов. При незамедлительно оказанной в этот промежуток времени медицинской помощи происходящие изменения в мышце могут быть обратимы.
При формировании некроза в пораженной области восстановить клетки и повернуть процесс вспять невозможно, повреждения приобретают необратимый характер. Страдает сократительная функция миокарда, т.к. некротизированная ткань не участвует в сокращении сердца. Чем обширнее область поражения, тем сильнее снижается сократимость миокарда.
Единичные кардиомиоциты или небольшие их группы гибнут спустя примерно 12 часов от начала острого заболевания. Через сутки микроскопически подтверждается массовое омертвление клеток сердца в зоне поражения. Замещение области некроза соединительной тканью начинается через 7–14 дней от начала инфаркта. Постинфарктный период продолжается 1,5–2 месяца, в течение которых окончательно формируется рубец.
Передняя стенка левого желудочка – наиболее частое место локализации некротической зоны, поэтому в большинстве случаев выявляется трансмуральный ИМ именно этой стенки. Реже поражается верхушечная область, задняя стенка или межжелудочковая перегородка. Инфаркты правого желудочка в кардиологической практике встречаются редко.
Классификация инфаркта миокарда
Относительно размера поражения ткани инфаркт миокарда бывает:
- Мелкоочаговый. Формируется один или несколько маленьких по размеру некротических участков. Диагностируется в 20% случаев от общего числа инфарктников. У 30% пациентов мелкоочаговый инфаркт трансформируется в крупноочаговый.
- Крупноочаговый (чаще трансмуральный). Образуется обширная область некроза.
По глубине некротического поражения различают:
- Трансмуральный. Некротическая область охватывает всю толщу миокарда.
- Субэпикардиальный. Участок с отмершими кардиомиоцитами прилегает к эпикарду.
- Субэндокардиальный. Некроз сердечной мышца в районе прилегания к эндокарду.
- Интрамуральный. Участок некроза находится в толще левого желудочка, но не доходит до эпикарда или эндокарда.
В зависимости от кратности возникновения:
- Первичный. Возникает первый раз.
- Повторный. Развивается через 2 месяца или позже после начала первичного.
- Рецидивирующий. Появляется на стадии формирования рубцовой ткани первичного инфаркта, т.е. в течение первых 2 мес. от первичного острого поражения миокарда.
Относительно локализации процесса:
- Левожелудочковый.
- Правожелудочковый.
- Септальный, или инфаркт межжелудочковой перегородки.
- Сочетанный, к примеру переднебоковой ИМ.
Отталкиваясь от электрокардиологических изменений, фиксируемых на кардиограмме:
- Q-инфаркт. Электрокардиограмма фиксирует сформировавшийся патологический з. Q или желудочковый комплекс QS. Изменения характерны для крупноочаговых ИМ.
- Не Q-инфаркт с инверсией з. Т и без патологии з. Q. Чаще встречается при мелкоочаговых инфарктах.
В зависимости от развития осложнений:
- Неосложненный.
- Осложненный.
Формы острого ИМ, относительно наличия и места расположения болей:
- Типичная. Боль сосредоточена в прекардиальной либо загрудинной области.
- Атипичная. Форма заболевания с атипичной локализацией болей:
Периоды заболевания:
- Острейший.
- Острый.
- Подострый.
- Постинфарктный.
Симптомы инфаркта миокарда
Интенсивность и характер болевых ощущений зависят от нескольких факторов: размера и локализации некротического очага, а также стадии и формы инфаркта. У каждого пациента клинические проявления различны в силу индивидуальных особенностей и состояния сосудистой системы.
Признаки типичной формы инфаркта миокарда
Яркая клиническая картина с типичным и выраженным болевым синдромом наблюдается при крупноочаговом (трансмуральном) инфаркте сердца. Течение болезни разделяю на определенные периоды:
- Прединфарктный, или продромальный период. У 43–45% инфарктников этот период отсутствует, т.к. болезнь начинается внезапно. Большинство пациентов перед инфарктом отмечают учащение приступов стенокардии, загрудинные боли становятся интенсивными и продолжительными. Изменяется общее состояние – снижается настроение, появляется разбитость и страх. Эффективность антиангинальных средств значительно снижается.
- Острейший период (от 30 мин до нескольких часов). При типичной форме острый инфаркт сопровождается нестерпимой загрудинной болью с иррадиацией в левую сторону туловища – руку, нижнюю челюсть, ключицу, предплечье, плечо, область между лопатками. Редко под лопатку или левое бедро. Боли могут быть жгучими, режущими, давящими. Некоторые ощущают распирание в груди или ломоту. В течение нескольких минут боль достигает своего максимума, после чего сохраняется до часа и дольше, то усиливаясь, то ослабевая.
- Острый период (до 2 суток, при рецидивирующем течении до 10 дней и дольше). У подавляющего большинства больных ангинозная боль проходит. Ее сохранение свидетельствует о присоединении эпистеноперикардиального перикардита либо о продолжительном течении ИМ. Нарушения проводимости и ритма сохраняются, также как и артериальная гипотензия.
- Подострый период (длительность – 1 мес). Общее состояние пациентов улучшается: температура нормализуется, проходит одышка. Полностью или частично восстанавливается сердечный ритм, проводимость, звучность тонов, но блокада сердца регрессу не поддается.
- Постинфарктный период – завершающий этап течения острого ИМ, длящийся до 6 месяцев. Некротическая ткань окончательно заменяется плотным рубцом. Сердечная недостаточность устраняется за счет компенсаторной гипертрофии сохранившегося миокарда, но при обширной площади поражения полная компенсация невозможна. В этом случае проявления сердечной недостаточности прогрессируют.
Начало боли сопровождается сильной слабостью, появлением обильного липкого (профузного) пота, чувством страха смерти, учащением сердцебиения. При физикальном обследовании выявляется бледность кожи, липкий пот, тахикардия и другие нарушения ритма (экстрасистолия, фибрилляция предсердий), возбуждение, одышка в покое. В первые минуты повышается артериальное давление, потом резко понижается, что свидетельствует о развивающейся недостаточности сердца и кардиогенном шоке.
При тяжелом течении развивается отек легких, иногда сердечная астма. Тоны сердца при аускультации приглушены. Появление ритма галопа говорит о левожелудочковой недостаточности, от степени выраженности которой зависит аускультативная картина легких. Жесткое дыхание, хрипы (влажные) подтверждают застой крови в легких.
Ангинозная боль в этом периоде нитратами не купируется.
В результате перифокального воспаления и некроза появляется лихорадка, сохраняющаяся на протяжении всего периода. Температура поднимается до 38,50 С, высота ее подъема зависит от размера некротического очага.
При мелкоочаговом инфаркте мышцы сердца симптоматика менее выражена, течение болезни не такое четкое. Редко развивается недостаточность сердца. Аритмия выражается в умеренной тахикардии, которая бывает не у всех больных.
Признаки атипичных форм инфаркта миокарда
Подобные формы характеризуются нетипичной локализацией болей, затрудняющей своевременную установку диагноза.
- Астматическая форма. Характерен кашель, приступы удушья, проливной холодный пот.
- Гастралгическая (абдоминальная) форма проявляется болями в эпигастральной области, рвотой, тошнотой.
- Отечная форма бывает при массивной очаге некроза, приводящем к тотальной сердечной недостаточности с отеками, одышкой.
- Церебральная форма характерна для пожилых пациентов с выраженным атеросклерозом не только сердечных, но и мозговых сосудов. Проявляется клиникой ишемии головного мозга с головокружениями, потерей сознания, шумом в ушах.
- Аритмическая форма. Единственным ее признаком может быть пароксизмальная тахикардия.
- Стертая форма отличается отсутствием жалоб.
- Периферическая форма. Боли могут быть только в руке, подвздошной ямке, нижней челюсти, под лопаткой. Иногда опоясывающая боль схожа с болями, возникающими при межреберной невралгии.
Осложнения и последствия инфаркта миокарда
- Тромбоз в желудочках.
- Острый эрозивный гастрит.
- Острый панкреатит либо колит.
- Парез кишечника.
- Желудочное кровотечение.
- Синдром Дресслера.
- Острая, а в дальнейшем хроническая прогрессирующая недостаточность сердца.
- Кардиогенный шок.
- Постинфарктный синдром.
- Эпистенокардиальный перикардит.
- Тромбоэмболии.
- Аневризма сердца.
- Отек легких.
- Разрыв сердца, приводящий к его тампонаде.
- Аритмии: пароксизмальная тахикардия, экстрасистолия, внутрижелудочковая блокада, фибрилляция желудочков и другие.
- Инфаркт легких.
- Пристеночный тромбоэндокардит.
- Психические и нервные расстройства.
Диагностика инфаркта миокарда
Анамнез болезни, электрокардиографические признаки (изменения на ЭКГ) и характерные сдвиги ферментативной активности в сыворотке крови являются основным критериями при диагностике острого ИМ.
Лабораторная диагностика
В первые 6 часов острого состояния в крови выявляется повышенный уровень белка – миоглобина, участвующего в транспортировке кислорода внутрь кардиомиоцитов. В течение 8–10 часов больше чем на 50% увеличивается креатинфосфокиназа, показатели активности которой нормализуются к концу 2 суток. Этот анализ повторяют каждые 8 часов. Если получают троекратный отрицательный результат, то инфаркт сердца не подтверждается.
На более позднем сроке необходим анализ на определение уровня лактатдегидрогеназы (ЛДГ). Активность этого фермента увеличивается спустя 1–2 суток от начала массового омертвления кардиомиоцитов, по прошествии 1–2 недель приходит в норму. Высокой специфичностью отличается повышение изоформ тропонина, увеличение уровня аминотрансфераз (АСТ, АЛТ). В общем анализе – повышение СОЭ, лейкоцитоз.
Инструментальная диагностика
ЭКГ фиксирует появление отрицательного з. Т либо его двухфазность в определенных отведениях (при мелкоочаговом ИМ), патологии комплекса QRS или з. Q (при крупноочаговом ИМ), а также различные нарушения проводимости, аритмии.
Электрокардиография помогает определить обширность и локализацию области омертвения, оценить сократительную способность сердечной мышцы, выявить осложнения. Рентгенологическое исследование малоинформативно. На поздних этапах проводят коронарографию, выявляющую место, степень сужения или непроходимости коронарной артерии.
Лечение инфаркта миокарда
При подозрении на инфаркт сердца срочно вызывают скорую помощь. До приезда медиков нужно помочь больному принять полусидячее положение с согнутыми в коленях ногами, ослабить галстук, расстегнуть одежду, чтобы она не стягивала грудь и шею. Открыть форточку или окно для доступа свежего воздуха. Под язык положить таблетку аспирина и нитроглицерина, которые предварительно измельчить или попросить больного их разжевать. Это необходимо для более быстрого всасывания действующего вещества и получения скорейшего эффекта. Если ангинозные боли не прошли от одной таблетки нитроглицерина, то его следует рассасывать через каждые 5 минут, но не больше 3 таблеток.
Больной с подозрением на инфаркт сердца подлежит незамедлительной госпитализации в кардиологическую реанимацию. Чем раньше реаниматологи начнут лечение, тем благоприятнее дальнейший прогноз: можно предупредить развитие ИМ, предотвратить появление осложнений, сократить площадь очага некроза.
Основные цели первоочередных лечебных мероприятий:
- снятие болевого синдрома;
- ограничение некротической зоны;
- предотвращение осложнений.
Купирование болевых ощущений – один из важнейших и неотложных этапов лечения ИМ. При неэффективности таблетированного нитроглицерина, его вводят в/в капельно либо наркотический анальгетик (например, морфин) + атропин в/в. В некоторых случаях проводят нейролептанальгезию – в/в нейролептик (дроперидол) + анальгетик (фентанил).
Тромболитическая и антикоагулянтная терапия направлена на сокращение зоны некроза. Впервые сутки от появления первых признаков инфаркта для рассасывания тромба и восстановления кровотока возможно проведение процедуры тромболизиса, но для предотвращения гибели кардиомиоцитов эффективнее ее делать в первые 1–3 часа. Назначают тромболитические препараты – фибринолитики (стрептокиназа, стрептаза), антиагреганты (тромбо-АСС), антикоагулянты (гепарин, варфарин).
Антиаритмическая терапия. Для устранения нарушений ритма, сердечной недостаточности, восстановления метаболизма в ткани сердца применяют антиаритмические препараты (бисопролол, лидокаин, верапамил, атенолол), анаболики (ретаболил), поляризующую смесь и т.д.
Для лечения острой недостаточности сердца используют сердечные гликозиды (коргликон, строфантин), диуретики (фуросемид).
Для устранения психомоторного возбуждения применяют нейролептики, транквилизаторы (седуксен), седативные средства.
Прогноз заболевания зависит от быстроты оказания первой квалифицированной помощи, своевременности проведения реанимационных мероприятий, размера и локализации очага поражения миокарда, наличия либо отсутствия осложнений, возраста пациента и имеющихся у него сопутствующих сердечно-сосудистых патологий.
Источник
