Бета блокаторы и сердечная недостаточность

Бета-адреноблокаторы при хронической сердечной недостаточности (ХСН)
Применение бета-адреноблокаторов в терапии сердечной недостаточности находит все больше сторонников. Ранее считавшиеся абсолютно противопоказанными, теперь они рассматриваются как хорошие средства прерывания неблагоприятной хронической эндогенной адренергической стимуляции. Во многих исследованиях показано положительное действие бета-блокады на процесс ремоделирования левого желудочка, оцениваемое по увеличению фракции выброса в среднем на 5-10 %.
Пациенты, принимавшие бета-блокаторы, реже госпитализировались и у них отмечалось улучшение гемодинамических показателей в покое и при физической нагрузке. Эффекты бета-блокирующих средств на способность переносить максимальную физическую нагрузку, NYHA-функциональный класс застойной сердечной недостаточности и качество жизни неоднозначны. Лучший эффект наблюдался при лечении бета-селективными блокаторами, нежели при использовании неселективных препаратов.
Карведилол — неселективное средство, обладающее вазодилататорными и антиоксидантным свойствами, одобрен для применения у пациентов, страдающих ишемической и неишемической кардиомиопатией. Однако о влиянии этого препарата на показатель смертности пока нет окончательного заключения. Важно отметить, что недавно прекращено испытание бисопролола по программе CIBIII, так как уже промежуточные результаты продемонстрировали снижение смертности пациентов на 25 %.
В целом эти препараты хорошо переносятся при условии, что начальные дозы очень низкие (1/10-1/20 стандартной дозы), а титрование — постепенное, с увеличением не чаще чем через две недели. Для многих бета-блокаторов оптимальные лечебные дозы точно не установлены; однако, как правило, положительные эффекты являются дозозависимыми, поэтому целесообразно доводить дозу до максимально переносимой или рекомендованной.
При сердечной недостаточности часто встречаются нарушения ритма. Дилатация предсердий может вызвать трепетание или мерцание предсердий, а возникшая в результате этого тахикардия желудочков может спровоцировать ишемию и нарушение их заполнения. Желудочковые экстрасистолы и устойчивая или неустойчивая желудочковая тахикардия могут перейти в фибрилляцию желудочков. Внезапная смерть от нарушений ритма имеет место у 25 % (или более) пациентов с сердечной недостаточностью.
Прежде всего необходимо проводить интенсивное лечение сердечной недостаточности. Антиаритмические препараты следует использовать осторожно у пациентов со сниженной функцией желудочков. У таких больных особенно велик риск возникновения проаритмогенных побочных эффектов и низка эффективность данных препаратов. Их назначение должно ограничиваться жизнеугрожающими нарушениями ритма и сопровождаться соответствующим контролем. В настоящее время формируются группы пациентов для участия в экспериментальных исследованиях, включающих оценку использования антиаритмических препаратов III класса (например, амиодарона) и автоматических вживляемых дефибрилляторов, с целью найти лучший метод предотвращения смерти от нарушений ритма у больных с застойной сердечной недостаточносотью.
– Также рекомендуем “Имплантируемые сердечные дефибрилляторы (ИСД) и трансплантация сердца при сердечной недостаточности”
Оглавление темы “Аритмии сердца”:
- Бета-адреноблокаторы при хронической сердечной недостаточности (ХСН)
- Имплантируемые сердечные дефибрилляторы (ИСД) и трансплантация сердца при сердечной недостаточности
- Принципы анализа ритма сердца – диагностика аритмий
- Что такое синусовый ритм и синусовая тахикардия на ЭКГ? Диагностика
- Лечение предсердных экстрасистол. Критерии диагностики
- Лечение пароксизмальных наджелудочковых тахикардий (ПНЖТ) с механизмом re-entry. Критерии диагностики
- Лечение пароксизмальной наджелудочковой тахикардии (ПНЖТ) при синдроме Вольфа-Паркинсона-Уайта. Критерии диагностики
- Лечение предсердных тахикардий. Критерии диагностики
- Лечение трепетаний предсердий. Критерии диагностики
- Лечение фибрилляции предсердий. Выбор лекарства
Источник
Хроническая сердечная недостаточность (ХСН) — это синдром, развивающийся в результате различных заболеваний сердечно-сосудистой системы, приводящий к снижению насосной функции сердца, хронической гиперактивации нейрогормональных систем и проявляющийся одышкой, сердцебиением, повышенной утомляемостью, ограничением физической активности и избыточной задержкой жидкости в организме. Синдром ХСН может осложнять течение практически всех заболеваний сердечно-сосудистой системы.
Интерес во всем мире к изучению различных аспектов ХСН обусловливается плохим прогнозом заболевания, увеличением числа больных с ХСН, увеличением числа госпитализаций из-за обострения ХСН, неудовлетворенностью качеством лечения, ростом затрат на борьбу с ХСН. Статистика свидетельствует о неуклонном росте числа больных с ХСН во всех странах, независимо от политической и экономической ситуации. В настоящее время распространенность клинически выраженной ХСН в популяции составляет не менее 2,0%. С возрастом (у лиц старше 65 лет) частота встречаемости ХСН возрастает до 6–10% и является самой частой причиной госпитализации пожилых больных. За последние 15 лет число госпитализаций больных с ХСН утроилось, а за 40 лет увеличилось в 6 раз. Пятилетняя выживаемость больных с ХСН все еще ниже 50%, а риск внезапной смерти в 5 раз выше, чем в популяции. Точной статистики о количестве пациентов в России нет, тем не менее можно предположить, что их не менее 3–3,5 млн человек, причем это только пациенты со сниженной насосной функцией левого желудочка (ЛЖ) и явными симптомами ХСН. Примерно столько же больных имеют симптомы ХСН при нормальной систолической функции сердца и их вдвое больше, чем имеющих бессимптомную дисфункцию ЛЖ, поэтому речь может идти о 12–14 млн больных с ХСН [1]. Доказано, что в наши дни именно ишемическая болезнь сердца (ИБС) (в сочетании с артериальной гипертонией или без нее) является самой частой причиной ХСН, составляя до 60% всех случаев декомпенсации. В связи со сказанным своевременная диагностика ХСН и знание современных методов лечения весьма актуально.
Подходы к лечению во многом зависят от понимания основных патофизиологических процессов, обусловливающих клинические проявления ХСН. Следует отметить, что в последние десятилетия ХХ века произошли значительные изменения взглядов как на саму проблему понимания развития ХСН, так и ее лечения. Получила распространение так называемая «миокардиальная теория патогенеза хронической сердечной недостаточности». В ее основе лежало представление о чрезмерной активации нейрогормональных систем — ренин-ангиотензин-альдостероновой (РААС) и симпатико-адреналовой (САС). Хорошо известно, что при снижении сердечного выброса, обусловленного нарушением систолы ЛЖ, происходит активация САС, которая носит компенсаторный характер. Это приводит к следующему:
- повышение частоты сердечных сокращений и сократимости миокарда обеспечивает насосную функцию сердца;
- происходит поддержание артериального давления (АД) в условиях сниженного сердечного выброса (СВ);
- потенцируется веноконстрикция, обеспечивая венозный возврат и повышение давления наполнения сердца через механизм Франка–Старлинга.
Когда необходимость в интенсификации кровообращения проходит, то нет необходимости в повышении активности САС. В условиях же постоянной гемодинамической (и иной) перегрузки сердца происходит длительная гиперактивация САС, нивелирующая положительные моменты активации данной системы.
Нежелательные эффекты длительной активации САС заключаются в следующем:
- Происходит дополнительная (помимо основного патологического процесса) гибель кардиомиоцитов в результате некроза и апоптоза. Развитие дисфункции и некроза мышечных волокон происходит вследствие их перегрузки кальцием и угнетения митохондрий, что опосредуется через бета1- и бета2-адренорецепторы сердца и циклического АМФ.
- Увеличение частоты сердечных сокращений (ЧСС) способно непосредственно негативно влиять на работу сердца при ХСН, независимо от развития ишемии миокарда и нарушений ритма сердца. В норме сила сокращений возрастает при увеличении ЧСС, в пораженном же сердце происходит дальнейшее снижение сократительной способности миокарда.
- Провоцируется ишемия вне зависимости от состояния коронарного русла.
- Провоцируются нарушения ритма сердца.
- Стимулируется секреция ренина, снижается почечный кровоток, задерживается жидкость вследствие повышения реабсорбции натрия.
Однако длительная терапия бета-адреноблокаторы (бета-АБ) больных ХСН тормозит и вызывает регрессию патологического ремоделирования сердца (гипертрофию и изменение формы полостей сердца), улучшает функцию сердца (уменьшение тахикардии, торможение апоптоза и кардиотоксического действия катехоламинов, электрическую нестабильность миокарда и косвенно активность РААС). Без преувеличения можно сказать, на сегодняшний день бета-АБ являются неотъемлемой частью лечения ХСН. Долгое время считалось, что бета-АБ противопоказаны у больных ХСН, обусловленной систолической дисфункцией ЛЖ.
Пересмотр представлений о возможности применения бета-АБ у больных ХСН начался в 80-е годы, когда Swedberg и соавт. [2] сообщили, что длительное назначение небольших доз бета-АБ (в сочетании с диуретиками) улучшает функцию ЛЖ и увеличивает продолжительность жизни больных с дилатационной кардиомиопатией (за 3 года наблюдения смертность среди больных, получавших бета-АБ, составила 48%, тогда как в контрольной группе — 90%). С того времени выполнено достаточное количество контролируемых исследований, посвященных изучению влияния различных бета-АБ на показатели функции ЛЖ и продолжительность жизни больных с ХСН.
В настоящее время бета-АБ являются неотъемлемым компонентом комплекса лекарственных средств, предназначенных для лечения больных ХСН различной этиологии. Особое внимание привлекает кардиоселективный бета-АБ 2-й генерации бисопролол (Конкор®). Так, в 1994 г. было проведено двойное слепое многоцентровое европейское исследование CIBIS [3]. В это исследование был включен 641 больной с III–IV функциональным классом ХСН, в добавление к ингибиторам ангиотензинпревращающего фермента (иАПФ) и мочегонным больные получали бисопролол (2,5–5 мг/сут) или плацебо в течение 2 лет. Риск смерти снизился на 20% среди больных, получавших бисопролол, наиболее успешной была терапия у тех пациентов, ЧСС которых была более 80 уд./мин, а также среди больных с ХСН неишемической этиологии. Это исследование отчетливо показало целесообразность применения бета-АБ (а конкретно, бисопролола) у больных с ХСН (достаточно тяжелой). Исследование CIBIS II [4] включало уже 2647 больных с ХСН III-IV функциональных классов и фракцией выброса ЛЖ менее 35%. Период наблюдения составил в среднем 1,3 года. Бисопролол (Конкор®) назначали в дозе 1,25 мг/сут с постепенным увеличением дозы до 10 мг/сут. Результаты исследования оказались весьма впечатляющими: выявлено снижение общей смертности на 32%, снижение частоты внезапной смерти на 42%, снижение частоты госпитализаций на 15% (в том числе по поводу сердечной декомпенсации на 32%). Важно отметить, что эффективность бисопролола (Конкора®) не зависела от тяжести и этиологии ХСН (у больных с ИБС эффект был даже более выраженным, чем при дилатационной кардиомиопатии). Риск декомпенсации, требующей госпитального лечения, под влиянием бисопролола снижался на 30%. Существенно, что бисопролол переносился так же хорошо, как и плацебо, частота вынужденной отмены препарата составила всего 15%. Основной опасностью при лечении больных с ХСН может быть развитие атриовентрикулярной блокады или выраженной гипотонии. Предупредить эти осложнения можно, начиная с назначения небольшой дозы препарата (1,25 мг), которая постепенно повышается. CIBIS II — первое крупное исследование, доказавшее положительное влияние кардиоселективного бета-АБ бисопролола на течение заболевания у больных с выраженной ХСН независимо от характера заболевания, приведшего к развитию декомпенсации. Это исследование показало способность бисопролола продлевать жизнь больных с ХСН.
В настоящее время бисопролол внесен Международными кардиологическими обществами, а также ВНОК в число препаратов, предназначенных для лечения ХСН различной этиологии.
Представляется также весьма интересным вопрос: можно ли начинать лечение больных с ХСН с назначения бета-АБ и, в частности, бисопролола? Дело в том, что в процессе развития ХСН САС активируется раньше, чем РААС, в то же время бета-АБ более эффективно снижают концентрацию норадреналина, нежели иАПФ (кроме того, бета-АБ способны снижать также активность РААС). иАПФ, в свою очередь, более эффективно снижают концентрацию ангиотензина II (А II) у больных ХСН (которые уже находятся на терапии бета-АБ, последние положительно влияют на «ускользание» влияния иАПФ на содержание АII). Сказанное позволяет утверждать, что на начальных этапах развития ХСН, возможно, более целесообразно назначать бета-АБ. На этот вопрос весьма недвусмысленный ответ дает многоцентровое исследование CIBIS III [5], основная гипотеза которого состоит в утверждении, что начало терапии больных с ХСН можно начинать с бета-АБ (в частности, бисопролола) к которому в дальнейшем добавляется иАПФ. Таким образом, основная цель CIBIS III состояла в том, чтобы показать, что стартовая терапия бисопрололом (к которому затем присоединялся эналаприл) сравнима (не хуже) с обратным назначением препаратов (сначала эналаприл, а затем бисопролол) в профилактике смерти и госпитализации по различным причинам (в первую очередь — кардиальным). В исследовании участвовало 1010 пациентов с ХСН II–III функционального класса. В одной группе больных бисопролол (Конкор®) титровался начиная с 1,25 мг/сут до целевой дозы в 10 мг/сут, в другой — эналаприл (Энап) начальную дозу составил 5 мг/сут, конечная доза была равна 20 мг/сут (данная фаза исследования составила 6 мес, затем в течение 18 мес больные получали одновременно оба препарата (бисопролол (Конкор®)— с 1,25 мг/сут до 10 мг/сут, эналаприл (Энап) — начиная с 5 мг/сут до 20 мг/сут). Было установлено, что монотерапия бисопрололом в начале лечения ХСН не только не уступает по эффективности эналаприлу, а по некоторым показателям даже превосходит монотерапию иАПФ. Конкор® так же безопасен, как и иАПФ, при использовании в качестве монотерапии в начальной стадии лечения ХСН. Таким образом, результаты исследования CIBIS III поддерживают концепцию «свободного выбора» для начальной терапии ХСН бета-АБ или иАПФ, основанную на личном решении врача с учетом индивидуальных особенностей больного. Вопрос стоит так: можно ли назначить больному с ХСН бета-АБ без иАПФ? Однако вопрос стоит не в противопоставлении иАПФ бета-АБ, а в выборе оптимального режима стартовой терапии. Внезапная смерть во время первых 6 месяцев монотерапии в группе больных, получавших бисопролол, отмечена в 8 из 23 смертельных исходов; смертельных исходов в группе, получавших эналаприл, — 16 из 32. В течение первого года в группе начинавших лечение бисопрололом было 16 (из 42), в группе начинавших лечение эналаприлом эти показатели равнялись соответственно 29 из 60 (то есть на 46% меньше в группе больных, начинавших лечение Конкором®). Это позволило сделать вывод, что у больных 65 лет и старше с легкой или умеренной стабильной ХСН (фракцией выброса, равной или менее 35%) начало терапии с назначения Конкора® достоверно превосходит начало терапии с назначения эналаприла по снижению случаев внезапной смерти в течение первого года. Достоверные различия в количестве случаев внезапной смерти между стратегиями терапии сохранялись после 6 месяцев комбинированной терапии. Тем не менее современные рекомендации предлагают начинать лечение ХСН с иАПФ, вслед за чем советуют добавлять высококардиоселективный бета-АБ (в данном случае — бисопролол).
Применение бета-АБ существенно снижает смертность больных с ХСН. Таким образом, всех пациентов с ХСН и кардиомегалией следует рассматривать как претендентов на лечение бета-АБ. Для начала терапии необходима гемодинамическая стабильность пациента. Применение бета-АБ не является вариантом неотложной терапии в большинстве случаев ХСН. Необходимо начинать лечение с малых доз (применительно к бисопрололу — это 1,25 мг/сут), через две недели доза удваивается, что делается с целью предотвращения побочных явлений. Не следует значительно увеличивать дозу в интервале 2 нед. Именно постепенность в наращивании дозы препарата — залог успеха в применении бета-АБ у больных ХСН. Снижение ЧСС более 10 уд./мин является достоверным критерием бета-адреноблокады.
В настоящее время трудно представить лечение ХСН без применения высокоселективных бета-АБ; не случайно в учебнике «Внутренние болезни» S. Davidson (20-е издание, 2006 г.) приведены следующие слова: «Добавление пероральных бета-АБ в увеличивающихся дозах к стандартной терапии, включающей иАПФ, у больных с ХСН уменьшает частоту смерти и госпитализации. Число больных, которых следует лечить 1 год, чтобы предотвратить одну смерть, равно 21» [6].
Литература
- Беленков Ю. Н., Мареев В. Ю., Агеев Ф. Т. Эпидемиологические исследования сердечной недостаточности: состояние вопроса // Cons medicum. 2002, № 3, с. 112–114.
- Swedberg K., Hjalmarson A. et al. Prolongation of survival in congestive cardiomyopathy during treatment with beta-blocer // Lancet. 1; 1374–1376.
- CIBIS Investigators. A randomized trial of beta-blocade in heart failure. The Cardiac Insufficiensy Bisoprolol Study (CIBIS) // Circulation. 1994; 90: 1765–1773.
- CIBIS-II Investigators and Committees. The Cardiac InsufficiensyBisoprolol Study II (CIBIS-II): a randomized trial. 1999; 353: 9–13.
- Willenheimer R., van Veldhuisen D. J., Silke B. et al. Effect on survival and hospitalization of initiating treatment for chronic heart failure with bisoprolol by enalapril, as compared with the opposite sequence // Circulation. 2005; 112: 2426–2435.
- Lechat P., Parker M., Chalon S. et al. Clinicaleffects of beta-adrenergic blokad in chronic heart failure: a meta-analysis of double, placebo-controlled trials // Circulation. 1998, vol. 98, p. 1184–1199.
В. И. Маколкин, доктор медицинских наук, профессор, член-корреспондент РАМН
Ф. Н. Зябрев
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова Минздравсоцразвития РФ, Москва
Контактная информация об авторах для переписки: dvmak@mail.ru
Источник
А. Н. КАЛЯГИН, доцент кафедры пропедевтики внутренних болезней Иркутского государственного медицинского университета, заместитель главного врача по терапии МУЗ «Клиническая больница №1 г. Иркутска», кандидат медицинских наук
На протяжении долгого промежутка времени перспективность применения бета-адреноблокаторов (БАБ) в лечении больных хронической сердечной недостаточностью (ХСН) ставилась под сомнение в связи с наличием отрицательного инотропного эффекта. Однако с 1997 г. был достигнут консенсус в вопросах использования этой группы лекарств, основой чего явилась целая серия исследований, выполненных на основании принципов доказательной медицины (COMET, BEST, CIBIS, MERITHF, COPERNICUS, SENIORS), и продемонстрированная двуфазность их действия. В настоящее время они обозначены как основной препарат для этой категории больных в Европейских (2005) и Национальных (2007) рекомендациях. Фактически, по меткому выражению Г.И. Сторожакова и А.В. Мелихова (2008), «назначение БАБ — это финальный штрих в создании индивидуальной для каждого пациента программы лечения сердечной недостаточности».
Теоретическими предпосылками для применения БАБ при ХСН послужили неблагоприятные изменения, возникающие при активации симпатоадреналовой системы:
- Гемодинамические — уменьшение фракции выброса, вазоконстрикция и уменьшение перфузии жизненно важных органов (сердце, почки и др.).
- Метаболические — повышение частоты сердечных сокращений увеличивает потребность миокарда в кислороде, а констрикция коронарных сосудов уменьшает доставку кислорода.
- Морфологические — развитие гипертрофии миокарда левого желудочка, дилатация полостей сердца.
- Проаритмические — вследствие высокой концентрации катехоламинов в крови, гипокалиемии, увеличения полостей сердца.
- Повышение риска внезапной смерти — за счет предрасположенности к аритмиям (в особенности желудочковым).
Установлено, что степень активации симпатоадреналовой системы (в частности, определяемая по уровню норадреналина) тесно коррелирует с тяжестью ХСН. В соответствии с Национальными рекомендациями Всероссийского научного общества кардиологов и Общества специалистов по сердечной недостаточности (2007) к ключевым благоприятным эффектам БАБ при ХСН относят:
- уменьшение дисфункции и смерти кардиомиоцитов путем некроза и апоптоза;
- уменьшение числа гибернирующих («спящих») кардиомиоцитов;
- улучшение показателей гемодинамики при длительном использовании за счет увеличения площади сокращающейся зоны;
- повышение плотности и афинности бета-рецепторов, которая резко снижена у больных ХСН;
- уменьшение гипертрофии миокарда;
- снижение частоты сердечных сокращений;
- уменьшение степени ишемии миокарда в покое и особенно при физической нагрузке;
- некоторое снижение частоты желудочковых аритмий;
- антифибрилляторное действие и уменьшение вероятности внезапной смерти.
Изучение клинической эффективности БАБ осуществлялось в целой серии исследований (табл. 1). Было установлено, что препаратами выбора в ведении больных ХСН являются неселективный препарат карведилол и селективные — бисопролол, метопролола сукцинат и для больных старше 70 лет — небиволол (рис.).
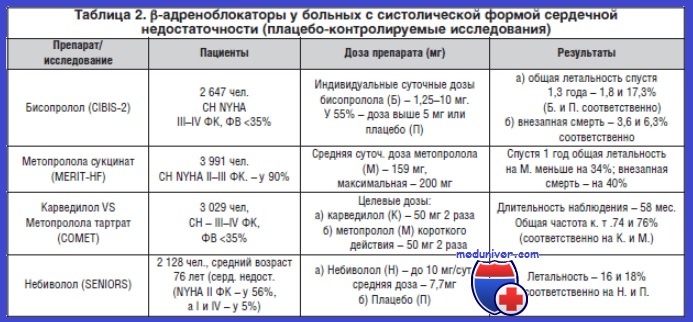
БАБ показаны всем больным со стабильной ХСН любой степени тяжести (обычно II—IV функционального класса (ФК)) и генеза, а также больным, которые имеют снижение фракции выброса левого желудочка. Обязателен долгосрочный прием БАБ в сочетании с ингибиторами ангиотензин-превращающего фермента (АПФ) у больных со сниженной систолической функцией левого желудочка после инфаркта миокарда с целью улучшения выживаемости. Эффективность применения БАБ во многом определяется клиническими предикторами (табл. 2), которые выявляются у больного.
Назначение БАБ для больных ХСН возможно только в стабильном состоянии больного на фоне применения адекватной дозы диуретиков и ингибиторов АПФ или антагонистов АТ1 рецепторов ангиотензина. В первые 10—15 дней приема БАБ возможно развитие отрицательного инотропного действия и вазоконстрикции, потому подбор их дозы целесообразно начинать в условиях стационара для больных с III—IV ФК или в амбулаторных условиях (дневном стационаре) для больных с II—III ФК ХСН. В круглосуточном или дневном стационаре возможен мониторинг клинического состояния, частоты сердечных сокращений, АД, данных электрокардиограммы. Осторожная тактика ведения больных в условиях стационара позволит отследить частоту сердечных сокращений (целевой уровень 55—60 уд./мин), а также лицами, которые имели отмену БАБ и уровень АД (целевой уровень 100/60—135/85 мм рт. ст.) в связи с побочными реакциями или ухудшением симптоматики ХСН.
Дозы препаратов медленно титруют, начиная со стартовых, которые составляют 1/8 от терапевтических (табл. 3). Дозы увеличивают вдвое в условиях стационара каждые 7—10 дней, амбулаторно — каждые 15—30 дней. Медленное титрование дозы позволяет достичь терапевтического уровня, а быстрое зачастую вызывает побочные эффекты (брадикардию, гипотонию и т.д.). В ряде случаев с целью профилактики снижения фракции выброса и обострения ХСН в первое время к лечению присоединяют небольшие дозы сердечных гликозидов, немного увеличивают дозы диуретиков и ингибиторов АПФ. При возникновении на более высокой дозе побочных эффектов БАБ (бронхообструкция, брадикардия или сердечная блокада) их дозу уменьшают (возвращаются к предыдущей дозе) или отменяют. При развитии признаков задержки жидкости первоначально увеличивают дозу ингибиторов АПФ и/или диуретиков, а уж потом, при неэффективности этих мероприятий, присоединяют левосимендан, снижают дозу или отменяют БАБ. После ликвидации побочных эффектов необходимо вновь повторить попытку назначения БАБ, но использовать меньшую дозу и более медленный режим титрования.
БАБ при ХСН абсолютно противопоказаны в следующих ситуациях:
- Бронхообструктивные заболевания (бронхиальная астма, хроническая обструктивная болезнь легких) в тяжелой стадии.
- Симптомная брадикардия (менее 48 уд./мин.).
- Симптомная гипотония (систолическое АД менее 85/60—65 мм рт. ст.).
- Синоатриальная блокада и атриовентрикулярная блокада 2-й и более степеней.
- Серьезные нарушения периферического кровообращения (тяжелый облитерирующий тромбангиит).
Необходимо помнить, что при хронической обструктивной болезни легких возможно использование высококардиоселективных средств, в частности бисопролола. При сахарном диабете типа 2 целесообразно выбрать среди БАБ карведилол, который повышает чувствительность периферических тканей к инсулину. При этом целесообразно больным с хронической обструктивной болезнью легких осуществлять регулярную пикфлоуметрию с оценкой пиковой скорости выдоха при каждом общении с врачом, а больным сахарным диабетом типа 2 внимательно следить за показателями гликемии и серьезнее относиться к диетическим правилам.
Особенно внимательно при использовании БАБ нужно наблюдать за больными с тяжелой ХСН (III—IV ФК), ХСН неизвестной этиологии, при наличии относительных противопоказаний (брадикардия, гипотония, плохая переносимость даже малых доз БАБ, сопутствующая хроническая обструктивная болезнь легких).
К сожалению, реальная частота назначения БАБ ХСН остается недостаточной, в частности, в наших работах по изучению ХСН у больных с ревматическими пороками сердца выявлено, что назначение БАБ составляет 62% от реальной потребности, причем в 54% случаев больные получают препараты, которые не показали своей эффективности в отношении больных ХСН (атенолол, метопролола тартрат и т.д.). В этой связи актуальным является перевод больных с неэффективных препаратов на более эффективные (табл. 4).
Таким образом, применение БАБ в ведении больных с ХСН является насущной необходимостью. Значимость этой группы препаратов показана в многоцентровых плацебоконтролируемых исследованиях, реальной клинической практике и имеет теоретическое обоснование.
К сожалению, следует отметить, что необходимость в применении БАБ и реальная частота его назначения существенно разнятся. По данным исследования ЭПОХА-ХСН (2001), частота использования этой группы лекарств составляет 8,2%. В нашем исследовании, выполненном на популяции больных с клапанными пороками сердца, было установлено, что БАБ в 2001 г. применялись в 7,4% случаев, а в 2005 г. их применение возросло до 42,9%. Эти данные внушают оптимизм и позволяют предполагать, что российские врачи будут лучше использовать средства медикаментозной терапии ХСН в своей повседневной практической деятельности.
Источник
