Узи печени при хронической сердечной недостаточности

УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
Неинвазивная допплерографическая оценка печеночной гемодинамики – новое направление ультразвуковой и функциональной диагностики. Как известно, печеночная гемодинамика складывается из артериальной, портальной и венозной кавальной составляющих. Кроме того, существенную роль при патологии печени играют различные артериовенозные и веновенозные коллатерали. В настоящее время не разработано оптимального комплекса допплерэхографической оценки нарушений системного кровообращения печени и сердца.
Ангиоархитектоника печени уникальна в организме человека, она объединяет портальную и кавальную венозные, артериальную, лимфатическую и билиарную системы в единое целое. Печеночная гемодинамика чрезвычайно чувствительна к любому воздействию на организм, а ее первичные нарушения могут влиять на функцию сердца, являясь причиной легочной гипертензии. Врачи, подчас, не задумываются о влиянии этих патологических процессов в печени на состояние сердечно-сосудистой системы, тем более, что масса лекарств, будучи вазоактивной, изменяет гемодинамику печени. Поэтому назрела необходимость разработки простого комплекса допплерэхографической оценки разнообразных нарушений кровообращения печени и гемодинамики сердца. Одной из составляющих кровотоков, исследуемых в комплексе при оценке печеночной гемодинамики, является артериальный печеночный кровоток, изучение которого требует определенных подходов.
Цель настоящей работы – допплерографическое изучение состояния артериального кровообращения и вариантов нарушения артериальной гемодинамики печени при диффузных поражениях печени и портальной гипертензии, при ишемической болезни сердца с сердечной недостаточностью. Задачи исследования – определить наиболее информативные показатели артериального печеночного кровотока и их изменение при сердечной недостаточности и портальной гипертензии.
Материалы и методы
Обследовано 287 человек. Все больные были разделены на 4 группы: 1-я группа – 56 пациентов с ишемической болезнью сердца со стенокардией покоя и напряжения 1-2 функционального класса (ф.к.) (NYHA) без недостаточности кровообращения; 2-я группа – 48 пациентов с ишемической болезнью сердца, атеросклеротическим и постинфарктным кардиосклерозом, стенокардией покоя и напряжения 2-4 ф.к. (NYHA), с недостаточностью кровообращения в большом и малом кругах; 3-я группа – 93 больных с хроническими вирусными гепатитами (B,C) с индексами Кноделля до 4-6 баллов с минимальными степенями активности по классификации 1994 г. (Лос-Анжелес); 4-я группа – 51 больной с достоверно установленным диагнозом цирроза печени с активностью воспалительного процесса по Кноделлю до 10-14 баллов и с критериями тяжести портальной гипертензии по шкале Чайлд-Пью от А до В. Диагноз верифицирован, по клинико-лабораторным и инструментальным данным, у 43% – гистологически, а у 13% – интраоперационно по поводу портосистемного шунтирования. К 5-й контрольной группе отнесено 39 практически здоровых лиц.
Всем обследованным лицам проводилось допплерографическое исследование в импульсно-волновом режиме, цветного допплеровского картирования и энергетической цветной допплерографии, на ультразвуковых томографах датчиками 3,5 и 3,75 Мгц (30°-90°). Допплерэхография общей печеночной артерии проводилась из субкостального доступа в месте ее отхождения от чревного ствола, где угол между УЗ-лучом и ходом сосуда не превышает 45°, а также собственно печеночной артерии во внутрипеченочном участке, где она расположена между воротной веной и желчным протоком. Для дифференциации сосудов обязательным является подключение режимов цветного допплеровского картирования и энергетического допплера (рис. 1, 2).
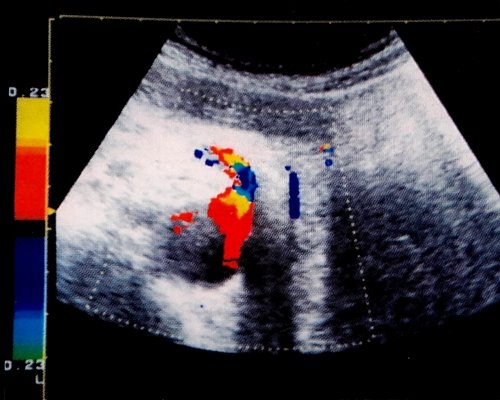
Рис. 1. Общая печеночная артерия в режиме цветного допплеровского картирования.
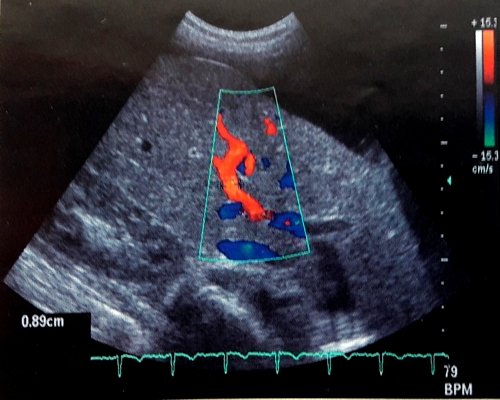
Рис. 2. Печеночная артерия в режиме энергетического допплера.
Анализировались допплерограммы с максимальным спектром кровотока. Оценивались диаметр общей печеночной артерии (ДоПА) и площадь сечения (ПСоПА) во внепеченочном отделе, конечные систолическая и диастолическая (Vмакс, Vмин), средняя скорости, RI, PI. Рассчитывались следующие параметры объемного кровотока:
- ИОКоПА – индекс объемного кровотока в общей печеночной артерии за 1 мин:
ИОКоПА [мл/мин · м²] = 1,055 · ПсоПА [см²] · VсрПА [см/с] · ЧСС [уд. в 1 мин] / BSA [м²],
где ЧСС – частота сердечных сокращений; BSA – площадь поверхности тела; - VoОПА%МОС – объемный кровоток в общей печеночной артерии относительно минутного объема сердца:
VoОПА%МОС = 0,1 · ИОКоПА [мл/мин · м²] / СИдопл [л/мин · м²],
где СИ – сердечный индекс, рассчитанный по трансаортальному потоку методом постоянноволновой допплерэхокардиографии.
Расчет допплерэхографических индексов печеночной гемодинамики проводился в рамках стандартного блока математических функций и статистики программы EXCEL пакета программ MS-Office для WINDOWS-95.
Результаты исследования
По данным цветного допплеровского картирования и энергетического допплера, артериальные пульсирующие спектры проанализированы в подкапсульных, интрамуральных и перипортальных полях паренхимы печени во всех исследуемых группах. Признаки артериальной перфузии при энергетическом цветном допплере отчетливо выявлены в подкапсульных участках в среднем у 84,5% лиц контрольной группы, у 78% больных ишемической болезнью сердца без недостаточности кровообращения и у 89% больных хроническим вирусным гепатитом. Существенно хуже определяются аналогичные признаки у больных ишемической болезнью сердца с недостаточностью кровообращения и циррозом печени с портальной гипертензией. Так, в 4-й группе пациентов артериальные спектры выявлены у 57%, а во 2-й группе – лишь у 43% больных. Из качественных характеристик цветных спектров во 2-й группе больных преобладали смешанные или с высоким коэффициентом турбулентности, в 4-й группе при ретроспективном анализе допплерограмм отмечены турбулентные спектры чаще, чем в 1-й и 3-й группах больных.
Во 2-й группе пациентов стенки общей печеночной артерии чаще были гиперэхогенными, утолщенными, неровными, а сама общая печеночная артерия выглядела более извитой и удлинненной. Это объясняется атеросклеротическими изменениями стенки общей печеночной артерии. Вероятно, этим же объясняются наименьшие среди всех групп, кроме контрольной, значения угла между УЗ-лучом и центральной осью общей печеночной артерии при проведении импульсной допплерэхографии сосуда. Было отмечено, что в 1-й и 2-й группах преобладали изменения во внепеченочном отделе общей печеночной артерии, тогда как в 3-й и 4-й группах – во внутрипеченочном отделе собственно печеночной артерии. Диаметр и соответственно площадь поперечного сечения общей печеночной артерии оказались минимальными во 2-й и 4-й группах при максимальном значении в контрольной группе. Результаты приведены в таблице 1.
Анализ линейных скоростных параметров кровотока в общей печеночной артерии выявил значительное снижение максимальной и минимальной скоростей у больных 2-й группы по сравнению с другими группами. Средние интегральные скорости кровотока в общей печеночной артерии у больных 2-й группы были лишь немного меньше, чем в 4-й группе (табл. 1).
Колебания пульсативного индекса Гослинга (PI) во всех группах больных были недостоверными. В контрольной группе PI был максимальным, составляя 1,53. Нами не выявлено информативности индекса Гослинга в дифференциальной диагностике нарушения кровообращения печени. Индекс резистивности Пурсело (RI) оказался минимальным у больных 4-й и 3-й групп, составив 0,628 и 0,643 соответственно, тогда как во 2-й, 1-й и контрольной группах он составил 0,70, 0,71 и 0,72, достоверно не отличаясь один от другого, но выше, чем у больных с диффузными поражениями печени (рис. 3).

Рис. 3. Соотношение линейных скоростей и индексов в общей печеночной артерии.
Анализ традиционно исследуемых индексов линейного кровотока в общей печеночной артерии у больных с диффузными поражениями печени первичного и вторичного характера не выявил их высокой точности и специфичности. Индексы объемного артериального кровотока в общей печеночной артерии у больных с сердечной недостаточностью при ишемической болезни сердца и у больных циррозом печени с портальной гипертензией также оказались информативными. Так, анализ результатов индекса объемного кровотока в общей печеночной артерии (ИОКоПА) выявил закономерное снижение его у больных 2-й относительно 1-й группы до 281,4±9,94 против 541,18±10,08 мл/мин/м² (р

Рис. 4. Относительный объемный артериальный приток к печени.
Качественное состояние общей и собственно печеночной артерии должно быть оценено с подключением цветного допплеровского картирования и энергетического допплера на уровнях отхождения от чревного ствола и в области ворот печени, а количественный анализ печеночной артериальной гемодинамики должен базироваться на оценке объемных индексов, тогда как традиционные линейные показатели являются дополнительными.
Таблица 1. Сравнительный анализ артериального притока к печени по ОПА.
| Показатель | ДоПА | ПСоПА | VмаксПА | VминПА | VсрПА | PI-ОПА | RI-ОПА | ИОКоПА | VоОПА%МОС |
|---|---|---|---|---|---|---|---|---|---|
| Группа 1 ИБС без НК | 5,555± 0,054 | 0,244± 0,005 | 96,848± 0,831 | 28,239± 0,586 | 60,859± 0,655 | 1,137± 0,015 | 0,709± 0,005 | 541,179± 10,076 | 22,484± 0,542 |
| Группа 2 ИБС с НК | 5,358± 0,100 | 0,230± 0,009 | 46,472± 0,982 | 13,698± 0,325 | 31,283± 0,624 | 1,044± 0,014 | 0,705± 0,007 | 281,401± 9,940 | 16,087± 0,271 |
| Группа 3 ХВГ | 5,835± 0,031 | 0,268± 0,003 | 92,624± 0,446 | 33,054± 0,472 | 55,452± 0,546 | 1,090± 0,020 | 0,643± 0,005 | 564,809± 8,298 | 23,693± 0,573 |
| Группа 4 Цирроз с ПГ | 5,491± 0,079 | 0,239± 0,007 | 57,447± 0,696 | 21,298± 0,334 | 33,298± 0,539 | 1,099± 0,027 | 0,628± 0,007 | 309,989± 11,960 | 12,918± 0,384 |
| Группа 5 Контрольная | 6,170± 0,062 | 0,302± 0,006 | 93,535± 1,131 | 26,263± 0,337 | 44,424± 0,759 | 1,530± 0,015 | 0,718± 0,003 | 530,277± 6,857 | 21,796± 0,383 |
| р<0,001 (1-2) | Н | Н | Д | Д | Д | Н | Н | Д | Д |
| р<0,001 (1-3) | Н | Н | Н | Н | Н | Н | Д | Н | Н |
| р<0,001 (1-4) | Н | Н | Н | Н | Д | Н | Д | Д | Н |
| р<0,001 (1-5) | Д | Н | Н | Н | Д | Д | Н | Н | Н |
| р<0,001 (2-3) | Н | Н | Н | Д | Д | Н | Д | Д | Д |
| р<0,001 (2-4) | Н | Н | Н | Д | Н | Н | Д | Н | Д |
| р<0,001 (2-5) | Д | Д | Н | Д | Д | Д | Н | Д | Д |
| р<0,001 (3-4) | Н | Н | Д | Д | Д | Н | Р<0,05 | Д | Д |
| р<0,001 (3-5) | Н | Н | Н | Д | Д | Д | Д | Н | Н |
| р<0,001 (4-5) | Д | Д | Н | Н | Д | Д | Д | Д | Д |
Примечание:
ДоПА – диаметр общей печеночной артерии;
ПСоПА – площадь сечения общей печеночной артерии;
VмаксПА – конечная систолическая скорость кровотока в общей печеночной артерии;
VминПА – конечная диастолическая скорость кровотока в общей печеночной артерии;
VсрПА – средняя скорость кровотока в общей печеночной артерии;
PI-ОПА – пульсативный индекс Гослинга в общей печеночной артерии;
RI-ОПА – индекс резистивности Пурсело в общей печеночной артерии;
ИОКоПА – индекс объемного кровотока в общей печеночной артерии за 1 мин;
VоОПА%МОС- индекс артериального объемного кровообращения печени (процентное соотношение объемного артериального кровотока в общей печеночной артерии и минутного объема сердца);
Д – достоверное отличие;
Н – недостоверное отличие.
Выводы
При ишемической болезни сердца с сердечной недостаточностью и при циррозе печени с портальной гипертензией выявлено пропорциональное сужение общей печеночной артерии и снижение максимальной пиковой скорости по сравнению с контролем. Минимальная диастолическая скорость снижается достоверно лишь при сердечной недостаточности и сочетается с утолщением и уплотнением стенок общей печеночной артерии.
Для дифференциальной диагностики диффузных поражений печени важно оценивать среднюю интегральную скорость в общей печеночной артерии, которая при циррозе печени и портальной гипертензией достоверно меньше, чем при хроническом вирусном гепатите.
Из традиционных линейных скоростных индексов оценки артериального кровотока более информативен индекс Пурсело, чем индекс Гослинга.
Допплерографические индексы объемного артериального кровотока информативны в комплексной оценке гемодинамики печени.
Литература
- Зубарев А.В. Диагностический ультразвук // М.: Видар, 1999.
- Кунцевич Г.И., Кокова Н.И., Белолапотко Е.А. Возможности дуплексного сканирования для оценки кровотока в артериях и венах брюшной полости // Визуализация в клинике. – 1995. – N 6. – С. 33-39.
- Bombelli I., Genitoni V., Biasi S. et al. Liver hemodynamic flow balance by image – directed doppler ultrasound evaluation in normal subjects // J. Clin. Ultrasound 19; 257-262, 1991.
- Brown B., AbuEYousef M., Farner R. et al. Doppler sonography: a noninvasive method for evaluatin of hepatic venocclusive disease // AJR, 154: 721-724, 1990.
- Goldberg B.B. Textbook of abdominal ultrasound // Williams Wilkins, 1993.
- Grant G.E., Schiller V.L., Millener P. et al. Color Doppler Imaging of the Hepatic Vasculature // AJR 159: 943-950, November 1992.
- Ohnishi K., Saito M., Sato S. et al. Clinical utility of pulsed Doppler flowmetry in patients with portal hypertension // Am. J. Gastroenterol., 1986: 81: pp. 1-8.
- Ralls P.W. Color Doppler Sonography of the Hepatic Artery and Portal Venous System // Am. Roentgen Ray Society., Sept.,1990: 155, pp. 517-525.
- Tanaka K., Mitsui K. Morimoto M. et al. Increased Hepatic Atrial Blood Floow in Acute Viral Hepatitis: Assesment by Color Doppler Sonography // Hepatology, 1993; 18:21-7.
- Weill F.S. Ultrasound diagnosis of digestive diseases. – 1993.

УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Источник
Морфологические изменения
У умерших от сердечной недостаточности процесс аутолиза в печени протекает особенно быстро. Таким образом, полученный при аутопсии материал не даёт возможности достоверно оценить прижизненные изменения печени при сердечной недостаточности.
Макроскопическая картина. Печень, как правило, увеличена, с закруглённым краем, цвет её багровый, дольковая структура сохранена. Иногда могут определяться узловые скопления гепатоцитов (узловая регенераторная гиперплазия). На разрезе обнаруживают расширение печёночных вен, стенки их могут быть утолщены. Печень полнокровна. Отчётливо определяется зона 3 печёночной дольки с чередованием жёлтых (жировые изменения) и красных (кровоизлияние) участков.
Микроскопическая картина. Как правило, венулы расширены, впадающие в них синусоиды полнокровны на участках различной протяжённости — от центра к периферии. В тяжёлых случаях определяются выраженные кровоизлияния и очаговый некроз гепатоцитов. В них обнаруживают различные дегенеративные изменения. В области портальных трактов гепатоциты относительно сохранны.
В цитоплазме дегенеративно-изменённых клеток зоны 3 часто обнаруживают коричневый пигмент липофусцин. При разрушении гепатоцитов он может располагаться вне клеток. У больных с выраженной желтухой в зоне 1 определяются жёлчные тромбы. В зоне 3 с помощью ШИК-реакции выявляют гиалиновые тельца, устойчивые к диастазе.
Ретикулярные волокна в зоне 3 уплотнены. Количество коллагена увеличено, определяется склероз центральной вены. Эксцентрическое утолщение венозной стенки или окклюзия вен зоны 3 и перивенулярный склероз распространяются в глубь печёночной дольки. При длительно существующей или рецидивирующей сердечной недостаточности образование «мостов» между центральными венами ведёт к формированию кольца фиброза вокруг неизменённой зоны портального тракта («обратное дольковое строение»).
Биохимические сдвиги обычно умеренно выражены и определяются степенью тяжести сердечной недостаточности.
Концентрация билирубина в сыворотке у больных с застойной сердечной недостаточностью обычно превышает 17,1 мкмоль/л (1 мг%), а в трети случаев составляет более 34,2 мкмоль/л (2 мг%). Желтуха может быть выраженной, с уровнем билирубина более 5 мг% (до 26,9 мг%). Концентрация билирубина зависит от тяжести сердечной недостаточности.
У больных с далеко зашедшим митральным пороком сердца нормальный уровень билирубина в сыворотке при его нормальном захвате печенью объясняется сниженной способностью органа к выделению конъюгированного билирубина из-за уменьшения печёночного кровотока. Последнее является одним из факторов развития желтухи после операции.
Активность ЩФ может быть незначительно повышенной или нормальной. Возможно небольшое снижение концентрации альбумина в сыворотке, чему способствуют потери белка через кишечник.
Определение и причины
Застойная печень или кардиальный цирроз – это патологическое состояние, при котором печень из-за высокого давления в нижней полой вене и печёночных венах переполняется кровью. Как итог происходит её перерастяжение. Длительно находящаяся внутри кровь застаивается, нарушая снабжение паренхимы органа кислородом (возникает ишемия).
Ишемия неизбежно приводит к некрозу клеток печени (гепатоцитов). Погибшие гепатоциты фиброзируются (замещаются соединительной тканью), что и составляет морфологическую суть цирроза. Участок, где произошёл фиброз, бледнеет, кровоснабжение там отсутствует; он полностью выпадает как функциональная единица.
Застойные явления в печени отмечаются при митральном стенозе, перикардите, недостаточности трёхстворчатого клапана.
Патогенез
Гипоксия вызывает дегенерацию гепатоцитов зоны 3, расширение синусоидов и замедление секреции жёлчи. Эндотоксины, поступающие в систему воротной вены через кишечную стенку, могут усугублять эти изменения. Компенсаторно увеличивается поглощение кислорода из крови синусоидов. Небольшое нарушение диффузии кислорода может возникать в результате склероза пространства Диссе.
Снижение артериального давления при низком сердечном выбросе приводит к некрозу гепатоцитов. Рост давления в печёночных венах и связанный с ним застой в зоне 3 определяются уровнем центрального венозного давления.
Возникающий в синусоидах тромбоз может распространяться на печёночные вены с развитием вторичного местного тромбоза воротной вены и ишемии, утратой паренхиматозной ткани и фиброзом.
Клиническая картина
Больные обычно слегка желтушны. Выраженная желтуха наблюдается редко и обнаруживается у больных с хронической застойной недостаточностью на фоне ИБС или митрального стеноза. У госпитализированных больных наиболее частой причиной повышения концентрации билирубина в сыворотке служат заболевания сердца и лёгких.
Желтуха имеет отчасти печёночное происхождение, и чем больше распространённость некроза зоны 3, тем больше выраженность желтухи.
Гипербилирубинемия вследствие инфаркта лёгкого или застоя крови в лёгких создаёт повышенную функциональную нагрузку на печень в условиях гипоксии. У больного с сердечной недостаточностью появление желтухи в сочетании с минимальными признаками повреждения печени характерно для инфаркта лёгкого. В крови обнаруживают повышение уровня неконъюгированного билирубина.
Больной может жаловаться на боли в правых отделах живота, вызванные, вероятнее всего, растяжением капсулы увеличенной печени. Край печени плотный гладкий болезненный, может определяться на уровне пупка.
Повышение давления в правом предсердии передаётся на печёночные вены, особенно при недостаточности трёхстворчатого клапана. При использовании инвазивных методов кривые изменения давления в печёночных венах у таких больных напоминают кривые давления в правом предсердии. Пальпаторно определяемое расширение печени во время систолы также может объясняться передачей давления.
У больных с трикуспидальным стенозом обнаруживают пресистолическую пульсацию печени. Набухание печени выявляют путём бимануальной пальпации. При этом одну руку располагают в проекции печени спереди, а вторую — на области задних отрезков правых нижних рёбер. Увеличение размеров позволит отличить пульсацию печени от пульсации в эпигастральной области, передающейся от аорты или гипертрофированного правого желудочка. Важно установление связи пульсации с фазой сердечного цикла.
У больных с сердечной недостаточностью давление на область печени приводит к увеличению венозного возврата. Нарушенные функциональные возможности правого желудочка не позволяют справиться с возросшей преднагрузкой, что обусловливает повышение давления в яремных венах. Гепатоюгулярный рефлюкс используют для выявления пульса на яремных венах, а также с целью определения проходимости венозных сосудов, связывающих печёночные и яремные вены.
Давление в правом предсердии передаётся на сосуды вплоть до портальной системы. С помощью импульсного дуплексного допплеровского исследования можно определить усиление пульсации воротной вены; при этом амплитуда пульсации определяется выраженностью сердечной недостаточности. Однако фазные колебания кровотока обнаруживают не у всех больных с высоким давлением в правом предсердии.
Установлена связь асцита со значительно повышенным венозным давлением, низким сердечным выбросом и выраженным некрозом гепатоцитов зоны 3. Это сочетание обнаруживают у больных с митральным стенозом, недостаточностью трёхстворчатого клапана или констриктивным перикардитом. При этом выраженность асцита может не соответствовать тяжести отёков и клиническим проявлениям застойной сердечной недостаточности. Высокое содержание белка в асцитической жидкости (до 2,5 г%) соответствует таковому при синдроме Бадда-Киари.
Гипоксия мозга приводит к сонливости, ступору. Иногда наблюдается развёрнутая картина печёночной комы. Часто встречается спленомегалия. Остальные признаки портальной гипертензии обычно отсутствуют, за исключением больных с тяжёлым сердечным циррозом в сочетании с констриктивным перикардитом. В то же время у 6,7% из 74 больных с застойной сердечной недостаточностью при аутопсии обнаружены варикозно-расширенные вены пищевода, из них только у одного больного отмечался эпизод кровотечения.
При КТ непосредственно после внутривенного введения контрастного вещества отмечается ретроградное заполнение печёночных вен, а в сосудистой фазе — диффузное неравномерное распределение контрастного вещества.
У больных с констриктивным перикардитом или длительно существующим декомпенсированным митральным пороком сердца с формированием трикуспидальной недостаточности следует предполагать развитие сердечного цирроза печени. С внедрением хирургических методов лечения этих заболеваний частота сердечного цирроза печени значительно снизилась.
Первыми признаками хронической сердечной недостаточности являются сердцебиение и одышка при физических нагрузках. Со временем тахикардия становится постоянной, а одышка возникает и в покое, появляется цианоз. В нижних отделах легких выслушиваются влажные хрипы. Увеличивается печень, появляются отеки на ногах, затем жидкость скапливается в подкожной клетчатке и на теле, в серозных полостях, развивается анасарка.
На первых этапах сердечной недостаточности печень увеличивается в переднезаднем направлении и пальпаторно не определяется. Выявить увеличение печени можно с помощью инструментальных исследований (реогепатография, УЗИ). С нарастанием сердечной недостаточности печень заметно увеличивается, при этом она пальпируется в виде выступающего из подреберья болезненного края.
Болезненность печени при пальпации связана с растяжением ее капсулы. Определяются тяжесть и давящие боли в правом подреберье, вздутие живота. Печень заметно увеличена, чувствительная или болезненная, поверхность ее гладкая, край острый. Нередко наблюдается желтуха. Функциональные печеночные пробы умеренно изменены. Эти изменения в большинстве случаев обратимы.
При гистологическом исследовании биоптатов печени выявляются расширение центральных вен и синусоидов, утолщение их стенок, атрофия гепатоцитов, развитие центроло-булярного фиброза (застойный фиброз печени). С течением времени фиброз распространяется на всю дольку (развивается септальный застойный цирроз печени).
Развитие кардиального цирроза печени у пациентов с сердечной недостаточностью зачастую прогнозировано. Если заболевание сердца диагностировано на поздней стадии, то следует ожидать выявления данного заболевания. Оно характеризуется такими симптомами:
- гепатомегалия (увеличение печени) – происходит расширение границ органа, край печени можно без труда пальпировать ниже правого ребра, чего в норме наблюдаться не должно;
- интенсивная боль в правом подреберье, обусловленная сильным растяжением печёночной капсулы;
- слабость, вялость, быстрая потеря веса;
- отсутствие аппетита, тошнота, рвота:
- отёки нижних конечностей;
- пожелтение кожи и слизистых.
Указанные признаки являются отражением патологического процесса в печени. Но пациента могут беспокоить также проявления, спровоцированные сердечной недостаточностью:
- выраженная одышка при физической нагрузке, даже минимальной, или в состоянии покоя;
- ортопноэ (вынужденное положение сидя) – для облегчения дыхания во время приступа одышки;
- появление пароксизмальной (максимально выраженной) одышки в ночное время суток:
- кашель, сопровождающий одышку;
- чувство страха, тревоги, сильного беспокойства.
Застой крови в печени всегда неблагоприятен. Цирроз может продолжить патологическую цепь и привести к осложнениям. Из-за увеличения давления в воротной вене развивается портальная гипертензия.
Не исключено развитие печёночной недостаточности. По мере прогрессирования цирроза в печени всё большее количество функционирующих гепатоцитов замещает соединительная ткань. Оставшиеся клетки неспособны долго противостоять ишемии, они увеличиваются в размерах, чтобы взять на себя нагрузку. Это позволяет печени некоторое время находиться в стадии компенсации, когда симптомы отсутствуют или почти не беспокоят больного. Как только истощаются компенсаторные возможности, наступает декомпенсация – печёночная недостаточность.
Диагностика
Выявляют заболевание, которое может быть причиной сердечной недостаточности. Большую роль играет правильная оценка тахикардии и обнаружение признаков венозного застоя. Немаловажное значение имеет благоприятная динамика симптомов в процессе лечения сердечными гликозидами и мочегонными.
Чтобы выявить застойные явления в печени, нужно провести комплексное обследование. Оно включает в себя такие методы:
- Биохимический анализ крови (уровень трансаминаз (ферментов) печени, общего белка, билирубина, щелочной фосфатазы).
- Коагулограмма (исследование свёртывающей системы крови).
- Электрокардиография, эхокардиография (определение функционального состояния сердца).
- Рентгенография органов грудной клетки (выявление увеличения размеров сердца, сопутствующей патологии лёгких).
- Ультразвуковое исследование печени (определение её размеров и структуры).
- Пункционная биопсия печени (показана только кандидатам на пересадку сердца).
- Лапароцентез (взятие жидкости из брюшной полости).
- Коронарная ангиография (оценка состояния коронарных сосудов сердца).
Лечение
Терапия кардиального цирроза заключается в диете с ограничением натрия и устранении сердечной патологии, его спровоцировавшей. Медикаментозное лечение подразумевает назначение диуретиков (мочегонных средств), а также препаратов группы бета-блокаторов и ингибиторов АПФ.
Показан индивидуально подобранный спектр умеренных физических нагрузок. Хирургическое лечение для устранения собственно застойной печени не применяется.
Лечение бывает успешным при правильном распознавании основного заболевания, которое привело к сердечной недостаточности, и проведении соответствующей каузальной терапии. Больным ограничивают двигательные нагрузки, потребление жидкости и поваренной соли.
При недостаточной эффективности общих мероприятий применяют внутрь сердечные гликозиды, длительно или постоянно (дигоксин, дигитоксин, изоланид, целанид, ацетилдигитоксин, настой адониса), тиазиды (фуросемид, бринальдикс, гипотиазид, юринекс, буринекс, урегит и др.) и калийсберегающие диуретики (триамтерен, триампур, амилорид, модуретик, верошпирон). Выбор мочегонного препарата и способ его применения определяются степенью отечного синдрома, стадией сердечной недостаточности и переносимостью.
Назначают также препараты, улучшающие обмен в миокарде,- анаболические стероиды (нероболил, ретаболил и др.), АТФ, витамины группы В, С, Е.
При наличии цианоза показана оксигенотерапия, при тяжелых нарушениях ритма — противоаритмическое лечение. Многие больные нуждаются в седативной терапии.
И.И.Гoнчapик
Нарушение функции печени и аномалии сердечно-сосудистой системы в детском возрасте
У детей с сердечной недостаточностью и «синими» пороками сердца выявляют нарушение функции печени. Гипоксемия, венозный застой и сниженный сердечный выброс приводят к увеличению протромбинового времени, повышению уровня билирубина и активности трансаминаз сыворотки. Наиболее выраженные изменения обнаруживают при сниженном сердечном выбросе. Функция печени тесно связана с состоянием сердечно-сосудистой системы.
Печень при констриктивном перикардите
У больных с констриктивным перикардитом обнаруживают клинические и морфологические признаки синдрома Бадда-Киари.
Из-за значительного уплотнения печёночная капсула приобретает сходство с сахарной глазурью («глазурная печень» — «Zuckergussleber»). При микроскопическом исследовании выявляют картину сердечного цирроза.
Желтуха отсутствует. Печень увеличена, уплотнена, иногда определяется её пульсация. Имеется выраженный асцит.
Необходимо исключить цирроз печени и обструкцию печёночных вен в качестве причины асцита. Диагностику облегчает наличие у больного парадоксального пульса, пульсации вен, обызвествлений перикарда, характерных изменений при эхокардиографии, электрокардиографии и катетеризации сердца.
Лечение направлено на устранение сердечной патологии. У больных, перенёсших перикардэктомию, прогноз благоприятный, однако восстановление функции печени происходит медленно. В течение 6 мес после успешной операции отмечается постепенное улучшение функциональных показателей и уменьшение размеров печени. Нельзя ожидать полного обратного развития сердечного цирроза, однако фиброзные септы в печени истончаются и становятся аваскулярными.
Источник
