Ушко левого предсердия инсульт

Фибрилляция предсердий (мерцательная аритмия) – форма тахикардии, вероятность которой значительно возрастает с возрастом. Эта патология опасна в том числе потому, что из-за нелинейного потока крови в левом предсердии могут формироваться тромбы, которые с током крови могут достичь сосудов головного мозга и вызвать ишемический инсульт.
Факты:
- Пациенты с мерцательной аритмией находятся в группе риска по поводу возникновения ишемического инсульта
- Каждый 5-й инсульт связан с мерцательной аритмией. Кроме того, инсульт может возникнуть как у пациентов с пароксизмальной формой мерцательной аритмии, так и с постоянной формой.
- Чем старше пациент, тем выше риск инсульта. Так, в 70-79 лет риск инсульта 25%, старше 80 лет – 32,8%.
- 90% инсультов у пациентов с мерцательной аритмией связаны с тромбообразованием в ушке левого предсердия и лишь у 10% – другая причина.
- Приём антикоагулянтов (препаратов, разрежающих кровь) позволяет снизить риск возникновения инсульта на 70%.
К сожалению, у около 10% пациентов возникают побочные эффекты на приём антикоагулянтов. Наиболее грозным побочным эффектом является кровотечение (носовые кровотечения, кровотечения из желудочно-кишечного тракта, мочевых путей и др.). Чем старше пациент и чем больше у него сопутствующих заболеваний (гипертоническая болезнь, сахарный диабет, заболевания почек и печени, язвенная болезнь желудка) – тем больший риск возникновения у него кровотечения на фоне приёма антикоагулянтов.
Другой проблемой с приёмом одного из антикоагулянтов – ВАРФАРИНА – является необходимость постоянного контроля эффективности “разжижения” крови, так называемое МНО (международное нормализованное отношение), что необходимо контролировать 1-2 раза в месяц. У некоторых пациентов не получается удерживать МНО на стабильном целевом уровне 2,5-3.
А ещё есть категория пациентов, у которых несмотря на приём антикоагулянтов, нормальные значения МНО и отсутствие видимого тромба в ушке левого предсердия происходит несколько повторных инсультов. Микротромбы, являющиеся причиной таких инсультов, “прячутся” в складках ушка левого предсердия.
Всем этим пациентам с мерцательной аритмией, которым противопоказан приём антикоагулянтов, у которых есть кровотечения на приём препаратом или у которых нестабильные значения МНО или возникают инсульты несмотря на приём препаратов , показано ЗАКРЫТИЕ УШКА ЛЕВОГО ПРЕДСЕРДИЯ (как источника тромбообразования). Ещё одним показанием к закрытию ушка левого предердия может быть отказ пациента принимать антикоагулянты по любым причинам.
В нашем отделении процедура закрытия ушка левого предсердия проводится под контролем УЗИ и рентгена через сосуды бедра с помощью специального устройства – окклюдера.
Видео 1: процесс имплантации окклюдера в ушко левого предсердия
Устройство представляет собой зонтик и диск (рис. 1), оба из нитинола (сплав элементов титана и никеля), который является немагнитным металлом. Так пациентам с имплантированным окклюдером разрешается проводить МРТ по медицинским показаниям (до 3 Тл). Также нитинол владеет “эффектом памяти формы”, что позволяет сложить его в тоненькую трубочку и завести через сосуды бедра в камеры сердца. После введения окклюдера из доставляющей трубочки, благодаря описанному выше эффекту, он приобретает заданную производителем форму. Во время проведения операции в ушко левого предсердия вводится катетер, через который вводится контрастное вещество. Контрастирование ушка позволяет выучить его анатомию и выбрать размер и форму окклюдера. Дальше зонтик окклюдера располагают в полости ушка, а диск прикрывает вход в ушко. Процедура длится около часа. На следующий день, как правило, пациента выписывают домой.

Рис. 1: окклюдер для закрытия ушка левого предсердия
Реабилитация: Через шесть месяцев окклюдер покрывается собственными клеточками сердца – происходит так называемый процесс эндотелизации. С момента окончания эндотелизации (в среднем 6 месяцев) пациент может полностью отказаться от приёма антикоагулянтов.
Подбор антикоагулянтов в послеоперационном периоде для каждого пациента проводится индивидуально. Большинство пациентов принимают варфарин, ксарелто или прадаксу ещё 45 дней после имплантации окклюдера с целью профилактики тромбообразования на нём. Пациентам с кровотечениями на приём вышеуказанных препаратов предлагают комбинацию аспирина и клопидогреля или подбирают лекарства индивидуально. Через 45 дней после процедуры ОБЯЗАТЕЛЬНО проводится транспищеводное УЗИ для контроля положения окклюдера. Дальше до 6 месяцев после имплантации пациенты принимают комбинацию аспирина с клопидогрелем. Через 6 месяцев по окончанию периода эндотелизации проводится повторный контроль положения импланта на транспищеводном УЗИ.
Итак, мы ждём Вас, если у Вас мерцательная аритмия и:
- У Вас противопоказания к приёму антикоагулянтов
- У Вас возникло кровотечение на приём антикоагулянтов
- Вы принимаете ВАРФАРИН, и Вашему кардиологу не удаётся подобрать адекватную дозу препарата из-за нестабильного МНО.
- У Вас случился инсульт, несмотря на приём ВАРФАРИНА, ПРАДАКСЫ или КСАРЕЛТО и нет тромбов в ушке левого предсердия.
- Или по любым причинам Вы отказываетесь принимать антикоагулянты.
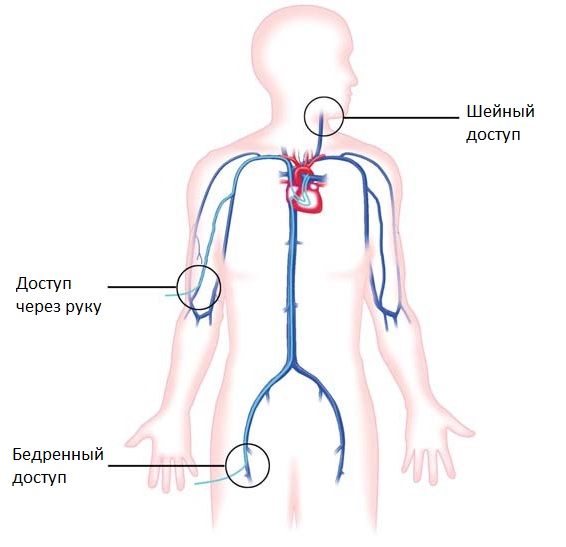
Операции на сердце проводятся доступом через сосуды под контролем рентгеновских лучей специальными миниатюрными инструментами. Благодаря этому методу пороки сердца исправляются без разреза грудной клетки, без применения искусственного кровообращения и остановки сердца, без глубокого наркоза. Для доступа используются сосуды бедра, шеи или руки. После пункции сосуда в отверстие вводятся миниатюрные инструменты (катетеры, баллоны, стенты, спирали, окклюдеры и другие), с помощью которых и проводятся вмешательства.
Читать подробнее
В настоящее время рентгенэндоваскулярная хирургия привлекает к себе все больше и больше внимания практически всех СМИ, включая печатные издания, интернет и телевидение. Мы ежедневно сталкиваемся с массивным потоком информации, посвященной различным аспектам этой современной области медицины. Ежедневно о ней пишут и говорят но, к сожалению, не все и не всегда объективно. Есть множество ошибочных утверждений, слухов или даже мифов, которые необходимо исправить с помощью фактической информации.
Миф 1. Это очень новая, практически экспериментальная область сердечнососудистой хирургии.
Это не так! Эндоваскулярная хирургия имеет богатую историю и уже давно широко используется в медицинской практике. Впервые катетеризация сердца выполнена в 1929 году Р. Форсманом (Германия), за что в 1956 году получил Нобелевскую премию. В 1964 году проведена первая баллонная ангиопластика и с тех пор эндоваскулярная хирургия перестала быть сугубо диагностической областью медицины. Далее открытия и изобретения устройств следовали одно за одним: 1975 год – спирали, 1976 год – окклюдеры, 1979 год – эмболы, 1986 год – коронарные стенты, 1994 год – стенты для крупных сосудов, 2005 год – эндоваскулярные клапаны сердца! На сегодняшний день все вышеперечисленные устройства эволюционировали до более совершенных аналогов. Самым распространенным окклюдером в мире стал окклюдер Амплацера – более полумиллиона имплантаций с 1995 года. В Институте Амосова окклюдеры Амплацера их аналоги ставят с 2003 года. Тенденция в мире такова, что диагностика переместилась из рентгеноперационной в кабинеты эхокардиографии и компьютерной томографии, а лечение пороков сердца переместилось из операционной в рентгеноперационную. В развитых странах мира (США, Канада, Австралия, Европа) боталловы протоки, дефекты перегородок, и коарктации аорты практически не оперируют хирургически. В нашем институте учитываются все современные мировые тенденции при лечении пациентов.
Миф 2. Устройства, с помощью которых происходит лечение пороков (окклюдеры, спирали, стенты) являются инородными телами и могут отторгаться.
Все эти устройства выполнены из современных высокотехнологичных биосовместимых материалов, которые не вызывают реакций отторжения. Через полгода после операции эти устройства полностью покрываются эндотелием (прорастают своими клетками) и не отличаются от внутренней поверхности сердца. Все устройства немагнитные, после их имплантации пациенту может быть выполнено МРТ. Они не издают звуковых сигналов на металлодетекторах в аэропорту, торговом центре и т.д.
Миф 3. Окклюдеры смещаются (улетают).
Действительно, в нашей и мировой практике такие случаи случаются, однако частота их около 1%. Осложнение неприятное, но не критическое. Не было ни одного случая в мире, когда сместившийся окклюдер привел бы к летальному исходу. Как правило, такой окклюдер извлекают эндоваскулярно и устанавливают повторно или заменяют на больший. Наибольшее количество смещений приходится на первые часы или дни после операции, когда пациент еще находиться в клинике. Далее вероятность этого резко снижается, отдаленные смещения являются казуистическими.
Миф 4. Дефекты межпредсердной перегородки с отсутствием края или истонченными краями не подлежат эндоваскулярному закрытию.
Отсутствие аортального края перегородки не является противопоказанием к постановке окклюдера. То же касается и истонченной или аневризматической перегородки. Помните, что обычная (трансторакальная) эхокардиография не дает полной картины о дефекте. Даже если ставиться диагноз отсутствие края, это не означает, что его там нет. О четкой анатомии дефекта можно судить лишь после проведения транспищеводной эхокардиографии, которая является золотым стандартом при отборе пациентов для эндоваскулярного лечения.
Миф 5. Окклюдеры со временем требуют замены.
Ни с ростом пациента, ни со временем замена устройства не нужна. Окклюдер уже через 6 месяцев врастает в перегородку и создает основу для ее дальнейшего роста. В случае стентирования сосудов, возможно эндоваскулярное увеличение просвета стента с ростом сосуда без замены импланта.
Миф 6. Это дорого…
Эндоваскулярная хирургия это высокие технологии, которые действительно стоят дороже обычных операций. В ряде случаев устройство для имплантации покупает пациент, однако существует очередь на бесплатные импланты, которые закупает институт. К тому же мы сотрудничаем с многочисленными фондами помощи, которые за относительно небольшое время собирают средства для приобретения устройств для детей. В большинстве случаев срочности в операции нет, и пациенты имеют достаточно времени, чтобы собрать средства на имплант, подождать своей очереди или найти спонсора. Поэтому, если больной желает оперироваться эндоваскулярно, преград для этого на сегодняшний день не существует.
– Как долго я буду лежать в больнице?
Среднее время пребывания в стационаре 3-4 дня. Как правило, в день поступления утром вы проходите обследование, включающее в себя клинический и биохимический анализ крови (приезжать нужно натощак), делаете рентгеновский снимок, ЭКГ, ультразвуковое исследование сердца и консультацию кардиолога и кардиохирурга. Если все показатели в норме, на следующий день проводится операция по устранению порока. На третий день мы проводим контрольные исследования и выписываем Вас.
+ Какие документы нужны для госпитализации?
Для госпитализации в наш стационар вам понадобится паспорт или свидетельство о рождении ребенка.
Если пациент детского возраста, нужна справка о санэпидокружении (о том, что в последнее время ребенок не контактировал с инфицированными больными), которую вы получите в поликлинике по месту жительства.
Желательно иметь при себе предыдущие консультативные заключения, ЭКГ и рентгеновский снимок органов грудной.
Направление от кардиолога по месту жительства НЕ ТРЕБУЕТСЯ. Вы можете приехать на консультацию и последующее лечение в порядке самообращения. Если Вам более 30 лет или вы ощущали перебои в работе сердца, желательно провести холтеровское мониторирование по месту жительства. Такое исследование можно провести и у нас, но это увеличит Ваше время пребывания в стационаре на 1-2 дня.
Если вы страдаете хроническим гастритом, язвенной болезнью желудка или двенадцатиперстной кишки необходимо сделать фиброгастродуоденоскопию. В случае подтверждения заболевания, Вам необходимо пройти курс лечения по месту жительства. Такое исследование можно провести и у нас, но это увеличит Ваше время пребывания в стационаре на 1-2 дня в случае отсутствия язв и эррозий.
+ Сколько длится операция?
Как правило, длительность операции в пределах 1-1,5часа. Но при сложных анатомических вариантах время операции может увеличится.
+ Какой вид анестезии применяется при эндоваскулярной хирургии?
Всем взрослым пациентам операция проводится под местной анестезией. Пациент может наблюдать за ходом операции и общаться с персоналом. Исключение составляют пациенты с дефектом межпредсердной перегородки, которым во время операции требуется контроль транспищеводного УЗИ и для комфорта пациента операция проводится в состоянии медикаментозного сна. Все эндоваскулярные операции у детей и мнительных пациентов проводятся под общей анестезией.
+ Будет ли мне больно?
Самый неприятный момент – это укол местного анестетика в паховую область. Затем болевая чувствительность полностью исчезает.
+ Как приживаются имплантированные устройства?
Через 3-6 месяцев имплантированные устройства полностью прорастают своими клетками – покрываются эндотелием и их уже не отличить от внутренней поверхности сердца. Все устройства выполнены из высокотехнологичного медицинского сплава, который не вызывает реакций отторжения или аллергических реакций.
+ Можно ли делать КТ и МРТ после установки импланта?
Да, на КТ ограничений нет. На МРТ производители имплантов гарантируют безопасность при 1,5 и 3 Тесла. Перед обследованием обязательно сообщите радиологу о том, что у Вас установлен внутрисердечный имплант.
+ Как себя вести после эндоваскулярной операции?
Необходимо ограничить сильную физическую нагрузку на 6 месяцев. Необходима профилактика респираторных инфекций, тонзиллита, кариеса. В случае, если заболевание начало развиватьс я, в схему лечения нужно включить антибактериальные препараты, после консультации с врачом. В течении первого месяца после операции необходимо также ограничить половую жизнь.
Источник
Около 30–40% ишемических инсультов (ИИ) развивается по неизвестным причинам [1, 2]. Недавно обнаружили связь между биомаркерами дисфункции предсердия, или предсердной кардиопатии, с риском развития эмболического инсульта даже при отсутствии фибрилляции предсердий (ФП), что позволяет предположить необязательность наличия ФП для развития тромбоэмболии из левого предсердия – ЛП [3].
Наиболее часто тромбы в ЛП формируются в его ушке (УЛП), но параметры дисфункции УЛП, такие как скорость кровотока в УЛП и форма УЛП, редко используют в прогнозировании риска развития ИИ.
В настоящей работе мы изучили литературные данные об ассоциации дисфункции УЛП и ИИ с акцентом на пациентов с необъяснимым, или криптогенным инсультом (КИ).
Криптогенный инсульт
Ежегодно в Соединенных Штатах приблизительно у 200 тыс. человек развивается КИ [1, 2]. Традиционно инсульт классифицировали как криптогенный, т.е. вариант инсульта неустановленного происхождения, если при первоначальном обследовании при инсульте не находили причину его развития независимо от объема проведенного обследования (исчерпывающее, традиционное или неполное) [4]. В последнее время исследователи стали использовать термин эмболический инсульт с неопределенным источником по отношению к нелакунарным инфарктам, появляющимся в отсутствие определенных идентифицируемых механизмов развития инсульта высокого риска, таких как ФП, пороки сердца или стеноз крупной артерии [5]. Концепцию, согласно которой причиной развития таких инфарктов является удаленный источник эмболии, поддерживают результаты банка данных Национального института неврологических расстройств и инсульта, свидетельствующие об обнаружении незарегистрированных сердечных или аортальных источников эмболии приблизительно у двух третей пациентов с КИ при проведении последующего обследования [2]. Одним из самых распространенных механизмов, который выявляют при последующем обследовании при КИ, является пароксизмальная ФП, встречающаяся у ≤30% пациентов с КИ при амбулаторном мониторинге ритма сердца [6, 7].
Тем не менее причина развития более половины КИ остается загадкой даже после длительного мониторинга ритма сердца. Для оптимизации стратегий вторичной профилактики развития инсульта большое значение имеет выявление других причин эмболии, особенно тех, для лечения которых необходимы антикоагулянты.
Связь между левым предсердием и инсультом
ФП с характерным внутриполостным застоем крови в условиях нерегулярного сокращения стенок предсердий уже давно считали прямым механистическим объяснением тромбоэмболии из ЛП. Такой механизм согласуется с выводами многочисленных рандомизированных клинических испытаний о том, что лечение антикоагулянтами приводит к снижению риска развития ИИ при ФП [8]. Однако существует проблема в выявлении эпизодов пароксизмальной ФП, особенно при их субклиническом течении.
В испытание Asymptomatic AF and Stroke Evaluation in Pacemaker Patients and the AF Reduction Atrial Pacing Trial (ASSERT) зачислили пациентов в возрасте ≥65 лет с артериальной гипертензией и без ФП в анамнезе. Результаты этого испытания показали, что эпизоды субклинической ФП выявили у ≈35% пациентов через 2,5 года, и только у 16% пациентов были клинические проявления ФП. Субклиническая ФП была ассоциирована с риском развития инсульта (отношение рисков 2,50; 95% доверительный интервал [ДИ] от 1,28 до 4,89; р=0,008) [9]. Важно, что отметили отсутствие временны’х отношений между ФП и инсультом, при этом у многих пациентов ФП впервые выявляли после развития у них инсульта [10], что оспаривает концепцию о наличии ФП самой по себе как необходимой и достаточной причины развития инсульта у пациентов с такой аритмией.

Недавно обнаружили ассоциацию между биомаркерами дисфункции предсердий, или предсердной кардиопатии и инсультом независимо от наличия ФП. Было показано, что N-концевой пептид промозгового натрийуретического пептида является маркером дисфункции предсердий, повышенного риска развития ФП [11] и кардиоэмболии [12, 13]. ЭКГ-признаки дисфункции ЛП, такие как пароксизмальная наджелудочковая тахикардия и высокий зубец Р в отведении V1 (PTFV1), были ассоциированы с риском развития инсульта [14, 15], в частности его нелакунарных вариантов [16] даже при отсутствии ФП. Кроме того, увеличение размера ЛП, по результатам эхокардиографии (ЭКГ), было ассоциировано с повышенным риском развития ИИ [17] и повторных ишемических эмболических инсультов [18], снова независимо от наличия ФП. В совокупности эти данные позволяют предположить, что маркеры патологии и дисфункции ЛП могут иметь большое значение в понимании патогенеза инсульта.
Ушко левого предсердия в качестве зоны образования тромбов при фибрилляции предсердий
УЛП является остатком эмбрионального ЛП, тогда как ЛП с гладкими стенками развивается из первич…
- Petty G.W., Brown R.D., Jr., Whisnant J.P., Sicks J.D., O’Fallon W.M., Wiebers D.O. Ischemic stroke subtypes: a population-based study of incidence and risk factors. Stroke. 1999;30:2513–2516. doi: 10.1161/01.STR.30.12.2513.
- Sacco R.L., Ellenberg J.H., Mohr J.P., Tatemichi T.K., Hier D.B., Price T.R., et al. Infarcts of undetermined cause: the NINCDS Stroke Data Bank. AnnNeurol. 1989;25:382–390. doi: 10.1002/ana.410250410.
- Kamel H., Okin P.M., Longstreth W.T., Jr, Elkind M.S., Soliman E.Z. Atrial cardiopathy: a broadened concept of left atrial thromboembolism beyond atrial fibrillation. Future Cardiol. 2015;11:323–331. doi: 10.2217/fca.15.22.
- Yaghi S., Elkind M.S. Cryptogenic stroke: A diagnostic challenge. Neurol Clin Pract. 2014;4:386–393. doi: 10.1212/CPJ.0000000000000086.
- Hart R.G., Diener H.C., Coutts S.B., Easton J.D., Granger C.B., O’Donnell M.J., et al; Cryptogenic Stroke/ESUS International Working Group. Embolic strokes of undetermined source: the case for a new clinical construct. Lancet Neurol. 2014;13:429–438. doi: 10.1016/S1474–4422(13)70310-7.
- Sanna T., Diener H.C., Passman R.S., Di Lazzaro V., Bernstein R.A., Morillo C.A., et al; CRYSTAL AF Investigators. Cryptogenic stroke and underlying atrial fibrillation. N Engl J Med. 2014;370:2478–2486. doi: 10.1056/NEJMoa1313600.
- Gladstone D.J., Spring M., Dorian P., Panzov V., Thorpe K.E., Hall J., et al; EMBRACE Investigators and Coordinators. Atrial fibrillation in patients with cryptogenic stroke. N Engl J Med. 2014;370:2467–2477. doi:10.1056/NEJMoa1311376.
- Goldstein L.B., Bushnell C.D., Adams R.J., Appel L.J., Braun L.T., Chaturvedi S., et al; American Heart Association Stroke Council; Council on Cardiovascular Nursing; Council on Epidemiology and Prevention; Council for High Blood Pressure Research, Council on Peripheral Vascular Disease, and Interdisciplinary Council on Quality of Care and Outcomes Research. Guidelines for the primary prevention of stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2011;42:517–584. doi: 10.1161/STR.0b013e3181fcb238.
- Healey J.S., Connolly S.J., Gold M.R., Israel C.W., Van Gelder I.C., Capucci A., et al; ASSERT Investigators. Subclinical atrial fibrillation and the risk of stroke. N Engl J Med. 2012;366:120–129. doi: 10.1056/NEJMoa1105575.
- Brambatti M., Connolly S.J., Gold M.R., Morillo C.A., Capucci A., Muto C., et al; ASSERT Investigators. Temporal relationship between subclinical atrial fibrillation and embolic events. Circulation. 2014;129:2094–2099. doi: 10.1161/CIRCULATIONAHA.113.007825.
- Sinner M.F., Stepas K.A., Moser C.B., Krijthe B.P., Aspelund T., Sotoodehnia N., et al. B-type natriuretic peptide and C-reactive protein in the prediction of atrial fibrillation risk: the CHARGE-AF Consortium of community-based cohort studies. Europace. 2014;16:1426–1433. doi: 10.1093/europace/euu175.
- Folsom A.R., Nambi V., Bell E.J., Oluleye O.W., Gottesman R.F., Lutsey P.L., et al. Troponin T, N-terminal pro-B-type natriuretic peptide, and incidence of stroke: the atherosclerosis risk in communities study. Stroke. 2013;44:961–967. doi: 10.1161/STROKEAHA.111.000173.
- Cushman M., Judd S.E., Howard V.J., Kissela B., Gutiйrrez O.M., Jenny N.S., et al. N-terminal pro-B-type natriuretic peptide and stroke risk: the reasons for geographic and racial differences in stroke cohort. Stroke. 2014;45:1646–1650. doi: 10.1161/STROKEAHA.114.004712.
- Kamel H., Elkind M.S., Bhave P.D., Navi B.B., Okin .PM., Iadecola C., et al. Paroxysmal supraventricular tachycardia and the risk of ischemic stroke. Stroke. 2013;44:1550–1554. doi: 10.1161/STROKEAHA.113.001118.
- Kamel H., Soliman E.Z., Heckbert S.R., Kronmal R.A., Longstreth W.T., Jr., Nazarian S., et al. P-wave morphology and the risk of incident ischemic stroke in the Multi-Ethnic Study of Atherosclerosis. Stroke. 2014;45:2786–2788. doi: 10.1161/STROKEAHA.114.006364.
- Kamel H., O’Neal W.T., Okin P.M., Loehr L.R., Alonso A., Soliman E.Z. Electrocardiographic left atrial abnormality and stroke subtype in atherosclerosis risk in communities study. Ann Neurol. 2015. doi: 10.1002/ana.24482.
- Di Tullio M.R., Sacco R.L., Sciacca R.R., Homma S. Left atrial size and the risk of ischemic stroke in an ethnically mixed population. Stroke. 1999;30:2019–2024.
- Yaghi S., Moon Y.P., Mora-McLaughlin C., Willey J.Z., Cheung K., Di Tullio M.R., et al. Left atrial enlargement and stroke recurrence: the Northern Manhattan Stroke Study. Stroke. 2015;46:1488–1493. doi: 10.1161/STROKEAHA.115.008711.
- Al-Saady NM, Obel OA, Camm AJ. Left atrial appendage: structure, function, and role in thromboembolism. Heart. 1999;82:547–554.
- Davis C.A .III, Rembert J.C., Greenfield J.C., Jr. Compliance of left atrium with and without left atrium appendage. Am J Physiol. 1990;259(4 pt 2): H1006–H1008.
- Chapeau C., Gutkowska J., Schiller P.W., Milne R.W., Thibault G. Garcia R., et al. Localization of immunoreactive synthetic atrial natriuretic factor (ANF) in the heart of various animal species. J Histochem Cytochem. 1985;33:541–550.
- Stoddard M.F. Dawkins P.R., Prince C.R., Ammash N.M. Left atrial appendage thrombus is not uncommon in patients with acute atrial fibrillation and a recent embolic event: a transesophageal echocardiographic study. J Am Coll Cardiol. 1995;25:452–459.
- Blackshear J.L., Odell J.A. Appendage obliteration to reduce stroke in cardiac surgical patients with atrial fibrillation. Ann Thorac Surg. 1996;61:755–759. doi: 10.1016/0003-4975(95)00887-X.
- Brott T.G. Novel approaches to stroke prevention in atrial fibrillation: introduction. Stroke. 2007;38(2 suppl):614. doi: 10.1161/01. STR.0000255982.72103.7f.
- Romero J., Cao J.J., Garcia M.J., Taub C.C. Cardiac imaging for assessment of left atrial appendage stasis and thrombosis. Nat Rev Cardiol. 2014;11:470–480. doi: 10.1038/nrcardio.2014.77.
- Beigel R., Wunderlich N.C., Ho S.Y., Arsanjani R., Siegel R.J. The left atrial appendage: anatomy, function, and noninvasive evaluation. JACC Cardiovasc Imaging. 2014;7:1251–1265. doi: 10.1016/j.jcmg.2014.08.009.
- Veinot J.P., Harrity P.J., Gentile F., Khandheria B.K., Bailey K.R., Eickholt J.T., et al. Anatomy of the normal left atrial appendage: a quantitative study of age-related changes in 500 autopsy hearts: implications for echocardiographic examination. Circulation. 1997;96:3112–3115.
- Yamamoto M., Seo Y., Kawamatsu N., Sato K., Sugano A., Machino-Ohtsuka T., et al. Complex left atrial appendage morphology and left atrial appendage thrombus formation in patients with atrial fibrillation. Circ Cardiovasc Imaging. 2014;7:337–343. doi: 10.1161/CIRCIMAGING.113.001317.
- Petersen M., Roehrich A., Balzer J., Shin D.I., Meyer C., Kelm M., et al. Left atrial appendage morphology is closely associated with specific echocardiographic flow pattern in patients with atrial fibrillation. Europace. 2015;17:539–545. doi: 10.1093/europace/euu347.
- Di Biase L., Santangeli P., Anselmino M., Mohanty P., Salvetti I., Gili S., et al. Does the left atrial appendage morphology correlate with the risk of stroke in patients with atrial fibrillation? Results from a multicenter study. J Am Coll Cardiol. 2012;60:531–538. doi: 10.1016/j.jacc.2012.04.032.
- Jue J., Winslow T., Fazio G., Redberg R.F., Foster E., Schiller N.B. Pulsed Doppler characterization of left atrial appendage flow. J Am Soc Echocardiogr. 1993;6(3 pt. 1):237–244.
- Uretsky S., Shah A., Bangalore S., Rosenberg L., Sarji R., Cantales D.R., et al. Assessment of left atrial appendage function with transthoracic tissue Doppler echocardiography. Eur J Echocardiogr. 2009;10:363–371. doi:10.1093/ejechocard/jen339.
- Fukuda N., Shinohara H., Sakabe K., Onose Y., Nada T., Tamura Y. Transthoracic Doppler echocardiographic measurement of left atrial appendage blood flow velocity: comparison with transoesophageal measurement. Eur J Echocardiogr. 2003;4:191–195.
- Fuster V., Rydйn L.E., Cannom D.S., Crijns H.J., Curtis A.B., Ellenbogen K.A., et al. 2011 ACCF/AHA/HRS focused updates incorporated into the ACC/AHA/ESC 2006 Guidelines for the management of patients with atrial fibrillation: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines developed in partnership with the European Society of Cardiology and in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. J Am Coll Cardiol. 2011;57:e101–e198. doi: 10.1016/j.jacc.2010.09.013.
- Acar J., Cormier B., Grimberg D., Kawthekar G., Iung B., Scheuer B., et al. Diagnosis of left atrial thrombi in mitral stenosis–usefulness of ultrasound techniques compared with other methods. Eur Heart J.1991;12(Suppl. B):70–76.
- Manning W.J., Weintraub R.M., Waksmonski C.A., Haering J.M., Rooney P.S., Maslow A.D., et al. Accuracy of transesophageal echocardiography for identifying left atrial thrombi. A prospective, intraoperative study. Ann Intern Med. 1995;123:817–822.
- Ono M., Asanuma T., Tanabe K., Yoshitomi H., Shimizu H., Ohta Y., et al. Improved visualization of the left atrial appendage by transthoracic 2-dimensional tissue harmonic compared with fundamental echocardiographic imaging. J Am Soc Echocardiogr. 1998;11:1044–1049.
- Sallach J.A., Puwanant S., Drinko J.K., Jaffer S., Donal E., Thambidorai S.K., et al. Comprehensive left atrial appendage optimization of thrombus using surface echocardiography: the CLOTS multicenter pilot trial. J Am Soc Echocardiogr. 2009;22:1165–1172. doi: 10.1016/j.echo.2009.05.028.
- Bellotti P., Spirito P., Lupi G., Vecchio C. Left atrial appendage function assessed by transesophageal echocardiography before and on the day after elective cardioversion for nonvalvular atrial fibrillation. Am J Cardiol. 1998;81:1199–1202.
- Warraich H.J., Gandhavadi M., Manning W.J. Mechanical discordance of the left atrium and appendage: a novel mechanism of stroke in paroxysmal atrial fibrillation. Stroke. 2014;45:1481–1484. doi: 10.1161/STROKEAHA.114.004800.
- Di Biase L., Burkhardt J.D., Mohanty P., Sanchez J., Mohanty S., Horton R., et al. Left atrial appendage: an underrecognized trigger site of atrial fibrillation. Circulation. 2010;122:109–118. doi: 10.1161/CIRCULATIONAHA.109.928903.
- Fatkin D., Kelly R.P., Feneley M.P. Relations between left atrial appendage blood flow velocity, spontaneous echocardiographic contrast and thromboembolic risk in vivo. J Am Coll Cardiol. 1994;23:961–969.
- Kamalesh M., Copeland T.B., Sawada S. Severely reduced left atrial appendage function: a cause of embolic stroke in patients in sinus rhythm? J Am Soc Echocardiogr. 1998;11:902–904.
- Lee J.M., Shim J., Uhm J.S., Kim Y.J., Lee H.J., Pak H.N., et al. Impact of increased orifice size and decreased flow velocity of left atrial appendage on stroke in nonvalvular atrial fibrillation. Am J Cardiol. 2014;113:963–969. doi: 10.1016/j.amjcard.2013.11.058.
- Goldman M.E., Pearce L.A., Hart R.G., Zabalgoitia M., Asinger R.W., Safford R., et al. Pathophysiologic correlates of thromboembolism in nonvalvular atrial fibrillation: I. Reduced flow velocity in the left atrial appendage (The Stroke Prevention in Atrial Fibrillation
- Lee J.M., Seo J., Uhm J.S., Kim Y.J., Lee H.J., Kim J.Y., et al. Why is left atrial appendage morphology related to strokes? An analysis of the flow velocity and orifice size of the left atrial appendage. J Cardiovasc Electrophysiol. 2015. doi: 10.1111/jce.12710.
- Kimura T., Takatsuki S., Inagawa K., Katsumata Y., Nishiyama T., Nishiyama N., et al. Anatomical characteristics of the left atrial appendage in cardiogenic stroke with low CHADS2 scores. Heart Rhythm. 2013;10:921–925. doi: 10.1016/j.hrthm.2013.01.036.
- Anselmino M., Scaglione M., Di Biase L., Gili S., Santangeli P., Corsinovi L., et al. Left atrial appendage morphology and silent cerebral ischemia in patients with atrial fibrillation. Heart Rhythm. 2014;11:2–7. doi:10.1016/j.hrthm.2013.10.020.
- Khurram I.M., Dewire J., Mager M., Maqbool F., Zimmerman S.L., Zipunnikov V., et al. Relationship between left atrial appendage morphology and stroke in patients with atrial fibrillation. Heart Rhythm. 2013;10:1843–1849. doi: 10.1016/j.hrthm.2013.09.065.
- Akoum N, Marrouche N. Assessment and impact of cardiac fibrosis on atrial fibrillation. Curr Cardiol Rep. 2014;16:518. doi: 10.1007/s11886-014-0518-z.
- Fukushima K., Fukushima N., Kato K., Ejima K., Sato H., Fukushima K., et al. Correlation between left atrial appendage morphology and flow velocity in patients with paroxysmal atrial fibrillation. Eur Heart J Cardiovasc Imaging. 2015.
- Kishima H., Mine T., Ashida K., Sugahara M., Kodani T., Masuyama T. Does left atrial appendage morphology influence left atrial appendage flow velocity? Circ J. 2015;79:1706–1711. doi: 10.1253/circj. CJ-14-1380.
- Akoum N., Fernandez G., Wilson B., Mcgann C., Kholmovski E., Marrouche N. Association of atrial fibrosis quantified using LGE-MRI with atrial appendage thrombus and spontaneous contrast on transesophageal echocardiography in patients with atrial fibrillation. J Cardiovasc Electrophysiol. 2013;24:1104–1109. doi: 10.1111/jce.12199.
- Di Biase L., Santangeli P., Gaita F., Natale A. Reply: To PMID 22858289. J Am Coll Cardiol. 2013;61:690–691. doi: 10.1016/j.jacc.2012.10.039.
- Reddy V.Y., Doshi S.K., Sievert H., Buchbinder M., Neuzil P., Huber K., et al; PROTECT AF Investigators. Percutaneous left atrial appendage closure for stroke prophylaxis in patients with atrial fibrillation: 2.3-year followup of the PROTECT AF (Watchman Left Atrial Appendage System for Embolic Protection in Patients with Atrial Fibrillation) Trial. Circulation. 2013;127:720–729. doi: 10.1161/CIRCULATIONAHA.112.114389.
- Reddy V.Y., Sievert H., Halperin J., Doshi S.K., Buchbinder M., Neuzil P., et al; PROTECT AF Steering Committee and Investigators. Percutaneous left atrial appendage closure vs warfarin for atrial fibrillation: a randomized clinical trial. JAMA. 2014;312:1988–1998. doi: 10.1001/jama.2014.15192.
- Kernan W.N., Ovbiagele B., Black H.R., Bravata D.M., Chimowitz M.I., Ezekowitz M.D., et al; American Heart Association Stroke Council, Council on Cardiovascular and Stroke Nursing, Council on Clinical Cardiology, and Council on Peripheral Vascular Disease. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke. 2014;45:2160–2236. doi: 10.1161/STR.0000000000000024.
- Mohr J.P., Thompson J.L., Lazar R.M., Levin B., Sacco R.L., Furie K.L., et al; Warfarin-Aspirin Recurrent Stroke Study Group. A comparison of warfarin and aspirin for the prevention of recurrent ischemic stroke. N Engl J Med. 2001;345:1444–1451. doi: 10.1056/NEJMoa011258.
- Longstreth W.T., Jr., Kronmal R.A., Thompson J.L., Christenson R.H., Levine S.R., Gross R., et al. Amino terminal pro-B-type natriuretic peptide, secondary stroke prevention, and choice of antithrombotic therapy. Stroke. 2013;44:714–719. doi: 10.1161/STROKEAHA.112.675942.
Источник
