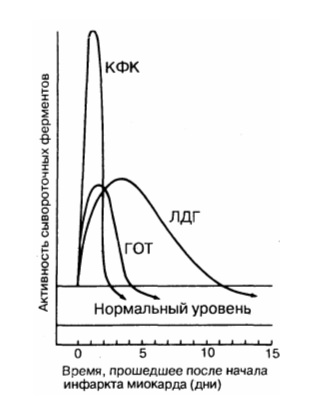
Уровень ферментов в крови при инфаркте миокарда


Для постановки диагноза инфаркта миокарда требуется сочетание типичной боли в сердце (затянувшийся приступ стенокардии), изменений на ЭКГ и анализа крови на ферменты. Кардиоспецифическими являются МВ-фракция креатинфосфокиназа, лактатдегидрогеназа, тропонин, соотношение аминотрасфераз. Этот метод является вспомогательным, он позволяет косвенным образом оценить размер разрушения миокарда и составить прогноз для выздоровления.
Изменение показателей крови при инфаркте
Из-за острого прекращения кровоснабжения сердечной мышцы в организме формируется ответная реакция. Она связана с такими процессами:
- разрушение мышечных клеток;
- проникновение продуктов распада в кровь;
- формирование воспаления вокруг очага инфаркта.
Поэтому, наряду со сбором жалоб, осмотром и аускультацией, ЭКГ, пациентам в обязательном порядке назначается клинический анализ крови и тест на выявление кардиоспецифических ферментов.
Основные лабораторные показатели зависят от обширности повреждения миокарда, наиболее характерными признаками являются:
- повышение содержания лейкоцитов (с первого дня до 7 — 10);
- резкое падение количества эозинофилов;
- незначительное смещение лейкоцитарной формулы влево;
- нарастание СОЭ (через 2 — 4 дня до 2 — 4 недели и дольше).
Эти данные не относятся к специфичным, так как они отражают степень воспалительной реакции на распад мышечной ткани. Поэтому их используют для косвенного определения степени тяжести инфаркта.
Рекомендуем прочитать о заднебазальном инфаркте. Вы узнаете о причинах возникновения, симптомах и диагностике, а также о лечении заднебазального инфаркта миокарда.
А здесь подробнее о лабораторной диагностике инфаркта миокарда.
Какие ферменты считаются кардиоспецифическими
К типичному симптому разрушения миокарда относится нарастание содержания ферментов, они названы кардиоспецифическими, так как содержатся преимущественно в клетках сердца. Для подтверждения диагноза используют ряд тестов, полученные результаты вместе с признаками ЭКГ и характерной болью в сердце составляют классическую триаду острого инфаркта миокарда
Креатинфосфокиназа
Этот фермент содержится в любой мышечной ткани, головном мозге и в клетках щитовидной железы. Поэтому для того, чтобы исключить ошибку при подозрении на некроз сердечной мышцы, исследуют его фракцию МВ. Она возрастает в первые часы после начала инфаркта и достигает пика через 10 часов, после 2-х суток возвращается к физиологическому уровню. Чем больше ее обнаруживают в крови, тем больше зона разрушения.
Лактатдегидрогеназа
Повышается медленнее, чем креатинфосфокиназа, и дольше теряет активность. Наивысшие значения появляются к концу второго дня после тяжелого приступа стенокардии, нормализация происходит к 9 — 10 дню, иногда остается повышенной до двух недель. Причинами нарастания содержания этого фермента также могут быть:
- болезни печени;
- шоковые состояния;
- застой крови при недостаточности кровообращения;
- разрушение эритроцитов;
- воспаления, в том числе и миокардит;
- тромбоэмболия легочных сосудов.
В связи с этим более точно отражает процесс некроза миокарда изофермент – лактатдегидрогеназа 1.
Аспартатаминотранфераза (АсАТ)
Повышается до максимума через сутки или 36 часов, а к концу первой недели возвращается к исходным значениям. Вместе с аланинаминотрасферазой (АлАТ) может увеличиваться при других заболеваниях, в том числе и при патологических изменениях в печени. Поэтому правильнее определять соотношение между этими соединениями – при инфаркте АсАТ/АлАТ превышает 1,33.
Тропонин
Относится к маркеру разрушения поперечнополосатых мышц. Его компонентами являются следующие виды белков: С (связывает кальций), Т (способствует соединению тропомиозина), I (тормозит С и Т). При этом тропонин Т и I находятся в типичных для сердечных клеток формах, что и позволяет их считать абсолютно кардиоспецифическими.
Тропонины появляются спустя 4 часа после образования зоны распада в миокарде и доходят до пика в первые сутки, их можно обнаружить на 7 — 14 день после приступа.
Тест на тропонин является достоверным критерием. На основании большого количества исследований доказано, что появление высокого уровня этого соединения является признаком острого инфаркта, а низкое содержание бывает при нестабильной стенокардии. Этот анализ используют для таких целей:
- установление диагноза в период до 2 недель;
- проведение дифференциальной диагностики со стенокардией;
- оценка размера некроза сердечной мышцы;
- определение прогноза и степени риска осложнений;
- исследование результативности терапии.
Миоглобин
Этот белок отвечает за транспорт кислорода в клетки сердца. Его можно обнаружить не только в миокарде, но и в других мышечных волокнах. Он повышается одним из первых при инфаркте – чаще всего это интервал между 4 и 6 часом после начала острой боли в сердце. Такое нарастание содержания в крови продолжается всего 3 — 4 часа, поэтому его легко пропустить, если не проводить мониторинговые исследования.
Поэтому данный показатель не всегда отражает истинное состояние сердца, а также не удается связать его концентрацию со степенью разрушения клеток.
Как правильно оценить полученные результаты
Для того, чтобы сориентироваться в наличии инфаркта миокарда, а также оценить его величину и давность развития, требуется определить различные показатели, проанализировать сочетание их изменений.
Могут быть следующие клинические ситуации:
- пациент госпитализирован в первые сутки от начала острой боли – нужен анализ МВ-креатинфосфокиназы, даже если на ЭКГ однозначно есть инфаркт, так как можно оценить размер некроза и составить прогноз. Нормальные значения не исключают инфаркт, нужно повторить исследование через сутки;
- больной поступил в период между 1 и 15 днем от начала приступа – проводится исследование лактатдегидрогеназы и соотношения АсАТ/АлАТ;
- если нет типичной боли в сердце и нормальная ЭКГ, то повышения ферментов для постановки диагноза недостаточно;
- рост содержания любого фермента не строго специфичен, но с большей долей вероятности на инфаркт указывает МВ-фракция креатинфосфокиназы и тропонин;
- нормальные показатели крови не исключают формирование острого инфаркта сердечной мышцы.
Рекомендуем прочитать о коронарной недостаточности. Вы узнаете о причинах появления и симптомах заболевания, а также о методах диагностики и лечения коронарной недостаточности.
А здесь подробнее об инфаркте правого желудочка.
Рост кардиоспецифических ферментов в крови связан с разрушением клеток сердца в период развития инфаркта миокарда. Каждый из показателей имеет свою динамику повышения и восстановления исходного уровня. Наиболее характерными именно для мышцы сердца являются МВ-фракция креатинфосфокиназы и компоненты тропонинового комплекса.
При нормальных показателях инфаркт не исключен, а на основании гиперферментемии диагноз не ставится, поэтому анализ крови оценивают только параллельно с клиническими симптомами и электрокардиографическими данными.
Полезное видео
Смотрите на видео о диагностике и лечении инфаркта миокарда:
Источник
Оглавление темы “Лабораторная диагностика инфаркта миокарда.”:
Лабораторные методы диагностики инфаркта миокарда. Ферменты инфаркта миокарда.Помимо клинических данных и ЭКГ, в диагностике инфаркта миокарда существенное значение имеет резорбционно-некротический синдром — неспецифическая реакция миокарда, возникающая вследствие асептического некроза, всасывания продуктов некроза и эндогенной интоксикации. Его критерии: лихорадка, гиперферментемия (ферменты выходят из погибших миоцитов при разрушении их мембран) и изменения общего анализа крови. Верификация инфаркта миокарда базируется на существенном росте уровня кардиоспецифических ферментов в плазме. Весьма важны сроки определения уровня ферментов у больного ИМ. Ферменты «быстрого реагирования», которые выходят в периферический кровоток из зоны некроза: • тропонин-Т (специфический миокардиальный белок, отсутствующий в скелетных мышцах) имеет первый пик роста через 2—3 ч с максимумом через 8—10 ч, и высокий уровень сохраняется на протяжении 4-7 дней. Однократное измерение этого теста через 72 ч может быть показателем распространенности ИМ. Тропониновый тест имеет прогностическое значение: если у больного с НСт нет повышения тропонина (в начале ангинозного приступа и через 12 ч), то у него отсутствует свежий инфаркт миокарда. Обычно для верификации диагноза ИМ достаточно двух исследований тропонина-Т (в отличие от необходимости многократных исследований МВ-КФК и КФК). При мелкоочаговом инфаркте миокарда тропонин начинает повышаться с такой же скоростью, как и МВ-КФК, но возвращается к норме более длительно (до 7—14 дней начального периода).
• изофермент МВ-КФК более специфичен (в высоких концентрациях отмечен только в сердце, но в небольших концентрациях содержится в скелетных мышцах). Уровень менее 10 мкг/л указывает на мелкоочаговый ИМ, а более 10 мкг/л — на крупноочаговый. Чтобы исключить ИМ, МВ-КФК регистрируют каждые 8 ч (нужны минимум 3 отрицательных результата). Оценка МВ-КФК весьма полезна, когда имеется сопутствующее поражение мышц или мозга (в них есть КФК, но нет МВ-КФК); • суммарная КФК (норма – 20-80 усл. ед., или до 1,2 ммоль/л, в СИ) повышается через 4—6 ч (пик через 1—2 суток), а нормализуется на 4-й день. КФК содержится не только в сердце, но и в скелете, мышцах, мозге, потому рост ее может быть обусловлен травмами или болезнями мышц (полимиозит, миопатия); катетеризацией сердца; ИЭ и миокардитом (при которых интервал ST может повышаться во многих отведениях); ЭИТ; длительной иммобилизацией; шоком или алкогольной интоксикацией. Необходимо определять КФК в динамике (3-4 раза). Уровень КФК ее возрастает в ходе первых, суток, сохраняется стабильным в течение 3—4 суток и снижается к 6-7-м суткам. Пиковый уровень КФК (и МВ-КФК) на 2-е сутки после ИМ в большей мере, чем другие сывороточные маркеры, указывает на размер некроза. Ранняя диагностика инфаркта миокарда (6—8 ч от начала) с помощью этих кардиоспецифических тестов важна для «сортировки» больных с наличием боли в грудной клетке, для определения соответствующего лечения вследствие объективных трудностей разграничения кардиальной ишемии от ИМ на основе клинических данных. В целом, исследование биохимических специфических маркеров некроза миокарда весьма важно (особенно, если данные ЭКГ позволяют сомневаться в диагнозе инфаркта миокарда). На основе их величин выделяют ОКС с некрозом (ИМ) и без некроза (НСт). Диагностика кардиоспецифических сывороточных ферментов (находившихся в миокардиоцитах и при их разрушении оказавшихся в кровяном русле) имеет большое значение для верификации ИМ без Q.
Видео урок изменений в анализе крови при инфаркте миокардаПри проблемах с просмотром скачайте видео со страницы Здесь – Также рекомендуем “Трансаминазы при инфаркте миокарда. Лактатдегидрогеназы при инфаркте миокарда.” |
Источник
Что такое АЛАТ анализ крови, и почему ALT увеличивается?
АЛТ-анализ крови – что это? Данное исследование позволяет обнаруживать заболевания на ранних стадиях. В ходе теста проверяется показатель фермента – аланинаминотрансферазы, занимающегося расщеплением амино- и кетокислот. Они, в свою очередь, являются составляющими клеток печени, почек и сердечной мышцы.
В клетках органов находятся ферменты, которые носят общее название – трансаминаза. Повреждение тканей или их разрушение способствует выходу ферментов из клеток. Таким образом, анализы показывают увеличение их уровня.
Для диагностики содержание трансаминазы является очень важным, поскольку помогает выявлять патологии.
Лабораторная диагностика инфаркта миокарда
Лабораторное подтверждение острого инфаркта миокарда основано на выявлении.
• неспецифических показателей тканевого некроза и воспалительной реакции миокарда
• гиперферментемии (входит в классическую триаду признаков острого инфаркта миокарда: болевой синдром; типичные изменения ЭКГ; гиперферментемия)
НЕСПЕЦИФИЧЕСКИЕ ПОКАЗАТЕЛИ ТКАНЕВОГО НЕКРОЗА И ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ МИОКАРДА
Неспецифическая реакция организма на возникновение острого инфаркта миокарда связана прежде всего с.
•распадом мышечных волокон
•всасыванием продуктов расщепления белков в кровь
•местным асептическим воспалением сердечной мышцы, развивающимся преимущественно в периинфарктной зоне
Основными клинико-лабораторными признаками, отражающими эти процессы, являются (выраженность всех приведенных лабораторных признаков инфаркта миокарда прежде всего зависит от обширности очага поражения, поэтому при небольших по протяженности инфарктах эти изменения могут отсутствовать).
• повышение температуры тела от субфебрильных цифр до 38,5–39°С (выявляются обычно к концу первых суток от начала заболевания и при неосложненном течении инфаркта сохраняются примерно в течение недели)
• лейкоцитоз. не превышающий обычно 12–15 х 109/л (выявляются обычно к концу первых суток от начала заболевания и при неосложненном течении инфаркта сохраняются примерно в течение недели)
• анэозинофилия
• небольшой палочкоядерный сдвиг формулы крови влево
• увеличение СОЭ (увеличивается обычно спустя несколько дней от начала заболевания и может оставаться повышенной на протяжении 2-3 недель и дольше даже при отсутствии осложнений инфаркта миокарда)
Правильная трактовка этих показателей возможна только при сопоставлении с клинической картиной заболевания и данными ЭКГ.
. длительное сохранение — более 1 недели — лейкоцитоза или/и умеренной лихорадки у больных острым инфарктом миокарда свидетельствует о возможном развитии осложнений: пневмония, плеврит, перикардит, тромбоэмболия мелких ветвей легочной артерии и др.
ГИПЕРФЕРМЕНТЕМИИЯ
Основной причиной повышения активности и содержания ферментов в сыворотке крови у больных острым инфарктом миокарда является разрушение кардиомиоцитов и выход высвобождающихся клеточных ферментов в кровь.
Наиболее ценным для диагностики острого инфаркта миокарда является определение активности нескольких ферментов в сыворотке крови.
• креатинфосфокиназы (КФК) и особенно ее МВ-фракции (МВ-КФК)
• лактатдегидрогеназы (ЛДГ) и ее изофермента 1 (ЛДГ1)
• аспартатаминотранферазы (АсАТ)
• тропонина
• миоглобина
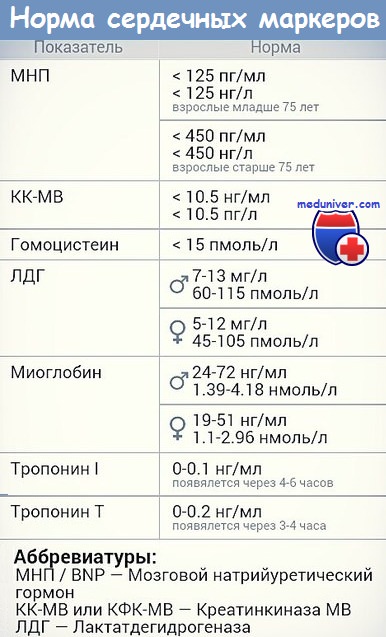
креатинфосфокиназа (КФК) (лабораторная норма 10—110 ME; в единицах Си: 0,60—66 ммоль неорганического фосфора/(ч•л); изоферменты КФК-MB 4—6 % общей КФК)
Специфичным лабораторным тестом острого инфаркта миокарда является определение МВ-фракции КФК (МВ-КФК).
КФК в большом количестве содержится в скелетных мышцах, миокарде, головном мозге и щитовидной железе. Поэтому увеличение активности этого фермента в сыворотке крови возможно не только при остром инфаркте миокарда, но и при целом ряде других клинических ситуаций: при внутримышечных инъекциях; при тяжелой физической нагрузке;
после любого хирургического вмешательства; у больных мышечной дистрофией, полимиозитом, миопатией; при повреждениях скелетных мышц, при травмах, судорожном синдроме, длительной иммобилизации; при инсультах и других повреждениях ткани головного мозга; при гипотиреозе; при пароксизмальных тахиаритмиях; при миокардите; при тромбоэмболии легочной артерии; после проведения коронароангиографии; после электроимпульсной терапии (кардиоверсии) и т. д.
Повышение активности МВ-фракции КФК, содержащейся преимущественно в миокарде, специфично для повреждения сердечной мышцы, в первую очередь, для острого инфаркта миокарда. МВ-фракция КФК не реагирует на повреждение скелетных мышц, головного мозга и щитовидной железы.
.следует помнить — любые кардиохирургические вмешательства, включая коронароангиографию, катетеризацию полостей сердца и электроимпульсную терапию, как правило, сопровождаются кратковременным подъемом активности МВ-фракции КФК; в литературе имеются также указания на возможность повышения уровня МВ-КФК при тяжелой пароксизмальной тахиаритмии, миокардитах и длительных приступах стенокардии покоя, расцениваемых как проявление нестабильной стенокардии
•через 3–4 часа ее активность начинает возрастать
•через 10–12 часов достигает максимума
•через 48 часов от начала ангинозного приступа возвращается к исходным цифрам
Степень повышения активности МВ-КФК в крови в целом хорошо коррелирует с размером инфаркта миокарда — чем больше объем поражения сердечной мышцы, тем выше активность МВ-КФК.
Динамика КФК при остром инфаркте миокарда.
•к концу первых суток уровень фермента в 3–20 раз превышает норму
•через 3–4 суток от начала заболевания возвращается к исходным значениям
.следует помнить — в ряде случаев при обширных инфарктах миокарда вымывание ферментов в общий кровоток замедлено, поэтому абсолютное значение активности МВ-КФК и скорость его достижения могут оказаться меньше, чем при обычном вымывании фермента, хотя и в том, и в другом случае площадь под кривой «концентрация-время» остается одинаковой
лактатдегидрогеназа (ЛДГ) (лабораторная норма — оптический тест до 460 ME (37°) или до 7668 нмоль/(с.л); по реакции с 2,4-динитрофенилгидразином (метод Севела — Товарека) при 37° в норме составляет 220—1100 нмоль/(с.л), или 0.8—4,0 мкмоль/(ч.мл); относительное содержание изоферментов ЛДГ устанавливают методом электрофоретического разделения фермента на пленках из ацетата целлюлозы при рН 8,6; окраску производят формазаном. Изофермент ЛДГ1 обладает наибольшей электрофоретической подвижностью)
Активность ЛДГ при остром инфаркте миокарда нарастает медленнее, чем КФК и МВ-КФК, и дольше остается повышенной.
Динамика ЛДГ при остром инфаркте миокарда.
•через 2–3 суток от начала инфаркта наступает пик активности
•к 8–14 суткам возвращение к исходному уровню
.следует помнить — активность общей ЛДГ повышается также при заболеваниях печени, шоке, застойной недостаточности кровообращения, гемолизе эритроцитов и мегалобластной анемии, тромбоэмболии легочной артерии, миокардите, воспалении любой локализации, коронароангиографии, электроимпульсной терапии, тяжелой физической нагрузке и т. д.
Иизофермент ЛДГ1 более специфичен для поражений сердца, хотя он также присутствует не только в мышце сердца, но и в других органах и тканях, включая эритроциты.
аспартатаминотранфераза (АсАТ) (лабораторная норма 8—40 ед.; в единицах СИ: 0,1—0,45 ммоль/(ч•л))
Динамика АсАТ при остром инфаркте миокарда.
•через 24–36 часа от начала инфаркта относительно быстро наступает пик повышения активности
•через 4–7 суток концентрация АсАТ возвращается к исходному уровню
Изменение активности АсАТ неспецифично для острого инфаркта миокарда: уровень АсАТ вместе с активностью АлАТ повышается при многих патологических состояниях, в том числе при заболеваниях печени.
•при поражениях паренхимы печени в большей степени возрастает активность АлАТ, а при заболеваниях сердца в большей степени возрастает активность АсАТ
•при инфаркте миокарда отношение АсАТ/АлАТ (коэффициент Ритиса) больше 1,33, а при заболеваниях печени отношение АсАТ/АлАТ меньше 1,33
тропонин (в норме содержание Тропонина I менее 0,07 нг/мл; в крови здоровых людей даже после чрезмерной физической нагрузки уровень тропонина Т не превышает 0,2 – 0,5 нг/мл)
Тропонин представляет собой универсальную для поперечно-полосатой мускулатуры структуру белковой природы, локализующуюся на тонких миофиламентах сократительного аппарата миокардиоцита.
•тропонина С — ответственный за связывание кальция
•тропонина Т — предназначен для связывания тропомиозина
•тропонина I — предназначен для ингибирования этих процессов выше указанных двух процессов
. тропонин Т и I существуют в специфичных для миокарда изоформах, отличающихся от изоформ скелетных мышц, чем и обусловливается их абсолютная кардиоспецифичность
•спустя 4 – 5 часов после гибели кардиомиоцитов вследствие развития необратимых некротических изменений тропонин поступает в периферический кровоток и определяются в венозной крови
•в первые 12 – 24 часа от момента возникновения острого инфаркта миокарда достигается пик концентрации
Кардиальные изоформы тропонина длительно сохраняют свое присутствие в периферической крови.
•тропонин I определяется на протяжении 5 – 7 дней
•тропонин Т определяется до 14 дней
https://www.youtube.com/watch?v=BlMr1WTbyZ4
Источник