Тропонин миоглобин при инфаркте

Аспартатаминотрансфераза и лактатдегидрогеназа при инфаркте миокарда. Миоглобин и тропонины при коронарном синдроме
Хотя содержание аспартатаминотрансферазы (АсАТ) в сердце и наибольшее из всех внутренних органов, этот фермент содержится также в мозге, лёгких, скелетных мышцах, почках, печени и в других органах и тканях. Поэтому повышение активности АсАТ в крови — чувствительный, но недостаточно специфичный маркер поражения миокарда. Большинство лабораторий отказываются от его определения в связи с доступностью и информативностью определения КФК, не говоря уже о тех случаях, когда есть возможность определять кардиоспецифические тропонины.
Активность в крови лактатдегидрогеназы (ЛДГ) возрастает при инфаркте миокарда медленнее и остаётся повышенной дольше, чем КФК либо её МВ-фракции. Это полезный тест для ретроспективной диагностики инфаркта миокарда, когда больной поступает в стационар спустя сутки — неделю от начала развития коронарной катастрофы. Правда, во многих лабораториях с этой целью всё чаще используют определение кардиоспецифических тропонинов.
Подъём общей ЛДГ не является специфичным при поражении миокарда. Общая активность ЛДГ в крови может возрастать при острой и хронической мышечной патологии, тромбоэмболии лёгочной артерии, шоке любой этиологии, мегалобластной анемии, лейкозе, патологии печени и почек, а также при ряде других заболеваний. Говоря об изоферментах ЛДГ, напомним, что ЛДГ1 находится преимущественно в сердце и почках, тогда как ЛДГ4 и ЛДГ5 — в печени и скелетной мускулатуре. При гемолизе можно получить завышенные значения ЛДГР так как этот изофермент содержится и в эритроцитах.
Миоглобин — ранний маркер поражения миокарда — появляется в плазме крови в первые часы после развития инфаркта мышцы сердца. Однако интерпретация результатов определения миоглобина затруднена из-за неспецифичности этого маркера (он содержится в скелетной мускулатуре). Иными словами, при неинформативной ЭКГ нельзя диагностировать инфаркт миокарда, основываясь только на подъёме уровня миоглобина в крови. Этот результат следует “подкрепить” аналогичными сдвигами концентрации МВ-фракции КФК либо кардиоспецифических тропонинов.
Тропонины — это регуляторные белки мышечного сокращения. В сердце присутствует три их вида: С (“си”), I (“ай”), Т (“ти”). Тропонин С, который есть не только в кардиомиоцитах, но и в гладкомышечных волокнах, не подходит для диагностики повреждения миокарда. С этой целью используют определение в крови тропонина I либо Т. Хотя незначительное количество последнего и может присутствовать в скелетной мускулатуре, считается, что в крови используемые в настоящее время тесты его не определяют.
Определение тропонинов повышает чувствительность диагностики повреждения миокарда. Образно говоря, этот тест позволяет определить гибель “считанных” кардиомиоцитов. В клиническом отношении это и хорошо, и плохо. Хорошо, так как позволяет подтвердить развитие даже самого мелкоочагового инфаркта миокарда или же выделить подгруппу с неблагоприятным прогнозом среди больных нестабильной стенокардией. У части последних длительность временной обтурации коронарной артерии оказывается достаточной для развития некроза кардиомиоцитов без характерных для инфаркта изменений на ЭКГ и/или подъёма КФК. Определение кардиоспецифичных тропонинов у больных нестабильной стенокардией служит мерилом нестабильности бляшки.
Плохо потому, что у пациентов с сердечной недостаточностью и/или гипертрофией миокарда на фоне артериальной гипертензии также может повышаться уровень кардиоспецифических тропонинов в крови без развития инфаркта миокарда. Это, естественно, осложняет диагностику инфаркта миокарда у данного контингента больных. Отметим ещё раз, что подъём уровня тропонинов крови — свидетельство поражения кардиомиоцитов любого генеза (токсического, воспалительного, электрического — при кардиоверсии, термического — при абляции) и вовсе не обязательно ишемического. Динамика подъёма тропонинов в плазме крови при инфаркте миокарда сходна с таковой МВ-фракции КФК.
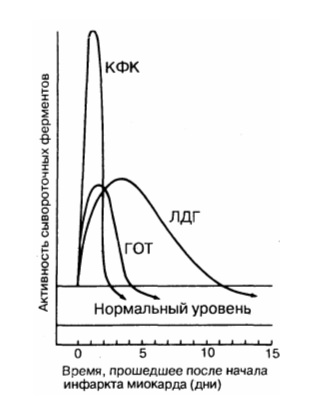
Динамика сывороточных ферментов после типичного инфаркта миокарда.
КФК – креатинфосфокиназа; ЛДГ – лактатдегидрогеназа; ГОТ – глутаматрксалоацетаттрансаминаза.
Видео урок изменений в анализе крови при инфаркте миокарда
При проблемах с просмотром скачайте видео со страницы Здесь
– Также рекомендуем “Динамика тропонинов при инфаркте миокарда. Диагностика острого коронарного синдрома”
– Вернуться в оглавление раздела “Кардиология.”
Оглавление темы “Причины и диагностика инфаркта миокарда”:
1. Эпидемиология инфаркта миокарда. Смертность от сердечно-сосудистой патологии
2. Социальные факторы инфаркта миокарда. Стресс и депрессия как причина инфаркта миокарда
3. Патогенез инфаркта миокарда. Механизмы развития инфаркта миокарда
4. Нестабильная атеросклеротическая бляшка. Диагностика нестабильной бляшки
5. Кокаин как причина инфаркта миокарда. Время развития инфаркта миокарда
6. Жалобы при инфаркте миокарда. Типы дебюта инфаркта миокарда
7. Боль при инфаркте миокарда. Дифференциация боли в грудной клетке
8. Дифференциация коронарной боли. Анамнез при инфаркте миокарда
9. Лабораторная диагностика инфаркта миокарда. Креатинфосфокиназа (КФК) при инфаркте миокарда
10. Аспартатаминотрансфераза и лактатдегидрогеназа при инфаркте миокарда. Миоглобин и тропонины при коронарном синдроме
Источник
Измерение уровней кардиомаркеров ускоряет и уточняет такого мероприятия, как диагностика инфаркта миокарда, а также возможность предсказать его дальнейшее развитие. Основные биохимические маркеры, которые использует диагностика инфаркта миокарда — миоглобин, тропонин I, тропонин Т, креатин-фосфокиназа и лактатдегидрогеназа.
Миоглобин
Миоглобин — кислородсвязывающий белок поперечно-полосатых скелетных мышц и миокарда. Его молекула содержит железо, структурно похожа на молекулу гемоглобина и отвечает за транспорт 02 в скелетных мышцах. Миоглобин является одним из самых первых маркеров повреждения миокарда, так как повышение его уровня в крови определяется уже через 2-4 часа после возникновения острого инфаркта миокарда. Пик концентрации достигается в срок до 12 часов, а затем в течение 1-2 суток снижается до нормы. В связи с тем, что выход свободного миоглобина в кровь может быть обусловлен рядом другим патологических состояний, для точной постановки диагноза инфаркта миокарда лишь одного этого маркера недостаточно.
Тропонины
Наиболее специфичные и надежные маркеры некроза миокарда — кардиальные тропонины Т и I (позволяют выявить даже самые незначительные повреждения миокарда).
Тропонины представляют собой белки, участвующие в процессе регуляции мышечного сокращения. Тропонин-I и тропонин-Т миокарда и скелетных мышц имеют структурные различия, что позволяет изолированно выделять их кардиоспецифичные формы методами иммуноанализа. Приблизительно 5% тропонина-I находится в свободном виде в цитоплазме кардиомиоцитов. Именно за счет этой фракции тропонин-I обнаруживается в плазме крови уже через 3-6 часов после повреждения сердечной мышцы. Большая же часть тропонина-I в клетке находится в связанном состоянии и при повреждении миокарда освобождается медленно. В результате увеличенная концентрация тропонина в крови сохраняется в течение 1 −2 недель. Обычно пик концентрации тропонина-I наблюдается на 14-20 часах после появления болей в груди. Приблизительно у 95% пациентов через 7 часов после развития острого инфаркта миокарда определяется увеличение концентрации тропонина-I.
Небольшой подъем уровня сердечного тропонина-I должен интерпретироваться со значительной осторожностью, так как это может быть обусловлено разными патологическими состояниями, вызывающими повреждение клеток миокарда. То есть увеличенный уровень тропонина изолированно не может служить основанием для постановки диагноза инфаркта миокарда.
Если у больного с подозрением на острый коронарный синдром без подъема сегмента ST повышен уровень тропонина Т и/или тропонина I, то такое состояние следует расценивать как инфаркт миокарда и проводить соответствующую терапию.
Определение тропонинов позволяет обнаружить повреждение миокарда примерно у трети больных, не имеющих повышения МВ-КФК. Для выявления или исключения повреждения миокарда необходимы повторные взятия крови и измерения в течение 6- 12 часов после поступления и после любого эпизода сильной боли в грудной клетке.
Креатинфосфокиназа (креатинкиназа)
Креатинфосфокиназа (креатинкиназа) — фермент, содержащийся в миокарде и скелетных мышцах (в небольшом количестве содержится в гладких мышцах матки, желудочно-кишечного тракта и головном мозге). В мозге и в почках содержится преимущественно изоэнзим ВВ (brain), в скелетных мышцах — ММ (muscle) и в сердце MB энзим. Наибольшей специфичностью обладает именно креатинкиназа MB. Имеется высокая корреляция между уровнем ее активности и массой некроза. При повреждении миокарда и скелетных мышц наблюдается выход фермента из клеток, приводящий к повышению активности креатинкиназы в крови. Через 2-4 часа после ангинозного приступа уровень креатинкиназы MB в крови значительно повышается, в связи с чем определение креатинфосфокиназы и креатинкиназы MB в крови широко применяется в ранней диагностике инфаркта миокарда.
Нормальный уровень креатинкиназы в крови у мужчин < 190 Ед/л и < 167 Ед/л у женщин. Нормальным содержанием креатинкиназы-МВ в крови считается 0-24 Ед/л. Креатинфосфокиназа (КФК) и ее изофермент MB КФК недостаточно специфичны, так как возможны ложноположительные результаты при травме скелетных мышц. Кроме того, имеет место значительное перекрывание между нормальными и патологическими сывороточными концентрациями указанных ферментов.
Лактатдегидрогеназа (ЛДГ)
Лактатдегидрогеназа (ЛДГ) — фермент, участвующий в процессе окисления глюкозы и образовании молочной кислоты. Она содержится практически во всех органах и тканях человека. Больше всего ее содержится в мышцах. Лактат в норме образуется в клетках в процессе дыхания и, при полноценном снабжении кислородом, в крови не накапливается. Происходит его разрушение до нейтральных продуктов, после чего он выводится из организма. При гипоксических состояниях лактат накапливается, вызывая чувство мышечной усталости и нарушая тканевое дыхание.
Более специфично исследование изоэнзимов этого фермента ЛДГ1-5. Наибольшей специфичностью обладает ЛДГ1. При инфаркте миокарда специфично превышение соотношения ЛДГ1 и ЛДГ2 более 1 (в норме ЛДП/ЛДГ2 < 1). Норма лактатдегидрогеназы для взрослых составляет 250 Ед/л.
При некрозе миокарда повышение концентрации этих маркеров в сыворотке крови происходит не одновременно. Наиболее ранний маркер — миоглобин. Увеличение концентрации MB КФК и тропонина происходит несколько позже. Следует учитывать, что при пограничных уровнях кардиомаркеров существует следующая тенденция:
- чем ниже их уровень, тем больше ложноположительных диагнозов;
- чем выше, тем больше ложноотрицательных диагнозов.
Определение тропонина и кардиомаркеров
Экспресс диагностика инфаркта миокарда легко осуществима в любое время с помощью различных качественных тест-систем для определения «Тропонина Т». Результат определяется через 15 минут после нанесения крови на тест-полоску. Если тест положительный и появилась вторая полоса, то уровень тропонина превышает 0,2 нг/мл. Следовательно, инфаркт есть. Чувствительность и специфичность этого теста более 90%.
Изменения других лабораторных показателей
Повышение уровня АсАТ отмечается у 97-98% больных с крупноочаговым инфарктом миокарда. Повышение определяется через 6-12 часов, достигая максимума через 2 суток. Показатель обычно нормализуется на 4-7 день от начала заболевания.
При развитии инфаркта миокарда отмечается увеличение числа лейкоцитов в крови, повышение скорости оседания эритроцитов (СОЭ), возрастание уровня гамма-глобулинов, снижение уровня альбумина, положительная проба на С-реактивный белок.
Лейкоцитоз наблюдается приблизительно у 90% больных. Выраженность его в определенной степени зависит от обширности инфаркта (в среднем 12- 15×109/л). Лейкоцитоз появляется через несколько часов от начала болевого приступа, достигая максимума на 2-4 день и, в неосложненных случаях, постепенно снижаясь до нормы в течение недели. Лейкоцитоз преимущественно обусловлен увеличением числа нейтрофилов.
При инфаркте миокарда СОЭ начинает увеличиваться на 2-3-й день, достигая максимума на 2-й неделе. Возвращение к исходному уровню происходит в течение 3-4 недель. В целом эти изменения свидетельствуют о существовании воспаления или некроза в организме и лишены какой-либо органоспецифичности.
Эхокардиография при инфаркте миокарда
Эхокардиография — неинвазивный метод, с помощью которого можно поручить достоверную информацию о состоянии регионарной и общей сократительной функции миокарда, изучить движение крови в полостях сердца, а также изучить структуру и функции его клапанного аппарата. С помощью эхокардиографии возможно получение сведений о таких показателях, как сердечный выброс, конечно-систолический и конечно-диастолический объемы левого желудочка, фракция выброса и др.
Эхокардиография, применительно к диагностике острых коронарных синдромов, позволяет:
- исключить или подтвердить диагноз острого инфаркта миокарда;
- идентифицировать не ишемические состояния, вызывающие боль в грудной клетке;
- оценить кратковременный и долгосрочный прогноз;
- идентифицировать осложнения острого инфаркта.
Инфаркт миокарда вызывает нарушения локальной сократимости левого желудочка разной степени выраженности. Структура ткани в области с нарушенной сократимостью может указать на давность инфаркта. Нередко на границе с нормальными сегментами видна резкая демаркационная линия. Граница между акинетичным и нормальным миокардом иногда хорошо визуализируется.
Для появления сегментарного нарушения сократимости миокарда, определимого при помощи эхокардиографии, необходимо повреждение более 20% толщины стенки желудочка. Могут быть определены локализация и распространенность инфаркта миокарда.
Эхокардиография особенно полезна в ранние сроки. Легко идентифицируются дисфункция митрального клапана, протяженность инфаркта, пристеночный тромб и механические осложнения инфаркта миокарда. Во время эпизода ишемии миокарда могут быть обнаружены локальная гипокинезия или акинезия стенки левого желудочка. После исчезновения ишемии может отмечаться восстановление нормальной сократимости.
Количество вовлеченных сегментов, полученное при оценке сократительной способности стенки сердца, как мера остаточной функции левого желудочка имеет раннее и позднее прогностическое значение при предсказании возможности осложнений и выживаемости. Истончение стенки левого желудочка указывает на ранее перенесенный инфаркт миокарда. При хорошей визуализации, когда виден весь эндокард, нормальная сократимость левого желудочка почти исключает инфаркт миокарда.
Источник
Признаки неосложненного инфаркта (продолжение)
Резорбционно-некротический синдром является одним из основных проявлений острого периода инфаркта миокарда. Он обусловлен резорбцией некротических масс и развитием асептического воспаления в зоне некроза.
Важнейшие признаки резорбционно-некротического синдрома: повышение температуры тела; лейкоцитоз; увеличение СОЭ; появление «биохимических признаков воспаления»; появление в крови биохимических маркеров гибели кардиомиоцитов.
Подъем температуры тела обычно отмечается на 2—3-й день, она достигает величины 37,1—37,9 °С, иногда превышает 38°С. Длительность повышения температуры тела около 3—7 дней, при обширном трансмуральном инфаркте миокарда лихорадка может продолжаться до 10 дней. Более продолжительный субфебрилитет может свидетельствовать о развитии осложнений — тромбэндокардита, пневмонии, перикардита, или о затяжном течении инфаркта миокарда. Величина температуры тела и длительность ее повышения в определенной мере зависят от обширности некроза и возраста больных. При распространенном инфаркте миокарда и более молодом возрасте повышение температуры тела более значительное и продолжительное, чем при мелкоочаговом инфаркте и у лиц пожилого возраста. При осложнении инфаркта кардиогенным шоком температура тела может оказаться даже сниженной.
Повышение количества лейкоцитов в крови при данном заболевании обусловлено развитием асептического воспаления в зоне некроза и повышением глюкокортикоидной функции надпочечников. Лейкоцитоз развивается уже через 3—4 ч, достигает максимума на 2—4-й день и сохраняется около 3—7 дней. Более длительное сохранение лейкоцитоза свидетельствует о затяжном течении инфаркта, появлении новых очагов некроза, развитии осложнений, присоединении пневмонии. Обычно количество лейкоцитов повышается до 10—12 х 109/л, при распространенном и трансмуральном инфаркте — до 15 х 109/л и даже выше. Лейкоцитоз более 20 х 109/л обычно является неблагоприятным прогностическим фактором. Лейкоцитоз сопровождается сдвигом лейкоцитарной формулы влево. В первые дни болезни можно отметить полное исчезновение из крови эозинофилов, в дальнейшем, по мере улучшения состояния больного, количество эозинофилов в крови нормализуется.
Основным фактором, определяющим увеличение СОЭ, является белковый состав крови. Увеличение в крови количества белковых молекул снижает отрицательный заряд, способствующий отталкиванию эритроцитов и поддержанию их во взвешенном состоянии. Наибольшее влияние на увеличение СОЭ оказывают фибриноген, иммуноглобулины, гаптоглобин. Увеличение СОЭ отмечается со 2— 3-го дня, достигает максимума между 8—12-м днем, затем постепенно снижается, и чёрез 3—4 недели СОЭ нормализуется. Характерным при инфаркте миокарда считается феномен «ножниц» между лейкоцитозом и СОЭ: в конце 1-й—начале 2-й недели лейкоцитоз начинает снижаться, а СОЭ возрастает.
При инфаркте миокарда в крови возрастает уровень неспецифических показателей некроза и асептического воспаления, получивших образное название «биохимических маркеров воспаления». Речь идет о повышении содержания в крови фибриногена, серомукоида, гаптоглобина.
Появление в крови биохимических маркеров гибели кардиомиоцитов. При инфаркте миокарда из кардиомиоцитов выходят различные ферменты, белковые молекулы — компоненты мышечных волокон. Они поступают в межклеточную жидкость, оттекают от сердца по лимфатическим путям и далее поступают в кровь, являясь, таким образом, маркерами некроза миокарда. К маркерам гибели кардиомиоцитов относятся ферменты АсТ, ЛДГ, креатинфосфокиназа (КФК), гликогенфосфорилаза (ГФ), а также миоглобин, миозин, кардиотропонины. Указанные вещества поступают в кровь при некрозе не только миокарда, но и скелетной мускулатуры. От момента гибели кардиомиоцитов до появления маркеров в крови проходит определенный период, характерный для каждого маркера. Длительность данного периода зависит от величины белковых молекул-маркеров, обширности и продолжительности некроза миокарда. Вначале повышается концентрация в крови миоглобина, тропонина Т, далее — КФК, ее изофермента КФК-МВ, АсТ; позже увеличивается уровень в крови ЛДГ и ее изофермента ЛДГ-1.
Другой характерной особенностью маркеров гибели кардиомиоцитов является характерная для каждого маркера динамика повышения и снижения его концентрации. Объясняется это тем, что миокард постоянно сокращается — это приводит к быстрой элиминации белков-маркеров из участка некроза, а затем и к полному вымыванию этих белков в кровь.
Определение содержания в крови миоглобина. Миоглобин — гемсодержащий хромопротеид, представляющий собой легкую цепь миозина. Миоглобин транспортирует кислород в скелетной мускулатуре и миокарде, он идентичен в миоцитах скелетных мышц и кардиомиоцитах, Миоглобин постоянно присутствует в плазме крови в связанном с белками состоянии. Содержание миоглобина в крови в норме составляет: у мужчин — 22— 66 мкг/л, у женщин — 21—49 мкг/л или 50—85 нг/мл. При повреждении миокарда или скелетной мускулатуры миоглобин поступает в кровь и затем выделяется с мочой.
Кинетика миоглобина при инфаркте миокарда
1) Повышение содержания миоглобина в крови начинается через 2—3 ч;
2) максимальный уровень миоглобина в крови наблюдается через 6—10 ч от начала инфаркта;
3) длительность повышения содержания миоглобина в крови составляет 24—32 ч.
Чувствительность миоглобинового теста колеблется от 50 до 100%. Уровень миоглобина в крови может повышаться при инфаркте в 10—20 раз. Повторное повышение уровня миоглобина в крови на фоне уже наступающей нормализации может указывать на расширение зоны некроза или образование новых некротических очагов.
Определение содержания в крови легких и тяжелых цепей миозина. В миофибриллах содержатся белки миозин, актин, актомиозин, тропомиозин, тропонин, а— и в-актинин. Все перечисленные белки связаны с сократительной функцией мышц.
Определение активности общей КФК в сыворотке крови. КФК катализирует обратимое фосфорилирование креатина с участием АДФ. Наибольшее количество КФК содержится в сердечной мышце, скелетной мускулатуре, менее богаты этим ферментом головной мозг, щитовидная железа, матка, легкие.
Содержание в сыворотке крови общей КФК в норме составляет 10-195 МЕ/л.
Аспартатаминотрансфераза и лактатдегидрогеназа при инфаркте миокарда. Миоглобин и тропонины при коронарном синдроме
Хотя содержание аспартатаминотрансферазы (АсАТ) в сердце и наибольшее из всех внутренних органов, этот фермент содержится также в мозге, лёгких, скелетных мышцах, почках, печени и в других органах и тканях. Поэтому повышение активности АсАТ в крови — чувствительный, но недостаточно специфичный маркер поражения миокарда. Большинство лабораторий отказываются от его определения в связи с доступностью и информативностью определения КФК, не говоря уже о тех случаях, когда есть возможность определять кардиоспецифические тропонины.
Активность в крови лактатдегидрогеназы (ЛДГ) возрастает при инфаркте миокарда медленнее и остаётся повышенной дольше, чем КФК либо её МВ-фракции. Это полезный тест для ретроспективной диагностики инфаркта миокарда, когда больной поступает в стационар спустя сутки — неделю от начала развития коронарной катастрофы. Правда, во многих лабораториях с этой целью всё чаще используют определение кардиоспецифических тропонинов.
Подъём общей ЛДГ не является специфичным при поражении миокарда. Общая активность ЛДГ в крови может возрастать при острой и хронической мышечной патологии, тромбоэмболии лёгочной артерии, шоке любой этиологии, мегалобластной анемии, лейкозе, патологии печени и почек, а также при ряде других заболеваний. Говоря об изоферментах ЛДГ, напомним, что ЛДГ1 находится преимущественно в сердце и почках, тогда как ЛДГ4 и ЛДГ5 — в печени и скелетной мускулатуре. При гемолизе можно получить завышенные значения ЛДГР так как этот изофермент содержится и в эритроцитах.
Миоглобин — ранний маркер поражения миокарда — появляется в плазме крови в первые часы после развития инфаркта мышцы сердца. Однако интерпретация результатов определения миоглобина затруднена из-за неспецифичности этого маркера (он содержится в скелетной мускулатуре). Иными словами, при неинформативной ЭКГ нельзя диагностировать инфаркт миокарда, основываясь только на подъёме уровня миоглобина в крови. Этот результат следует «подкрепить» аналогичными сдвигами концентрации МВ-фракции КФК либо кардиоспецифических тропонинов.

Тропонины — это регуляторные белки мышечного сокращения. В сердце присутствует три их вида: С («си»), I («ай»), Т («ти»). Тропонин С, который есть не только в кардиомиоцитах, но и в гладкомышечных волокнах, не подходит для диагностики повреждения миокарда. С этой целью используют определение в крови тропонина I либо Т. Хотя незначительное количество последнего и может присутствовать в скелетной мускулатуре, считается, что в крови используемые в настоящее время тесты его не определяют.
Определение тропонинов повышает чувствительность диагностики повреждения миокарда. Образно говоря, этот тест позволяет определить гибель «считанных» кардиомиоцитов. В клиническом отношении это и хорошо, и плохо. Хорошо, так как позволяет подтвердить развитие даже самого мелкоочагового инфаркта миокарда или же выделить подгруппу с неблагоприятным прогнозом среди больных нестабильной стенокардией. У части последних длительность временной обтурации коронарной артерии оказывается достаточной для развития некроза кардиомиоцитов без характерных для инфаркта изменений на ЭКГ и/или подъёма КФК. Определение кардиоспецифичных тропонинов у больных нестабильной стенокардией служит мерилом нестабильности бляшки.
Плохо потому, что у пациентов с сердечной недостаточностью и/или гипертрофией миокарда на фоне артериальной гипертензии также может повышаться уровень кардиоспецифических тропонинов в крови без развития инфаркта миокарда. Это, естественно, осложняет диагностику инфаркта миокарда у данного контингента больных. Отметим ещё раз, что подъём уровня тропонинов крови — свидетельство поражения кардиомиоцитов любого генеза (токсического, воспалительного, электрического — при кардиоверсии, термического — при абляции) и вовсе не обязательно ишемического. Динамика подъёма тропонинов в плазме крови при инфаркте миокарда сходна с таковой МВ-фракции КФК.
— Вернуться в оглавление раздела « Кардиология. «
Оглавление темы «Причины и диагностика инфаркта миокарда»:
Миоглобин
Миоглобин является железосодержащим белком клеток мышц.
Миоглобин выполняет приблизительно те же функции, что и гемоглобин эритроцитов в крови, то есть транспортирует кислород в мышцах и в сердечных мышцах. При инфаркте миокарда миоглобин попадает в кровь и быстро выводится почками, то же самое происходит при повреждении мышц скелета.
Через два или три часа после появления боли в сердце при инфаркте миокарда наблюдается повышение уровня миоглобина в крови, высокий уровень миоглобина в крови наблюдается приблизительно двое суток. Это самый первый маркер инфаркта миокарда. Степень его повышения зависит от площади поражения сердечной мышцы. За три – шесть часов до повышения уровня креатинкиназы наблюдается пик повышения концентрации миоглобина.
Другие маркеры инфаркта миокарда достигают своего пика приблизительно через двенадцать — девятнадцать часов.
Белок миоглобин самый недолговечный маркер инфаркта миокарда, он нормализуется за двадцать четыре часа и в этом его высокая диагностическая ценность. Высокий уровень миоглобина после острого приступа инфаркта миокарда свидетельствует о развитии осложнений, о том, что зона инфаркта расширяется.
Если повышение уровня миоглобина происходит на фоне нормализации состояния, это свидетельствует о том, что образуются новые некротические очаги. Белок миоглобин самый ранний и практически единственный маркер повторного инфаркта миокарда. Становится ясно, что при приступе инфаркта миокарда особенно важно вести наблюдение за изменением концентрации уровня миоглобина в крови в течении пяти дней с начала острого приступа. Подходящим для диагностики считается только количественное определение уровня концентрации миоглобина в крови.
Высокое диагностическое значение имеет маркер миоглобин при подозрении на инфаркт миокарда, подозрения снимаются после получения двух отрицательных результатов определения белка миоглобина.
При обширных травмах, тяжелом электрошоке, ожогах, артериальной окклюзии и ишемией мышц, повреждении мышц скелета, особенно важно определить уровень миоглобина в крови. Очень часто такие травмы сопровождаются острой почечной недостаточностью.
Наблюдение за концентрацией миоглобина в крови также является важным для спортсменов, таким образом, оценивается тренированность их мышц. Повышение уровня миоглобина здесь свидетельствует о мышечном перенапряжении спортсмена.
Клоуны Пуки и Рабдо — символы Кроссфита!
Источник
