Тромболизис при инфаркте миокарда или стентирование

а) Спасительное стентирование (чрескожное коронарное вмешательство, ЧКВ). Несмотря на увеличение случаев применения первичного ЧКВ, большинство пациентов получает реперфузионную ТЛТ. Имеется небольшое количество данных относительно значимости спасительного ЧКВ у пациентов, у которых ТЛТ была неэффективна.
Рандомизированное исследование больных с передним ИМ (n = 151) показало снижение 30-суточной комбинированной конечной точки, включающей СН и смерть (6,4% vs 16,6%, р = 0,05). В объединенном анализе нескольких небольших исследований были отмечены снижение числа случаев СН и улучшение выживаемости в течение 1 года больных со средним и большим ИМ.
В более позднем исследовании MERLIN (Middlesbtough Early Revascularization to Limit Infarction) рандомизировали на спасительное ЧКВ и консервативную терапию 307 пациентов со снижением подъема сегмента ST < 50% через 60 мин после введения стрептокиназы. Не было получено достоверной разницы в первичной конечной точке (смерть).
Последующая реваскуляризация была меньше (6,5% vs 20,1%, р < 0,01) в группе спасительного ЧКВ (стенты — 50%; ингибиторы рецепторов гликопротеина IIb/IIIа — 3%), но в группе ЧКВ было больше МИ (4,6% vs 0,6%, р < 0,03). Следует отметить, что применение ингибиторов рецепторов гликопротеина IIb/IIIа и стентирования привело к более значительному количеству спасенного миокарда по сравнению с баллонной ангиопластикой (n = 181; индекс сохраненного миокарда 0,35 vs 0,25, р = 0,005).
Недавно опубликованы результаты исследования REACT, в котором 427 пациентов после неэффективной ТЛТ (снижение подъема сегмента ST < 50% за 90 мин) были рандомизированы на консервативное лечение, повторную ТЛТ и спасительное ЧКВ (88% — стенты).
Хотя различий в показателях смертности не было, 6-месячный период без сердечно-сосудистых событий (СССоб) был больше в группе спасительного ЧКВ (84,6% vs 70,1% для консервативного лечения и 68,7% для повторной ТЛТ, р = 0,004).
Ошибки неинвазивной оценки состояния перфузии инфаркт-связанной коронарной артерии (КА) остаются серьезным ограничением данного подхода. Комплексная оценка клинической картины, определение биомаркеров в начале ИМ и через 60 мин, снижение подъема сегмента ST могут улучшить точность прогноза.
Считается, что лучше иметь клинические подозрения и направить пациента на ангиографию до появления нестабильности гемодинамики. Современные руководства рекомендуют спасительное ЧКВ для пациентов с кардиогенным шоком и СН и с меньшим уровнем доказательности — для пациентов с электрической нестабильностью или стойкой ишемией. Кроме этого, результаты недавних исследований свидетельствуют о необходимости такого подхода и к пациентам с признаками сохраняющейся ишемии.
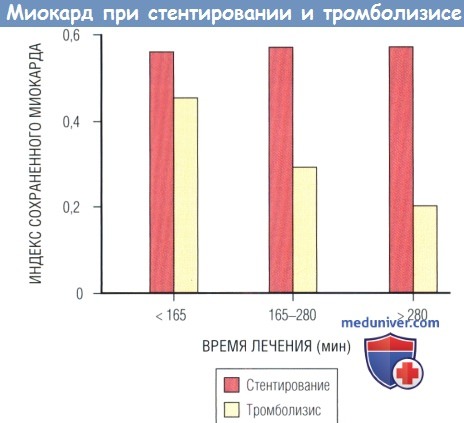
Медиана индекса сохраненного миокарда по терцилям временных интервалов лечения.
Было отмечено уменьшение индекса сохраненного миокарда в зависимости от времени в группе ТЛТ (р = 0,03), но не в группе стентирования (р = 0,59).
б) Упрощенное стентирование (чрескожное коронарное вмешательство, ЧКВ). Совершенствование ТЛТ и ЧКВ привело к комбинированию этих методов при лечении ОИМ с целью восстановления просвета коронарной артерии (КА) и уменьшения риска ишемии. Однако несколько исследований, выполненных за последние 10 лет, продемонстрировали неблагоприятный результат ангиопластики, проведенной непосредственно после ТЛТ: наблюдалось значительно больше кровотечений, повторных ишемий, КШ и летальных исходов.
Эти события возникали из-за вызванной ТЛТ активации тромбоцитов и/или обширного внутрисосудистого кровоизлияния. Современные методы ангиопластики улучшили безопасность процедуры в этом отношении. В исследованиях T1MI-10B (тенектеплаза vs ТАП) и TIMI-14 (уменьшенная доза ТАП и/или абциксимаб) у пациентов, подвергшихся дополнительному или отсроченному вмешательству (стенты в > 60% случаев), мультивариабельный анализ выявил более низкую 30-суточную смертность и/или более низкий риск реинфаркта по сравнению с пациентами с успешной ТЛТ (кровоток TIMI-3 в течение 90 мин) без вмешательства.
Мощный толчок к продолжению фармакоинвазивной стратегии лечения ИМ дали результаты исследований, показавших улучшение выживаемости пациентов высокого риска со спонтанной реперфузией (кровоток TIMI-3) до первичного ЧКВ. Действительно, достижение эффективного раннего восстановления коронарного кровотока у пациентов в течение 2-3 час от начала ИМ приводит к спасению большей части миокарда и росту благоприятных исходов, особенно у доставленных в больницу пациентов. Это обстоятельство стимулировало дальнейшее развитие понятия «упрощенная ангиопластика», которая сочетает в себе преимущества фармакологической реперфузии относительно скорости эффекта и безопасность механического воздействия для полноценного восстановления просвета КА.
Предварительные исследования с полной или уменьшенной дозой тромболитиков с ингибиторами рецепторов гликопротеина IIb/IIIa или без них подтвердили возможность достижения кровотока TIMI-3 при первичной ангиографии. В крупномасштабном исследовании упрощенного ЧКВ ASSENT-4 рандомизировали 1667 пациентов (< 6 час от начала заболевания) на первичное ЧКВ и первичное ЧКВ с предшествующей полной дозой тенектеплазы. Несмотря на большее количество лиц с кровотоком TIMI-3 до ЧКВ (43% vs 15%, р < 0,001) в группе ТЛТ, исследование было завершено досрочно из-за увеличенной смертности в группе упрощенного ЧКВ (6% vs 3%, р = 0,01).
Кроме того, первичная конечная точка (СН, шок или смерть в течение 90 сут) была выше в группе упрощенного ЧКВ (19% vs 13%, р = 0,0045). В этой же группе также было значительно больше МИ (1,8% vs 0%, р < 0,0001) и ишемических осложнений (реинфаркты 6% vs 4%, р = 0,03). В большом исследовании FINESSE (Facilitated Intervention with Enhanced Reperfusion Speed to Stop Events) сравнивают раннее применение абциксимаба vs уменьшенная доза ретеплазы плюс абциксимаб vs абциксимаб и ЧКВ (отбор пациентов в это исследование продолжается). Исследование BRAVE (n = 253) сравнило применение 1/2 дозы ретеплазы и абциксимаба vs один абциксимаб перед ЧКВ и не выявило различий в размере ИМ и клинических исходах.
Недавний метаанализ 17 исследований упрощенного ЧКВ (включая ASSENT-4) показал, что, хотя упрощенное ЧКВ более чем в 2 раза увеличивает начальный кровоток TIMI-3, после ЧКВ кровоток не отличается (89% vs 88%) по сравнению с первичным ЧКВ [100]. Показатели смертности (5% vs 3%, р = 0,04), РСМ (4% vs 1%, р = 0,01), массивных кровотечений (7% vs 5%, р = 0,01) и МИ (1,1% vs 0,3%, р = 0,0008) были значительно выше в группе упрощенного ЧКВ. Неблагоприятные исходы наблюдались у пациентов, получавших тромболитик, в то время как применение одного ингибитора гликопротеина IIb/IIIa не приводило к неблагоприятным результатам.
Геморрагические осложнения, связанные с применением тромболитика (местное артериальное, миокардиальное и церебральное повреждения) и фактором времени (позднее обращение, длительность тромболитического эффекта), взаимодействуют при таком подходе, по-видимому, неблагоприятно. Имеющиеся данные не подтверждают обоснованность комбинации ТЛТ с упрощенным ЧКВ.
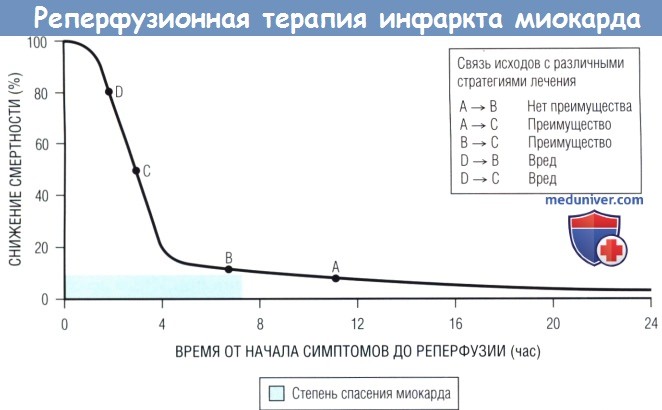
Преимущество реперфузионной терапии в отношении снижения смертности особенно проявляется при проведении в первые 2-3 нас после появления симптомов ОИМ.
Наиболее вероятный результат вмешательства — спасение миокарда.
На длительность этого раннего критинеского периода могут повлиять такие факторы, как наличие функционирующих коллатералей коронарных артерий,
предшествующая ишемия, потребность миокарда в кислороде и продолжительность ишемии.
По прошествии этого раннего периода преимущество реперфузионной терапии в отношении смертности резко уменьшается (кривая снижения смертности сглаживается),
и фактор времени проведения реперфузии становится менее важным.
Преимущество при смещении от точки А или В к точке С будет значительным, а при смещении от точки А к точке В — небольшим.
Лечебная стратегия, отдаляющая начало терапии в ранний критический период, например транспортировка пациента для проведения ЧКВ, может приносить вред (смещение от точки D к точке С или В).
в) Дополнительное стентирование (чрескожное коронарное вмешательство, ЧКВ) после успешного тромболизиса. Как было отмечено ранее, после успешного тромболизиса в большинстве артерий сохраняется существенный остаточный стеноз. Реинфаркты после тромболизиса характеризуются увеличенной смертностью и являются непредсказуемыми событиями. Ранние исследования, оценивавшие эффективность рутинной баллонной ангиопластики, проведенной через несколько часов или суток после успешной ТЛТ, не выявили преимуществ в отношении реинфарктов, функции ЛЖ или выживаемости.
У пациентов со спонтанной или провоцируемой ишемией после тромболитической терапии (ТЛТ) меньше повторных ИМ или эпизодов ишемии после ЧКВ. В связи с этим в современных руководствах рекомендуется проведение дополнительного ЧКВ пациентам после ТЛТ при повторном ИМ, провоцируемой ишемией, или находящимся в шоке (класс IIа) и предлагают рассматривать это вмешательство для пациентов с СИ, ФВ ЛЖ < 40% или серьезными желудочковыми аритмиями.
Усовершенствование техники ЧКВ позволило пересмотреть рутинный подход к пациентам после успешной ТЛТ. Например, в исследованиях TIMI-4, TIMI-10B и TIMI-17 проведение ЧКВ после тромболизиса снижало риск реинфарктов и двухлетнюю смертность. В исследовании GRACIA-1 (GRupo de Analisis de la Cardiopatia Isque’mica Aguda) 500 пациентов были рандомизированы на ангиографию и дополнительное ЧКВ со стентированием и абциксимабом через 6-24 час после ТЛТ или консервативное лечение.
Стентирование артерий было выполнено в 80% случаев в группе инвазивного лечения и в 20% — в группе консервативного лечения. Через 1 год первичная конечная точка, включавшая реинфаркт, реваскуляризацию и смерть, была меньше (9% vs 21%, р = 0,0008) в группе инвазивной терапии. В группе консервативного лечения количество внеплановых реваскуляризаций за время госпитализации в связи со спонтанной ишемией было в 5 раз выше. Хотя это исследование не выявило преимуществ в выживаемости больных, оно показало, что современное дополнительное ЧКВ как часть посттромболитической инвазивной стратегии может быть безопасным и полезным для пациентов.
– Читать “Плюсы и минусы первичного стентирования при инфаркте миокарда”
Оглавление темы “Инфаркт миокарда и нестабильная стенокардия.”:
- Клеточные технологии при инфаркте миокарда
- Сочетание стентирования и тромболитической терапии при инфаркте миокарда
- Плюсы и минусы первичного стентирования при инфаркте миокарда
- Показания для первичного стентирования с фибринолизом при инфаркте миокарда
- Показания для стентирования после фибринолиза при инфаркте миокарда
- Показания для позднего стентирования при инфаркте миокарда после госпитализации
- Требования к врачу, отделению для стентирования (чрескожного коронарного вмешательства, ЧКВ)
- Определение и классификация нестабильной стенокардии по Браунвальду
- Патогенез нестабильной стенокардии
- Клиника и ЭКГ при нестабильной стенокардии
Источник
Экстренная помощь при ОИМ на догоспитальном этапе должна быть направлена на:
- адекватное обезболивание;
- возобновление проходимости поврежденного сосуда, предупреждение реокклюзии (повторного прекращения кровообращения);
- поддержание проходимости венечных артерий, уменьшение агрегации тромбоцитов;
- ограничение зоны ишемии, профилактику или устранение осложнений.
Что такое тромболизис и как его проводят?
Тромболизис (ТЛТ) – это процесс растворения тромба под влиянием введённого в системный кровоток фермента, который вызывает разрушение основы тромба.
 Препараты для проведения ТЛТ (тканевые активаторы плазминогена) делятся на прямые (Стрептокиназа) и непрямые (Альтеплаза, Актилизе, Тенектеплаза).
Препараты для проведения ТЛТ (тканевые активаторы плазминогена) делятся на прямые (Стрептокиназа) и непрямые (Альтеплаза, Актилизе, Тенектеплаза).
В механизме действия ТАП условно выделяют 3 этапа:
- Связывание фермента с плазминогеном, который находится на фибрине (образование тройного комплекса);
- ТАП способствует проникновению плазминогена в фибрин, превращая его в плазмин;
- Образовавшийся плазмин расщепляет фибрин на мелкие фрагменты (разрушает тромб).
Существует прямая зависимость между временем начала ТЛТ и прогнозом для пациента. В методических рекомендациях Европейской ассоциации кардиологов указано на проведение тромболизиса до 12 часов от начала заболевания (далее введение препарата нецелесообразно).
Процедура ТЛТ вызывает активацию тромбоцитов, повышает концентрацию свободных мелких тромбов. Поэтому ТЛТ необходимо проводить вместе с адъювантной антитромбоцитарной терапией.
Тенектеплазу используют для ТЛТ на догоспитальном этапе. Ее вводят внутривенно болюсно (внутривенно струйно, с помощью шприца) на протяжении 10 секунд. Это ТАП III поколения, который имеет высокий профиль безопасности (низкий риск развития геморрагических и гемодинамических осложнений, аллергических реакций), не требует специфических условий хранения и просто в использовании.
 Альтеплаза вводится в условиях стационара. После введения 5 тис ОД гепарина, болюсно вводят 15 мг препарата. Далее переходят на капельное введение 0,75 мг/кг на протяжении 30 минут и 0,5 мг/кг за 60 минут. Общая доза составляет 100 мг. Вся процедура проводиться на фоне непрерывной инфузии гепарина.
Альтеплаза вводится в условиях стационара. После введения 5 тис ОД гепарина, болюсно вводят 15 мг препарата. Далее переходят на капельное введение 0,75 мг/кг на протяжении 30 минут и 0,5 мг/кг за 60 минут. Общая доза составляет 100 мг. Вся процедура проводиться на фоне непрерывной инфузии гепарина.
Стрептокиназа вводится внутривенно капельно в дозировке 1,5 млн ОД разведенной на 100 мл физиологического раствора на протяжении 30-60 минут. Перед применением препарата вводят болюсно 5 тыс ОД гепарина с последующим возобновлением инфузии не ранее чем через 4 часа после окончания введения Стрептокиназы.
Согласно приказу министерства, после проведения ТЛТ пациента нужно доставить в специализированный стационар с возможностью проведения балонной ангиопластики или стентирования не позже 12 часов.
Показания к проведению
Показаниями к тромболизису при инфаркте миокарда являются:
- Длительный (более 20 минут) ангинозный приступ в первые 12 часов от его начала;
- Элевация сегмента ST на 0,1 мВ и более в двух смежных стандартных или 0,2 мВ в соседних перикардиальных отведениях ЭКГ;
- Полная блокада левой ножки пучка Гиса, которая возникла впервые в присутствии болевого синдрома.
ТЛТ показана в условиях отсутствия возможности проведения ПКВ за 90-120 минут с момента первого контакта с больным.
Тромболизис в случае инфаркта миокарда имеет право выполнять специализированная кардиологическая бригада скорой помощи укомплектована всем необходимым для купирования возможных осложнений.
Противопоказания
Абсолютные противопоказания к тромболизису при инфаркте миокарда:
- Перенесенное геморрагическое ОНМК менее 6 месяцев назад;
- ЧМТ в анамнезе, хирургическое вмешательство до 3 недель;
- Желудочно-кишечное кровотечение менее 1 месяца назад;
- Нарушения свертывающей системы крови;
- Расслаивающая аневризма аорты;
- Рефрактерная артериальная гипертензия (САТ более 200 мм.рт.ст., ДАТ выше 110 мм.рт.ст.).
Относительные противопоказания:
- ТИА менее 6 месяцев назад;
- Систематическое применение прямых антикоагулянтов;
- Беременность, первые 28 дней после родов;
- Пунктированные сосудов крупного диаметра недоступных для компрессии;
- Длительная травматическая сердечно-легочная реанимация;
- Недавняя лазеротерапия заболеваний сетчатки глазного дна;
- Печеночная недостаточность;
- Язвенная болезнь желудка в стадии обострения;
- Инфекционный эндокардит;
- Диабетическая геморрагическая ретинопатия и другие кровоизлияния в сетчатку глаза.
Врач обязан предупредить пациента обо всех возможных противопоказаниях и осложнениях процедуры. Согласие на ТЛТ пациент подтверждает письменно в протоколе проведения тромболизиса.
Возможные осложнения тромболитической терапии (встречаются не более чем у 0,7% случаев):
- Паренхиматозные кровоизлияния, кровотечение в месте введения;
- Острые нарушения ритма – фибрилляция предсердия рассматривается как показатель реканализации (восстановление кровообращения) сосуда;
- Аллергическая реакция, лихорадка.
Клинические критерии успешной реперфузии (возобновление кислородного питания) миокарда:
- Быстрая регрессия болевого синдрома;
- Проявления во время введения тромболитика реперфузионных аритмий;
- Инволюция изменений ЭКГ (приближение сегмента ST к изолинии;
- Снижение уровня кардиоспецифических биохимических маркеров некроза.
На эффективность ТЛТ влияет и время суток – реканализация происходит хуже в утренние часы. В это время имеют максимальную дневные показатели активность тромбоцитов, коагуляторных процессов, вязкости крови, вазомоторного тонуса и природного ингибирования фибринолиза.
Выводы
Тромболитическая терапия входит в перечень стандартных мероприятий при оказании помощи больным с острым коронарным синдромом на догоспитальном этапе. Использование ТЛТ в первые часы от появления симптомов ОИМ позволяет спасти пациентов с потенциально некротизированным миокардом, улучшить функцию левого желудочка и снизить показатель смертности от ОИМ. Риск ретромбоза (повторная закупорка) снижает комбинация тромболизиса с гепаринотерапией и длительным применением Аспирина.
Источник
Заболевания сердечно-сосудистой системы нередко приводят к летальным последствиям. Своевременное адекватное лечение – условие сохранения жизни. Стентирование при инфаркте миокарда – процедура, которая способна остановить патологические процессы и предотвратить осложнения.
Общая информация об инфаркте
Сколько человек будет жить после инфаркта, зависит от того, насколько сильно повреждены ткани сердца, и какую площадь охватил процесс. Миокард – главная сердечная мышца, отвечающая за перекачку крови из желудочков в предсердия. При инфаркте происходит омертвение части этой мышцы. Это приводит к нарушениям в работе сердца вплоть до его остановки.
Инфаркт происходит из-за нехватки питания миокарда. Виной тому нередко служат холестериновые бляшки, которые перекрывают ток крови по коронарной артерии и другим сосудам. Дело в том, что обеспечение миокарда кислородом зависит от тонких сосудов, в которые разветвляется коронарная артерия. Недостаток питательных компонентов приводит к омертвению тканей или инфаркту.
Если жизнь удалось сохранить, на месте инфаркта образуется соединительная ткань. В итоге сердце не выполняет своих функций в полном объеме, а на органе образуется рубец, занимающий прежнее место мышц.
Что такое стентирование
Стентирование сосудов сердца – сложная процедура. Она особенно эффективна в первые часы после наступления инфаркта. Если случился инфаркт миокарда, провести стентирование должен опытный врач. Эта операция преграждает дальнейшее омертвение тканей и уменьшает осложнения.
Стент – тончайшая металлическая конструкция, своего рода пружина. Такое оборудование ставят в просвет коронарной артерии внутри сосуда. Расширяясь, оно обеспечивает нормальный просвет сосуда и способствует восстановлению полноценного кровообращения.
Чтобы установить стент, не требуется выполнять разрезы грудины. Его вводят через небольшое отверстие в бедренной артерии. Обычно операция не сопровождается кровопотерей или осложнениями. Длительность процедуры составляет от 15 минут до полутора часов.
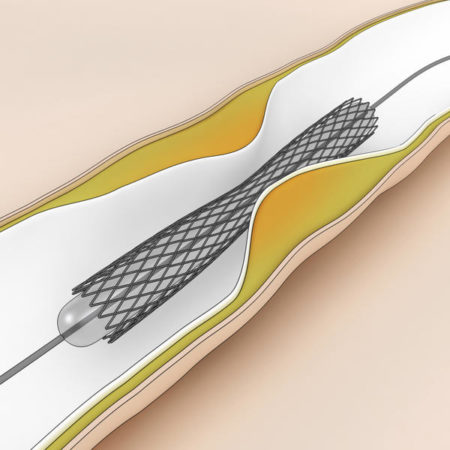
Когда оборудование установлено внутрь сосуда, состояние пациента постепенно стабилизируется. Буквально через 2-3 суток больного выписывают и наблюдают в рамках амбулаторного лечения.
После операции требуется принимать лекарства, назначенные врачом. Обычно это таблетки, разжижающие кровь. Их нужно пить столько, сколько рекомендовано.
Повод для стентирования сосудов
Чаще всего стент устанавливается при инфаркте для снижения рисков и постинфарктных осложнений. Но почему требуются такие крайние меры?
Заболевание проще предупредить, чем бороться с тяжелыми последствиями. Многие люди не знают, что недостаточное кровоснабжение миокарда приводит к ишемии. Ухудшение кровообращения происходит по разным причинам. Чаще всего нарушение в сосудах вызвано атеросклеротическими изменениями.
Холестериновые бляшки уменьшают просвет сосудов. Это изменение наблюдается в разных местах в организме. Однако сужение коронарной артерии наиболее опасно.
Когда возрастает нагрузка на органы и сосуды, например, при интенсивной ходьбе или физических упражнениях, организм нуждается в большем количестве кислорода. Это стимулирует сердце сокращаться быстрее. Из-за холестериновых отложений питание миокарда нарушается, и ускорение сокращений затрудняется. Возрастает риск инфаркта.
Важно! Если человек испытывает боли за грудиной или в области сердца, и они не проходят в течение 20 минут, состояние может закончиться инфарктом!
Проведение стентирования сосудов показано в таких случаях:
- неоднократные предынфарктные состояния,
- периодические приступы стенокардии,
- тяжелый инфаркт.
В вышеописанных случаях установка стента внутрь сосуда крайне желательна.
Применение ангиопластики
Некоторые считают, что установка стента должна проводиться уже при явных признаках ухудшения кровообращения. Однако есть процедура, которая, обеспечивая временный эффект, восстанавливает кровообращение в сосудах.
Увеличение просвета в артериях, заполненных холестериновыми бляшками, выполняется с помощью баллонной ангиопластики. Хирург вводит в полость закупоренного сосуда специальный баллон, который раздувается и вдавливает холестериновое отложение в стенку сосуда. В итоге восстанавливается кровообращение в артерии.
Недостаток этой процедуры в том, что результата хватает ненадолго. У большей половины прооперированных лиц наблюдалась повторная закупорка сосудов. Чаще всего нормальное кровообращение в коронарной артерии сохранялось не больше, чем на полгода.
Виды стендов
От правильно поставленного стента эффекта больше, чем от ангиопластики. Операция позволяет надолго сохранить нормальное кровообращение в сосудах.
Стенты различают по размерам и структуре. Они бывают:
- сеточные,
- кольцевые,
- проволочные,
- тубулярные.
Разработано более 400 видов стентов. Для их изготовления используются высококачественные металлы, которые не окисляются и не взаимодействуют с кровью. Стала возможной установка стента со специальным полимерным покрытием, которое в течение нескольких месяцев выделяет лекарственные вещества, препятствующие обрастанию конструкции гладкомышечной тканью внутри сосуда.

Внимание! Хотя стоимость стентов, покрытых лекарством, в несколько раз дороже обычных, пациенту с таким оборудованием требуется принимать меньше медицинских препаратов. Стенты с полимерным покрытием служат намного дольше, обеспечивая качественное кровообращение.
Ход операции
Стентирование сосудов сердца проводится опытным хирургом. В зависимости от сложности состояния пациента операция длится до трех часов. Общий наркоз не требуется, что позволяет проводить процедуру тем, кому такой тип анестезии противопоказан.
Подготовка к операции
Хотя операция проводится с помощью высокоточного современного оборудования, организм пациента следует правильно подготовить.
- Проводится анестезия.
- Вводятся препараты для разжижения крови.
После подготовительного этапа врач приступает к самой процедуре.
Установка стента
Место введения катетера обрабатывается антисептиком. В отверстие вводится небольшое оборудование. Все манипуляции внутри кровеносной системы отражаются на мониторе.
Катетер-проводник подводится к месту суженного сосуда. Высвобождается надувной баллон, который раздвигает стенки сосуда, возвращая их нормальный просвет.
Через то же отверстие вводится другой катетер с подготовленным стентом на конце. Он располагается в нужном месте, раздувается до требуемого диаметра и прижимается к стенкам сосуда.
Катетер удаляется. Место разреза фиксируется тугой повязкой для предотвращения кровопотери. В ближайшие часы после проведения операции пациент должен лежать в обездвиженном состоянии. Необходим медицинский контроль.
Самочувствие во время операции
Так как процедура проводится только под местным наркозом, во время операции человек постоянно находится в сознании. По просьбе врача пациент может выполнять различные дыхательные манипуляции.
Нет каких-либо болевых ощущений. Место введения катетера обезболивается. Перемещение оборудования внутри сосудистой системы не ощущается, так как стенки сосудов лишены нервных окончаний.
Нет никаких болей и во время расширения сосуда. Процедура практически никак не ощущается. Буквально через несколько дней человек может продолжить полноценную жизнь.
Подробнее процедура описана на видео:
Возможные осложнения
От поставленного стента осложнений практически не возникает. Люди быстро восстанавливаются, так как операция очень щадящая.

К наиболее вероятным осложнениям относятся:
- рестеноз,
- тромбоз.
Рестеноз – повторная закупорка сосуда. К счастью, после установления стентов такое состояние возникает крайне редко. Использование стентов с полимерным лекарственным покрытием значительно снижает риск данного осложнения.
Чтобы предотвратить образование тромбов в месте установки стента, необходимо строго по графику принимать все лекарства, назначенные хирургом. В частности, назначают аспирин.
Грамотная реабилитация
Многие, кому была проведена такая операция, говорят: «Мне поставили стент: как жить дальше?». На самом деле правильно проведенный этап реабилитации становится залогом долгой и счастливой жизни без потребности в проведении повторного стентирования.
Для полноценно восстановления необходимы такие мероприятия:
- лечебная физкультура,
- диета,
- правильный настрой.
Хорошее здоровье зависит от физической активности. Не стоит заниматься тяжелыми видами спорта и перегружать сердце. Это противопоказано. Нужно подобрать комплекс упражнений, которые будут эффективно поддерживать организм. Этот вопрос рекомендуется обсудить с врачом.

Тренироваться лучше каждый день. Если трудно, допускаются однодневные перерывы 1-2 раза в неделю. Каждое занятие длится примерно полчаса. Избавившись от избыточного веса и жировых отложений, станет легче поддерживать состояние сосудов.
Грамотно подобранный комплекс упражнений стабилизирует артериальное давление. Это снижает риск инсультов и инфаркта и увеличивает продолжительность жизни.
Холестерин необходим нашему организму каждый день. Однако чаще человек употребляет намного больше, чем нужно. Это приводит к росту показателя липопротеинов пониженной плотности. Если следить за уровнем вредного холестерина, проще предотвратить нарастание бляшек на сосудах.
Поддерживать уровень холестерина в норме поможет диета. Рацион должен содержать жиры. Однако лучше увеличить количество жиров растительного происхождения и уменьшить животного. Важно включить в меню такие продукты:
- бобовые,
- свежие овощи и фрукты,
- нежирная рыба.
После проведения стентирования запрещены алкогольные напитки, соления, жирная и жареная пища. Это поможет поддерживать здоровье в норме.
Хотя после проведения стентирования люди испытывают определенные переживания, лучше сосредоточиться на положительном, соблюдать все рекомендации врача и принимать назначенные препараты. От этого зависит жизнь, ведь поставить стент – только начало. Жизненно важно вести правильный образ жизни.
Важно! Чтобы сохранить жизнь после проведения серьезных вмешательств на сердце, важно и дальше внимательно следить за состоянием организма. Регулярно измерять артериальное давление, пульс, если нужно, корректировать эти показатели.
Своевременное проведение грамотного хирургического вмешательства поможет сохранить жизнь и здоровье человека, избежав инвалидности. Полный отказ от вредных привычек и здоровое питание – не сложный процесс, а стиль жизни, приносящий настоящее удовлетворение и отличное самочувствие каждый день!
Загрузка…
Источник
