Тромбоэндокардит как осложнение инфаркта миокарда
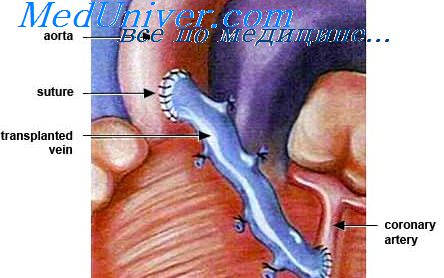
Венозный тромбоз и ТЭЛА при инфаркте миокарда. Тромбоэндокардит.Венозный тромбоз и ТЭЛА часто взаимосвязаны. Почти все легочные эмболы возникают из вен нижних конечностей, реже — из муральных тромбов в зоне ИМ ПЖ. Постельный режим и ХСН (часто имеющиеся у больных ИМ) предрасполагают к венозному тромбозу (а в последующем — и к ТЭЛА). В настоящее время в связи с ранней иммобилизацией больных и применением малых доз гепарина для профилактики ТЭЛА последняя стала редкой причиной смерти при ИМ. При появлении ТЭЛА у инфарктного больного она лечится по общим правилам. Тромбоэндокардит (мурольные тромбы, пристеночный тромбоз ЛЖ) возникает примерно в 20% случаев при ИМ, а при обширных ИМ передней локализации (трансмуральных или субэндокардиальных) его частота повышается до 60% (особенно у лиц, не получавших антикоагулянтную терапию). Тромбоэндокардит является эндокардитом в сочетании с отложениями тромботических масс в ЛЖ, чаще (до 70%) в зоне верхушки или аневризмы. Показано, что больные ИМ имели особенно плохой прогноз вследствие развития осложнений (КШ, разрывы стенки ЛЖ, желудочковые тахиаритмии), если у них рано (в течение первых 48-72 ч) развивался муральный тромбоз. Обычно тромбоэндокардит выявляется в первые 5 дней ИМ, причем опасность его развития наиболее велика в первые 10 дней и сохраняется до 3 месяцев. Воспаление эндокарда в острой фазе ИМ стимулирует развитие тромбогенной поверхности, благоприятствующей формированию тромбов в ЛЖ. Но муральные тромбы могут выявляться и в ПЖ. У половины больных с тромбоэндокардитом на секции были системные осложнения (почти в 10% случаев выявлялись тромбоэмболии).
Специфической симптоматики у тромбоэндокардита нет. Могут отмечаться потливость, слабость, тупая боль в области сердца, СТ, длительный субфебрилитет, который не поддается действию антибиотиков (АБ), длительный умеренный лейкоцитоз и рост СОЭ. Достоверным признаком тромбоэндокардита являются эмболии артерий или вен внутренних органов. Большинство эмболии происходит в первые 3 месяца. Риск тромбоэмболии резко повышается, если тромб подвижен. Диагностика тромбоэндокардита. Наличие на ЭхоКГ аневризмы, эндокардита и тромбомасс, тромбоэмболических осложнений. Ранняя антикоагулянтная терапия при ИМ снижает риск развития пристеночных тромбов и частоту последующих эмболии. Лечение тромбоэндокардита. Показаны нестероидные противовоспалительные препараты (НПВП), индометацин (200 мг/сут). При наличии тромбоэмболических осложнений (если эмболии были и ранее), обширного переднего ИМ (хотя на ЭхоКГ и не определяется тромб в ЛЖ), ИМ другой локализации, но при выявлении тромба или патологического движения стенки ЛЖ назначают антикоагулянты: внутривенно гепарин (АЧТВ должно увеличиться в 1,5—2 раза) во время пребывания больного в стационаре, а позднее — варфарин в дозе, необходимой для адекватного уровня MHO в течение 3—6 месяцев. Аспирин не может влиять на размер исходного тромба, но способен предотвращать отложение на нем тромбоцитов. Поэтому иногда комбинируют аспирин с варфарином у больных, являющихся кандидатами на длительное лечение антикоагулянтами. – Также рекомендуем “Перикардит при инфаркте миокарда. Синдром Дресслера.” Оглавление темы “Разрыв миокарда. Аневризмы сердца. Постинфарктные тромбоэмболии и перикардиты.”: |
Источник
Основные осложнения после перенесенного инфаркта миокарда
Тяжесть осложнений острого инфаркта миокарда (ОИМ) связана со степенью нарушения венечного кровотока, сократительной способности сердечной мышцы и локализацией ишемии. Важную роль играет оперативность оказания медицинской помощи, адекватность терапии, наличие сопутствующей патологии, возраст пациента. Кратковременное нарушение кровоснабжения вызывает отмирание клеток субэндокардиальной зоны. Если длительность ишемии превышает 6 часов, развивается некроз 80% пораженного миокарда.
Стадии развития:
- Острейшая (первые 6 часов).
- Острая (до 14 дней).
- Подострая (до 2 месяцев).
- Рубцевания.
Осложнения инфаркта могут возникать на любом этапе. В этом его опасность. Особенно рискуют больные, которых госпитализировали через 6-12 часов после начала приступа и тромболитическая терапия или другие методы восстановления кровотока не проводились. При развитии осложненного инфаркта летальный исход может наступить в течение года.
Все осложнения ОИМ можно разделить на четыре блока:
- Электрические (нарушение ритма и проводимости импульса).
- Механические (связаны со структурными нарушениями в миокарде).
- Гемодинамические (вызваны функциональной неспособностью пораженного миокарда обеспечивать прежний кровоток).
- Реактивные (связаны с резорбтивными и аутоиммунными процессами, активацией симпатической нервной системы, а также вторичными дисфункциями внутренних органов).
Ранние
Осложнения острого периода инфаркта миокарда развиваются в первые 10 суток после болевого приступа и существенно не ухудшают прогноз заболевания при своевременном лечении.
Нарушения ритма и проводимости – самые частые осложнения острого периода инфаркта (до 80%). Аритмии в основном развиваются из-за изменения электрофизиологических свойств и метаболизма в пораженной зоне, снижения порога фибрилляции, выброса в кровоток большого количества активных веществ — катехоламинов и развития феномена re-entry (круговой циркуляции волны возбуждения в миокарде).
Клинико-прогностическая классификация аритмий:
Неопасные для жизни:
- синусовая аритмия, брадикардия (пульс медленный, но >50), тахикардия (<110 уд/мин);
- миграция водителя ритма по предсердиям;
- редкие (<5 за минуту) предсердные и желудочковые экстрасистолы;
- переходящая AV-блокада I степени.
Прогностически серьезные:
- синусовая тахикардия с пульсом >110 уд/мин, брадикардия <50 уд/мин;
- частые предсердные, а также групповые, политопные ранние желудочковые экстрасистолы (предикторы фибрилляции и мерцательной аритмии);
- синоаурикулярная блокада;
- AV-блокада II-III степеней;
- идиовентрикулярный ритм;
- ритм из АV-соединения;
- суправентрикулярная пароксизмальная тахикардия;
- мерцание и трепетание предсердий;
- синдром слабости синусового узла.
Опасные для жизни:
- пароксизмальная желудочковая тахикардия;
- фибрилляция, трепетание желудочков;
- субнодальная полная AV-блокада;
- асистолия желудочков.
Клинически нарушения ритма проявляются:
- сердцебиением;
- ощущением перебоев в работе сердца;
- падением артериального давления;
- головокружением, потерей сознания.
Благодаря широкому внедрению тромболизиса на догоспитальном этапе и экстренной реваскуляризации миокарда частота внутрижелудочковых и полных AV-блокад не превышает 5%. Ранее эти осложнения становились причиной смерти более 50% пациентов как следствие прогрессирования сердечной недостаточности и развития кардиогенного шока.
В случае повторения жизнеугрожающих нарушений ритма устанавливают трансвенозный электрод для временной стимуляции миокарда в режиме of demand (по требованию). После возобновления адекватного сердцебиения устройство оставляют до полной стабилизации гемодинамических показателей (на 7-10 дней).
Острая сердечная недостаточность развивается из-за нарушения функции левого желудочка. К ней приводят обширные и трансмуральные инфаркты, осложненные тахиаритмией или AV-блокадой. Некротизированная зона миокарда «выключается» из сократительной массы При отмирании более 40% мышечной ткани желудочка развивается кардиогенный шок.
Резкое снижение функции выброса левого желудочка приводит к:
- увеличению конечного диастолического объема крови в нем;
- повышению давления сначала в левом предсердии, затем в легочных венах;
- развитию кардиогенного отека легких;
- недостаточному кровоснабжению жизненно важных органов (головного мозга, печени, почек, кишечника.
Клинически острая сердечная недостаточность проявляется:
- прогрессирующей одышкой;
- тахикардией, снижением давления;
- влажными хрипами в легких, крепитацией;
- цианозом (посинением кожи);
- снижением диуреза;
- нарушением сознания.
Кардиогенный шок – крайняя степень недостаточности левого желудочка, летальность при котором превышает 85%.
Лечение острой сердечной недостаточности, кардиогенного шока и альвеолярного отека легких должно проводиться в условиях реанимационного блока.
Механические осложнения в раннем периоде (разрывы сердца). Этот тяжелейший, чаще всего летальный исход инфаркта развивается на 5-7 сутки после приступа.
Разрывы сердца делят на:
- Наружные. Разрыв стенки желудочка в области ишемического поражения с истечением крови в перикард.
Выделяют предразрывный период, который интенсивной болью, проявлениями шока, и собственно разрыв стенки. В этот момент быстро происходит остановка кровообращения с признаками клинической смерти. Иногда этот процесс может затянуться на несколько суток.
К сожалению, лишь малому проценту больных удается выполнить экстренную пункцию перикарда и срочную операцию по восстановлению целостности левого желудочка с дополнительным аортокоронарным шунтированием.
2. Внутренние:
- Разрыв межжелудочковой перегородки. Возникает при передней локализации некроза. Диаметр дефекта колеблется от 1 до 6 см. Клинически это проявляется нарастанием некупируемой боли, развитием кардиогенного шока, появлением за несколько часов тотальной сердечной недостаточности. Лечение исключительно хирургическое.
- Разрыв сосочковой мышцы. Папиллярные мускулы удерживают митральный и трикуспидальный клапаны закрытыми во время систолы, не давая крови забрасываться обратно в предсердия. Полностью несовместим с жизнью, так как молниеносно развивается митральная недостаточность и альвеолярный отек легких.
Аневризма левого желудочка. Локальное выбухание стенки левого желудочка во время диастолы. Дефект состоит из отмершей или рубцовой ткани и не участвует в сокращении, а его полость зачастую заполнена пристеночным тромбом. Состояние опасно развитием эмболических осложнений или разрывом сердца.
Психические нарушения. Обычно развиваются на первой неделе заболевания и вызваны недостаточным поступлением крови в мозг, низким содержанием в ней кислорода и влиянием продуктов распада сердечной мышцы.
Нарушения поведения могут протекать в форме психотических (сопор, делирий, сумрачное состояние) и непсихотических реакций (астения, депрессия, эйфория, невроз).
Особое внимание следует уделить депрессивному синдрому (он может послужить причиной суицида).
Поздние
 По истечении 10 суток после сердечного приступа могут развиться:
По истечении 10 суток после сердечного приступа могут развиться:
- Ранняя постинфарктная стенокардия. Чаще возникает при поражении нескольких венечных сосудов или недостаточном тромболизисе, а также из-за нарушения диастолической функции левого желудочка. Является предиктором рецидива инфаркта миокарда и внезапной сердечной смерти.
- Тромбоэмболические осложнения:
- ТЭЛА (тромбоэмболия легочной артерии);
- бифуркации брюшного отдела аорты, артерий нижних конечностей (с развитием гангрены);
- тромбоз мезентериальных сосудов (клиническая картина острого живота), почечной артерии (инфаркт почки), церебральных артерий (инсульт).
3. Тромбоэндокардит. Асептическое воспаление эндокарда с пристеночным тромбообразованием в зоне некроза. Служит источником материала для эмболии сосудов большого круга кровообращения.
4. Стрессовые эрозии и язвы желудочно-кишечного тракта, кровотечение. Может развиваться и в остром периоде инфаркта миокарда. Причиной развития патологии служит нарушение кровоснабжения кишечной стенки, гиперактивация симпатической нервной системы, терапия антиагрегантами и антикоагулянтами.
5. Парез кишечника. Нарушение мочеиспускания (атония мочевого пузыря). Особенно часто встречается у пожилых пациентов на фоне действия нейролептаналгезии, строгого постельного режима, применения атропина.
Также в позднем периоде возможно развитие нарушений ритма и проводимости и хронической аневризмы сердца.
Отдаленные
 В отдаленном периоде возможно развитие:
В отдаленном периоде возможно развитие:
- Хронической сердечной недостаточности, которая требует пожизненной медикаментозной терапии.
- Постинфарктного кардиосклероза. Снижение и нарушения функции миокарда, вызванное рубцовыми и склеротическими процессами, что повышает риск повторного ОИМ.
- Постинфарктного синдрома (Дресслера). Это аутоиммунный процесс, вызванный неадекватным ответом организма больного на продукты распада отмерших клеток сердца: образуются антитела к собственным серозным оболочкам. Развивается на 2-8 неделе заболевания и характеризуется классической триадой: сухой перикардит, плеврит, пневмонит. Реже наблюдается поражение грудинно-реберных и плечевых суставов с развитием синовита.
Как не допустить ухудшения
Большинство осложнений ОИМ развиваются по причинам, не зависящим от пациента. Но существует ряд превентивных мер, способных снизить вероятность возникновения и тяжесть последствий:
- Обучение азам первой медицинской помощи при ОИМ и алгоритму реанимационных мероприятий.
- Своевременное обращение за медицинской помощью. Реваскуляризация (тромболизис, стентирование, аортокоронарное шутнирование) возобновляет кровоток в пораженном сосуде и ограничивает зону некроза миокарда.
- Строгий постельный режим в первые сутки заболевания, максимальный эмоциональный покой.
- Следование курсу лечения и своевременный прием медикаментов.
- Дозированные физические нагрузки, физиотерапия согласно стадии инфаркта.
Что делать при осложнениях: как лечить и к кому обращаться
 Ранние осложнения лечатся в условиях палаты интенсивной терапии кардиологической клиники с постоянным мониторингом жизненных показателей. Ритм восстанавливают путем введения антиаритмических препаратов (класс медикамента зависит от вида аритмии), электроимпульсной терапией или имплантацией кардиостимулятора. Механические осложнения требуют хирургического вмешательства на открытом сердце с использованием искусственного кровообращения.
Ранние осложнения лечатся в условиях палаты интенсивной терапии кардиологической клиники с постоянным мониторингом жизненных показателей. Ритм восстанавливают путем введения антиаритмических препаратов (класс медикамента зависит от вида аритмии), электроимпульсной терапией или имплантацией кардиостимулятора. Механические осложнения требуют хирургического вмешательства на открытом сердце с использованием искусственного кровообращения.
Поздние осложнения развиваются на стационарном или санаторно-курортном этапе. Лечение тромбоэмболических эпизодов зависит от состояния пораженного сосуда и длительности ишемии. Допускается консервативное введение антикоагулянтов, тромболизис, эндоваскулярное удаление эмбола, открытая тромбэктомия. В случае необратимых повреждений выполняют резекцию.
С осложнениями отдаленного периода пациент должен обратиться к лечащему кардиологу, который проведет диагностику и назначит лечение.
Выводы
Вероятность ранних и поздних осложнений инфаркта миокарда возрастает при несвоевременном обращении за медицинской помощью, а также у пациентов с нелеченной гипертонией, сахарным диабетом и атеросклерозом.
Для профилактики инфаркта и его осложнений стоит придерживаться здорового образа жизни, полноценно питаться, избегать стрессов и влияния неблагоприятных факторов окружающей среды, отказаться от курения, ограничить употребление алкоголя, регулярно делать зарядку.
Пациентам с сердечно-сосудистыми заболеваниями стоит систематически проходить профилактические осмотры 2 раза в год и следовать рекомендациям врача.
Источник
Венозный тромбоз и ТЭЛА часто взаимосвязаны. Почти все легочные эмболы возникают из вен нижних конечностей, реже — из муральных тромбов в зоне ИМ ПЖ. Постельный режим и ХСН (часто имеющиеся у больных ИМ) предрасполагают к венозному тромбозу (а в последующем — и к ТЭЛА). В настоящее время в связи с ранней иммобилизацией больных и применением малых доз гепарина для профилактики ТЭЛА последняя стала редкой причиной смерти при ИМ. При появлении ТЭЛА у инфарктного больного она лечится по общим правилам.
Тромбоэндокардит (мурольные тромбы, пристеночный тромбоз ЛЖ) возникает примерно в 20% случаев при ИМ, а при обширных ИМ передней локализации (трансмуральных или субэндокардиальных) его частота повышается до 60% (особенно у лиц, не получавших антикоагулянтную терапию). Тромбоэндокардит является эндокардитом в сочетании с отложениями тромботических масс в ЛЖ, чаще (до 70%) в зоне верхушки или аневризмы. Показано, что больные ИМ имели особенно плохой прогноз вследствие развития осложнений (КШ, разрывы стенки ЛЖ, желудочковые тахиаритмии), если у них рано (в течение первых 48-72 ч) развивался муральный тромбоз. Обычно тромбоэндокардит выявляется в первые 5 дней ИМ, причем опасность его развития наиболее велика в первые 10 дней и сохраняется до 3 месяцев.
Воспаление эндокарда в острой фазе ИМ стимулирует развитие тромбогенной поверхности, благоприятствующей формированию тромбов в ЛЖ. Но муральные тромбы могут выявляться и в ПЖ. У половины больных с тромбоэндокардитом на секции были системные осложнения (почти в 10% случаев выявлялись тромбоэмболии).
Специфической симптоматики у тромбоэндокардита нет. Могут отмечаться потливость, слабость, тупая боль в области сердца, СТ, длительный субфебрилитет, который не поддается действию антибиотиков (АБ), длительный умеренный лейкоцитоз и рост СОЭ. Достоверным признаком тромбоэндокардита являются эмболии артерий или вен внутренних органов. Большинство эмболии происходит в первые 3 месяца. Риск тромбоэмболии резко повышается, если тромб подвижен.
Диагностика тромбоэндокардита. Наличие на ЭхоКГ аневризмы, эндокардита и тромбомасс, тромбоэмболических осложнений. Ранняя антикоагулянтная терапия при ИМ снижает риск развития пристеночных тромбов и частоту последующих эмболии.
Лечение тромбоэндокардита. Показаны нестероидные противовоспалительные препараты (НПВП), индометацин (200 мг/сут). При наличии тромбоэмболических осложнений (если эмболии были и ранее), обширного переднего ИМ (хотя на ЭхоКГ и не определяется тромб в ЛЖ), ИМ другой локализации, но при выявлении тромба или патологического движения стенки ЛЖ назначают антикоагулянты: внутривенно гепарин (АЧТВ должно увеличиться в 1,5—2 раза) во время пребывания больного в стационаре, а позднее — варфарин в дозе, необходимой для адекватного уровня MHO в течение 3—6 месяцев. Аспирин не может влиять на размер исходного тромба, но способен предотвращать отложение на нем тромбоцитов. Поэтому иногда комбинируют аспирин с варфарином у больных, являющихся кандидатами на длительное лечение антикоагулянтами.
При субэндокардиальном и трансмуральном ИМ течение заболевания может осложниться тромбоэндокардитом. Особенно часто тромбоэндокардит имеет место при аневризме сердца (не менее 70— 80% случаев). О тромбоэндокардите можно думать при наличии потливости, слабости, склонности к тахикардии, а также длительной субфебрильной температуры, которая не поддается действию антибиотиков. Длительное время отмечаются увеличение числа лейкоцитов в крови, повышение СОЭ. Однако в ряде случаев тромбоэндокардит протекает скрыто при нормальной температуре тела и без лейкоцитоза. Достоверным признаком тромбоэндокардита являются эмболии артерий и внутренних органов, головного мозга, конечностей. Тромбоз полостей сердца трудно диагностировать клинически. Диагноз можно считать достоверным при наличии эндокардита, аневризмы сердца и тромбоэмболии. Для диагностики внутрисердечного тромбоза используют радиоактивный фибриноген, а также фибринолизин, который обладает тропностью к тромбу и концентрируется в нем [Боголюбов В. М., 1967]. С этой же целью применяют эхосканирование сердца и вентрикулографию.
Обновление статических данных: 11:00:01, 19.09.19
Заболевания сердечно-сосудистой системы являются проблемой современной медицины. Они быстро прогрессируют и часто приводят к летальному исходу. К таким патологиям относится тромбоэндокардит, он может протекать скрытно и вызвать стойкое ухудшение состояния человека.
Тромбоэндокардит развивается на фоне различных патологических состояний, к которым относятся:
- Аневризма сердца.
- Инфаркт миокарда.
- Злокачественные новообразования.
- Системная красная волчанка.
- Наличие воспалительного процесса в эндокарде, выстилающем полости сердца изнутри.
- Диссеминированное внутрисосудистое свертывание.
- Инфекционный процесс.
- Пороки сердца.
При наличии воспалительных и дегенеративных изменений в полости сердца на ее стенках и клапанах образуются вегетации (наросты) из тромбоцитов. Инфицирование вегетаций происходит в условиях бактериемии. Причинами бактериемии могут послужить стоматологические процедуры, оперативные вмешательства на органах брюшной полости и малого таза. Вегетации разрастаются и нарушают работу сердечно-сосудистой системы.
В зависимости от локализации вегетаций различают клапанный и пристеночный тромбоэндокардит. Для пристеночного тромбоэндокардита характерно наличие вегетаций на стенках полостей сердца. При клапанном тромбоэндокардите вегетации поражают митральный, трикуспидальный, аортальный и легочной клапаны.
Тромбоэндокардит также бывает инфекционным и неинфекционным. Неинфекционный асептический тромбоэндокардит Либмана-Сакса сопровождается образованием вегетаций в виде бородавок, поражающих створки клапанов. Инфекционный тромбоэндокардит развивается на фоне первичного заболевания, он характеризуется заселением патогенной микрофлоры на стерильных вегетациях.
В данном ролике бактериальный эндокардит рассматривается на клиническом примере: симптоматика, течение заболевания, рекомендации кардиолога:
У больных с тромбоэндокардитом наблюдается стойкая и длительная лихорадка.
Пациенты высказывают характерные жалобы:
При прогрессировании заболевания проявляется клиническая картина сердечной недостаточности.
В первую очередь, каждому пациенту рекомендуется сдать общий и биохимический анализ крови. В ходе лабораторных исследований выявляются характерные признаки воспалительного процесса:
- увеличение количества лейкоцитов;
- наличие С-реактивного белка;
- повышение скорости оседания эритроцитов (СОЭ).
На электрокардиограмме определяется гипертрофия полостей, нарушение проводимости сердца, экстрасистолия и фибрилляция.
Наиболее информативным инструментальным методом является эхокардиография. Она позволяет определить степень поражения клапанного аппарата и наличие осложнений. При асептическом эндокардите Либмана-Сакса эхокардиографическое исследование выявляет утолщение створок клапанов.
Для выявления тромбоза также используются методы, основанные на регистрации излучения от радиоактивного фибриногена, введенного в полость сердца.
В видеоролике демонстрируется результат проведения эхокардифического исследования, возможные поражения митрального клапана.
При наличии инфекционного эндокардита активизируется иммунная система и образуется множество антител. Эти антитела могут атаковать собственные клетки, в результате чего развиваются аутоиммунные заболевания (гломерулонефрит, артрит, васкулит).
Вегетации (наросты), возникшие при тромбоэндокардите, нарушают работу клапанов, приводят к их стенозу и недостаточности. Отрывы отростков вегетаций способны привести к эмболии артерий сердца, головного мозга, легких и других жизненно важных органов. При поражении стенок сосудов развиваются септические аневризмы.
Тактика лечения тромбоэндокардита заключается в таких мероприятиях:
- При наличии инфекции показана антибактериальная терапия. Производится посев флоры для определения чувствительности патогенных штаммов к антибиотикам. Также проводится симптоматическая терапия, направленная на устранение симптомов и нормализацию жизненно важных функций.
- Нестероидные противовоспалительные средства (НПВС) назначаются с целью подавления воспалительного процесса на разных стадиях. НПВС предупреждают высвобождение медиаторов воспаления и предупреждают пристеночную адгезию тромбоцитов с фибрином.
- При развитии инфаркта миокарда с целью профилактики осложнений назначаются препараты с антикоагулянтной активностью. Антикоагулянты снижают активность тромбоцитов и предупреждают развитие диссеминированного внутрисосудистого свертывания крови.
- B-блокаторы применяют для борьбы с синусовой тахикардией. Показанием к оперативному вмешательству служит отсутствие терапевтического эффекта в ходе консервативного лечения и развитие осложнений, угрожающих жизни пациента.
Прогноз благоприятен при раннем выявлении тромбоэндокардита, грамотном лечении и неотягощенном анамнезе пациента. При наличии у больного иммунодефицита, аутоиммунных заболевании, первичной патологии сердечно-сосудистой системы и пороках растет риск летального исхода.
Ситуация также осложняется выявлением в крови микрофлоры, резистентной к действию антибактериальных средств.
К мерам профилактики относятся:
- Активный и подвижный образ жизни.
- Своевременная санация очагов инфекции в организме.
- Поддержание иммунной системы.
- Выполнение рекомендаций лечащего врача.
Тромбоэндокардит является тяжелой патологией сердечно-сосудистой системы, которая может за короткий период времени нанести необратимый вред здоровью. Однако своевременное лечение увеличивает шансы к выздоровлению.
Источник
