Стентирование при инфаркте миокарда после тромболизиса

Для восстановления проходимости коронарной артерии используется установка металлического каркаса (стента), который не дает стенкам сжиматься. Такая операция называется стентированием и проводится при помощи катетера с баллоном на конце. Назначается для лечения ишемической болезни, в том числе и в постинфарктный период. После стентирования пациентам показана кардиореабилитация.
Зачем проводят стентирование после инфаркта
Основной причиной инфаркта миокарда является закупорка венечных артерий сердца холестериновыми бляшками. Они вызывают ишемические процессы в сердечной мышце, приступы боли. Тяжелый приступ стенокардии может перерасти в инфаркт. Если удается возобновить проходимость артерии в первые часы, то это существенно снижает зону разрушения мышечного слоя сердца и способствует восстановлению нормальной функции клеток.
Если острое нарушение коронарного кровотока все же привело к некротическим изменениям в миокарде, то стентирование в постинфарктном периоде помогает решить такие задачи:
- избежать повторных приступов;
- предотвратить осложнения в виде нарушения ритма и сердечной недостаточности;
- улучшить переносимость физических нагрузок;
- восстановить трудоспособность;
- повысить качество жизни пациентов;
- избежать длительной и массивной медикаментозной терапии.
Стент
Метод стентирования обладает многими достоинствами: не требуется открытый доступ в грудную клетку, что снижает риск осложнений и инфекций, сама операция продолжается до 2 — 3 часов, а период восстановления обычно не превышает месяца. После стентирования нет жестких ограничений по физической нагрузке и трудовой деятельности после прохождения реабилитации.
Рекомендуем прочитать статью о кофе после инфаркта. Из нее вы узнаете о воздействии кофе на организм и о том, можно ли пить напиток сердечникам.
А здесь подробнее об ЛФК после инфаркта.
Проведение ангиопластики
Стент представляет собой сетчатую трубочку из кобальта. В последнее время их покрывают специальным составом, который предотвращает фиксацию тромбов. Покрытие позволяет дольше поддерживать просвет сосуда открытым и избавляет от повторной операции по реканализации артерии.
Хирургическое вмешательство проводится таким образом:
- Пунктируют бедренную артерию (делают небольшой разрез).
- Проводят через нее катетер с баллончиком на конце.
- Под контролем рентгеновского исследования продвигают катетер до места закупорки.
- Заполняют баллончик воздухом, придавливая бляшку к стенкам.
- При расширении баллона раскрывается стент и фиксируется в артерии.
- После установки катетер удаляется.
На место прокола накладывается давящая повязка, а пациента переводят в палату. Наблюдение за работой сердца проводится путем контроля за артериальным давлением, частотой пульса и показаниями ЭКГ. Назначается медикаментозная терапия.
Возможные осложнения после
Риск послеоперационных нарушений работы сердца довольно низкий, но при наличии патологий свертывания крови, сахарного диабета или болезней почек возможны такие последствия:
- рестеноз – артерия повторно перекрывается из-за образования тромба, спазма, отслоения или надрыва внутреннего слоя;
- кровотечение, тромбоз или гематома в области бедренной артерии;
- закупорка коронарных артерий оторвавшимися сгустками (инфаркт в новой зоне);
- остановка сердца;
- нарушение работы почек.
Лечение больного после стентирования сосудов, инфаркта
Если после контрольного обследования у пациента не выявлено нарушений сердечной деятельности и признаков осложнений, то через 2 — 5 суток его выписывают для амбулаторного лечения. Назначается комплексная терапия для разжижения крови и восстановления микроциркуляции в миокарде. Для улучшения отдаленных результатов стентирования используют такие группы средств:
Группы средств | Названия препаратов |
Дезагреганты | Аспирин, Плавикс или Брилинта |
Снижающие содержание холестерина в крови | Зокор, Аторис, Крестор, Трайкор |
Слокаторы системы ренин-ангиотензин-альдостерона | Диротон, Престариум, Хартил |
С целью воздействия на основные симптомы ишемической болезни назначают:
Группы средств | Названия препаратов |
Бета-блокаторы | Беталок, Конкор, Небилет |
Нитраты | Кардикет, Оликард ретард |
Антагонисты кальция | Изоптин, Диакордин, Норваск, Адалат |
Средства разных групп | Кораксан, Сиднофарм, Кординик, Ранекса, Предуктал |
Терапия медикаментами проводится не менее трех месяцев, после чего показано обследование, которое включает ЭКГ и нагрузочные пробы для выявления признаков рестеноза и определения переносимости физической активности. По результатам диагностики вносят коррективы в план лечения.
Жизнь, реабилитация и восстановление после
Необходимость изменения образа жизни, обязательного отказа от вредных привычек, дозированных физических нагрузок и диеты связана с тем, что при стентировании можно убрать не причину ишемии миокарда, а и ее последствия. При этом коронарные артерии остаются измененными атеросклерозом, поэтому для профилактики повторных инфарктов пациентам показан комплекс реабилитационных мероприятий.
Дают ли инвалидность
Сама операция по восстановлению проходимости венечной артерии при ангиопластике со стентированием не является причиной для утраты трудоспособности и назначения группы инвалидности. В большинстве случаев происходит восстановление утраченной работоспособности, пациент может вернуться к своей профессиональной деятельности.
Сроки полной реабилитации различны. Они зависят от состояния больного и вида нагрузок. Есть профессиональные ограничения – виды занятий, которые противопоказаны после имплантации стента:
- летчики;
- водители;
- высотные работы;
- с ночными сменами;
- промышленные предприятия с вредными условиями работы (горячий цех, вибрация, химические соединения).
Если больной относится к этой категории, то ему временно показано ограничение трудоспособности с рекомендацией о смене работы.
Давление у больного
Высокая артериальная гипертензия создает гемодинамические условия для повышенной нагрузки на сердечную мышцу и ускоряет процесс образования кровяных сгустков. Поэтому для более долговечной работы стента рекомендуется поддерживать давление крови не выше 140/90 мм рт. ст.
Если у пациента имеются сопутствующие заболевания почек или сахарный диабет, то верхняя допустимая граница ниже на 10 единиц для каждого показателя. Контролировать уровень давления требуется ежедневно утром и перед сном, при частых колебаниях показано не менее раза в неделю проводить мониторирование показателей с ведением дневника самочувствия.
Допустимая нагрузка
Стентирование считается успешным только в том случае, если у пациента повышается переносимость физических нагрузок. Для расширения возможностей организма тренировки сердечной мышцы обязательны. Регулярная дозированная активность тормозит прогрессирование нарушений жирового и углеводного обмена, улучшает устойчивость к кислородному голоданию и способствует поддержанию нормального веса.
На первых этапах всем пациентам показана лечебная физкультура, дыхательная гимнастика и ходьба. Конкретный уровень нагрузок определяет врач по результатам обследования. После стабилизации состояния можно заниматься плаванием, ездой на велосипеде, легким бегом. Подъемы тяжести и виды спорта, при которых возможен удар в область сердца, категорически запрещены.
Диетическое питание
Для нормализации содержания холестерина в крови и предотвращения дальнейшей закупорки артерий нужно снизить ослепление жиров животного происхождения и простых углеводов в организм. Для этого из рациона исключают:
- баранину, свинину, утку, сало, субпродукты;
- жирные колбасы, полуфабрикаты;
- маргарин, майонез;
- выпечку, белый хлеб;
- кондитерские изделия, сладости, сахар;
- сладкие соки и газированные напитки, соусы промышленного производства;
- консервы;
- алкогольные напитки.
В ограниченных количествах используют:
- сливочное масло (не более 5 г в день);
- сметану;
- жирные сливки;
- творожные десерты;
- яйца (в неделю 3 штуки);
- соль (не более 3 г для добавления в готовые блюда);
- кофе, крепкий чай.
Первые блюда нужно готовить вегетарианскими. После стабилизации содержания холестерина – на овощном бульоне с рыбными или куриными фрикадельками, навары пациентам с ишемией миокарда не рекомендуются.
Для вторых блюд можно использовать нежирные виды мяса (курица, индейка) и рыбу. Предпочтительные виды кулинарной обработки – приготовление на пару, отваривание в воде, запекание. Гарниром к ним могут быть цельнозерновые каши (овсяная и гречневая), отварные или паровые овощи. В основной прием пищи обязательно включать салат из свежих овощей с растительным маслом. На десерт готовят фруктовые компоты, муссы и желе. Полезны сухофрукты, ягоды и орехи.
Поддерживающие лекарственные препараты
Важной частью процесса восстановления миокарда является медикаментозная терапия. Ее продолжают даже после ликвидации основных проявлений болезни. Хотя стентирование и позволяет значительно уменьшить потребность в лекарственных средствах, но для предотвращения тромбообразования и нормального обмена в сердечной мышце некоторые препараты приходится принимать длительное время.
Самая оптимальная комбинация средств для снижения свертывания крови – это ацетилсалициловая кислота и Клопидогрел. Эти медикаменты предотвращают закупорку установленного стента и значительно снижают риск повторного инфаркта. Аспирин может раздражать слизистую оболочку желудка, поэтому рекомендуются специальные кардиологические формы со сниженной дозировкой, таблетки которых покрыты кислотоустойчивой оболочкой – Тромбо Асс, Лоспирин, Кардиомагнил.
Есть ли отличия между стентированием после обширного инфаркта и мелкоочагового
Одним из показаний к проведению чрескожной баллонной ангиопластики является обширный инфаркт сердечной мышцы. Для таких пациентов это является шансом на ограничение площади повреждения миокарда, предотвращение осложнений и повторных приступов.
Техника операций при любом размере очага не имеет принципиальных отличий, но при закупорке более крупной артерии дополнительно может быть использован тромболизис (растворение тромба).
Он заключается во введении ферментов для растворения тромба – Стрептокиназа, Урокиназа. Эти средства проявляют свою эффективность только в том случае, если от времени начала инфаркта прошло не более 12 часов.
Успех операции определяется степенью атеросклеротического изменения артерий. У пациентов с единичным поражением и отсутствием кальцификации стенок коронарных сосудов он выше, а менее благоприятные результаты получены при таких условиях:
- закупорены несколько сосудов;
- артерии длинные, извитые, много боковых ветвей, которые также изменены;
- в артериальной стенке есть отложения кальция, а в просвете можно обнаружить тромбы.
Стентирование после инфаркта показано для ограничения зоны поражения миокарда, предотвращения осложнений и рецидива. Операция проводится эндоваскулярным методом – через катетер в место сужения подводят баллон для расширения просвета, затем устанавливают стент. Это обеспечивает поддержание проходимости сосуда и ликвидацию ишемии сердечной мышцы.
Рекомендуем прочитать статью об алкоголе после инфаркта. Из нее вы узнаете о том, можно ли пить алкоголь после инфаркта и о том, что лучше — пиво, вино или водка.
А здесь подробнее о рационе питания после инфаркта миокарда.
После стентирования пациенты должны соблюдать рекомендации по контролю за артериальным давлением, увеличить до нужного уровня физическую активность, придерживаться диеты и принимать медикаменты. Это позволяет вернуться к прежней трудовой детальности и повысить качество жизни.
Полезное видео
Смотрите на видео о стентировании после инфаркта миокарда:
Источник
а) Спасительное стентирование (чрескожное коронарное вмешательство, ЧКВ). Несмотря на увеличение случаев применения первичного ЧКВ, большинство пациентов получает реперфузионную ТЛТ. Имеется небольшое количество данных относительно значимости спасительного ЧКВ у пациентов, у которых ТЛТ была неэффективна.
Рандомизированное исследование больных с передним ИМ (n = 151) показало снижение 30-суточной комбинированной конечной точки, включающей СН и смерть (6,4% vs 16,6%, р = 0,05). В объединенном анализе нескольких небольших исследований были отмечены снижение числа случаев СН и улучшение выживаемости в течение 1 года больных со средним и большим ИМ.
В более позднем исследовании MERLIN (Middlesbtough Early Revascularization to Limit Infarction) рандомизировали на спасительное ЧКВ и консервативную терапию 307 пациентов со снижением подъема сегмента ST < 50% через 60 мин после введения стрептокиназы. Не было получено достоверной разницы в первичной конечной точке (смерть).
Последующая реваскуляризация была меньше (6,5% vs 20,1%, р < 0,01) в группе спасительного ЧКВ (стенты — 50%; ингибиторы рецепторов гликопротеина IIb/IIIа — 3%), но в группе ЧКВ было больше МИ (4,6% vs 0,6%, р < 0,03). Следует отметить, что применение ингибиторов рецепторов гликопротеина IIb/IIIа и стентирования привело к более значительному количеству спасенного миокарда по сравнению с баллонной ангиопластикой (n = 181; индекс сохраненного миокарда 0,35 vs 0,25, р = 0,005).
Недавно опубликованы результаты исследования REACT, в котором 427 пациентов после неэффективной ТЛТ (снижение подъема сегмента ST < 50% за 90 мин) были рандомизированы на консервативное лечение, повторную ТЛТ и спасительное ЧКВ (88% — стенты).
Хотя различий в показателях смертности не было, 6-месячный период без сердечно-сосудистых событий (СССоб) был больше в группе спасительного ЧКВ (84,6% vs 70,1% для консервативного лечения и 68,7% для повторной ТЛТ, р = 0,004).
Ошибки неинвазивной оценки состояния перфузии инфаркт-связанной коронарной артерии (КА) остаются серьезным ограничением данного подхода. Комплексная оценка клинической картины, определение биомаркеров в начале ИМ и через 60 мин, снижение подъема сегмента ST могут улучшить точность прогноза.
Считается, что лучше иметь клинические подозрения и направить пациента на ангиографию до появления нестабильности гемодинамики. Современные руководства рекомендуют спасительное ЧКВ для пациентов с кардиогенным шоком и СН и с меньшим уровнем доказательности — для пациентов с электрической нестабильностью или стойкой ишемией. Кроме этого, результаты недавних исследований свидетельствуют о необходимости такого подхода и к пациентам с признаками сохраняющейся ишемии.
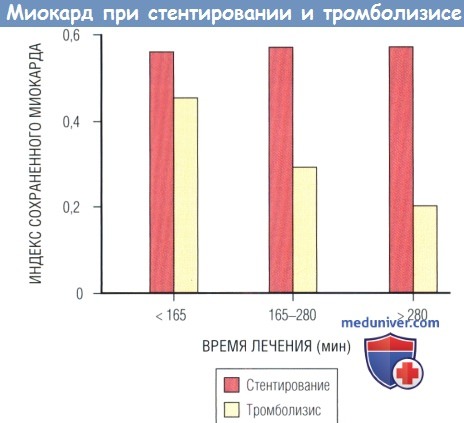
Медиана индекса сохраненного миокарда по терцилям временных интервалов лечения.
Было отмечено уменьшение индекса сохраненного миокарда в зависимости от времени в группе ТЛТ (р = 0,03), но не в группе стентирования (р = 0,59).
б) Упрощенное стентирование (чрескожное коронарное вмешательство, ЧКВ). Совершенствование ТЛТ и ЧКВ привело к комбинированию этих методов при лечении ОИМ с целью восстановления просвета коронарной артерии (КА) и уменьшения риска ишемии. Однако несколько исследований, выполненных за последние 10 лет, продемонстрировали неблагоприятный результат ангиопластики, проведенной непосредственно после ТЛТ: наблюдалось значительно больше кровотечений, повторных ишемий, КШ и летальных исходов.
Эти события возникали из-за вызванной ТЛТ активации тромбоцитов и/или обширного внутрисосудистого кровоизлияния. Современные методы ангиопластики улучшили безопасность процедуры в этом отношении. В исследованиях T1MI-10B (тенектеплаза vs ТАП) и TIMI-14 (уменьшенная доза ТАП и/или абциксимаб) у пациентов, подвергшихся дополнительному или отсроченному вмешательству (стенты в > 60% случаев), мультивариабельный анализ выявил более низкую 30-суточную смертность и/или более низкий риск реинфаркта по сравнению с пациентами с успешной ТЛТ (кровоток TIMI-3 в течение 90 мин) без вмешательства.
Мощный толчок к продолжению фармакоинвазивной стратегии лечения ИМ дали результаты исследований, показавших улучшение выживаемости пациентов высокого риска со спонтанной реперфузией (кровоток TIMI-3) до первичного ЧКВ. Действительно, достижение эффективного раннего восстановления коронарного кровотока у пациентов в течение 2-3 час от начала ИМ приводит к спасению большей части миокарда и росту благоприятных исходов, особенно у доставленных в больницу пациентов. Это обстоятельство стимулировало дальнейшее развитие понятия «упрощенная ангиопластика», которая сочетает в себе преимущества фармакологической реперфузии относительно скорости эффекта и безопасность механического воздействия для полноценного восстановления просвета КА.
Предварительные исследования с полной или уменьшенной дозой тромболитиков с ингибиторами рецепторов гликопротеина IIb/IIIa или без них подтвердили возможность достижения кровотока TIMI-3 при первичной ангиографии. В крупномасштабном исследовании упрощенного ЧКВ ASSENT-4 рандомизировали 1667 пациентов (< 6 час от начала заболевания) на первичное ЧКВ и первичное ЧКВ с предшествующей полной дозой тенектеплазы. Несмотря на большее количество лиц с кровотоком TIMI-3 до ЧКВ (43% vs 15%, р < 0,001) в группе ТЛТ, исследование было завершено досрочно из-за увеличенной смертности в группе упрощенного ЧКВ (6% vs 3%, р = 0,01).
Кроме того, первичная конечная точка (СН, шок или смерть в течение 90 сут) была выше в группе упрощенного ЧКВ (19% vs 13%, р = 0,0045). В этой же группе также было значительно больше МИ (1,8% vs 0%, р < 0,0001) и ишемических осложнений (реинфаркты 6% vs 4%, р = 0,03). В большом исследовании FINESSE (Facilitated Intervention with Enhanced Reperfusion Speed to Stop Events) сравнивают раннее применение абциксимаба vs уменьшенная доза ретеплазы плюс абциксимаб vs абциксимаб и ЧКВ (отбор пациентов в это исследование продолжается). Исследование BRAVE (n = 253) сравнило применение 1/2 дозы ретеплазы и абциксимаба vs один абциксимаб перед ЧКВ и не выявило различий в размере ИМ и клинических исходах.
Недавний метаанализ 17 исследований упрощенного ЧКВ (включая ASSENT-4) показал, что, хотя упрощенное ЧКВ более чем в 2 раза увеличивает начальный кровоток TIMI-3, после ЧКВ кровоток не отличается (89% vs 88%) по сравнению с первичным ЧКВ [100]. Показатели смертности (5% vs 3%, р = 0,04), РСМ (4% vs 1%, р = 0,01), массивных кровотечений (7% vs 5%, р = 0,01) и МИ (1,1% vs 0,3%, р = 0,0008) были значительно выше в группе упрощенного ЧКВ. Неблагоприятные исходы наблюдались у пациентов, получавших тромболитик, в то время как применение одного ингибитора гликопротеина IIb/IIIa не приводило к неблагоприятным результатам.
Геморрагические осложнения, связанные с применением тромболитика (местное артериальное, миокардиальное и церебральное повреждения) и фактором времени (позднее обращение, длительность тромболитического эффекта), взаимодействуют при таком подходе, по-видимому, неблагоприятно. Имеющиеся данные не подтверждают обоснованность комбинации ТЛТ с упрощенным ЧКВ.
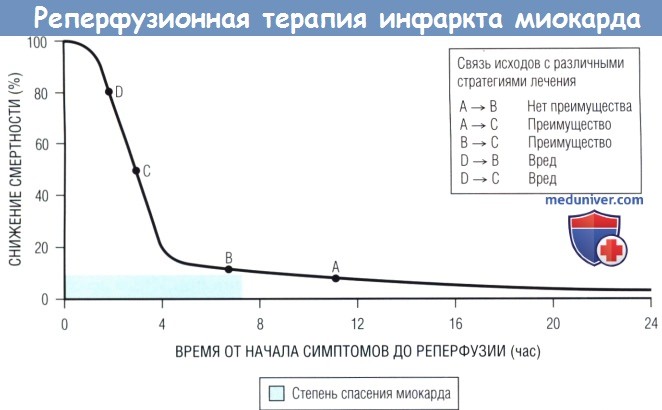
Преимущество реперфузионной терапии в отношении снижения смертности особенно проявляется при проведении в первые 2-3 нас после появления симптомов ОИМ.
Наиболее вероятный результат вмешательства — спасение миокарда.
На длительность этого раннего критинеского периода могут повлиять такие факторы, как наличие функционирующих коллатералей коронарных артерий,
предшествующая ишемия, потребность миокарда в кислороде и продолжительность ишемии.
По прошествии этого раннего периода преимущество реперфузионной терапии в отношении смертности резко уменьшается (кривая снижения смертности сглаживается),
и фактор времени проведения реперфузии становится менее важным.
Преимущество при смещении от точки А или В к точке С будет значительным, а при смещении от точки А к точке В — небольшим.
Лечебная стратегия, отдаляющая начало терапии в ранний критический период, например транспортировка пациента для проведения ЧКВ, может приносить вред (смещение от точки D к точке С или В).
в) Дополнительное стентирование (чрескожное коронарное вмешательство, ЧКВ) после успешного тромболизиса. Как было отмечено ранее, после успешного тромболизиса в большинстве артерий сохраняется существенный остаточный стеноз. Реинфаркты после тромболизиса характеризуются увеличенной смертностью и являются непредсказуемыми событиями. Ранние исследования, оценивавшие эффективность рутинной баллонной ангиопластики, проведенной через несколько часов или суток после успешной ТЛТ, не выявили преимуществ в отношении реинфарктов, функции ЛЖ или выживаемости.
У пациентов со спонтанной или провоцируемой ишемией после тромболитической терапии (ТЛТ) меньше повторных ИМ или эпизодов ишемии после ЧКВ. В связи с этим в современных руководствах рекомендуется проведение дополнительного ЧКВ пациентам после ТЛТ при повторном ИМ, провоцируемой ишемией, или находящимся в шоке (класс IIа) и предлагают рассматривать это вмешательство для пациентов с СИ, ФВ ЛЖ < 40% или серьезными желудочковыми аритмиями.
Усовершенствование техники ЧКВ позволило пересмотреть рутинный подход к пациентам после успешной ТЛТ. Например, в исследованиях TIMI-4, TIMI-10B и TIMI-17 проведение ЧКВ после тромболизиса снижало риск реинфарктов и двухлетнюю смертность. В исследовании GRACIA-1 (GRupo de Analisis de la Cardiopatia Isque’mica Aguda) 500 пациентов были рандомизированы на ангиографию и дополнительное ЧКВ со стентированием и абциксимабом через 6-24 час после ТЛТ или консервативное лечение.
Стентирование артерий было выполнено в 80% случаев в группе инвазивного лечения и в 20% — в группе консервативного лечения. Через 1 год первичная конечная точка, включавшая реинфаркт, реваскуляризацию и смерть, была меньше (9% vs 21%, р = 0,0008) в группе инвазивной терапии. В группе консервативного лечения количество внеплановых реваскуляризаций за время госпитализации в связи со спонтанной ишемией было в 5 раз выше. Хотя это исследование не выявило преимуществ в выживаемости больных, оно показало, что современное дополнительное ЧКВ как часть посттромболитической инвазивной стратегии может быть безопасным и полезным для пациентов.
– Читать “Плюсы и минусы первичного стентирования при инфаркте миокарда”
Оглавление темы “Инфаркт миокарда и нестабильная стенокардия.”:
- Клеточные технологии при инфаркте миокарда
- Сочетание стентирования и тромболитической терапии при инфаркте миокарда
- Плюсы и минусы первичного стентирования при инфаркте миокарда
- Показания для первичного стентирования с фибринолизом при инфаркте миокарда
- Показания для стентирования после фибринолиза при инфаркте миокарда
- Показания для позднего стентирования при инфаркте миокарда после госпитализации
- Требования к врачу, отделению для стентирования (чрескожного коронарного вмешательства, ЧКВ)
- Определение и классификация нестабильной стенокардии по Браунвальду
- Патогенез нестабильной стенокардии
- Клиника и ЭКГ при нестабильной стенокардии
Источник
