Сердечная недостаточность при миоме
Введение
Миома тела матки (МТМ) представляет собой гормонозависимое опухолеподобное доброкачественное заболевание, возникающее из гладкомышечных структур маточной стенки. По данным различных источников, у 30–70% женщин в периоде менопаузального перехода имеется МТМ [1–7]. Однако истинная распространенность этого заболевания в популяции, вероятно, недооценена из-за отсутствия данных о распространенности опухолей без клинической симптоматики. Симптоматическая МТМ может вызывать боли в области таза, поясницы, диспептические явления, обильные менструальные кровотечения, а также осложненные роды и бесплодие [8].
К установленным факторам риска (ФР) МТМ относятся возраст, раннее наступление менархе, отсутствие родов в анамнезе, поздний возраст первой беременности, синдром поликистозных яичников [1]. Артериальная гипертензия, сахарный диабет, образ жизни (курение и др.) и ожирение [9] одновременно являются распространенными ФР сердечно-сосудистых заболеваний (ССЗ) и связаны с развитием атеросклероза [10]. Общие паттерны подтверждают предположение о том, что развитие атеросклеротических бляшек и МТМ имеют общий биологический механизм. Помимо этого, пролиферация гладкомышечных клеток моноклонального происхождения имеет решающее значение в развитии и атеросклероза, и МТМ [11].
С-реактивный белок (СРБ) служит характерным воспалительным предиктором атеросклероза. Повышение уровня СРБ может указывать на субклинический атеросклеротический процесс [12]. Гипергомоцистеинемия, являясь независимым ФР развития атеросклероза, может привести к усилению окислительного стресса, угнетению синтеза оксида азота, пролиферации гладких мышц, дисфункции эндотелия и тромбозу [13]. Повышение концентрации гомоцистеина от легкой до умеренной степени связано с повышенным риском развития атеросклеротических сосудистых заболеваний. Кроме того, гипергомоцистеинемия была предложена в качестве ФР эстроген-индуцированного онкогенеза. В исследовании Y. He et al. уровень СРБ был положительно связан с риском развития МТМ. В этом же исследовании была выявлена обратная связь между уровнем гомоцистеина и развитием МТМ, данная корреляция исчезла после хирургического удаления миомы [14].
В настоящее время в Российской Федерации ишемической болезнью сердца (ИБС) страдают 15–17% взрослого населения, причем после 30 лет ИБС выявляется у 30% женщин [15]. По данным зарубежных авторов, распространенность МТМ варьирует в пределах 20–40% [16, 17]. Однако на сегодняшний день нет данных о распространенности сочетанной патологии (ИБС и МТМ) в общей популяции. Назначение дезагрегантной, а в отдельных случаях антикоагулянтной терапии при проведении чрескожных коронарных вмешательств (ЧКВ) у пациенток с МТМ должно настораживать относительно повышенного риска кровотечений.
Аномальное маточное кровотечение является распространенным состоянием и часто сопутствует МТМ. В ретроспективном исследовании A. Själander et al. частота жалоб на обильные маточные кровотечения в группе исследуемых увеличилась с 17,8% до 29,5% после назначения антикоагулянтной терапии. Аномальные маточные кровотечения усугубляются не только при приеме антагонистов витамина К, но и при комбинированной дезагрегантной терапии [18]. Помимо этого, при назначении новых пероральных антикоагулянтов по поводу фибрилляции предсердий в периоде менопаузального перехода не оценивается их безопасность в отношении маточных кровотечений. В дополнение к этому долгосрочные последствия маточных кровотечений при моно- или двойной дезагрегантной терапии (ДДТ) часто игнорируются или недооцениваются. В частности, ДДТ, назначенная после ЧКВ, может приводить к обильному маточному кровотечению, увеличивая риск анемии, что особенно опасно для пациенток с установленной ИБС [19, 20].
Клиническое наблюдение
Пациентка Ю., 1970 г. р., поступила в отделение кардиологии медико-санитарной части ФГАОУ ВО «Казанский (Приволжский) федеральный университет» с жалобами на боли в прекардиальной области (за грудиной, в 3–4-м межреберьях слева), иррадирующие в спину при физической нагрузке (ходьбе, подъеме по лестнице на 1–2 этажа), купирующиеся в покое, повышение артериального давления до 160/90 мм рт. ст., общую слабость, периодические боли в низу живота, обильные менструации.
Anamnesis morbi et vitae
Вышеуказанные жалобы беспокоят пациентку около 2 лет. Ранее наблюдалась у кардиолога с диагнозом ИБС, стенокардия напряжения, функциональный класс II. Амбулаторно принимает периндоприл 2 мг/сут, розувастатин 20 мг/сут. Последние 2 мес. отмечает значительное снижение толерантности к физической нагрузке. Инсульты, инфаркты отрицает, гиперхолестеринемия выявлена около 4 лет назад. Вредные привычки отрицает. Амбулаторно проведена мультиспиральная компьютерная томография коронарных артерий (МСКТ), по данным которой выявлены критические стенозы правой коронарной артерии (ПКА). Находилась на диспансерном учете в женской консультации по поводу МТМ с 2005 г., наблюдался прогрессивный рост. Трижды проведены диагностические выскабливания полости матки по поводу гиперпластических процессов эндометрия (подтвержденных гистологически), от радикальных оперативных вмешательств в гинекологических отделениях пациентка отказывалась в связи с ИБС. Амбулаторно был назначен агонист гонадотропин-рилизинг-гормона № 6, с последующей установкой внутриматочной системы с левоноргестрелом.
Госпитализирована в отделение кардиологии в плановом порядке.
Предварительный клинический диагноз
Основное заболевание: ИБС. Стенокардия напряжения, функциональный класс III. Атеросклероз коронарных артерий (по данным МСКТ-коронарографии). Гипертоническая болезнь III степени, риск 4.
Осложнения: хроническая сердечная недостаточность
I стадии (функциональный класс III).
Сопутствующее заболевание: множественная интерстициально-субсерозная МТМ с геморрагическим синдромом.
Результаты обследования и лечения
С учетом сопутствующего диагноза совместно кардиологом и гинекологом принято решение о первичном проведении коронароангиографии (КАГ) и дальнейшей тактике лечения.
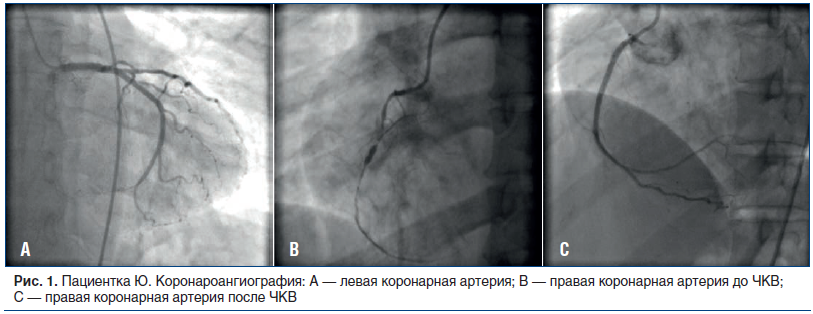
КАГ: тип коронарного кровоснабжения миокарда — правый. При ангиографии левой коронарной артерии (ЛКА) выявлены стенозы в пределах 35–40%, межсистемные коллатерали в дистальные отделы ПКА (рис. 1 А). При ангиографии ПКА выявлены: стеноз устья 80%, критический стеноз проксимального сегмента, функциональная окклюзия с уровня медиального сегмента (рис. 1 В). С учетом результатов КАГ принято решение о проведении ЧКВ на ПКА на первом этапе лечения и эмболизации маточных артерий (ЭМА) на втором этапе.

В отделении ангиографических и рентгенооперационных исследований выполнены баллонная ангиопластика и стентирование устья, проксимального и медиального сегментов ПКА (установлено 3 стента с лекарственным покрытием — эверолимусом) с удовлетворительным ангиографическим результатом (рис. 1С).
В раннем послеоперационном периоде пациентка отмечала улучшение самочувствия в виде отсутствия ангинозных болей при физической нагрузке и в покое. При выписке назначено медикаментозное лечение: антиагрегантная и антикоагулянтная терапия (ацетилсалициловая кислота 100 мг/сут; клопидогрел 75 мг/сут), гиполипидемическая терапия (розувастатин 20 мг/сут), антигипертензивная терапия (периндоприл 4 мг/сут), рекомендована гиполипидемическая диета. До второй госпитализации в гинекологическое отделение находилась на амбулаторном наблюдении у кардиолога и гинеколога, отмечала увеличение объема кровопотери при менструации.
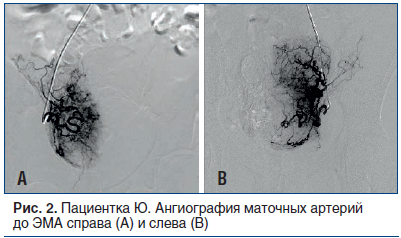
Спустя месяц пациентка поступила на второй этап лечения. Через лучевой доступ проведена ЭМА левой и правой маточных артерий микросферами размером 500–700 µm до стаза контраста в дистальных сегментах артерий (рис. 2 и 3). По результатам послеоперационного ультразвукового исследования (УЗИ) с цветным допплеровским картированием (ЦДК) признаков кровотока в миоматозных узлах не выявлено. Жалобы на момент выписки отсутствовали. Выписана на 5-е сут под амбулаторное наблюдение кардиолога и гинеколога.
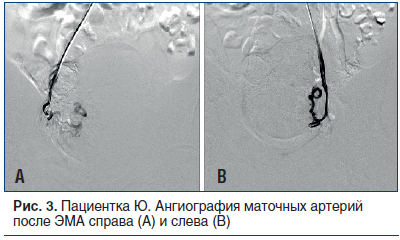
Через 6 мес. проведена контрольная КАГ: ЛКА — без динамики, стенты, установленные в ПКА, проходимы на всем протяжении, без признаков рестеноза. Повторно обследована кардиологом и гинекологом, наблюдалась положительная динамика по обеим патологиям: выявлены повышение толерантности к физической нагрузке (по результатам нагрузочных проб) и регрессия размеров миоматозных узлов с отсутствием признаков кровотока (по результатам УЗИ с ЦДК органов малого таза).
Обсуждение
Выявление у пациентов кардиологического профиля сопутствующих заболеваний, повышающих риск развития геморрагических осложнений, должно быть неотъемлемой частью первичного обследования. В связи с ростом числа женщин, получающих антикоагулянтную и/или дезагрегантную терапию по поводу ССЗ, распространенность аномальных маточных кровотечений увеличивается. Лечение пациенток с ИБС и МТМ должно проводиться совместно кардиологом и гинекологом, с проведением ЧКВ на первом этапе лечения ввиду превалирующего значения ИБС как более жизнеугрожающего заболевания.
Кардиолог должен оценить репродуктивный статус пациентки перед началом ДДТ, гематологические параметры при аномальных маточных кровотечениях, возможность смены ДДТ при возникновении патологических кровотечений, а также своевременно направить к гинекологу для дальнейшего обследования. Гинекологу в свою очередь следует провести оценку менструального анамнеза, выполнить УЗИ с ЦДК органов малого таза, а также избегать назначения гормонального лечения при установленной ИБС, перенесенном инсульте или венозных тромбоэмболических осложнениях [21, 22].
Таким образом, лечение пациенток с сочетанием ССЗ и ММТ требует привлечения различных специалистов (рентгенэндоваскулярных и сосудистых хирургов, гинекологов, кардиологов) для определения наиболее подходящей тактики лечения. Проведение рентгенэндоваскулярного вмешательства позволяет не только объективно подтвердить, но и получить полноценное представление о характере и распространенности патологии. Выбор тактики лечения в пользу ренттгенэндоваскулярной эмболизации привел к адекватному и быстрому устранению патологии с учетом основного заболевания.
В настоящее время не существует клинических рекомендаций по тактике лечения пациенток с сочетанной ИБС и МТМ, а также данных о влиянии ДДТ на возникновение рецидивов кровотечений после проведения ЭМА. Проведение клинических исследований позволит выработать оптимальный междисциплинарный подход к ведению этой категории больных.
Источник


Платон сравнил матку со зверем, который живет в теле женщины. «Сбесившись», он начинает «бегать» по организму и вызывать различные симптомы. Так появился термин «истерия» — тысячелетия назад считалось, что в возникновении этого состояния повинна именно «бешеная» матка, которую современники Гиппократа называли hystera («хистера»).
Времена античности давно прошли, но некоторые мифы существуют до сих пор. Современный «непонятный зверек» в теле женщины, с которым плохо знакомы даже некоторые гинекологи — миома матки. Эта «доброкачественная опухоль» окутана густым туманом из заблуждений и домыслов.
В последние десятилетия в понимании миомы многое изменилось. То, что раньше даже для врачей казалось самим собой разумеющимся, сегодня — не более чем пережиток прошлого. Попробуем разобраться, что же это за зверь такой — миома, и чего она боится.
Миома боится хирургов
В частности, тех, которые занимаются миомэктомиями (удалением миом) и гистерэктомиями (удалением матки). Сама матка тоже боится таких операций, да и весь организм от них не в восторге. Иногда хирургическое вмешательство по поводу миомы становится оптимальным решением, но в большинстве случаев это — стрельба из пушки по мухам. Стоит ли готовить тяжелую артиллерию там, где можно обойтись мухобойкой? И насекомых нет, и стены в доме целы (впрочем, всё по порядку, о «мухобойках» против миом поговорим ниже).
Главные недостатки операции:
- Собственно, то, что это — операция. С наркозом и со всеми вытекающими рисками.
- В 7-14 случаях из ста через год после операции миома вырастает снова.
- Риск рецидива можно снизить, но для этого придется принимать гормоны. Чему организм тоже не всегда бывает рад.
- Одно из осложнений после операции — спайки в малом тазу. Из-за них могут возникнуть проблемы с зачатием ребенка.
- Если врач предлагает удалить миому вместе с маткой, то стоит задуматься о последствиях. Они могут оказаться серьезнее, чем проблемы, которые вызывала сама миома. Даже если женщина уже не планирует заводить детей.
Вывод: Миома боится хирургического вмешательства, но не боятся его, пожалуй, только гинекологи. Недостатков у этого метода лечения хватает. Обычно к операции прибегают, когда есть большие узлы, и женщина планирует беременность в самое ближайшее время.
Миома немного боится лекарств
Если быть точнее, легкий страх она испытывает всего перед одним препаратом — блокатором гестагеновых рецепторов Улипристалом (он же Эсмия). При правильном курсе лечения около 60% миоматозных узлов уменьшаются. Однако эффект различается у разных женщин. Ученые не могут точно сказать, надолго ли лекарство поможет уменьшить миому.
Прочие гормональные препараты и спирали «Мирена» миоме нипочем. Как бы ни хотелось верить в обратное некоторым гинекологам «старой школы».
Миома боится остаться без кислорода
Об этом врачи и ученые знают уже давно (с 70-х годов прошлого века), но некоторые до сих пор отказываются верить. Существует такая процедура — эмболизация маточных артерий, когда в сосуд, питающий миому, через катетер вводят специальные микросферы. Они перекрывают просвет артерии, миома остается без кислорода и питательных веществ, «усыхает» и по сути превращается в соединительную ткань. Была большая виноградина, превратилась в маленькую изюминку. А то и вовсе отделилась от стенки матки и «вышла» через влагалище.
В настоящее время американские врачи считают эмболизацию маточных артерий (сокращенно — ЭМА) золотым стандартом лечения миомы, потому что она имеет ряд преимуществ:
- Рецидивов, в отличие от хирургического лечения, практически не бывает.
- Если миома вызывала симптомы, после ЭМА они полностью проходят у 99% женщин.
- Процедура длится 15-30 минут. Нет никакого разреза. Врачу нужно лишь проколоть кожу, чтобы ввести в сосуд катетер. Наркоз тоже не нужен.
Вывод: Эмболизация маточных артерий — та самая процедура, которую современные эксперты рекомендуют применять у большинства женщин с миомой. Возможно, вы слышали другую точку зрения, но это — лишь точка зрения. Эффективность и безопасность ЭМА доказаны научно.
Миома боится климакса
И поэтому женщин старшего возраста нужно лечить не всегда. Когда в организме снижается уровень гормонов, что неминуемо происходит у здоровых женщин после менопаузы, узлы перестают расти.
Чего не боится миома?
Миоматозные узлы не боятся народных средств, БАДов, гомеопатии и всевозможных методов альтернативной медицины. Пока женщина ставит эксперименты над своим здоровьем, вместо того чтобы обратиться к врачу, миома может сильно вырасти. Потребуется более серьезное лечение.
К чему миома равнодушна?
Классически считается, что миому нужно «носить» в своем теле аккуратно, как бомбу замедленного действия, соблюдать массу ограничений. У современных ученых для женщин хорошие новости: скорость роста миомы почти не зависит от образа жизни. С миомой можно:
- заниматься сексом;
- заниматься спортом (если миома не приводит к обильным месячным и не настолько огромна, что сдавливает соседние органы);
- принимать оральные контрацептивы — но только как средство контрацепции, от миомы они не лечат;
- принимать ванну и ходить в сауну;
- делать массаж;
- есть всё, что вам нравится (при обильных месячных нужно позаботиться, чтобы в рационе присутствовало достаточное количество железа).
И строго говоря, миому нельзя назвать опухолью, даже доброкачественной. Рак в ней развивается не чаще, чем в здоровом миометрии (мышечном слое стенки матки). Поэтому бояться её не стоит. Но наблюдаться у гинеколога нужно однозначно.
Подробнее о миоме матки на сайте www.embolization.ru
Источник
![]()
Обновлено: 13 Мая 2020
Борис Юрьевич Бобров | Эндоваскулярный хирург, кандидат медицинских наук, самый большой персональный опыт ЭМА в России
Содержание статьи
Миома матки – одно из самых распространенных гинекологических заболеваний. Оно встречается у 87% женщин. До сих пор из-за страха перед «перерождением» миомы в злокачественную опухоль или в силу других сложившихся стереотипов, к этому заболеванию применяют излишне агрессивные методы лечения. По данным ВОЗ, в России из-за наличия миомы более 800 тысяч женщин в год лишаются матки. Между тем, современная медицина кардинально изменила представления о природе этого заболевания. Принципиально изменились и подходы к его лечению.
Об устаревших стереотипах
В 1980-е годы основной причиной развития миомы считался дисбаланс половых гормонов. Предполагалось, что миоматозные узлы растут из-за повышенного уровня женского полового гормона эстрадиола. Следовательно, прогестерон, как антагонист эстрадиола, должен подавлять его эффекты и останавливать рост миоматозных узлов. Это ошибочное представление привело к повсеместному внедрению в практику лечения миомы матки препарата «Дюфастон». Однако такой подход приводил лишь к прогрессированию заболевания.
Сегодня многочисленные исследования доказали, что развитие миомы матки не связано с гормональными нарушениями в организме женщины. А прогестерон – это основной гормон, который не останавливает, а стимулирует рост миомы. Поэтому прием препаратов прогестерона при этом заболевании противопоказан!
Неминуемое перерождение миомы из доброкачественной опухоли в злокачественную – еще один устаревший стереотип, не имеющий ничего общего с реальностью. В настоящее время есть достоверные научные доказательства того, что миома не перерождается в злокачественную опухоль и не увеличивает риск развития онкологических заболеваний матки.
Очень редкая злокачественная опухоль матки (лейомиосаркома) никак не связана с наличием миомы. Она развивается, как независимое, самостоятельное заболевание.
Современное представление о миоме матки
С точки зрения современной медицины, миома матки – это хроническое заболевание матки, при котором в ней образуются единичные или множественные узлы различной локализации. Рост миоматозного узла начинается с дефекта в одной гладкомышечной клетке матки. То есть это локальное (местное), а не системное заболевание. С гормональным дисбалансом в организме женщины оно не связано. Что еще важно знать о миоме?
- Каждый миоматозный узел растет из одной конкретной клетки мышцы матки. Если в матке возникает несколько узлов, то каждый из них развивается независимо от других, из отдельной дефектной клетки.
- Деление гладкомышечной клетки запускает прогестерон. Дефектная клетка имеет повышенную чувствительность к этому гормону. Клетки миомы матки активно делятся во время второй фазы менструального цикла и в период беременности – то есть, когда уровень прогестерона в организме значительно возрастает.
- Нет ни одной достоверной теории, объясняющей причину возникновения клеток-предшественниц миомы матки. Предполагается, что повреждающим фактором может быть множество менструальных циклов при малом количестве беременностей. Согласно другой теории, дефект в клетках возникает во время внутриутробного периода, когда гладкомышечные клетки матки длительное время находятся в нестабильном состоянии.
- Миома матки не возникает до начала менструаций (до полового созревания) и, как правило, самостоятельно регрессирует (останавливается в развитии и уменьшается) после менопаузы. То есть это заболевание ограничено репродуктивным периодом жизни женщины.
Группы риска: у кого чаще всего развивается миома матки?
К провоцирующим факторам, повышающим вероятность развития миомы матки, относят:
- раннее начало менструации и более позднее наступление менопаузы;
- расовую принадлежность (у женщин негроидной расы вероятность формирования миоматозных узлов в несколько раз выше);
- ожирение или избыточную массу тела;
- дефицит витамина D;
- наследственность (наличие миоматозных узлов у близких родственниц повышает риск);
- малое количество беременностей, закончившихся родами;
- множественные воспалительные заболевания органов малого таза, хирургические операции на матке, многочисленные выскабливания и аборты.
Какие осложнения может вызвать миома матки?
В большинстве случаев миома матки не опасна. У 65% женщин она протекает бессимптомно и не оказывает влияния на здоровье. Если же миома сопровождается симптомами, то самое частое осложнение, которое может возникнуть, – железодефицитная анемия. Причем это заболевание нередко протекает скрытно. На фоне такого течения железодефицитной анемии страдает множество органов и систем. Для оценки скрытой кровопотери обязательно назначаются общий анализ крови и исследование показателей железа и ферритина.
Другое осложнение миомы матки – компрессия (сдавливание) соседних органов (мочевого пузыря, кишки, крупных венозных стволов и т.д.) и нарушение функции этих органов. Миомы, растущие в полости матки или деформирующие ее, могут мешать наступлению и вынашиванию беременности.
Какими бывают миоматозные узлы?
У стенки матки есть три слоя:
- внутренний слой – слизистая оболочка, выстилающая полость матки (эндометрий);
- мышечная оболочка – это самый толстый мышечный слой (миометрий);
- наружный слой – серозная оболочка.
Миоматозные узлы могут располагаться в разных слоях матки. От того, в каком именно слое образовался узел, зависит его название.
- Субмукозные узлы (подслизистые) – их рост направлен в полость матки;
- интрамуральные (межмышечные) располагаются непосредственно в стенке матки;
- субсерозные (подбрюшинные) растут снаружи матки;
- шеечные (перешеечные) узлы локализуются в шейке матки или в области перешейка.
Помимо этого, бывают смешанные локализации узлов, то есть один узел может располагаться в нескольких слоях матки. Отдельно выделяют узлы «на ножке» (образования на тонком основании, растущие снаружи матки) и интралигаментарные узлы (располагающиеся в широкой связке матки).
Какие причины влияют на скорость роста миомы?
К сожалению, медицине пока неизвестно, какие именно причины влияют на скорость роста миоматозных узлов. Вопреки распространенному мнению, нет никаких научных подтверждений, доказывающих, что посещение бани или сауны, а также массаж, загар, физиопроцедуры и другие внешние факторы оказывают стимулирующее воздействие на рост миомы.
Динамика роста миомы совершенно непредсказуема. Узлы могут годами оставаться в одних и тех же размерах, а после начать стремительно расти. Некоторые узлы способны самостоятельно нарушить свое кровоснабжение и погибнуть. В среднем скорость роста узлов составляет не более 1-2 см в год.
Как распознать миому матки?
Симптомы миомы (обильные кровотечения, давление на мочевой пузырь, частые мочеиспускания, боль в низу живота и т.д.) проявляются только у 30–35% женщин. У остальных миома матки протекает бессимптомно. Чтобы вовремя выявить заболевание, достаточно регулярно (не реже раза в год) посещать гинеколога, даже если ничего не беспокоит.
Для диагностики миомы матки чаще всего достаточно ультразвукового исследования. Обычный гинекологический осмотр на кресле – неинформативный метод диагностики миомы. С его помощью невозможно выявить, например, небольшие миоматозные узлы, которые не увеличивают общие размеры матки. МРТ малого таза применяют только при очень больших размерах матки и узлов. Проведение гистероскопии (исследование полости матки миниатюрной камерой) целесообразно при субмукозных узлах (растущих в полость матки).
Как лечить миому матки?
Миому матки не всегда нужно лечить. Если она бессимптомна, не растет, не мешает наступлению и вынашиванию беременности, то достаточно наблюдения (УЗИ 1 раз в 6 месяцев).
На сегодняшний день есть три метода лечения миомы матки, которые позволяют эффективно решить проблему во всех случаях:
- медикаментозное лечение (прием лекарственного препарата «Эсмия», блокирующего рецепторы прогестерона в тканях). Этот метод оптимально использовать для лечения маленьких, впервые выявленных узлов. Но эффект от медикаментозного лечения временный, то есть через некоторое время после окончания приема препарата рост узлов возобновляется.
- Хирургическое лечение (миомэктомия) применяется в случае, если женщина планирует беременность, а миоматозные узлы могут этому помешать. После миомэктомии нередки рецидивы: через несколько лет после вмешательства узлы вырастают вновь более чем в половине случаев. Полное удаление матки целесообразно только в запущенных случаях, когда матка, измененная узлами, достигает гигантских размеров или у женщины имеется сопутствующая гинекологическая патология.
- Эмболизация маточных артерий (ЭМА). ЭМА – оптимальный метод лечения при множественной миоме у женщин, планирующих беременность. Принцип метода заключается в прекращении кровоснабжения миоматозных узлов. В результате они уменьшаются в размере и погибают. Эффективность ЭМА составляет 94-99%. Рецидивы после нее не наблюдаются.
Если у вас выявили миому матки и вы хотите получить мнение опытных специалистов о возможных вариантах лечения, врачи нашего экспертного совета готовы проконсультировать вас бесплатно в режиме онлайн (заполните анкету ниже). Наши специалисты владеют всеми современными методами лечения миомы матки и будут сопровождать вас на всех этапах лечебного процесса.
Список литературы:
- Савицкий Г. А., Иванова Р. Д., Свечникова Ф. А. Роль локальной гипергормонемии в патогенезе темпа прироста массы опухолевых узлов при миоме матки //Акушерство и гинекология. – 1983. – Т. 4. – С. 13-16.
- Сидорова И.С. Миома матки (современные аспекты этиологии, патогенеза, классификации и профилактики). В кн.: Миома матки. Под ред. И.С. Сидоровой. М: МИА 2003; 5—66.
- Мериакри А.В. Эпидемиология и патогенез миомы матки. Сиб мед журн 1998; 2: 8—13.
- Бобров Б.Ю. Эмболизация маточных артерий в лечении миомы матки. Современное состояние вопроса // Журнал акушерства и женских болезней. 2010. №2. С. 100-125
- Б. Ю. Бобров, С. А. Капранов, В. Г. Бреусенко и др. Эмболизация маточных артерий: современный взгляд на проблему. «Диагностическая и интервенционная радиология» том 1 № 2 / 2007

Эндоваскулярный хирург, кандидат медицинских наук, самый большой персональный опыт ЭМА в России

Гинеколог, кандидат медицинских наук

Акушер-гинеколог, онколог, кандидат медицинских наук

Врач акушер-гинеколог
Источник
