Сердечная недостаточность ишемическая болезнь сердца
Ишемическая болезнь сердца (ИБС) – органическое и функциональное поражение миокарда, вызванное недостатком или прекращением кровоснабжения сердечной мышца (ишемией). ИБС может проявляться острыми (инфаркт миокарда, остановка сердца) и хроническими (стенокардия, постинфарктный кардиосклероз, сердечная недостаточность) состояниями. Клинические признаки ИБС определяются конкретной формой заболевания. ИБС является самой распространенной в мире причиной внезапной смерти, в том числе лиц трудоспособного возраста.
Общие сведения
Ишемическая болезнь сердца является серьезнейшей проблемой современной кардиологии и медицины в целом. В России ежегодно фиксируется около 700 тыс. смертей, вызванных различными формами ИБС, в мире смертность от ИБС составляет около 70%. Ишемическая болезнь сердца в большей степени поражает мужчин активного возраста (от 55 до 64 лет), приводя к инвалидности или внезапной смерти. В группу ИБС входят остро развивающиеся и хронически протекающие состояния ишемии миокарда, сопровождающиеся последующими его изменениями: дистрофией, некрозом, склерозом. Эти состояния рассматриваются, в том числе, и в качестве самостоятельных нозологических единиц.
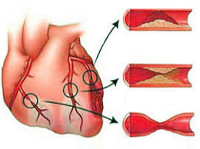
Ишемическая болезнь сердца
Причины
Подавляющее большинство (97-98%) клинических случаев ИБС обусловлено атеросклерозом коронарных артерий различной степени выраженности: от незначительного сужения просвета атеросклеротической бляшкой до полной сосудистой окклюзии. При 75%-ном коронаростенозе клетки сердечной мышцы реагируют на недостаток кислорода, и у пациентов развивается стенокардия напряжения.
Другими причинами, вызывающими ИБС, служат тромбоэмболия или спазм венечных артерий, развивающиеся обычно на фоне уже имеющегося атеросклеротического поражения. Кардиоспазм усугубляет обструкцию коронарных сосудов и вызывает проявления ишемической болезни сердца.
К факторам, способствующим возникновению ИБС, относятся:
- гиперлипедемия
Способствует развитию атеросклероза и увеличивает риск ишемической болезни сердца в 2-5 раз. Наиболее опасными в плане риска ИБС являются гиперлипидемии типов IIа, IIб, III, IV, а также уменьшение содержания альфа-липопротеинов.
- артериальная гипертония
Артериальная гипертония увеличивает вероятность развития ИБС в 2-6 раз. У пациентов с систолическим АД = 180 мм рт. ст. и выше ишемическая болезнь сердца встречается до 8 раз чаще, чем у гипотоников и людей с нормальным уровнем артериального давления.
- курение
По различным данным, курение сигарет увеличивает заболеваемость ИБС в 1,5-6 раз. Летальность от ишемической болезни сердца среди мужчин 35-64 лет, выкуривающих 20-30 сигарет ежедневно, в 2 раза выше, чем среди некурящих той же возрастной категории.
- гиподинамия и ожирение
Физически малоактивные люди рискуют заболеть ИБС в 3 раза больше, чем лица, ведущие активный образ жизни. При сочетании гиподинамии с избыточной массой тела этот риск возрастает в разы.
- нарушение толерантности к углеводам
При сахарном диабете, в т. ч. латентном, риск заболеваемости ишемической болезнью сердца увеличивается в 2-4 раза.
К факторам, создающим угрозу развития ИБС следует также отнести отягощенную наследственность, мужской пол и пожилой возраст пациентов. При сочетании нескольких предрасполагающих факторов, степень риска в развитии ишемической болезни сердца существенно возрастает.
Причины и скорость развития ишемии, ее длительность и выраженность, исходное состояние сердечно-сосудистой системы индивидуума определяют возникновение той или иной формы ишемической болезни сердца.
Патогенез
В основе развития ИБС лежит дисбаланс между потребностью сердечной мышцы в кровоснабжении и фактическим коронарным кровотоком. Этот дисбаланс может развиваться в связи с резко возросшей потребностью миокарда в кровоснабжении, но недостаточном его осуществлении, либо при обычной потребности, но резком снижении коронарного кровообращения. Дефицит кровоснабжения миокарда особенно выражен в случаях, когда коронарный кровоток снижен, а потребность сердечной мышцы в притоке крови резко возрастает. Недостаточное кровоснабжение тканей сердца, их кислородное голодание проявляется различными формами ишемической болезни сердца.
Классификация
В качестве рабочей классификации, по рекомендации ВОЗ (1979 г.) и ВКНЦ АМН СССР (1984 г.), кардиологами-клиницистами используется следующая систематизация форм ИБС:
1. Внезапная коронарная смерть (или первичная остановка сердца) – внезапно развившееся, непредвиденное состояние, в основе которого предположительно лежит электрическая нестабильность миокарда. Под внезапной коронарной смертью понимается мгновенная или наступившая не позднее 6 часов после сердечного приступа смерть в присутствии свидетелей. Выделяют внезапную коронарную смерть с успешной реанимацией и с летальным исходом.
2. Стенокардия:
- стенокардия напряжения (нагрузки):
- стабильная (с определением функционального класса I, II, III или IV);
- нестабильная: впервые возникшая, прогрессирующая, ранняя послеоперационная или постинфарктная стенокардия;
- спонтанная стенокардия (син. особая, вариантная, вазоспастическая, стенокардия Принцметала)
3. Безболевая форма ишемии миокарда.
4. Инфаркт миокарда:
- крупноочаговый (трансмуральный, Q-инфаркт);
- мелкоочаговый (не Q-инфаркт);
5. Постинфарктный кардиосклероз.
6. Нарушения сердечной проводимости и ритма (форма).
7. Сердечная недостаточность (форма и стадии).
В кардиологии существует понятие «острого коронарного синдрома», объединяющего различные формы ишемической болезни сердца: нестабильную стенокардию, инфаркт миокарда (с Q-зубцом и без Q-зубца). Иногда в эту же группу включают и внезапную коронарную смерть, вызванную ИБС.
Симптомы ИБС
Клинические проявления ИБС определяются конкретной формой заболевания (смотри инфаркт миокарда, стенокардия). В целом ишемическая болезнь сердца имеет волнообразное течение: периоды стабильно нормального самочувствия чередуются с эпизодами обострения ишемии. Около 1/3 пациентов, особенно с безболевой ишемией миокарда, совсем не ощущают наличия ИБС. Прогрессирование ишемической болезни сердца может развиваться медленно, десятилетиями; при этом могут изменяться формы заболевания, а стало быть, и симптомы.
К общим проявлениям ИБС относятся загрудинные боли, связанные с физическими нагрузками или стрессами, боли в спине, руке, нижней челюсти; одышка, усиленное сердцебиение или ощущение перебоев; слабость, тошнота, головокружение, помутнение сознания и обмороки, чрезмерная потливость. Нередко ИБС выявляется уже на стадии развития хронической сердечной недостаточности при появлении отеков на нижних конечностях, выраженной одышке, заставляющей пациента принимать вынужденное сидячее положение.
Перечисленные симптомы ишемической болезни сердца обычно не встречаются одновременно, при определенной форме заболевания наблюдается преобладание тех или иных проявлений ишемии.
Предвестниками первичной остановки сердца при ишемической болезни сердца могут служить приступообразно возникающие ощущения дискомфорта за грудиной, страх смерти, психоэмоциональная лабильность. При внезапной коронарной смерти пациент теряет сознание, происходит остановка дыхания, отсутствует пульс на магистральных артериях (бедренных, сонных), не прослушиваются тоны сердца, расширяются зрачки, кожные покровы становятся бледно-сероватого оттенка. Случаи первичной остановки сердца составляют до 60% летальных исходов ИБС, преимущественно на догоспитальном этапе.
Осложнения
Гемодинамические нарушения в сердечной мышце и ее ишемические повреждения вызывают многочисленные морфо-функциональные изменения, определяющие формы и прогноз ИБС. Результатом ишемии миокарда являются следующие механизмы декомпенсации:
- недостаточность энергетического метаболизма клеток миокарда – кардиомиоцитов;
- «оглушенный» и «спящий» (или гибернирующий) миокард – формы нарушения сократимости левого желудочка у пациентов с ИБС, имеющие преходящий характер;
- развитие диффузного атеросклеротического и очагового постинфарктного кардиосклероза – уменьшение количества функционирующих кардиомиоцитов и развитие на их месте соединительной ткани;
- нарушение систолической и диастолической функций миокарда;
- расстройство функций возбудимости, проводимости, автоматизма и сократимости миокарда.
Перечисленные морфо-функциональные изменения миокарда при ИБС приводят к развитию стойкого снижения коронарного кровообращения, т. е. сердечной недостаточности.
Диагностика
Диагностику ИБС осуществляют кардиологи в условиях кардиологического стационара или диспансера с использованием специфических инструментальных методик. При опросе пациента выясняются жалобы и наличие характерных для ишемической болезни сердца симптомов. При осмотре определяются наличие отеков, цианоза кожных покровов, шумов в сердце, нарушений ритма.
Лабораторно-диагностические анализы предполагают исследование специфических ферментов, повышающихся при нестабильной стенокардии и инфаркте (креатинфосфокиназы (в течение первых 4—8 часов), тропонина-I (на 7—10 сутки), тропонина-Т (на 10—14 сутки), аминотрансферазы, лактатдегидрогеназы, миоглобина (в первые сутки)). Эти внутриклеточные белковые ферменты при разрушении кардиомиоцитов высвобождаются в кровь (резорбционно-некротический синдром). Также проводится исследование уровня общего холестерина, липопротеидов низкой (атерогенных) и высокой (антиатерогенных) плотности, триглицеридов, сахара крови, АЛТ и АСТ (неспецифических маркеров цитолиза).
Важнейшим методом диагностики кардиологических заболеваний, в т. ч. ишемической болезни сердца, является ЭКГ – регистрация электрической активности сердца, позволяющая обнаружить нарушения нормального режима работы миокарда. ЭхоКГ – метод УЗИ сердца позволяет визуализировать размеры сердца, состояние полостей и клапанов, оценить сократимость миокарда, акустические шумы. В некоторых случаях при ИБС проводят стресс эхокардиографию – ультразвуковую диагностику с применением дозированной физической нагрузки, регистрирующую ишемию миокарда.
В диагностике ишемической болезни сердца широко используются функциональные пробы с нагрузкой. Они применяются для выявления ранних стадий ИБС, когда нарушения еще невозможно определить в состоянии покоя. В качестве нагрузочных тестов используются ходьба, подъем по лестнице, нагрузки на тренажерах (велотренажере, беговой дорожке), сопровождающиеся ЭКГ-фиксацией показателей работы сердца. Ограниченность применения функциональных проб в ряде случаев вызвана невозможностью выполнения пациентами требуемого объема нагрузки.
Холтеровское суточное мониторирование ЭКГ предполагает регистрацию ЭКГ, выполняемую в течение суток и выявляющую периодически возникающие нарушения в работе сердца. Для исследования используется портативный аппарат (холтеровский монитор), фиксируемый на плече или поясе пациента и снимающий показания, а также дневник самонаблюдения, в котором пациент отмечает по часам свои действия и происходящие изменения в самочувствии. Полученные в ходе мониторирования данные обрабатываются на компьютере. ЭКГ-мониторирование позволяет не только выявить проявления ишемической болезни сердца, но также причины и условия их возникновения, что особенно важно в диагностике стенокардии.
Чрезпищеводная электрокардиография (ЧПЭКГ) позволяет детально оценить электрическую возбудимость и проводимость миокарда. Суть метода состоит во введении датчика в пищевод и регистрации показателей работы сердца, минуя помехи, создаваемые кожными покровами, подкожно-жировой клетчаткой, грудной клеткой.
Проведение коронарографии в диагностике ишемической болезни сердца позволяет контрастировать сосуды миокарда и определять нарушения их проходимости, степень стеноза или окклюзии. Коронарография используется для решения вопроса об операции на сосудах сердца. При введении контрастного вещества возможны аллергические явления, в т. ч. анафилаксия.
Лечение ИБС
Тактика лечения различных клинических форм ишемической болезни сердца имеет свои особенности. Тем не менее, можно обозначить основные направления, применяемые для лечения ИБС:
- немедикаментозная терапия;
- лекарственная терапия;
- проведение хирургической реваскуляризации миокарда (аорто-коронарного шунтирования);
- применение эндоваскулярных методик (коронарной ангиопластики).
К немедикаментозной терапии относятся мероприятия по коррекции образа жизни и питания. При различных проявлениях ИБС показано ограничение режима активности, т. к. при физической нагрузке происходит увеличение потребности миокарда в кровоснабжении и кислороде. Неудовлетворенность этой потребности сердечной мышцы фактически и вызывает проявления ИБС. Поэтому при любых формах ишемической болезни сердца ограничивается режим активности пациента с последующим постепенным расширением его во время реабилитации.
Диета при ИБС предусматривает ограничение приема воды и соли с пищей для снижения нагрузки на сердечную мышцу. С целью замедления прогрессирования атеросклероза и борьбы с ожирением также назначается низкожировая диета. Ограничиваются, а по возможности, исключаются следующие группы продуктов: жиры животного происхождения (сливочное масло, сало, жирное мясо), копченая и жареная пища, быстро всасывающиеся углеводы (сдобная выпечка, шоколад, торты, конфеты). Для поддержания нормального веса необходимо соблюдать баланс между потребляемой и расходуемой энергией. При необходимости снижения веса дефицит между потребляемыми и расходуемыми энергозапасами должен составлять минимум 300 кКл ежедневно, с учетом, что за сутки при обычной физической активности человек тратит около 2000—2500 кКл.
Лекарственная терапия при ИБС назначается по формуле «A-B-C»: антиагреганты, β-адреноблокаторы и гипохолестеринемические препараты. При отсутствии противопоказаний возможно назначение нитратов, диуретиков, антиаритмических препаратов и др. Отсутствие эффекта от проводимой лекарственной терапии ишемической болезни сердца и угроза развития инфаркта миокарда являются показанием к консультации кардиохирурга для решения вопроса об оперативном лечении.
К хирургической реваскуляризации миокарда (аортокоронарное шунтирование – АКШ) прибегают с целью восстановления кровоснабжения участка ишемии (реваскуляризации) при резистентности к проводимой фармакологической терапии (например, при стабильной стенокардии напряжения III и IV ФК). Суть метода АКШ заключается в наложении аутовенозного анастомоза между аортой и пораженной артерией сердца ниже участка ее сужения или окклюзии. Тем самым создается обходное сосудистое русло, доставляющее кровь к участку ишемии миокарда. Операции АКШ могут проводиться с использованием искусственного кровообращения или на работающем сердце. К малоинвазивным хирургическим методикам при ИБС относится чрескожная транслюминальная коронарная ангиопластика (ЧТКА) – баллонное «расширение» стенозированного сосуда с последующей имплантацией каркас-стента, удерживающего достаточный для кровотока просвет сосуда.
Прогноз и профилактика
Определение прогноза при ИБС зависит от взаимосвязи различных факторов. Так неблагоприятно сказывается на прогнозе сочетание ишемической болезни сердца и артериальной гипертонии, тяжелых расстройств липидного обмена и сахарного диабета. Лечение может лишь замедлить неуклонное прогрессирование ИБС, но не остановить ее развитие.
Самой эффективной профилактикой ИБС является снижение неблагоприятного воздействия факторов угрозы: исключение алкоголя и табакокурения, психоэмоциональных перегрузок, поддержание оптимальной массы тела, занятия физкультурой, контроль АД, здоровое питание.
Источник
НИИ кардиологии им. А.Л.Мясникова РКНПК Минздрава РФ, Москва
Один из основных постулатов медицины гласит, что оптимальное лечение заболевания невозможно без знания его причины. Однако этот принцип трудно применим, когда речь заходит о хронической сердечной недостаточности (ХСН). Это связано с тем, что, хотя болезни, приводящие к развитию ХСН, многочисленны и разнообразны, финальный итог для всех один — декомпенсация сердечной деятельности. Возникает иллюзия, что причина ХСН уже не имеет значения и лечение во всех случаях одинаково: будь то ишемическая болезнь сердца (ИБС), дилатационная кардиомиопатия (ДКМП) или гипертоническое сердце. Однако это не так. Любая болезнь, лежащая в основе ХСН, имеет свои особенности, откладывающие отпечаток на течение сердечной недостаточности, ее терапию и прогноз. Тем более это относится к такому частому и серьезному заболеванию, каким в настоящее время является ИБС.
Эпидемиология
В настоящее время считается доказанным, что ИБС является основной этиологической причиной развития сердечной недостаточности. Этот вывод можно сделать на основании анализа результатов специальных эпидемиологических исследований в популяциях, а также по оценке контингента больных, включенных в многоцентровые исследования по выживаемости больных ХСН. Так, в 10 таких исследованиях, проведенных в последние годы, ишемическая этиология декомпенсации была отмечена в среднем у 64% больных (табл. 1). Разброс результатов этих исследований объясняется различием диагностических критериев ИБС, используемых в разных центрах, популяционными различиями, а также может быть связан с исследуемым препаратом. Так, в работах, связанных с b-блокаторами (в табл. — это исследования CIBISI и USCT), существенное место среди причин ХСН наряду с ИБС занимает ДКМП (36 и 52% соответственно); там же, где исследуются ингибиторы АПФ, основной причиной декомпенсации является, как правило, ИБС, а частота случаев ДКМП не превышает 22%.
Эпидемиологические исследования в популяциях также свидетельствуют о существенном преобладании ИБС среди основных причин развития ХСН (табл. 2). В исследовании распространенности ХСН в городе Глазго ИБС, как причина ХСН, наблюдалась у 95% больных (!). Из результатов этих же исследований следует, что артериальная гипертония также занимает значительное место в структуре причин развития ХСН, хотя в клинической практике гипертония чаще всего сочетается с ИБС. А вот роль ДКМП, как причины ХСН, в таких эпидемиологических исследованиях невелика и оценивается 0—11%.
В ретроспективном исследовании, проведенном в НИИ кардиологии им. А.Л. Мясникова, также было выявлено, что ИБС в последние годы стала главной причиной развития сердечной недостаточности [2], причем “вклад” ИБС в общую структуру заболеваемости ХСН постоянно увеличивается (табл. 3).
Патофизиология сердечной недостаточности при ИБС
Механизмов развития и прогрессирования сердечной недостаточности при ИБС может быть несколько. Самым важным из них является, безусловно, инфаркт миокарда (ИМ). Внезапная “потеря” более или менее обширного участка сердечной мышцы приводит к развитию дисфункции желудочка(ов), и если больной не погибает (что бывает в 50% случаев), дисфункция со временем, как правило, манифестирует симптомами сердечной недостаточности. В исследовании TRACE [3] у 40% больных, перенесших ИМ, уже в первые дни отмечалась тяжелая дисфункция ЛЖ, причем у 65% это был первый в жизни инфаркт; у 74% из них вскоре развилась клиническая картина сердечной недостаточности. Однако и те 60% больных, которым удается избежать развития дисфункции на раннем этапе заболевания, не могут считать себя в “безопасности”. За обширным инфарктом следуют изменения сердечной мышцы, получившие название “ремоделирование” сердца. Этот феномен включает в себя процессы, затрагивающие пораженную область и здоровые участки миокарда, когда инфарктная зона “растягивается”, не в силах противостоять возросшему внутрижелудочковому давлению, а непораженные участки гипертрофируются и дилатируются, приспосабливаясь к новым условиям функционирования. Ремоделирование — процесс, который включает изменение во времени формы и функции желудочков, экспансию рубцовой ткани, что тесно сопряжено с изменением нейрогуморального фона организма.
Однако особенности развития ХСН у больных ИБС обусловлены не только желудочковой дисфункцией, но также постоянным участием в этом процессе коронарной недостаточности.
Частые эпизоды локальной ишемии приводят к периодам усиления локальной систолической дисфункции, проявляющейся одышкой (эквивалент стенокардии). Так, например, в исследовании SOLVD 37% больных ХСН предъявляли жалобы также на стенокардитические боли [4]. Частые эпизоды появления и исчезновения ишемии способствуют продлению систолической дисфункции в этих областях, что эквивалентно состоянию “оглушенного” (stunning) миокарда, описанного при окклюзии и последующем “открытии” соответствующей коронарной артерии. Персистирующая коронарная недостаточность вносит важный вклад в развитие как систолической, так и диастолической дисфункции ЛЖ.
Другой механизм систолической дисфункции у больных ИБС связан с таким явлением, как “гибернация” миокарда, являющимся адаптивной реакцией в условиях постоянно сниженного коронарного кровотока. Тканевая перфузия в этих условиях достаточна для поддержания существования кардиомиоцитов (в том числе ионных токов), но недостаточна для их нормальной сократимости. Этот процесс приводит к постепенной гипоконтрактильности всего миокарда и прогрессированию дисфункции ЛЖ. Последние данные свидетельствуют, что гибернация миокарда неизбежно заканчивается некрозом, если коронарный кровоток не возрастает.
Таким образом, вдобавок к таким необратимым изменениям, как постинфарктный рубец, еще присоединяются персистирующая ишемия миокарда, оглушенный и гибернированный миокард — все вместе вносят свою специфику в развитие ХСН у больных ИБС.
Еще одним важным фактором возникновения миокардиальной дисфункции у больных ИБС является нарушение функции эндотелия коронарных сосудов, свойственное этой патологии. Эндотелиальной дисфункцией принято обозначать нарушение способности этих клеток продуцировать специфические (сосудистые) факторы релаксации (NO, простациклин, фактор гиперполяризации). Доказано, что дисфункция эндотелия активизирует деятельность нейрогормонов, ответственных за развитие и прогрессирование ХСН: эндотелина-1, ренин-ангиотензин-альдостероновой и симпато-адреналовой систем, фактора некроза опухоли-a. Кроме того, эндотелиальная дисфункция у больных ИБС блокирует миграцию гладкомышечных клеток и их пролиферацию в стенке сосуда, увеличивает проницаемость стенки для липидов, что способствует дальнейшему развитию атеросклероза и коронарного тромбоза, который, в свою очередь, вызывает персистирующую ишемию миокарда и дисфункцию ЛЖ.
Эффективность медикаментозной терапии ХСН при ИБС
Дигоксин
В исследовании DIG [5] было показано, что у больных ХСН дигоксин на 26% увеличивает частоту развития ИМ, что косвенно может свидетельствовать о потенциально неблагоприятном влиянии гликозидов на течение ИБС. Это может быть связано с ростом потребления О2 на фоне увеличения сократимости миокарда. Несмотря на это, такой важный показатель, как риск развития смерти и/или вынужденной госпитализации из-за прогрессирования ХСН при применении дигоксина, все-таки имел тенденцию к снижению, хотя степень этого снижения у больных ИБС была менее значима (на 21%), чем у пациентов с ХСН неишемической этиологии (снижение на 33%).
Ингибиторы АПФ
Практически все клинические исследования свидетельствуют о выраженном положительном влиянии иАПФ не только на показатели смертности, но и на развитие ИБС, в том числе и у больных с ХСН или систолической дисфункцией миокарда. Так, по данным основных многоцентровых исследований, снижение риска развития ИМ при применении иАПФ у таких пациентов достигает 12—25% (рис. 1).
Успех применения иАПФ у больных ХСН ишемического генеза может быть связан с уникальным свойством препаратов этого класса улучшать не только гемодинамический и нейрогуморальный статус, но также нормализовать эндотелиальную функцию коронарных артерий, роль которой в патогенезе сердечной недостаточности в настоящее время уже не вызывает сомнений. Кроме того, иАПФ способствуют улучшению показателей фибринолитической активности плазмы, что оказывает профилактическое действие на развитие коронарного тромбоза.
Клиническим подтверждением собственно “антиишемических” свойств иАПФ могут служить результаты исследования QUIET, в котором добавление иАПФ квинаприла больным ИБС при сохраненной функции желудочков снижало частоту коронарных осложнений на 10% [6]. При сочетании ИБС с ХСН среднее снижение риска смерти, связанное с применением препаратов этого класса, достигает 23%, о чем свидетельствуют результаты метаанализа Garg&Yusuf, проведенного по результатам 32 плацебо-контролируемых исследований [7]. Другой важный вывод этого метаанализа свидетельствует о том, что в подгруппе больных с сердечной недостаточностью неишемической этиологии (не ИБС) эффект АПФ был также положительным, но все-таки несколько меньшим, чем у пациентов с ишемией миокарда (табл. 4).
Несмотря на такие благоприятные для больных ИБС предпосылки, в 2 крупнейших исследованиях с эналаприлом (V-HeFT II и SOLVD prevention & treatment) эффективность лечения сердечной недостаточности ишемической этиологии была существенно ниже, чем при декомпенсации неишемического генеза (см. табл. 4).
То, что действие иАПФ зависит от этиологии декомпенсации и может быть менее эффективным при ХСН ишемического генеза, было подтверждено в ретроспективном исследовании, проведенном в НИИ кардиологии им. А.Л. Мясникова. 6-летнее применение иАПФ у больных ХСН ишемической этиологии уменьшало риск их смерти в среднем на 26%, а у аналогичных больных с ДКМП — на 60% [2].
b-Блокаторы
Ишемия миокарда является одним из основных показаний к применению b-блокаторов, однако присоединение к ИБС недостаточности кровообращения до последнего времени считалось опасным для применения препаратов с отрицательными инотропными свойствами и служило даже противопоказанием для такой терапии. Тем не менее еще в 80-х годах было известно, что эффективность b-блокаторов у больных с ИМ, осложненным ХСН, даже выше, чем у пациентов без сердечной недостаточности (рис. 2).
После продолжительного периода поиска и колебаний целесообразность применения b-блокаторов в лечении больных ХСН перестала быть предметом дискуссий и стала очевидной лишь в последние 1—2 года, после завершения трех крупных многоцентровых исследований с карведилолом (USCT), бисопрололом (CIBIS II) и метопрололом (MERIT-HF).
Во всех этих работах применение b-блокаторов дополнительно к основной терапии (иАПФ+диуретики/гликозиды) уменьшало риск смерти в среднем на 34—65%. Причем положительный эффект терапии наблюдался в подгруппах больных как с ишемическим, так и неишемическим генезом сердечной декомпенсации.
Противоишемические и антиангинальные свойства b-блокаторов теоретически предполагают их преимущество при использовании у больных с ХСН ишемической этиологии. Однако в реальной клинической практике это подтверждается лишь отчасти. Как видно из табл. 5, при ИБС b-блокаторы имели недостоверное преимущество лишь в 2 исследованиях из 4. Более того, в одном из исследований (CIBIS I) бисопролол практически не влиял на смертность пациентов с ишемией миокарда при выраженном положительном эффекте у больных ДКМП.
Амиодарон
Эффективность амиодарона у больных с ИБС ассоциируется главным образом со снижением внезапной, аритмической смерти.
Так, в Канадском (CAMIAT) и Европейском (EMIAT) исследованиях у больных в постинфарктном периоде амиодарон не влиял на общую смертность больных, но достоверно уменьшал риск внезапной (аритмической) смерти (табл. 6).
По данным метаанализа АТМА, включившего в себя 13 основных исследований у больных с дисфункцией ЛЖ и/или сердечной недостаточностью, наряду со снижением аритмической смерти (на 29%) применение амиодарона все же сопровождалось уменьшением риска и общей смертности в среднем на 13% [11].
Однако связь этиологии ХСН с эффективностью этого препарата неоднозначна. Так, в исследовании CHF-STAT тенденция к снижению смертности на фоне терапии амиодароном отмечалась только у больных с неишемическим характером декомпенсации (20%, p=0,07); в то же время эффективность терапии больных ИБС приближалась к 0. В отличие от этой работы в аргентинском исследовании GESICA снижение риска смерти и/или госпитализации при применении амиодарона у больных ХСН составило в среднем 31%, но относительный “успех” имели уже больные с ИБС: снижение риска у них составило 38% против 23% у больных с кардиомиопатиями.
Антагонисты кальция
Эффективность применения антагонистов кальция у больных ХСН исследована недостаточно. Однако данные даже единичных работ дают противоречивые результаты. Исследование PRAISE I с амлодипином показало, что назначение этого препарата (на фоне иАПФ, диуретиков, гликозидов) сопровождается недостоверным снижением фатальных и нефатальных осложнений, а также частоты смертельных исходов в среднем на 9%. Причем этот “успех” был достигнут исключительно “благодаря” больным с ХСН неишемической этиологии (ДКМП, гипертоническое сердце и т.п.), у которых снижение риска смерти, ассоциированное с амлодипином, составило 46%; в то же время у больных ИБС этот показатель практически не менялся (табл. 7).
Прямо противоположные результаты были получены в исследовании V-HeFT-III с антагонистом кальция III поколения фелодипином: при ХСН у больных ИБС отмечалось снижение смертности в среднем на 18%; в то же время в подгруппе пациентов без ИБС число смертельных исходов на фоне этой терапии даже несколько превысило показатели в контрольной группе.
Заключение
Ближайшие и отдаленные тенденции в развитии сердечно-сосудистых заболеваний свидетельствуют, что рост числа больных ИБС сохранится и ХСН, как осложнение ИБС, в следующем веке станет одной из главных причин госпитализаций и смертности населения, особенно в старшей возрастной группе. В этой связи возникает вопрос: существуют ли надежные способы профилактики и лечения этого синдрома?
Анализ основных многоцентровых исследований не дает однозначного ответа: эффективность лечения пациентов ХСН при ИБС нередко бывает хуже, чем больных с декомпенсацией неишемической этиологии, например при ДКМП.
Причины этого явления могут быть связаны с “двойным” патогенезом ХСН при окклюзивном поражении коронарных артерий, который требует воздействия не только на процессы ремоделирования сердца, но и эффективного восстановления перфузии миокарда. Отсюда можно предположить, что без адекватной реваскуляризации сердечной мышцы трудно добиться успеха в предупреждении и лечении недостаточности кровообращения у больных с коронарным атеросклерозом. К сожалению, серьезных подтверждений этой концепции пока нет, поскольку больные с симптомами сердечной недостаточности, как правило, исключаются из исследований по реваскуляризации миокарда. Отдельные работы, проведенные с больными без выраженной дисфункции миокарда, показывают, что при 3—11% операционной летальности, 5-летняя выживаемость оперированных пациентов относительно удовлетворительная, но не лучше (а возможно, и хуже), чем у тех, кто получал адекватную медикаментозную терапию [1]. Безусловно, эти выводы не могут быть окончательными, поскольку решение вопроса об эффективности хирургических методов лечения таких больных требует проведения специально организованных исследований.
Необходимость “сосудистого коронарного” воздействия на больных ХСН ишемической этиологии получила неожиданное подтверждение при исследовании эффектов гиполипидемических препаратов (статинов) у больных с дислипопротеидемией и ИБС. Так, в исследовании CARE применение правастатина снижало частоту повторных инфарктов и смертности у больных с асимптоматической дисфункцией ЛЖ, а симвастатин в исследовании 4S вообще предупреждал развитие сердечной недостаточности [1]. Результаты этих исследований наводят на мысль, что если ингибиторы АПФ могут стать важным средством лечения больных ИБС, то статины — необходимым компонентом терапии больных ХСН ишемической этиологии.
Таким образом, сердечная недостаточность у больных с ИБС в настоящее время остается серьезной проблемой, решение которой возможно лишь при объединении усилий эпидемиологов и терапевтов, кардиологов и кардиохирургов, направленных как на профилактику и лечение коронарной болезни, так и на устранение ее осложнений — дисфункции желудочков и сердечной недостаточности.
Литература
1. Cleland J.F.G., McGowan J. Heart Failure due to Ischaemic Heart Disease: Epidemiology, Pathophysiology and Progression. J Cardiovasc Pharmacol 1999; 33 (suppl. 3): S17—S29.
2. Ю.Н.Беленков, В.Ю.Мареев, Ф.Т.Агеев. Медикаментозные пути улучшения прогноза больных хронической сердечной недостаточностью. М., “Инсайт”, 1997.
3. Kober L., Torp Pedersen., Carlsen J.E. et al. A clinical trial of the angio-converting-enzyme inhibitor trandolapril in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 1995; 333: 1670—6.
4. Effects of enalapril on survival in patients with reduced left ventricular ejection fraction and congestive heart failure. The SOLVD investigators. N Engl J Med. 1991; 325: 293—302.
5. The Digitalis Investigation Group. The effect of Digoxin on mortality and morbidity in patients with heart failure. N Engl J Med 1997; 336: 525—33.
6. Cashin-Hemphill L, Dinsmore RE, Chan RC et al. Atherosclerosis progression in subjects with and without post-angioplasty restenosis in QUIET. J am Coll Cardiol 1997; 29 (suppl. A): 418A.
7. Garg R, Yusuf S. Overview of randomized trial of angiotensin-converting enzyme inhibitors on mortality and morbidity in patients with heart failure. JAMA 1995; 1450—6.
8. MERIT-HF Study Group. Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomized Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet 1999; 353: 2001—07.
9. Julian DG, Camm AJ, Frangin G. Et al. Randomozed trial of effect of amiodarone on mortality in patients with left-ventricular dysfunction after recent myocardial infarction: EMIAT. Lancet 1997; 349: 667—74.
10. Cairns JA, Connolly SJ, Roberts R. Et al. Randomozed trial of outcome after myocardial infarction in patient with frequent or repetitive premature depolarisation: CAMIAT. Lancet 1997; 349: 675—82.
11. Amiodaron Trials Meta-Analisis (ATMA). Lancet 1997; 350: 1417—24.
ИБС является основной этиологической причиной развития сердечной недостаточности.
Рис. 1. Риск развития ИМ (данные многоцентровых, плацебо-контролируемых исследований с различными ингибиторами АПФ).
Рис. 2. Абсолютное число спасенных жизней на 1000 пролеченных b-блокаторами больных, перенесших инфаркт миокарда. Зависимость эффекта от наличия или отсутствия сопутствующей сердечной недостаточности.
Тимолол – Норвежское исследование с тимололом;
ВНАТ – исследование с пропранололом;
Гётеборг – исследование с метопрололом (1).
Источник
