Рекомендации по реабилитации инсульта
Драматическая статистика инсульта – пугающая распространенность (более полумиллиона человек ежегодно в России испытывают острое нарушение мозгового кровообращения), его высокая летальность (123 на 100 000 населения), значительная инвалидизация (56–81%) и социальная дезадаптация1 пациентов определили особое положение в современном здравоохранении и повышенное внимание со стороны медицинской общественности к его проблемам. И прежде всего к реабилитации пациентов, перенесших его, – справедливо считаемой чрезвычайно важной, сложной и дискуссионной.
Постинсультная реабилитация – совокупность мер и методов, нацеленных на продолжение лечения, начатого в остром периоде, и способствующих устранению или компенсированию повреждений после инсульта.
В последние годы появилось достаточно данных, подтвержденных серьезными исследованиями, ставших причиной отхода специалистов от разработанной ранее GRADE-концепции (модели преемственной помощи) и других рекомендуемых принципов2 в пользу новых, делающих ставку на грамотную организацию инсультного отделения, которая позволяет снижать смертность и инвалидизацию именно за счет того, что в таком отделении проводятся не только диагностика и терапия, но и всесторонние реабилитационные мероприятия.
Акцентируют внимание врачей на острую необходимость постинсультной реабилитации и последние международные рекомендательные документы – Rehabilitation 2030 (ВОЗ), Report on Stroke in Europe (Европейского альянса по инсульту). Еще один документ ВОЗ (Global Stroke Bill of Rights) представляет реабилитацию и социальную реинтеграцию как основное право пациента после инсульта.3
Новые отношения к ведению пациентов, перенесших острое нарушение мозгового кровообращения, отражают последние (2018 г.) Рекомендации Американской ассоциации сердца/Американской ассоциации инсульта (American Heart Association/American Stroke Association) по раннему уходу за пациентами с острым ишемическим инсультом.4
Интересным и значимым событием стал и выход в 2018 году Австрийского руководства (Клинические рекомендации по реабилитации после инсульта).5 Согласно этому документу, цель реабилитации – «начать общие и специфические методы лечения как можно раньше, сразу после терапии в реанимации, чтобы помочь пациенту быстрее вернуться к прежней жизни или заново адаптироваться к окружающему пространству, социальной среде».
Сегодня становится все более очевидным, что реабилитация должна начинаться в первые 24–48 часов от развития инсульта, проводиться в отделении неотложной терапии и основываться на индивидуальном подходе, комплексной оценке, обоснованности выбора диагностических, лечебных методов. Основная регламентация реабилитационных мероприятий сегодня связана с Международной классификацией функционирования, жизнедеятельности и здоровья (МФК). Реабилитационные активности различаются по уровню (структурный, функциональный), по целям, видам и степени активности пациента. Мероприятия должны быть релевантными состоянию больного (уровень доказательности A), легко измеряться и подстраиваться под пациента, иметь достаточный мотивационный компонент.

И конечно же она требует наличия мультидисциплинарной команды, в которую, помимо невролога и физиотерапевта, должны войти логопед, психолог, эрготерапевт, социальный работник, другие специалисты.
Важный аспект реабилитации – физическая активность. В постинсультном периоде она снижает инвалидизацию, повышает кардиореспираторную толерантность к ходьбе, улучшает когнитивные функции и настроение, повышает работоспособность, а также влияет на другие аспекты, связанные с инсультом (уровень В). Комплексы физических упражнений должны разрабатываться для всех перенесших инсульт пациентов (кто способен их выполнять) вместе с программами по кардиореабилитации. Пациентам также должны предлагаться способы логопедической коррекции и когнитивные тренинги.
Хорошие результаты дают различные виды реабилитации в поликлинике, дневном стационаре или на дому в течение первого года после выписки больного из клиники. Далеко не последнее место занимает здесь и активное вовлечение в реабилитационный процесс родственников, близких для больного людей.
Эти основополагающие принципы позволяют снижать степень инвалидизации, повышать качество жизни пациентов и помогают более быстрой адаптации – и личной, и бытовой, и социальной, и профессиональной.6
Важную роль в этом подходе играет также медикаментозная нейрореабилитация, выстроенная на принципах доказательной медицины. Последние годы дали достаточно доказательств того, что защита нейрососудистой структуры от ишемического повреждения имеет первостепенное значение. Появилась и возможность применения современных репаративных лекарственных средств (терапия стволовыми клетками, моноклональными антителами). К этой группе относятся и экстракты из биологических тканей животных, другие ускорители восстановления.7 Новые возможности сегодня позволяют изучать патофизиологические процессы на молекулярном уровне, а это означает, что необходимо переоценить те исследования эффективности существующих нейропротекторов, которые были проведены с менее высокой степенью точности.7
Серьезного внимания требует и поздняя реабилитация после инсульта (после года). Стойкое нарушение жизнедеятельности организма ведет к дальнейшему ухудшению и сопутствующим дисфункциям. Спастичность, болевой синдром, парестезии, изменения температурной чувствительности часто развиваются только на этапе хронизации. Целевые физические тренировки для верхних конечностей пациентов, для развития равновесия и ходьбы оказывали положительный эффект даже спустя год (и более) после инсульта.8 Важно отметить и значение профессиональной реабилитации, которая для работающих пациентов – необходимый фактор для возвращения к полноценной жизни.
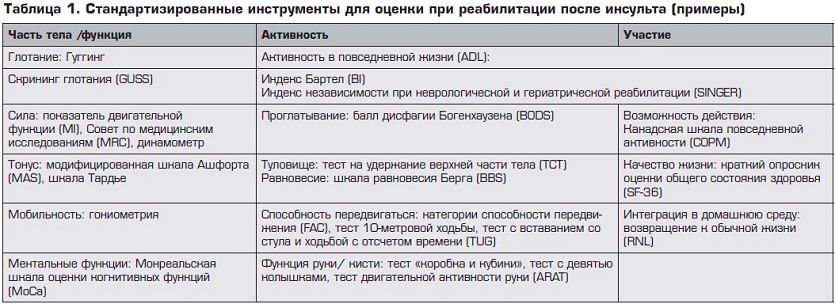
Перед началом реабилитации в течение первых 48 часов должна проводиться терапевтическая оценка. Оцениваются конкретные функциональные ограничения каждого пациента по отдельным системам организма и их функциональному состоянию, по уровню активности больного, его взаимодействию с социальной средой.9 После этого определяется набор соответствующих инструментов для достижения поставленных целей реабилитации (уровень B).
Медикаментозная терапия и нейровосстановление
С точки зрения экспертов, готовящих Австрийское руководство по реабилитации после инсульта,5 как и многих их зарубежных коллег, сегодня необходимо серьезное внимание обращать на такие понятия, как нейрорепарация, нейропластичность и нейровосстановление. Сам механизм развития заболевания ставит перед врачами важнейшую задачу – максимально раннее предотвращение смерти нейронов (нейропротекция) и затем реорганизацию нейрональных сетей, таким образом, обеспечивая преемственность между нейропротекцией и нейровосстановлением.
Медикаментозная терапия объективно способна ускорять нейровосстановление (нейропротективную терапию, цитопротекцию, метаболическую защиту мозга). Этот процесс сложен и разнообразен, отражает многогранность механизмов ишемического повреждения ткани мозга.10 Основные ее направления – антиоксидантная терапия, торможение местной воспалительной реакции (антагонисты провоспалительных цитокинов и молекул клеточной адгезии), улучшение трофического обеспечения мозга (нейротрофины), нейроиммуномодуляция (нейропептиды), регуляция рецепторных структур (ганглиозиды).11 Сегодня есть данные о положительном влиянии леводопы,12 специфических пептидных комплексов (Церебролизина).13–15
Действие последнего препарата стоит рассмотреть подробнее. В прошлом году он был включен в стандарты реабилитационных мероприятий после инсульта в Австрии.5
Институт инсульта Австрии признал возможности нейротрофической поддержки в реабилитации пациентов после инсульта. Клинические рекомендации по реабилитации содержат единственный нейротрофический препарат – Церебролизин (ЭВЕР Фарма Йена ГмбХ) (с уровнем доказательности II,B)5.
Особенность препарата, по мнению специалистов, заключается в том, что механизм его действия не ограничивается только нейропротекцией, его основное действие – модуляция эндогенного восстановления головного мозга после повреждения.
Как известно, естественная защитная реакция мозга в первые минуты ишемии – синтез нейротрофических факторов (и рецепторов к ним). Именно их высокий уровень обеспечивает регресс неврологического дефицита даже при сохранении вызвавшего его морфологического дефекта. Нейротрофическими и ростовыми свойствами обладают эндогенные низкомолекулярные нейрополипептиды, избирательно действующие на центральные холинергические нейроны, демонстрирующие нейропротективные, репаративные и пролиферативные эффекты. Они свободно преодолевают ГЭБ, их физиологическая активность во много раз выше, чем непептидных соединений. При этом они (в зависимости от места высвобождения) могут осуществлять разнообразные функции: медиаторную, модулятора реактивности определенных групп нейронов, регулятора тканевого метаболизма и многие другие.16
Нейротрофической активностью в полной мере обладает комплекс специфических пептидов – Церебролизин®. В его составе уникальное сочетание 24 нейропептидов и 17 L-аминокислот. Исследователи установили специфические трофическую и модуляторную функции каждого из этих компонентов,17 объясняющие способность препарата повышать выживаемость клеток мозга в условиях прекращения их нейротрофической поддержки со стороны клеток-мишеней, недостаточности кислорода и глюкозы (на уровне клеток – предотвращение повреждения дендритов).16,18
За более чем 60-летнюю историю (зарегистрирован в 1954 г. в Австрии) препарат участвовал в огромном числе клинических исследований, став единственным ноотропным пептидергическим препаратом с доказанной нейротрофической активностью, аналогичной таковой у естественных факторов роста нервов, но проявляющейся в условиях периферического введения.20 Большие и ограниченные, международные и отечественные исследования многократно доказывали его безопасность и эффективность при ишемическом инсульте как в острую стадию, так и в период реабилитации (а также при хронической нейродегенеративной и церебральной патологии).13-15, 17-26
И исследования продолжаются, в прошлом году профессором Натаном Борнштейном и его коллегами26 были опубликованы результаты большого метаанализа. Под их пристальное внимание попало 9 клинических исследований (по дизайну все: проспективные, рандомизированные, двойные слепые, плацебоконтролируемые) с оценкой эффективности этого ноотропного препарата в отношении улучшения общего неврологического состояния пациентов на ранних этапах после перенесенного инсульта (препарат в дозе 30–50 мл/1 раз в сутки в течение 10–21 дня).
В резюме проведенного метаанализа отмечены:
- Величина эффекта (непараметрический критерий MW) при проведении оценки с помощью шкалы тяжести инсульта NIHSS на 30 день (или 21) при обобщении результатов 9 РКИ указывала на большую эффективность данного препарата по сравнению с плацебо (MW 0,60; P
- Наиболее выраженные эффекты были отмечены в исследованиях с исходной высокой степенью тяжести инсульта – по шкале NIHSS: MW = 0,64; P = 0,0001.
- Совокупное NNT для клинически значимых изменений при проведении ранней оценки по шкале NIHSS составляло 7,7 (95% ДИ: 5,2–15,0).
- В предварительно запланированном развернутом ранговом анализе оценки по шкале mRS на 90-й день у пациентов с заболеванием умеренной и тяжелой степени был получен MW 0,61, свидетельствующий о статистически значимой большей эффективности препарата (95% ДИ 0,52-0,69; P = 0,0118; N = 314; процедура обобщения Вэй-Лачин [MERT]).
- Во всех анализах чувствительности подтверждены результаты анализа первой линии.
- В плане безопасности данный препарат был сопоставим с плацебо при наличии тенденции к уменьшению смертности (ОР 0,83). В целом препарат демонстрирует благоприятное соотношение «польза-риск».
Таким образом, предлагаемые в настоящее время основополагающие принципы и ранней, и отсроченной во времени реабилитации позволяют заметно снижать степень инвалидизации, повышать качество последующей жизни пациентов, способствовать более быстрому возвращению пациента к личной, бытовой, социальной и профессиональной активности. Важную роль в развитии этого подхода играет и современная медикаментозная нейрореабилитация, выстроенная на принципах доказательной медицины. При этом, как подчеркивают эксперты, успешность всех реабилитационных методик обеспечивается комплексным подходом, с учетом индивидуальных физических, эмоциональных, двигательных и когнитивных возможностей постинсультного пациента.
Ключевые слова: инсульт, реабилитация после инсульта, австрийские рекомендации по реабилитации больных после инсульта, нейропептиды, нейропротекция.
Литература
1 Пирадов М.А., Максимова М.Ю., Танашян М.М. Инсульт. Пошаговая инструкция. М. Гэлтар-Медиа, 2019, 272 с.
2 Wein T., Lindsay M.P., Cote R. et al. Canadian stroke best practice recommendations: Secondary prevention of stroke, sixth edition practice guidelines, update 2017. Int J Stroke. 2018, 13 (4), p. 420–443.
3 World Stroke Campaign. https://www.worldstrokecampaign.org/images/global_stroke_bill_of_rights/English_GlobalBO-Rights_web.pdf (zuletzt abgerufen 16.3.2018) 2018.
4 Powers W.J. et al. 2018 Guidelines for the Early Management of Patients With Acute Ischemic Stroke: A Guideline for Healthcare Professionals From the American Heart Association/American Stroke Association. Stroke. 2018, Mar., 49 (3), e46-e110. doi: 10.1161/STR.0000000000000158.
5 https://neurologic.ru/nejroreabilitacija-posle-insulta/
6 United Nations Organisation. https://www.un.org/development/desa/disabilities/convention-on-the-rights-of-persons-with-disabilities/article-26-habilitation-and- rehabilitation.html. 2018.
7 Neuhaus A.A., Couch Y., Hadley G., Buchan A.M. Neuroprotection in stroke: the importance of collaboration and reproducibility. Brain 2017, 140 (8), p. 2079–2092.
8 Pollock A., Baer G., Campbell P. et al. Physical rehabilitation approaches for the recovery of function and mobility following stroke. Cochrane Database Syst Rev. 2014, (4):CD001920.
9 World Health Organisation. https://www.who.int/classifications/icf/en/ (zuletzt abgerufen 16.3.2018) 2018.
10 Одинак М.М., Вознюк И.А., Янишевский С.Н. Ишемия мозга. Нейропротективная терапия. Дифференцированный подход. СПб. ВМедА, 2002, 77 с.
11 Завалишин И.А., Захарова М.Н. Оксидантный стресс – общий механизм повреждения при заболеваниях нервной системы. Журнал неврологии и психиатрии. Т. 96, № 2, 1996, с. 111–114.
12 Scheidtmann K., Fries W., Muller F., Koenig E. Effect of levodopa in combination with physiotherapy on functional motor recovery after stroke: a prospective, randomised, double-blind study. Lancet. 2001, 358 (9284), p. 787–90.
13 Bornstein N.M., Guekht A., Vester J. et al. Safety and efficacy of Cerebrolysin in early post-stroke recovery: a meta-analysis of nine randomized clinical trials. Neurol Sci. 2018, 39(4), p. 629–640.
14 Muresanu D.F., Heiss W.D., Hoemberg V. et al. Cerebrolysin and recovery after stroke (CARS): a randomized, placebo-controlled, double-blind, multicenter trial. Stroke. 2016, 47, p. 151–159.
15 Guekht A., Vester J., Heiss W.D. et al. Safety and efficacy of Cerebrolysin in motor function recovery after stroke: a meta-analysis of the CARS trials. Neurol Sci. 2017, 38, p. 1761–1769.
16 Windisch M., Gschanes A., Hutter–Paier B. Neurotrophic activities and therapeutic experience with brain derived peptide preparation. J. Neural. Transm. 1998, vol. 53, p. 289–298.
17 Windisch M., Albrecht E., Eggenreich U., Paier B. Neurotrophic effects of the nootropic drug cerebrolysin – a summary. 3rd Int. Conf. on Alzheimer’s disease and related disorders. Padova. 1992, p. 4–5.
18 Watanabe Y., Gould E., McEwen B.S. Stress-induced atrophy of apical dendrites of hippocampal CA3 pyramidal neurons. Brain Res. 1992, vol. 588, p. 341–345.
19 Востриков В.В., Шишляников Г.З., Зеленцов К.Е., Востриков М.В., Шабанов П.Д. Церебролизин в практической медицине. Обзоры по клинической фармакологии и лекарственной терапии. Т. 7, № 4, 2009, с. 21–75.
20 Читаева Г.Е., Никифорова А.Н., Сапон Н.А. Общепринятые и новые аспекты применения препарата церебролизин. Український нейрохірургічний журнал. 2005, №3, с. 123–131.
21 Ladurner G., Kalvach P., Gmeinbauer R. et al. The MCA stroke trial: A multicentre, randomized, double-blind, placebo-controlled trial of cerebrolysin in patients with ischaemic stroke. Neuroprotection in ischaemic stroke. 26-th Intern. stroke conf. of Amer. Heart As soc. 2001.
22 Коппи С., Баролин Г. Применение церебролизина в терапии ишемического инсульта. Журнал неврологии и психиатрии. Т. 98, № 10, 1998, с. 30–33.
23 Скворцова В.И. Ишемический инсульт: патогенез ишемии, терапевтические подходы. Неврологический журнал. Т. 6, № 3, 2001, с. 4–9.
24 Скворцова В.И. Нейропротективная терапия ишемического инсульта. Врач. № 6, 2004, с. 26–32.
25 Гусев Е.И., Гехт А.Б., Гаптов В.Б., Тихопой Е.В. Реабилитация в неврологии. М. 2000, 52 с.
26 Bornstein Natan M., Guekht Alla, Vester Johannes, Heiss Wolf-Dieter, Gusev Eugene et al. Safety and efficacy of Cerebrolysin in early post-stroke recovery: a meta-analysis of nine randomized clinical trials. Neurological Sciences. April 2018, vol. 39, iss.4, p. 629–640.
Источник
Ежегодно 6 млн человек во всем мире переносят инсульт. 4,5 млн случаев, к сожалению, завершаются летальным исходом. В нашей же стране фиксируется более 400 тысяч инсультов каждый год, и это число постоянно растет[1]. Основные факторы риска — артериальная гипертония, нарушения сердечного ритма, возраст старше 50. Последствия инсульта — двигательные, речевые и когнитивные нарушения, которые отчасти и в разной степени могут быть обратимы при активной реабилитации. Именно поэтому современные врачи считают, что начинать заниматься восстановлением пациента нужно, едва минует острый период.
Есть ли жизнь после инсульта?
Инсульт — это нарушение мозгового кровообращения, возникшее остро и продолжающееся более 24 часов. Именно продолжительностью он отличается от транзиторной ишемии, симптомы которой исчезают в течение суток. Независимо от механизма — резкой недостаточности кровотока или, напротив, кровоизлияния — гибнет часть клеток мозга, в том числе и клетки нервных центров, регулирующих движения, речь, познавательную активность. Это проявляется различными неврологическими нарушениями.
По механизму возникновения инсульт может быть:
- Ишемическим — «инфаркт мозга», возникающий из-за закупорки кровеносного сосуда (до 80% всех инсультов — ишемические)[2];
- Геморрагическим — вызванным кровоизлиянием в глубокие отделы мозга — паренхиматозным, или под его сосудистую (паутинную) оболочку — субарахноидальным кровоизлиянием. Возможны и смешанные формы, когда кровь изливается и в поверхностные, и в глубокие структуры головного мозга.
Любой инсульт — это финал сложного комплекса длительно развивающихся патологических процессов, возникающих при:
- артериальной гипертензии;
- атеросклеротическом сужении артерий головы и шеи;
- нарушении сердечного ритма, способствующем тромбообразованию;
- внутрисосудистом тромбообразовании.
Обычно все эти процессы так или иначе взаимосвязаны: гипертония нарушает структуру сосудистой стенки, делая ее более восприимчивой к атеросклеротическому поражению, атеросклероз коронарных артерий часто провоцирует нарушения сердечного ритма, возникающие из-за недостаточного питания сердечной мышцы, и так далее. Непосредственной же причиной инсульта становится гемодинамический криз — острое изменение кровотока.
Причиной гемодинамического криза может быть:
- резкое изменение тонуса сосудов из-за перепадов АД;
- декомпенсация деятельности сердца;
- повышение вязкости крови;
- формирование тромба в желудочке при аритмии и его миграция в сосуды мозга;
- распад атеросклеротической бляшки и возникновение тромба на ее месте.
И при ишемическом, и при геморрагическом инсульте симптомы примерно одинаковы. Заподозрить начало инсульта можно при появлении:
- слабости в отдельных группах мышц;
- нарушения чувствительности отдельных участков тела;
- внезапного головокружения;
- нарушений координации движений, походки;
- внезапного нарушения речи;
- внезапной потери зрения, двоения в глазах, выпадения полей зрения;
- нарушений глотания.
В тяжелых случаях, если поражен обширный участок мозга, возникает потеря сознания вплоть до комы. Кроме этого, в остром периоде болезни может измениться температура тела, нарушиться гемодинамика (резко повыситься или, наоборот, упасть давление).
Ишемический инсульт чаще происходит во сне, под утро, геморрагический — во время активной деятельности, физической и эмоциональной нагрузки.
Последствия инсульта делятся на 3 большие группы:
- нарушения моторики: парезы, параличи, контрактуры;
- нарушения речи — при поражении участков мозга, ответственных за понимание, распознавание речи, сопоставление понятий и слов, им соответствующих;
- когнитивные и эмоционально-волевые расстройства: нарушения памяти, внимания, познавательной и интеллектуальной деятельности, депрессия.
В нашей стране 48% переживших инсульт теряют способность двигаться, 18% — говорить, и только 20% восстанавливаются настолько, что не получают группу инвалидности[3]. Основной причиной такой статистики является пренебрежение ранней реабилитацией родственниками пострадавшего и отсутствие достаточного количества и качества государственных реабилитационных отделений в российских клиниках.
В связи с этим подчеркнем, что благоприятными прогностическими факторами, дающими обоснованную надежду, считаются:
- сохранность интеллекта больного;
- раннее начало реабилитации;
- адекватная программа восстановления;
- активное участие самого пациента в восстановительных мероприятиях.
Поэтому реабилитацию после инсульта нужно начинать как можно раньше, чтобы шанс вернуть человека к нормальной жизни был максимально высок.
Этапы и сроки реабилитации: когда дорога каждая минута
Время после инсульта, с точки зрения восстановительных мероприятий, можно разделить на 4 периода:
- Острый: первые 3–4 недели. Реабилитация начинается в неврологическом (или ангиохирургическом) отделении.
- Ранний восстановительный: первые 6 месяцев. Для восстановления двигательных навыков особенно (!) важны первые 3 месяца. Реабилитация может проводиться в реабилитационном отделении больницы (если таковое имеется), реабилитационном центре, санатории (при условии значительного самостоятельного восстановления функций), если все эти возможности недоступны — амбулаторно.
- Поздний восстановительный: 6 месяцев–1 год. Амбулаторно-клиническая реабилитация. Если пациент не может посещать реабилитационное отделение (кабинет), проводится на дому.
- Отдаленный: после 1 года. Может проводиться и на дому, и в медучреждении.
Человеческий организм, чтобы там не говорили, имеет невероятную способность к регенерации. По мере восстановления функции погибших клеток мозга берут на себя соседние, перестраиваются соотношения между мозговыми структурами, активируются до того неактивные нейроны. Но для успешной реабилитации и профилактики осложнений важно начинать восстановление буквально в первые же дни, и обязательно прилагая все внутренние усилия больного.
Основная причина инвалидизации после инсульта — двигательные нарушения. При этом контрактуры, т.е. состояния при которых невозможно полностью согнуть или разогнуть конечность, трофические поражения суставов развиваются во время острого периода, и противостоять им эффективней всего сразу же. Уже в остром периоде, как только становится ясно, что угроза жизни пациента миновала, можно начинать делать пассивную гимнастику, массаж, если сознание сохранено — то подключать дыхательные упражнения и занятия по восстановлению речи. Кстати, самая простая и эффективная дыхательная гимнастика — надувание шариков или детских игрушек.
Методы постинсультной реабилитации: программы и средства
Как после ишемического, так и после геморрагического инсульта методы и принципы восстановления одинаковы:
- раннее начало реабилитации — по возможности активизация пациента еще в отделении реанимации;
- преемственность на всех этапах проведения — мультидисциплинарный организованный подход: так как проблемы касаются нескольких сфер, контролировать восстановление должна слаженно действующая команда специалистов;
- непрерывность;
- последовательность;
- интенсивность ежедневной терапии.
Двигательные нарушения — самая частая проблема пациентов после инсульта. К центральным дисфункциям (вызванным поражением мозга) присоединяются патологии суставов из-за нарушения иннервации, контрактуры мышц, а также болевые синдромы, препятствующие правильному движению. Поскольку совокупность всех этих факторов у каждого конкретного пациента индивидуальна, общие рекомендации далеко не так эффективны, как персональная работа. Какие-то проблемы поддаются медикаментозной коррекции (например, при болях, ограничивающих подвижность, назначают анальгетики, при спазмах мышц — миорелаксанты, в том числе и ботулотоксин). Другие требуют долгой и упорной работы. Кинезитерапия в числе прочего использует лечение положением (пораженная конечность фиксируется в специальном лангете на определенное время), пассивную и активную гимнастику, выполняемую преимущественно индивидуально. Стандартная лечебная физкультура может проводиться как индивидуально, так и в группах: упражнения должны помочь расширить диапазон движений, а параллельно — укрепить дыхательную и сердечно-сосудистую систему, активировать активность мозга. Отдельное направление — так называемые функционально ориентированные техники: упражнения, приближенные к нормальным повседневным движениям.
Постоянно разрабатываются и совершенствуются нейрофизиологические техники — «переобучающие» программы. Например, методика PNF (проприоцептивного мышечного облегчения) помогает наладить двигательную активность ослабленных мышц за счет связанных с ними здоровых. А вот бобат-терапия направлена на то, чтобы создать новые двигательные стереотипы, более комфортные и выполнимые для пациента после инсульта.
Обязательно используются и физиотерапевтические методики: массаж, иглорефлексотерапия, электромиостимуляция, магнитная и лазерная стимуляции…
Разумеется, такой сложный комплекс мероприятий требует грамотной и слаженной работы группы специалистов: физического терапевта, эрготерапевта (помогающего восстановить повседневные навыки), массажиста, врача-реабилитолога.
Восстановление речи после инсульта
Более чем у трети пациентов к концу острого периода сохраняются те или иные речевые нарушения[4]. Афазия (потеря способности говорить) часто сопровождается и аграфией (потерей способности к письму): ведь прежде, чем написать слово, его нужно мысленно произнести. Логопед-афазиолог рекомендует специальные упражнения, по сути, его задача — заново научить пациента говорить. Упражнения на артикуляцию и фонацию повторяются много-много раз, пока у пациента не сформируются нужные связочные двигательные навыки. Активней всего речь восстанавливается в первые 3–6 месяцев после инсульта, но целиком процесс может занять и 2–3 года.
Восстановление когнитивных функций
Это память, внимание, способность усваивать новую информацию и использовать ее на практике. Для восстановления когнитивных функций проводятся занятия, цель которых — активизировать психическую деятельность пациента. Чтение, письмо, упражнения для тренировки памяти, ассоциативное мышление — и даже посильные для пациента компьютерные игры — существенно помогают восстановить интеллектуальные способности.
Восстановление глазодвигательных и зрительных функций
После инсульта могут «потеряться» поля зрения, нарушиться движения глазных яблок. Для коррекции этих нарушения применяют специальные упражнения, направленные на тренировку зрительного поиска и слежения за движущимися объектами.
Работа с психоэмоциональной сферой
Согласно медицинской статистике, у 32% перенесших инсульт развивается тяжелая депрессия[5]. В реальности эта цифра, скорее всего, намного больше. Депрессия не просто портит жизнь пациенту, она значительно ухудшает результаты реабилитации — ведь для успеха восстановления нужно активное участие больного, его позитивный настрой на долгую, трудную, но нужную работу. Поэтому обязательно необходима работа с психологом, а если потребуется медикаментозная коррекция, то консультация психиатра (психолог без медицинского образования не имеет права выписывать антидепрессанты).
Все указанные мероприятия проводятся на фоне лекарственной терапии, призванной улучшить кровоток и питание головного мозга.
Вероятность повторения: как снизить риск
Печальный факт: от 25 до 32% всех инсультов — повторные[6]. Говорить о точной статистике повторных инсультов и их исходах довольно трудно: по данным отечественного регистра инсультов, их реальная частота в 5–6 раз выше фиксируемой[7] — банальное отсутствие КТ создает минимум 10% диагностических ошибок даже при очевидной клинической картине[8].
Как бы то ни было, поскольку главная причина инсультов — гемодинамические нарушения, профилактика повторного инсульта направлена прежде всего на их коррекцию:
- Контроль АД. Желательно достичь значений артериального давления ниже 140/90. При этом снижение давления ни в коем случае не должно быть резким. Кроме лекарств, нужно обратить внимание на диету: по данным ВОЗ, употребление более 5 граммов соли в день повышает риск развития гипертонии и сердечно-сосудистых катастроф[9]. У здоровых людей потребление больших объемов соли не вызывает негативных последствий, поскольку организм сам приводит электролитный состав биологических жидкостей в баланс, но это не относится к людям, страдающим сердечно-сосудистыми и/или почечными заболеваниями. При этом нужно помнить: бόльшая часть соли поступает в рацион из консервов, полуфабрикатов, копченостей и подобных им продуктов.
- Нормализация холестерина и липидного состава крови. Помимо лекарств (назначенных врачом) можно добавить в рацион овсяные[10] и рисовые[11] отруби — содержащиеся в них растворимые пищевые волокна помогают снизить холестерин и липиды крови.
- Антитромботическая терапия. Чаще всего для профилактики тромбозов назначают ацетилсалициловую кислоту в дозировке до 325 мг/сут. Но пациентам, причиной инсульта которых стал тромб, сформировавшийся в полости сердца на фоне аритмии, назначают более сильные (но и более опасные в плане передозировки) препараты, такие как «Варфарин». Эти средства требуют постоянного контроля состояния свертывающей системы крови.
Восстановление после инсульта — задача, требующая комплексного подхода, участия как врачей многих специальностей, так и самого пациента и его родственников. Но последовательная и настойчивая реабилитация способна если не вернуть пациента к прежнему образу жизни полностью, то позволить ему сохранить самостоятельность и предупредить развитие тяжелых осложнений и повторных рецидивов.
Источник
