Повреждение и гибель клеток и тканей некроз и апоптоз инфаркт

Завершающим этапом повреждений тканей организма является их гибель. Однако сами повреждения связаны не только с патологическими процессами, возникающими в организме, но и со старением функционирующих биологических структур. Вместе с тем механизмы гибели клеток и тканей в условиях нормы и в условиях патологии значительно отличаются друг от друга и имеют разное морфологическое выражение.
АПОПТОЗ
Апоптоз — физиологическая гибель клеток в живом организме.
Общая характеристика.
Все ткани организма имеют свой срок жизни, после истечения которого и прекращения функции они должны погибнуть и на их месте появляются новые, аналогичные погибшим, клетки и ткани. Сроки жизни у разных живых структур различны. Они определены в их геноме, т. е. генетически запрограммированы. Поэтому апоптоз является генетически запрограммированной гибелью клеток. Это важнейший физиологический процесс, позволяющий организму постоянно сохранять функции своих структур на определенном уровне. Кроме того, в процессе образования новых клеток и внеклеточных структур возникают генетические ошибки, происходят мутации и появляются клетки, отличающиеся от клеток организма. Они должны быть немедленно уничтожены, и их гибель также осуществляется с помощью апоптоза, который является и механизмом генетического контроля синтеза веществ и клеток организма. Таким образом, апоптоз как физиологический процесс протекает непрерывно на протяжении всей жизни человека, и биологический смысл его заключается в поддержании постоянства клеток и тканей организма, т. е. тканевого гомеостаза. С помощью апоптоза происходит инволюция органов и тканей после завершения ими своих физиологических функций, например атрофия вилочковой железы после окончания формирования иммунной системы, атрофия половой системы женщин после завершения детородной функции, атрофия органов и тканей при старении человека и др.
Вместе стем апоптоз может развиваться и в условиях патологии — в тех случаях, когда повреждающие факторы действуют на гены, контролирующие включение программы апоптоза. Обычно это происходит с помощью определенных веществ — цитокинов, различных факторов роста, гормонов, активизирующихся при заболеваниях и функционирующих на молекулярном уровне. Эту особенность апоптоза нередко пытаются использовать в клинике. Например, в онкологии постоянно идет поиск возможностей стимулировать апоптоз в злокачественных опухолях с тем, чтобы активизировать распад опухолевых клеток, и это весьма перспективный путь онкотерапии.
Морфология апоптоза.
Апоптоз развивается в отдельных клетках, которые вначале теряют контакты с соседними клетками, затем уменьшаются в размерах, в их ядрах конденсируется хроматин. ядра становятся изрезанными, плотными и фрагментируются на отдельные глыбки. Одновременно происходит распад цитоплазмы, в которой сохраняются в конденсированной форме внутриклеточные структуры. В результате клетка распадается на апоптозные тельца, каждое из которых окружено мембраной. Апоптозные тельца очень быстро поглощаются окружающими клетками, иногда макрофагами. Однако в ответ на апоптоз никогда не развивается воспалительная реакция и на месте погибших клеток воспроизводятся клетки той же ткани. Следует подчеркнуть, что апоптозу подвергаются лишь клетки, но не ткани в целом.
НЕКРОЗ
Некроз — гибель клеток и тканей в результате патологических воздействий.
Причины некроза разнообразны, однако их можно объединить в пять групп:
- травматический некроз, который является результатом прямого действия на ткань физических или химических факторов (механических, температурных, радиационных, кислот, щелочей и др.);
- токсический некроз развивается при действии на ткани токсических факторов бактериальной или иной природы;
- трофоневротический некроз, который связан с нарушениями иннервации тканей при заболеваниях центральной или периферической нервной системы;
- аллергический некроз — следствие иммунных реакций немедленной или замедленной гиперчувствительности;
- сосудистый некроз, обусловленный прекращением циркуляции крови в артериях, реже — в венах.
По консистенции мертвых масс некроз может быть коагуляционным, казеозным и колликвационным.
Коагуляционный (плотный) некроз возникает при коагуляции распавшегося белка, обычно в мышечных тканях и в большинстве внутренних органов.
Разновидностью коагуляционного некроза является казеозный (творожистый) некроз, массы которого имеют замазкообразную консистенцию; развивается при некоторых видах воспаления.
Колликвационный некроз развивается в тканях, богатых жидкостью, например в головном мозге.
По механизму действия фактора, вызвавшего некроз, выделяют:
- прямой некроз, который возникает при непосредственном действии на ткань причины, вызывающей ее гибель, — травма, токсины, высокая или низкая температура и т. п.;
- непрямой некроз, когда причина гибели ткани связана с нарушениями функций сосудов, нервов или с аллергическими реакциями.
Некрозу предшествует период умирания, он никогда не возникает мгновенно. Период умирания может быть длительным или быстрым. В этот период в клетках и во внеклеточном матриксе развиваются изменения, представляющие собой тот или иной вид дистрофии, чаще белковый. Эти изменения называются некробиозом, или парабиозом. Функции клеток и органов при этом ослабевают и прекращаются, но на начальных этапах процесса они могут восстановиться, если ликвидирована причина, вызвавшая некробиоз. Если же причина продолжает действовать, дистрофия становится необратимой, некробиоз переходит в некроз и какие-либо функции прекращаются. Некротизированные ткани под действием гидролитических ферментов подвергаются разложению — аутолизу. В области очага некроза развивается воспаление как ответная реакция организма на гибель его части.
Морфология некроза зависит от его причины, но общим является изменение цвета некротизированной ткани и ее консистенции. Цвет некротических масс зависит от наличия примесей крови и различных пигментов. Мертвая ткань бывает белой или желтоватой, нередко окружена красно-бурым венчиком. При гнилостном расплавлении мертвая ткань издает характерный дурной запах. Микроскопические признаки некроза складываются из необратимых изменений ядер и цитоплазмы клеток. В период некробиоза клетки теряют воду, поэтому при некрозе ядра сморщиваются и уплотняются — развивается кариопикноз. Затем нуклеиновые кислоты в виде отдельных глыбок выходят из ядра в цитоплазму клетки — происходит распад ядра — кариорексис. Наконец, ядерное вещество растворяется — наступает кариолизис. Исчезновение клеточных ядер — один из основных признаков некроза. Та же динамика гибели наблюдается в цитоплазме, в которой развиваются плазморексис и плазмолиз. Наконец, растворяется вся клетка — происходит цитолиз.
При некрозе интерстициальной и сосудистой тканей экстрацеллюлярный матрикс набухает и расплавляется, волокнистые структуры подвергаются фибриноидному некрозу и уплотняются. Образовавшиеся некротические массы носят название некротический детрит. Вокруг очага некроза, отграничивая его от живых тканей, развивается демаркационная линия, представляющая собой зону воспаления. Эта линия имеет большое значение в хирургической практике, так как указывает на возможные пределы иссечения погибших тканей или уровень ампутации конечности.
Исходы некроза.
Благоприятный, при котором происходит ферментативное расплавление некротизированных тканей, после чего они подвергаются организации, т. е. замещению дефекта соединительной тканью, обычно с образованием рубца, или инкапсуляции, т. е. отграничению некротизированного участка соединительной тканью. При этом нередко некротизированные массы подвергаются петрификации. На месте колликвационного некроза образуется полость — киста.
Неблагоприятный, когда некроз ткани или органа заканчивается смертью больного, например инфаркт миокарда или некроз поджелудочной железы. Кроме того, некротизированные ткани могут подвергаться гнойному расплавлению, при котором токсичные продукты некроза и аутолиза всасываются в кровь, развивается интоксикация, которая также может привести к смерти.
Клинико-морфологические формы некроза.
В зависимости от локализации и особенностей некроза выделяют его следующие клинико-морфологические формы.
Гангрена — некроз тканей, соприкасающихся с внешней средой. При этом железо гемоглобина, находящегося в некротизированных тканях, соединяется с сероводородом воздуха и образуется сульфид железа, придающий некротизированным тканям черный цвет. Гангрена развивается в коже, конечностях, кишечнике, легких, влагалище, матке и т. д. Имеется несколько разновидностей гангрены (рис. 12):
- сухая гангрена развивается в тканях с малым содержанием жидкости, при этом ткани могут подвергаться мумификации. Она характерна для конечностей, возникает на разных участках тела при их отморожении, ожогах, при тяжелых инфекциях;
- влажная гангрена обычно развивается в тканях, богатых жидкостью, поэтому встречается в легких, матке, кишечнике. У ослабленных детей, страдающих корью или скарлатиной, иногда развивается влажная гангрена щеки — нома;
- анаэробная или газовая гангрена возникает при тяжелых, обычно массивных ранениях или травмах конечностей при попадании врану бактерий — анаэробов. Внекротизированных мышцах развивается коагуляционный некроз, они становятся грязно-серыми, при надавливании из них выделяются пузырьки газа.
Пролежень имеет трофоневротическое происхождение, возникает на участках кожи, подкожной клетчатки или слизистых оболочек. подвергающихся давлению у ослабленных больных, страдающих онкологическими, сердечно-сосудистыми и некоторыми инфекционными заболеваниями. Пролежни могут возникать вобласти крестца, ягодиц, пяточных костей, а также в трахее или гортани от давления трахеостомической трубки после операции трахеостомии.
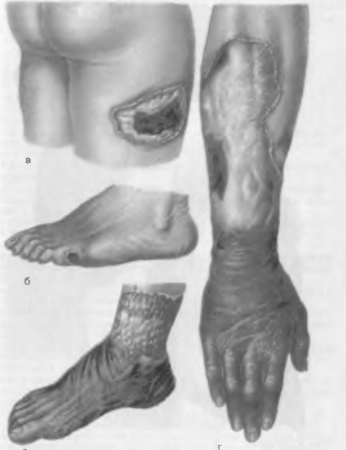
Рис. 12. Гангрена. Влажная гангрена кожи бедра (а) и стопы (б); сухая гангрена стопы (в), предплечья и кисти (г).
Секвестр — участок омертвевшей ткани, свободно располагающийся среди живых тканей, обычно сопровождающийся гнойным воспалением. Особенно часто секвестром является некротизированный фрагмент кости при остеомиелите.
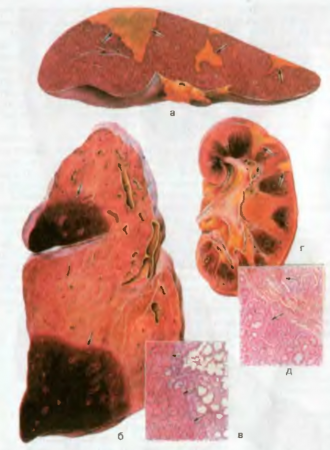
Рис. 13. Инфаркт. а — белые (ишемические) инфаркты селезенки; б — красные (геморрагические) инфаркты легкого; в — микроскопическая картина геморрагического инфаркта легкого; г — ишемические инфаркты почки; д — микроскопическая картина ишемического инфаркта почки. Участки некроза тканей показаны стрелками.
Инфаркт — некроз ткани внутренних органов, развивающийся в результате острого нарушения кровообращения в них при тромбозе, эмболии, длительном спазме артерий. Наиболее яркими примерами этого вида некроза являются инфаркты миокарда, головного мозга, легких, почек, селезенки (рис. 13). Инфаркты различают по форме и цвету, что зависит от особенностей органа и архитектоники его сосудистой системы:
- по форме
- — клиновидная;
- — неправильная.
- по цвету
- — белый;
- — красный;
- — белый с геморрагическим венчиком.
Сравнительная характеристика апоптоза и некроза
Отличия апоптоза от некроза связаны с различиями в их распространенности, генетических, биохимических, морфологических и клинических проявлениях:
- апоптоз — физиологический вид смерти, некроз возникает в условиях патологии;
- апоптоз генетически запрограммирован, некроз развивается под воздействием различных повреждающих причин и не связан с геномом клетки;
- апоптоз распространяется только на отдельные клетки, некроз развивается на территории ткани и даже целого органа;
- апоптоз не сопровождается дистрофическими изменениями клеток, некрозу предшествует дистрофия, имеющая характер некробиоза;
- апоптоз не сопровождается воспалением, вокруг некроза обязательно развивается воспалительная реакция;
- апоптоз заканчивается фагоцитозом апоптозных телец соседними клетками, некроз заканчивается аутолизом погибшей ткани;
- после апоптоза восстанавливаются клетки, аналогичные погибшим, на месте некроза обычно разрастается рубцовая соединительная ткань;
- апоптоз не сопровождается активацией внутриклеточных гидролитических ферментов, некроз развивается с помощью гидролаз;
- апоптоз не имеет клинических проявлений, некроз сопровождается выраженной клинической симптоматикой.
Апоптоз и некроз — два разных варианта гибели клеток и тканей в живом организме, хотя некоторые патогенные факторы, способные оказывать воздействие на генетический код, могут вызывать апоптоз. Однако при этом апоптоз все-таки остается физиологическим механизмом смерти, но активизирующимся в условиях определенной патологии.
Все описанные изменения — дистрофии, апоптоз и некроз — носят характер типовых (или стереотипных) реакций, которыми организм отвечает на различные воздействия, и те или иные их сочетания возникают при любых болезнях, что необходимо учитывать при назначении лечения.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Источник
I. ОБЩАЯ ПАТОЛОГИЧЕСКАЯ АНАТОМИЯ. ГЛАВА 1. ПОВРЕЖДЕНИЕ И ГИБЕЛЬ КЛЕТОК И ТКАНЕЙ
НЕКРОЗ. АПОПТОЗ
Повреждение
(альтерация) – это вызванное внешним (экзогенным) или внутренним
(эндогенным) воздействием нарушение структуры и функции клеток, тканей,
органов или частей тела. Виды повреждения (альтерации) клеток: дистрофии, некроз, апоптоз.
Дистрофии (внутриклеточные и внеклеточные накопления) – преимущественно обратимые нарушения обмена веществ (трофики), морфологически
выражающиеся изменением содержания (чаще – накоплением) в клетках или
тканях нормальных или качественно измененных, а также аномальных
метаболитов (воды, белков, жиров, углеводов, пигментов и др.).
Некроз –
это смерть клеток, тканей, органов и частей тела в живом организме.
Некроз – общепатологический процесс, вид повреждения (альтерации),
наиболее распространенный тип гибели клеток, вызванный экзоили
эндогенными повреждающими воздействиями. Стадии некроза: паранекроз, некробиоз, смерть клетки, аутолиз и гетеролиз. Аутолиз – ферментное самопереваривание (лизис) клетки, гетеролиз – ферментное переваривание погибшей клетки либо ее частей фагоцитами и соседними клетками. Клинико-морфологические виды некроза: коагуляционный (сухой) некроз, колликвационный (влажный) некроз, гангрена
(сухая и влажная гангрена, пролежень, нома), секвестр, казеозный
(творожистый) некроз, фибриноидный некроз, восковидный (ценкеровский)
некроз, жировой (ферментный) некроз (стеатонекроз), инфаркт (сосудистый,
ишемический, ангиогенный некроз). Исходы некроза: благоприятные – полная
репаративная регенерация (реституция), неполная репаративная
регенерация (субституция) – рубцевание, инкапсуляция, кальцификация
(обызвествление), оссификация, резорбция некротических масс –
формирование псевдокисты («кисты»), секвестрация, мутиляция
(«самоампутация»); неблагоприятные – гнойное расплавление (асептическое или инфицированное вплоть до развития сепсиса).
Апоптоз – общепатологический процесс, вид гибели клеток («программированная клеточная гибель»), реализующийся
вследствие последовательной активации «генов смерти» и ферментов
«суицидального биохимического пути». Апоптоз – это генетически
контролируемое и требующее затрат энергии самоуничтожение клетки
приспособительного характера или под влиянием слабых экзо- и эндогенных
повреждающих факторов, не вызывающих дистрофию и некроз.


Рис. 1 –1. Микропрепараты
(а, б). Баллонная дистрофия одонтобластов при глубоком кариесе:
одонтобласты увеличены в размерах (1), в их цитоплазме крупные вакуоли,
напоминающие баллоны, заполненные цитоплазматической жидкостью,
оттесняющие ядра и органеллы на периферию клетки (фокальный
колликвационный некроз клетки); 2 – дентин; 3 – пульпа зуба (пульпит).
Окраска гематоксилином и эозином: а – x 120, б – х400

Рис. 1-2. Электронограмма.
Баллонная дистрофия одонтобласта при глубоком кариесе: в цитоплазме
одонтобласта крупные вакуоли («баллоны») (1), органеллы и ядро (2)
клетки смещены на периферию, кариопикноз, деструктивные изменения
митохондрий (3)

Рис. 1-3. Костный
секвестр при хроническом остеомиелите челюстных костей.
некротизированный фрагмент челюстной кости, окруженный гнойным
экссудатом зеленовато-желтого цвета и сероватого цвета фиброзной
секвестральной капсулой (препарат Р.М. Пичхадзе)

Рис. 1-4. Микропрепараты
(а, б). Хронический остеомиелит челюстных костей, стадия секвестрации: а
– костный секвестр – бесклеточный фрагмент костной балки (1) и
секвестральная соединительнотканная капсула (2); б – гнойное воспаление
(гнойный экссудат состоит преимущественно из живых и погибших
нейтрофильных лейкоцитов – гнойных телец) (3). Окраска гематоксилином и
эозином: х200 (препараты Г.Н. Берченко)

Рис. 1-5. Макропрепарат.
Казеозный некроз шейного лимфатического узла при туберкулезе:
лимфатический узел увеличен, уплотнен, на разрезе – творожистого вида
крошащиеся массы желтовато-белого цвета, отграниченные от небольших
участков окружающей сохранившейся ткани белесовато-серыми прослойками
(соединительнотканной капсулой)

Рис. 1-6. Микропрепарат.
Казеозный некроз шейного лимфатического узла при туберкулезе:
эозинофильные очаги казеозного (творожистого) некроза (1) в ткани
лимфатического узла, окруженные «частоколом» из эпителиоидных клеток,
скоплениями макрофагов и лимфоцитов (2), среди которых видны единичные
гигантские многоядерные клетки Пирогова-Лангханса. Окраска
гематоксилином и эозином: χ 120

Рис. 1-7. Макропрепараты
(а, б). Инфаркт миокарда: очаг некроза (1) неправильной геометрической
формы, пестрого вида, желтовато-серого цвета с красными очагами, дряблой
консистенции, западает на разрезе, окружен геморрагическим венчиком
красного цвета (зона демаркационного воспаления); вид инфаркта – белый с
геморрагическим венчиком, давность инфаркта – около 3 сут

Рис. 1-8. Микропрепарат.
Исчезновение гликогена из кардиомиоцитов в зоне ишемии миокарда: 1 –
сохранные кардиомиоциты, содержащие в цитоплазме фиолетово-малинового
цвета гранулы гликогена; 2 – кардиомиоциты в зоне ишемии, их цитоплазма
не окрасилась. PAS-реакция: х100 (из [1]

Рис. 1-9. Макропрепараты
(а-в). Ишемический инфаркт почки: 1 – очаг некроза клиновидной (на
разрезе – треугольной) формы (основание клина обращено к капсуле почки,
вершина – к воротам органа), плотной консистенции, желтовато-белого
цвета, отграниченный от окружающей ткани геморрагическим венчиком –
зоной демаркационного воспаления; вид инфаркта – белый с геморрагическим
венчиком (в – препарат И.Н. Шестаковой)

Рис. 1-9. Окончание

Рис. 1-10. Макропрепараты
(а, б). Гангрена стопы: а – сухая гангрена, пальцы стопы уменьшены в
размерах, плотной суховатой консистенции (мумификация), серо-черного
цвета за счет образования сульфида железа, с четко выраженной границей и
сохранными тканями в виде полоски красного цвета (зона демаркационного
воспаления); б – влажная гангрена, стопа увеличена в размерах, отечная,
синюшного цвета с черными участками, мацерацией кожи, зона
демаркационного воспаления выражена нечетко (а – препарат И.Н.
Шестаковой)

Рис. 1-11. Микропрепарат.
Некроз миндалин при лейкозе (некротическая ангина): некроз покровного
многослойного плоского эпителия миндалины, обширные очаги некроза
лимфоидной ткани, окруженные воспалительным инфильтратом из
полиморфно-ядерных лейкоцитов, расширенные полнокровные сосуды
(демаркационное воспаление); 1 – некротический детрит с колониями
бактерий; 2 – ткань миндалины с демаркационным воспалением и лейкозной
инфильтрацией.
Окраска гематоксилином и эозином: х200

Рис. 1-12. Микропрепараты
(а, б). Некроз и апоптоз лимфоцитов фолликулов селезенки: в светлом
(герминативном) центре лимфоидного фолликула – апоптозные тельца и
фрагменты некротизированных лимфоцитов (с признаками кариопикноза,
кариорексиса) фагоцитируются фолликулярными дендритными клетками и
макрофагами. Окраска гематоксилином и эозином: а – х200, б – х400

Рис. 1-13. Микропрепарат.
Апоптозное тельце (тельце Каунсилмена) при вирусном гепатите: в составе
балок гепатоцитов (иногда могут выступать в пространства Диссе) –
крупное апоптозное тельце (1) с уплотненной эозинофильной цитоплазмой,
сохранившимся пикнотичным и фрагментированным ядром; 2 – гидропическая
(баллонная дистрофия гепатоцитов). Окраска гематоксилином и эозином: х600 (из [1])

Рис. 1-14. Электронограмма.
Апоптозное тельце (тельце Каунсилмена) при вирусном гепатите:
цитоплазма уплотнена, с компактным расположением органелл, фрагмент ядра
(1) с конденсацией хроматина под ядерной мембраной гепатоцита, ставшего
апоптозным тельцем (из [1])
Источник
