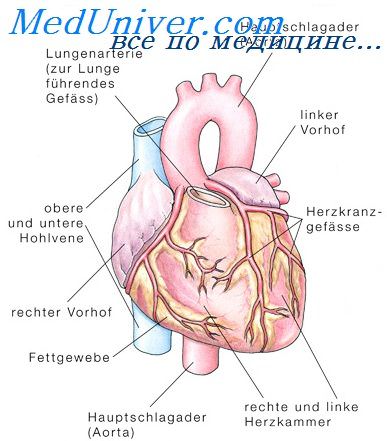
Первичное звено патогенеза инфаркта миокарда



С точки зрения анатомии сердце человека является органом, состоящим из тканей различных типов, среди которых ведущая роль принадлежит мышечной ткани.
В то же время существует, по меньшей мере, две особенности, кардинально отличающих сердечную мышечную ткань, состоящую из кардиомиоцитов, от других мышц:
- сердечная мышца регулярно сокращается и расслабляется «в автоматическом режиме» на протяжении всей жизни организма, причем число таких циклов сокращений и расслаблений миокарда составляет несколько десятков в течение каждой минуты;
- сердечная мышца обеспечивает снабжение кровью, насыщенной кислородом, не только всех органов и тканей организма, но и самой себя, благодаря 2 коронарным артериям – правой и левой.
Миокард, выполняющий очень большой объем работы, нуждается в значительном количестве кислорода из артериальной крови даже в том случае, когда человек находится в состоянии покоя (до 4% от общего сердечного выброса такой крови). А при физической нагрузке потребность миокарда в артериальной крови резко возрастает – до 20% от общего сердечного выброса.
При дефиците кислорода в том или ином участке сердечной мышцы быстро развивается одновременное кислородное голодание кардиомиоцитов, ведущее к их гибели, в чем и заключается суть инфаркта.
Ключевая причина
В подавляющем большинстве случаев инфаркта миокарда (свыше 90%) его причиной становится значительное уменьшение просвета одной из двух коронарных артерий (или артерий меньшего размера, отходящих от левой коронарной артерии), вызванное тромбом, сгустком крови. Кардиологи называют такое уменьшение просвета артерии, вызванное тромбом, «тромботическая окклюзия коронарной артерии» или «окклюзия коронарного сосуда».
Окклюзия коронарных артерий в свою очередь чаще всего является следствием такого хронического заболевания как атеросклероз. При атеросклерозе наблюдается нарушение обмена веществ в тканях стенок артерий (в первую очередь метаболизма жиров и белков), в результате чего на внутренних стенках этих кровеносных сосудов образуются бляшки, состоящие из «плохого» холестерина (липопротеинов низкой плотности – ЛПНП) и сложных белков липопротеинов. Кроме того, атеросклероз сопровождается и кальцинозом стенок коронарных артерий – отложением в тканях стенок сосудов солей кальция.
Атеросклероз постепенно приводит к сужению просвета артерий и снижению эластичности их стенок. Когда сужение просвета достигает определенного критического значения, развивается ишемическая болезнь сердца – хронический дефицит кислорода в миоцитах, которая без лечения способна привести к острой ишемии миокарда, то есть, к инфаркту.
Факторы риска развития инфаркта миокарда
Кроме атеросклероза к настоящему времени достоверно установлены и другие факторы риска развития инфаркта миокарда (ИМ):
- артериальная гипертензия. Гипертония приводит к постоянной перегрузке миокарда, которому приходится с усилием проталкивать необходимое количество крови, насыщенной кислородом, в аорту и отходящие от нее артерии. Перегрузка миокарда повышает его собственную потребность в кислороде и увеличивает риск развития ишемии и инфаркта даже при относительно незначительном дефиците крови, насыщенной этим газом;
- сахарный диабет также является фактором высокого риска развития инфаркта. Обусловлено это тем, что избыток глюкозы в крови диабетика с одной стороны пагубно действует на кровеносные сосуды, а с другой – ухудшает способность гемоглобина эритроцитов связываться с кислородом. В результате органы и ткани у больных диабетом начинают страдать от дефицита кислорода;
- наличие инфаркта миокарда в анамнезе. У людей, ранее уже перенесших инфаркт миокарда, повышенный риск развития повторного инфаркта сохраняется на протяжении десятилетий;
- наследственность (включая, в том числе генетическую предрасположенность к гипертонии, сахарному диабету, ожирению и т. д.);
- табакокурение (в том числе пассивное). Продукты горения табака обладают способностью сужать коронарные артерии, что также может спровоцировать инфаркт;
- ожирение и сидячий образ жизни. Обе эти патологии взаимосвязаны и способны вызвать уже упоминавшийся атеросклероз, а также гипертонию, болезни обмена веществ, которые сами по себе могут стать причиной инфаркта;
- возраст. Даже у очень здоровых людей вероятность развития инфаркта несколько повышается после 45-50 лет.
Источник
Патогенез инфаркта миокарда. Механизм развития инфаркта миокарда.Как правило, без атеросклероза коронарных артерий нет и инфаркта миокарда. Адекватность коронарного кровообращения метаболическим запросам миокарда определяется тремя основными факторами: величиной коронарного кровотока, составом артериальной крови и потребностью миокарда в кислороде. Для образования тромба в коронарной артерии обычно необходимы тоже три фактора: патологические изменения в ее интиме вследствие атеросклероза, активация в системе тромбообразования (рост коагуляции, агрегации тромбоцитов и эритроцитов, наличие сладж-феномена в МЦК, снижение фибринолиза) и пусковой фактор, способствующий взаимодействию двух первых (например, спазм артерии). Атеросклероз коронарных артерий прогрессирует с годами и суживает их просвет, порождая атеросклеротические бляшки. Затем вследствие действия факторов, способствующих разрыву (рост напряжения по всей окружности бляшки, ухудшение реологических свойств крови, большое количество воспалительных клеток, инфекция), нарушается целостность бляшки: обнажается ее липидное ядро, эрозируется эндотелий и обнажаются коллагеновые волокна. К дефекту прилипают активированные тромбоциты и эритроциты, чем запускается каскад свертывания и формирование тромбоцитарных пробок с последующим наслоением фибрина Возникает резкое сужение просвета коронарной артерии, вплоть до ее полной окклюзии Обычно от формирования тромбоцитарного тромба до тромботической окклюзии коронарной артерии проходит 2—6 дней, что клинически соответствует периоду нестабильной стенокардии. Хроническая тотальная закупорка коронарной артерии не всегда связана с последующим развитием ИМ От коллатерального кровотока, как и от других факторов (например, от уровня метаболизма миокарда, размеров и локализации зоны его поражения, снабжавшейся закупоренной артерией, скорости развития коронарной обструкции), зависит жизнеспособность клеток миокарда Коллатеральное кровообращение обычно хорошо развито у больных с тяжелой Ст (сужением просвета более чем на 75% в одной или нескольких коронарных артериях), выраженной гипоксией (тяжелые анемия, ХОБЛ и врожденные «синие» пороки) и ГЛЖ Наличие тяжелого стеноза коронарной артерии (более 90%) с регулярно повторяющимися периодами ее полной окклюзии позволяет существенно ускорить развитие коллатералей. Частота развития коронарных коллатералей через 1—2 недели после инфаркта миокарда варьирует, достигая 75-100% у больных с персистирующей окклюзией коронарных артерий и только 20—40% у пациентов с субтотальной окклюзией В случаях 1, 2, отмеченных на рисунке, инфаркт миокарда обычно не развивается вследствие доставки крови из соседней коронарной или другой артерии, а формируется в случае 3 (когда спазмирована дополнительно питающая миокард артерия) или 4 (ее просто нет) На фоне существенного сужения коронарной артерии разрыв атеросклеротической бляшки, приводящий к ИМ, происходит под действием триггеров, например ФН или стресса. Стресс (эмоциональный или физический) стимулирует выброс катехоламинов (они оказывают гистотоксический эффект) и повышает потребление кислорода миокардом. Сердце — это важная рефлексогенная зона. Негативный психоэмоциональный стресс (смерть близких, их тяжелая болезнь, выяснение отношений с начальством и др ) часто является «спичкой, дающей факел» – ИМ Инфаркт миокарда может спровоцировать и чрезмерная ФН (например, марафон, статический подъем больших тяжестей) даже у молодых лиц. Развитие инфаркта миокарда после острой окклюзии коронарной артерии. – Также рекомендуем “Банкетный инфаркт миокарда. Морфология инфаркта миокарда.” Оглавление темы “Инфаркт миокарда.”: |
Источник
Патогенез инфаркта миокарда. Механизмы развития инфаркта миокардаРассмотрим последовательно три составные части патогенеза инфаркта миокарда, а также связь между патогенезом и клиникой. Наиболее характерное проявление атеросклероза — это фиброзная атеросклеротическая бляшка, т. е. фиброатерома. Её “внешние черты” определяются двумя факторами (М. J. Davies, N. Woolf, 1991): а) соотношением липидного и соединительнотканного компонентов; Не существует какого-то типового “чертежа” атеросклеротической бляшки. От строения бляшки зависит клиническое течение заболевания (развитие осложнений). Именно разрыв таких поражений часто приводит у сорокалетних мужчин к тромбозу коронарной артерии с дальнейшим развитием обширного инфаркта (аневризмы сердца) или к внезапной смерти. Как отмечают М. J. Davies (1990); R. Т. Lee, P. Libby (1997), два варианта нарушения целостности бляшки могут приводить к тромбозу венечной артерии:
Разрыв атеросклеротической бляшки с полным или частичным тромбозом коронарной артерии — наиболее частая причина развития коронарных катастроф: нестабильной стенокардии, инфаркта миокарда, внезапной смерти (V. Fuster et al., 1992). Образование необтурирующих или кратковременно закупоривающих коронарную артерию тромбов обусловливает такие клинические проявления ИБС, как нестабильная стенокардия (с болями в состоянии покоя) и мелкоочаговый инфаркт миокарда. Обтурирующий (на протяжении длительного времени) тромбоз — патогенетическая основа крупноочагового (трансмурального) инфаркта миокарда (R. L. Ridolfi, G. M. Hutchins, 1977). Формирование вследствие разрыва бляшки как обтурирующего, так и не обтурирующего тромба может приводить к внезапной смерти. Кроме того, выброс в кровоток атероматозного содержимого расположенной в аорте бляшки может вызвать эмболию артерий мозга и других органов. Это объясняется хорошим развитием коллатеральных сосудов при длительно существующих стенозирующих бляшках (в ответ на часто возникающую ишемию миокарда — приступы стенокардии). Чем же отличаются на микроскопическом уровне “уязвимые” бляшки, которые, разорвавшись, могут вызвать острую коронарную недостаточность, от стабильных? “Уязвимые” бляшки: – “эксцентричны”, т. е. занимают лишь часть окружности артерии; – богаты липидами (липидное ядро занимает > 50 % их общего объёма); Уточним, что клетки воспаления (макрофаги, Т-лимфоциты), концентрация которых повышена в нестабильной бляшке, продуцируют различные цитокины, в частности интерлейкин 6 (interleukin 6, сокращённо IL6), которые могут активировать гладкомышечные клетки (S. Kinlay, P. Ganz, 1997). Программированная гибель (апоптоз) гладкомышечных клеток в оболочке бляшки, причины развития которой сейчас только изучаются, также может повышать вероятность разрыва бляшки (R. Т. Lee, P. Libby, 1997). – Также рекомендуем “Нестабильная атеросклеротическая бляшка. Диагностика нестабильной бляшки” Оглавление темы “Причины и диагностика инфаркта миокарда”: |
Источник
Причины инфаркта миокарда. Этиология инфаркта миокарда.Этиология инфаркта миокарда — полифакторная (в большинстве случаев действует не один фактор, а их комбинация). ФР ИБС (их более 20): АГ, гиперлипидемия, курение, физическая детренированность, избыточный вес, СД (у пожилых диабетиков на фоне ИМ в 4 раза чаще появляются аритмии и в 2 раза чаще — ОСН и КШ), выраженный стресс. В настоящее время можно так перечислить обстоятельства с максимальными коэффициентами риска ИБС (в порядке убывания): наличие близких родственников, у которых ИБС возникала до 55 лет, гиперхолестеринемия более 7 ммоль/л, курение более 0,5 пачки в сутки, гиподинамия, СД. Главный фактор инфаркта миокарда (в 95%) — неожиданный тромбоз коронарной артерии в области атеросклеротической бляшки с закупоркой артерии или ее субтотальным стенозом. Уже в 50 лет атеросклероз коронарных артерий отмечается у половины людей. Обычно тромб возникает на поврежденном эндотелии в месте разрыва волокнистой «шапки» бляшки (патофизиологический субстрат ОКС). В этой зоне также накапливаются медиаторы (тромбоксан Аг, серотонин, АДФ, фактор активации тромбоцитов, тромбин, тканевый фактор и др.), которые стимулируют дальнейшую агрегацию тромбоцитов, эритроцитов и механическое сужение коронарной артерии. Этот процесс имеет динамический характер и может циклично приобретать разные формы (частичная или полная окклюзия коронарной артерии или ее реперфузия). Если нет достаточного коллатерального кровообращения, то тромб закрывает просвет артерии и вызывает развитие ИМ с повышением сегмента ST. Тромб имеет размер 1 см в длину и состоит из тромбоцитов, фибрина, эритроцитов и лейкоцитов. На вскрытии тромб часто не находят вследствие его посмертного лизиса. После окклюзии коронарной артерии гибель клеток миокарда начинается не сразу, а через 20 мин (это — прелетальная фаза). Запаса кислорода в миокарде хватает только на 5 сокращений, потом сердце «голодает» с развитием «ишемического каскада» — последовательности событий после коронарной окклюзии. Нарушается диастолическое расслабление волокон миокарда, что приводит в последующем к уменьшению систолической сократимости сердца, появлению на ЭКГ признаков ишемии и клиническим проявлениям. При трансмуральном поражении миокарда (всей стенки) этот процесс завершается через 3 ч. Но гистологически кардиомиоцит некротизируется только через 12—24 ч после остановки коронарного кровотока. Более редкие причины ИМ:
• длительный спазм коронарной артерии (в 5%), особенно у молодых, на фоне стенокардии Принцметала. Ангиографически патологию в коронарных артериях могут и не выявить. Спазм коронарной артерии, обусловленный дисфункцией эндотелия, может повреждать целостность эндотелия атероскле-ротической бляшки, а возникает, как правило, на фоне длительных отрицательных эмоций, умственного или физического перенапряжения, избыточной алкогольной или никотиновой интоксикации. При наличии подобных факторов часто возникает «адреналовый некроз» миокарда вследствие большого выброса катехоламинов. Такой вид ИМ чаще возникает у молодых «интравертов» (которые «переваривают все в себе»). Обычно у этих больных нет выраженной Ст или указаний на нее в анамнезе, но есть воздействие коронарных ФР; • поражения коронарных артерий (коронариты) при узелковом панартериите (УГЛА), СКВ, болезни Такаясу, ревматоидном артрите, острой ревматической лихорадке (2-7% от всех ИМ), т.е. ИМ может быть синдромом, осложнением других заболеваний; • эмболия коронарных сосудов при инфекционном эндокардите, тромбоэмболии из левых камер сердца на фоне имеющегося мурального тромбоза ЛЖ или ЛПр, врожденных аномалиях коронарных артерий; • муральное утолщение коронарных артерий на фоне метаболических или пролиферативных заболеваний интимы (гомоцистеинурия, болезнь Фабри, амилоидоз, ювенильный склероз интимы, коронарный фиброз, обусловленный рентгеновским облучением грудной клетки); • миокардиальный дисбаланс кислорода — несоответствие притока крови по коронарным артериям к потреблению кислорода миокардом (например, при аортальных пороках, тиреотоксикозе, длительной гипотензии). Так, у ряда больных с достаточно выраженным атеросклеротическим поражением коронарных артерий, но без разрыва бляшки, ИМ возникает при состояниях, когда существенно снижена доставка кислорода к миокарду. На ЭКГ у этих больных обычно определяется глубокий отрицательный зубец Т и депрессия сегмента ST; – Также рекомендуем “Патогенез инфаркта миокарда. Механизм развития инфаркта миокарда.” Оглавление темы “Инфаркт миокарда.”: |
Источник