Осложнение на почки после инфаркта
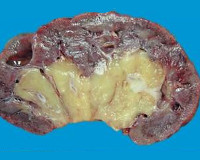
Инфаркт почки – это редкое нефрологическое заболевание, обусловленное эмболией артериальных сосудов органа с последующим некрозом его тканей и нарушением функциональной активности. Симптомы зависят от объема поражения, варьируются от полного отсутствия проявлений до резких болей в пояснице, гематурии, почечной недостаточности, увеличения уровня артериального давления. Диагностика производится на основании данных анамнеза, результатов анализов крови и мочи, УЗДГ сосудов почки, почечной ангиографии. Лечение преимущественно симптоматическое, также включает в себя применение антиагрегантных и антикоагулянтных средств, иногда показано хирургическое вмешательство.
Общие сведения
Инфаркт почки встречается намного реже других ишемических расстройств органов мочевыделительной системы. Данное состояние практически никогда не является изолированным нарушением, а выступает в качестве осложнений других, преимущественно сердечно-сосудистых патологий. Точные статистические данные относительно встречаемости болезни отсутствуют, поскольку определенная доля больных не обращается к специалистам из-за слабой выраженности симптомов.
Заболевание следует дифференцировать с мочекислым инфарктом почек у детей, являющимся одним из этапов адаптации мочевыделительной системы к внеутробному существованию. Из-за особенностей эпидемиологии болезней, способных осложняться инфарктом почки, патология чаще возникает у лиц старшего возраста, страдающих ожирением и обменными нарушениями.

Инфаркт почки
Причины
В подавляющем большинстве случаев состояние имеет ишемический характер и вызывается эмболией магистральных почечных сосудов. Чаще всего эмбол представлен тромботическим сгустком, реже в таком качестве могут выступать фрагменты атеросклеротических бляшек, жировые массы. Картину, схожую с эмболией ветвей почечной артерии, иногда провоцируют артериовенозные фистулы или кровотечения. Таким образом, основной причиной заболевания является наличие в артериальной части большого круга кровообращения эмболов, которые могут образовываться при следующих патологиях:
- Эндокардит. Воспаление внутренней оболочки левого желудочка или предсердия часто осложняется формированием пристеночного тромба. Его фрагменты периодически попадают в большой круг кровообращения и могут закупоривать просвет артерий почек.
- Аритмии и пороки сердца. Различные нарушения сердечного ритма сопровождаются нарушениями гемодинамики внутри полостей сердца, что иногда приводит к тромбообразованию. Схожий механизм возникновения тромбов отмечается при недостаточности митрального клапана или пролапсе его створок.
- Атеросклеротическое поражение. Выраженный атеросклероз аорты или венечных артерий являются одной из наиболее частых причин инфаркта почки. Закупорка сосуда может быть обусловлена как фрагментом собственно атеросклеротической бляшки, так и тромбом, который образовался на ее поверхности. Атеросклероз почечных сосудов может приводить к расслоению их стенок, что также провоцирует закупорку просвета и острую ишемию.
- Узелковый периартериит. Данное состояние неясной этиологии в случае вовлечения в патологический процесс сосудистой сети почек может становиться причиной инфарктов.
- Медицинские манипуляции. Различные диагностические и лечебные манипуляции на органах мочевыделительной системы могут осложняться стенозом сосудов с развитием острой ишемии почечной ткани.
Косвенной причиной патологии иногда является наркотическая зависимость, связанная с частыми внутривенными вливаниями (опиоидная или эфедриновая наркомания). В случае использования нестерильного инструментария развивается специфический эндокардит с образованием многочисленных тромбов. Различные формы инфаркта почки обнаруживаются у 20-30% инъекционных наркоманов. Множественные очаги инфарктов в почечной ткани возникают и при диссеминированном внутрисосудистом свертывании крови (ДВС-синдроме).
Патогенез
Основополагающим звеном патогенеза более чем в 90% случаев инфаркта почки считается образование эмболов, которые вызывают закупорку сосудов органа. В результате нарушается снабжение участка почечной ткани кислородом и питательными веществами. По своей кислородной потребности почки уступают только нервной ткани и миокарду, из-за чего в результате ишемии довольно быстро возникают дистрофические изменения в клетках нефронов. Размер поражения зависит от калибра артериального сосуда, перекрытого эмболом – чем он больше, тем распространеннее зона инфаркта. Характерная форма зоны ишемии – клиновидная или треугольная с вершиной у ворот почки и обращенным к корковому веществу основанием. Это обусловлено особенностями распределения кровеносных сосудов в органе.
После прекращения поступления артериальной крови дистрофия клеток нефронов постепенно нарастает, сменяясь их гибелью и формированием участков некроза. Одновременно возникает раздражение юкстагломерулярного аппарата с образованием больших количеств гормона ангиотензина 2, что приводит к развитию вазоренальной гипертензии и каскаду связанных с этим нарушений (повышается риск инфаркта миокарда или инсульта). Продукты распада некротизированных тканей всасываются в системный кровоток и становятся причиной интоксикации организма, проявляющейся повышением температуры, головными болями, тошнотой. Исходом некроза становится разрастание фиброзной ткани и формирование рубца.
Симптомы инфаркта почки
Клиническая картина заболевания характеризуется различной выраженностью симптомов, которая, прежде всего, зависит от объема ишемизированной и некротизированной ткани почек. При незначительных инфарктах субъективные жалобы отсутствуют, патология выявляется случайно по измененным данным диагностических исследований. В случае более обширных поражений симптоматика становится выраженной, однако большинство проявлений неспецифичны – боль в пояснице, гематурия, уменьшение объема выделяемой мочи.
Болезненные ощущения, возникающие сначала с двух сторон, постепенно смещаются в сторону пораженной почки – двухсторонние инфаркты встречаются крайне редко. Интенсивность болевого синдрома иногда сопоставима с почечной коликой, боль устраняется только приемом сильных наркотических анальгетиков. Степень выраженности гематурии при инфаркте почки также может сильно варьироваться – от микроскопических количеств эритроцитов в моче до ее ярко алой окраски и профузного почечного кровотечения.
Иногда наблюдается реальная почечная колика, обусловленная прохождением кровяного сгустка или кусочка некротизированной ткани по мочевыводящим путям. Проявления почечной недостаточности обычно выражены слабо, особенно при сохраненной функциональной активности второй почки. При тотальном инфаркте возможно токсическое поражение парного органа, что проявляется развитием ОПН – анурией, запахом аммиака изо рта и от кожных покровов больного.
Общие симптомы заболевания сводятся к повышению температуры тела до 38 градусов, явлениям интоксикации (тошноте, рвоте, разбитому состоянию), ознобу. В некоторых случаях из-за нарушенного кровоснабжения почки возникает стимуляция юкстагломерулярного аппарата, провоцирующая рост артериального давления. Вышеперечисленные проявления обычно сочетаются с симптомами основной патологии, которая спровоцировала ишемию и инфаркт почечной ткани. Таковыми могут быть боли в области сердца, нарушения сердечного ритма, признаки циркуляторных расстройств при пороках клапанов (цианоз, повышение давления крови в малом круге кровообращения).
Осложнения
Ранним и наиболее тяжелым осложнением инфаркта почки является развитие острой почечной недостаточности. ОПН наблюдается достаточно редко, поскольку для этого необходимо наличие ряда условий – двухсторонний характер инфаркта либо наличие у больного только одной почки. При тотальной ишемии недостаточность может возникать из-за чрезмерной нагрузки на второй орган или по причине его токсического поражения. В отдаленной перспективе из-за формирования рубцов в пораженной почке снижается ее функциональная активность, что создает предпосылки для возникновения ХПН в будущем. У ряда больных после разрешения инфаркта сохраняется стойкое увеличение артериального давления, обусловленное нарушениями кровообращения в почках.
Диагностика
Определение инфаркта почки осложняется неспецифичностью симптомов, поскольку боли в пояснице, ухудшение общего состояния, гематурия характерны и для иных нефрологических заболеваний. Во многих случаях врачу-нефрологу или урологу требуется кооперация с другими медицинскими специалистами (например, с кардиологом) для уточнения диагноза. Особую важность имеет скорость определения болезни, так как от своевременности лечебных мер зависит ее исход, а при неправильном лечении повышается риск развития осложнений. В числе диагностических мероприятий выделяют следующие группы методов:
- Опрос и общий осмотр. При опросе акцентируют внимание на субъективных симптомах и жалобах больного. Имеет значение выраженность и локализация болезненных ощущений, наличие или отсутствие расстройств мочеиспускания. В анамнезе определяют наличие сердечно-сосудистых, гематологических или иных заболеваний, способных спровоцировать ишемию тканей почки.
- Лабораторные исследования. В общем анализе мочи практически всегда определяется наличие эритроцитов – от выраженной макрогематурии до микроскопических примесей крови, часто возникает протеинурия. При биохимическом исследовании мочи специфическим признаком инфаркта является увеличение уровня лактатдегидрогеназы (ЛДГ), аналогичное повышение наблюдается и в сыворотке крови. У большинства пациентов также обнаруживается незначительный лейкоцитоз, изменяются показатели коагулограммы – последняя выполняется для оценки необходимости использования антикоагулянтов.
- Инструментальные исследования. Обычно при подозрении на инфаркт почки производят ультразвуковую допплерографию (УЗДГ почечных артерий), позволяющую оценить показатели кровотока в основных сосудах органа. Еще больше информации дает селективная контрастная почечная ангиография, по результатам которой выявляется участок ишемизированной ткани, не накапливающей контраст. Как альтернативу последнему исследованию могут назначать МСКТ или МРТ с контрастом и последующим 3Д-моделированием почечной сосудистой сети.
- Эндоскопические исследования. Цистография при данном заболевании производится с целью дифференциальной диагностики. С помощью этого метода исключается вероятность кровотечения из мочевого пузыря (наблюдаемого при опухолях, травмах), уточняется односторонний характер поражения.
Дифференциальную диагностику инфаркта почки проводят с опухолевыми поражениями мочевыводящих путей (чашечно-лоханочной системы, мочеточников, мочевого пузыря и уретры) и кровотечениями из них. Иногда проявления заболевания создают ложную клиническую картину гломерулонефрита – он исключается при подтверждении одностороннего характера процесса и наличии ишемизированного участка тканей. При помощи дополнительных исследований инфаркт почки дифференцируют с почечной коликой при мочекаменной болезни и расслоением стенки брюшной аорты.
Лечение инфаркта почки
Основные цели терапии данного заболевания изменяются в зависимости от этапа патологического процесса. На начальных этапах первоочередной задачей является восстановление адекватного кровотока в органах выделения, что позволяет минимизировать негативные последствия ишемии. В дальнейшем на первый план выступает устранение кровотечения (макрогематурии), явлений общей интоксикации и сохранение функциональности оставшейся части органа. Зачастую для этих целей используют препараты с противоположным действием (например, антикоагулянты и гемостатики), поэтому от специалиста требуется особая осторожность при их назначении. Консервативная терапия инфаркта сводится к использованию следующих лекарственных средств:
- Обезболивающие препараты. Боли могут быть очень интенсивными, в ряде случаев болевой синдром устраняется только мощными наркотическими анальгетиками – морфином, фентанилом и другими.
- Тромболитические средства. К ним относят стрептокиназу и другие препараты данной группы, цель их применения – устранение тромба в сосуде, восстановления адекватного кровотока. Медикаменты используются только на первых этапах заболевания, до развития выраженной гематурии. После начала выделения крови с мочой назначение этих средств строго запрещено.
- Гемостатические препараты. Применяются при выраженной гематурии и профузном почечном кровотечении. Основным лекарственным средством данной группы является этамзилат натрия, введение которого позволяет минимизировать кровопотерю и улучшить прогноз заболевания.
- Антикоагулянты. На любом этапе патологии рекомендуется принимать меры по нормализации работы свертывающей системы крови, с этой целью назначаются антикоагулянты прямого действия (например, гепарин). Схема, дозировки и длительность применения строго индивидуальны, определяются после изучения коагулограммы больного.
- Антиагрегантные средства. Антиагреганты (например, ацетилсалициловая кислота) редко используются в остром периоде заболевания. Их назначают через 1-2 недели после исчезновения гематурии для снижения риска рецидива и отдаленных осложнений. Дозировка и длительность курса лечения определяется с учетом функциональной активности выделительной системы.
В тяжелых случаях (например, тотальный инфаркт почки) проводят хирургическое лечение, которое на начальных стадиях болезни сводится к восстановлению проходимости магистральных артерий и почечного кровотока. При поздней диагностике и развитии некротических изменений в почке по показаниям осуществляют оперативное удаление зоны инфаркта вплоть до нефрэктомии (при наличии у больного второго здорового органа). В числе вспомогательных лечебных мероприятий используют гемодиализ (при почечной недостаточности), назначают диуретические, гипотензивные и другие средства по показаниям.
Прогноз и профилактика
Прогноз инфаркта почки определяется объемом пораженных тканей – обычно страдает относительно небольшой фрагмент органа, после рубцевания это слабо отражается на работе выделительной системы. При ишемии значительной области органа возможно развитие острой или хронической почечной недостаточности, кровотечения и прочих жизнеугрожающих состояний. Существует риск рецидива, особенно при сохранении провоцирующего фактора (эндокардитов, пороков сердца, атеросклероза магистральных сосудов).
Поскольку заболевание часто является осложнением болезней сердечно-сосудистой системы, его профилактика заключается в правильном лечении основной патологии – использовании антиагрегантных средств, антибиотиков при эндокардитах, антихолестеринемических средств в случае атеросклероза.
Источник
Основные осложнения после перенесенного инфаркта миокарда
Тяжесть осложнений острого инфаркта миокарда (ОИМ) связана со степенью нарушения венечного кровотока, сократительной способности сердечной мышцы и локализацией ишемии. Важную роль играет оперативность оказания медицинской помощи, адекватность терапии, наличие сопутствующей патологии, возраст пациента. Кратковременное нарушение кровоснабжения вызывает отмирание клеток субэндокардиальной зоны. Если длительность ишемии превышает 6 часов, развивается некроз 80% пораженного миокарда.
Стадии развития:
- Острейшая (первые 6 часов).
- Острая (до 14 дней).
- Подострая (до 2 месяцев).
- Рубцевания.
Осложнения инфаркта могут возникать на любом этапе. В этом его опасность. Особенно рискуют больные, которых госпитализировали через 6-12 часов после начала приступа и тромболитическая терапия или другие методы восстановления кровотока не проводились. При развитии осложненного инфаркта летальный исход может наступить в течение года.
Все осложнения ОИМ можно разделить на четыре блока:
- Электрические (нарушение ритма и проводимости импульса).
- Механические (связаны со структурными нарушениями в миокарде).
- Гемодинамические (вызваны функциональной неспособностью пораженного миокарда обеспечивать прежний кровоток).
- Реактивные (связаны с резорбтивными и аутоиммунными процессами, активацией симпатической нервной системы, а также вторичными дисфункциями внутренних органов).
Ранние
Осложнения острого периода инфаркта миокарда развиваются в первые 10 суток после болевого приступа и существенно не ухудшают прогноз заболевания при своевременном лечении.
Нарушения ритма и проводимости – самые частые осложнения острого периода инфаркта (до 80%). Аритмии в основном развиваются из-за изменения электрофизиологических свойств и метаболизма в пораженной зоне, снижения порога фибрилляции, выброса в кровоток большого количества активных веществ — катехоламинов и развития феномена re-entry (круговой циркуляции волны возбуждения в миокарде).
Клинико-прогностическая классификация аритмий:
Неопасные для жизни:
- синусовая аритмия, брадикардия (пульс медленный, но >50), тахикардия (<110 уд/мин);
- миграция водителя ритма по предсердиям;
- редкие (<5 за минуту) предсердные и желудочковые экстрасистолы;
- переходящая AV-блокада I степени.
Прогностически серьезные:
- синусовая тахикардия с пульсом >110 уд/мин, брадикардия <50 уд/мин;
- частые предсердные, а также групповые, политопные ранние желудочковые экстрасистолы (предикторы фибрилляции и мерцательной аритмии);
- синоаурикулярная блокада;
- AV-блокада II-III степеней;
- идиовентрикулярный ритм;
- ритм из АV-соединения;
- суправентрикулярная пароксизмальная тахикардия;
- мерцание и трепетание предсердий;
- синдром слабости синусового узла.
Опасные для жизни:
- пароксизмальная желудочковая тахикардия;
- фибрилляция, трепетание желудочков;
- субнодальная полная AV-блокада;
- асистолия желудочков.
Клинически нарушения ритма проявляются:
- сердцебиением;
- ощущением перебоев в работе сердца;
- падением артериального давления;
- головокружением, потерей сознания.
Благодаря широкому внедрению тромболизиса на догоспитальном этапе и экстренной реваскуляризации миокарда частота внутрижелудочковых и полных AV-блокад не превышает 5%. Ранее эти осложнения становились причиной смерти более 50% пациентов как следствие прогрессирования сердечной недостаточности и развития кардиогенного шока.
В случае повторения жизнеугрожающих нарушений ритма устанавливают трансвенозный электрод для временной стимуляции миокарда в режиме of demand (по требованию). После возобновления адекватного сердцебиения устройство оставляют до полной стабилизации гемодинамических показателей (на 7-10 дней).
Острая сердечная недостаточность развивается из-за нарушения функции левого желудочка. К ней приводят обширные и трансмуральные инфаркты, осложненные тахиаритмией или AV-блокадой. Некротизированная зона миокарда «выключается» из сократительной массы При отмирании более 40% мышечной ткани желудочка развивается кардиогенный шок.
Резкое снижение функции выброса левого желудочка приводит к:
- увеличению конечного диастолического объема крови в нем;
- повышению давления сначала в левом предсердии, затем в легочных венах;
- развитию кардиогенного отека легких;
- недостаточному кровоснабжению жизненно важных органов (головного мозга, печени, почек, кишечника.
Клинически острая сердечная недостаточность проявляется:
- прогрессирующей одышкой;
- тахикардией, снижением давления;
- влажными хрипами в легких, крепитацией;
- цианозом (посинением кожи);
- снижением диуреза;
- нарушением сознания.
Кардиогенный шок – крайняя степень недостаточности левого желудочка, летальность при котором превышает 85%.
Лечение острой сердечной недостаточности, кардиогенного шока и альвеолярного отека легких должно проводиться в условиях реанимационного блока.
Механические осложнения в раннем периоде (разрывы сердца). Этот тяжелейший, чаще всего летальный исход инфаркта развивается на 5-7 сутки после приступа.
Разрывы сердца делят на:
- Наружные. Разрыв стенки желудочка в области ишемического поражения с истечением крови в перикард.
Выделяют предразрывный период, который интенсивной болью, проявлениями шока, и собственно разрыв стенки. В этот момент быстро происходит остановка кровообращения с признаками клинической смерти. Иногда этот процесс может затянуться на несколько суток.
К сожалению, лишь малому проценту больных удается выполнить экстренную пункцию перикарда и срочную операцию по восстановлению целостности левого желудочка с дополнительным аортокоронарным шунтированием.
2. Внутренние:
- Разрыв межжелудочковой перегородки. Возникает при передней локализации некроза. Диаметр дефекта колеблется от 1 до 6 см. Клинически это проявляется нарастанием некупируемой боли, развитием кардиогенного шока, появлением за несколько часов тотальной сердечной недостаточности. Лечение исключительно хирургическое.
- Разрыв сосочковой мышцы. Папиллярные мускулы удерживают митральный и трикуспидальный клапаны закрытыми во время систолы, не давая крови забрасываться обратно в предсердия. Полностью несовместим с жизнью, так как молниеносно развивается митральная недостаточность и альвеолярный отек легких.
Аневризма левого желудочка. Локальное выбухание стенки левого желудочка во время диастолы. Дефект состоит из отмершей или рубцовой ткани и не участвует в сокращении, а его полость зачастую заполнена пристеночным тромбом. Состояние опасно развитием эмболических осложнений или разрывом сердца.
Психические нарушения. Обычно развиваются на первой неделе заболевания и вызваны недостаточным поступлением крови в мозг, низким содержанием в ней кислорода и влиянием продуктов распада сердечной мышцы.
Нарушения поведения могут протекать в форме психотических (сопор, делирий, сумрачное состояние) и непсихотических реакций (астения, депрессия, эйфория, невроз).
Особое внимание следует уделить депрессивному синдрому (он может послужить причиной суицида).
Поздние
 По истечении 10 суток после сердечного приступа могут развиться:
По истечении 10 суток после сердечного приступа могут развиться:
- Ранняя постинфарктная стенокардия. Чаще возникает при поражении нескольких венечных сосудов или недостаточном тромболизисе, а также из-за нарушения диастолической функции левого желудочка. Является предиктором рецидива инфаркта миокарда и внезапной сердечной смерти.
- Тромбоэмболические осложнения:
- ТЭЛА (тромбоэмболия легочной артерии);
- бифуркации брюшного отдела аорты, артерий нижних конечностей (с развитием гангрены);
- тромбоз мезентериальных сосудов (клиническая картина острого живота), почечной артерии (инфаркт почки), церебральных артерий (инсульт).
3. Тромбоэндокардит. Асептическое воспаление эндокарда с пристеночным тромбообразованием в зоне некроза. Служит источником материала для эмболии сосудов большого круга кровообращения.
4. Стрессовые эрозии и язвы желудочно-кишечного тракта, кровотечение. Может развиваться и в остром периоде инфаркта миокарда. Причиной развития патологии служит нарушение кровоснабжения кишечной стенки, гиперактивация симпатической нервной системы, терапия антиагрегантами и антикоагулянтами.
5. Парез кишечника. Нарушение мочеиспускания (атония мочевого пузыря). Особенно часто встречается у пожилых пациентов на фоне действия нейролептаналгезии, строгого постельного режима, применения атропина.
Также в позднем периоде возможно развитие нарушений ритма и проводимости и хронической аневризмы сердца.
Отдаленные
 В отдаленном периоде возможно развитие:
В отдаленном периоде возможно развитие:
- Хронической сердечной недостаточности, которая требует пожизненной медикаментозной терапии.
- Постинфарктного кардиосклероза. Снижение и нарушения функции миокарда, вызванное рубцовыми и склеротическими процессами, что повышает риск повторного ОИМ.
- Постинфарктного синдрома (Дресслера). Это аутоиммунный процесс, вызванный неадекватным ответом организма больного на продукты распада отмерших клеток сердца: образуются антитела к собственным серозным оболочкам. Развивается на 2-8 неделе заболевания и характеризуется классической триадой: сухой перикардит, плеврит, пневмонит. Реже наблюдается поражение грудинно-реберных и плечевых суставов с развитием синовита.
Как не допустить ухудшения
Большинство осложнений ОИМ развиваются по причинам, не зависящим от пациента. Но существует ряд превентивных мер, способных снизить вероятность возникновения и тяжесть последствий:
- Обучение азам первой медицинской помощи при ОИМ и алгоритму реанимационных мероприятий.
- Своевременное обращение за медицинской помощью. Реваскуляризация (тромболизис, стентирование, аортокоронарное шутнирование) возобновляет кровоток в пораженном сосуде и ограничивает зону некроза миокарда.
- Строгий постельный режим в первые сутки заболевания, максимальный эмоциональный покой.
- Следование курсу лечения и своевременный прием медикаментов.
- Дозированные физические нагрузки, физиотерапия согласно стадии инфаркта.
Что делать при осложнениях: как лечить и к кому обращаться
 Ранние осложнения лечатся в условиях палаты интенсивной терапии кардиологической клиники с постоянным мониторингом жизненных показателей. Ритм восстанавливают путем введения антиаритмических препаратов (класс медикамента зависит от вида аритмии), электроимпульсной терапией или имплантацией кардиостимулятора. Механические осложнения требуют хирургического вмешательства на открытом сердце с использованием искусственного кровообращения.
Ранние осложнения лечатся в условиях палаты интенсивной терапии кардиологической клиники с постоянным мониторингом жизненных показателей. Ритм восстанавливают путем введения антиаритмических препаратов (класс медикамента зависит от вида аритмии), электроимпульсной терапией или имплантацией кардиостимулятора. Механические осложнения требуют хирургического вмешательства на открытом сердце с использованием искусственного кровообращения.
Поздние осложнения развиваются на стационарном или санаторно-курортном этапе. Лечение тромбоэмболических эпизодов зависит от состояния пораженного сосуда и длительности ишемии. Допускается консервативное введение антикоагулянтов, тромболизис, эндоваскулярное удаление эмбола, открытая тромбэктомия. В случае необратимых повреждений выполняют резекцию.
С осложнениями отдаленного периода пациент должен обратиться к лечащему кардиологу, который проведет диагностику и назначит лечение.
Выводы
Вероятность ранних и поздних осложнений инфаркта миокарда возрастает при несвоевременном обращении за медицинской помощью, а также у пациентов с нелеченной гипертонией, сахарным диабетом и атеросклерозом.
Для профилактики инфаркта и его осложнений стоит придерживаться здорового образа жизни, полноценно питаться, избегать стрессов и влияния неблагоприятных факторов окружающей среды, отказаться от курения, ограничить употребление алкоголя, регулярно делать зарядку.
Пациентам с сердечно-сосудистыми заболеваниями стоит систематически проходить профилактические осмотры 2 раза в год и следовать рекомендациям врача.
Источник
