Нарушения в системе гемостаза при инфаркте миокарда

22 октября 2010
Острый инфаркт миокарда сопровождается значительными изменениями гемостаза.
Причиной изменения гемостаза при остром инфаркте миокарда могут служить и развившийся коронаротромбоз, и тромбопластин, поступающий в кровоток из некротизированного миокарда , и другие факторы: увеличение активности симпатико-адреналовой системы и содержания в крови кортикостероидов, тироксина, гистамина, серотонина, кининов и других биологически активных веществ [Павлович Л. А., 1980; Голиков А. П., Ивлева В. И., 1981; Хаткевич А. В., 1982; Магек П. et al., 1980].
При обобщении выясняется, что при инфаркте миокарда создается ситуация, которая укладывается в понятие дисфункции системы регуляции агрегатного состояния крови (PACK), рассмотренной О. К. Гавриловым и соавт. (1979, 1981).
По мнению авторов, факторы свертывания крови являются структурными элементами системы PACK, которая поддерживает жидкое состояние крови и обеспечивает своевременное восстановление поврежденных стенок сосудов в процессе нормального функционирования органов и систем.
Частота коронаротромбоза и изменения в системе PACK в виде нарушений гемостаза при инфаркте миокарда являются обоснованием проведения противосвертывающей и тромболитической терапии.
Лечебные мероприятия такого рода должны быть направлены на снижение адгезивно-агрегационной способности тромбоцитов, лизис нитей фибрина и снижение коагулирующей активности крови [Чазов Е. И., Лакин К. М., 1977;
Люсов В. А., Белоусов Ю. Б., 1981].
Таким образом, в задачи противосвертывающей и тромболитической терапии инфаркта миокарда входит:
- улучшение микроциркуляции миокарда путем положительного воздействия на свертываемость и реологические свойства крови, усиления лизиса тромбов в системе микроциркуляции периинфарктной зоны;
- предотвращение роста первичного тромба, находящегося в коронарной артерии;
- восстановление перфузии облитерированной венечной артерии посредством лизиса коронарного тромба;
- предупреждение тромбоэмболических осложнений.
«Инфаркт миокарда», Я.Д.Мамедов
О изменении свертывания крови при инфаркте миокарда нет единого мнения. Исследователи единодушны только в отношении фибриногена, содержание которого увеличивается в остром периоде инфаркта миокарда [Голиков А. П., Королева С. А., 1981; Насиров Ш., 1981; Sharma S. С., Seth П. N., 1978; Saxena К. К. et al., 1979]. М. А. Йрани (1968) обнаружил зависимость между увеличением…
Тромбиновое время на 1-е сутки определения было укороченным на 44,7% (р < 0,001) по сравнению с исходным показателем. На 3-и и 7-е сутки оно продолжало оставаться меньше на 34,9% и 28,2% соответственно (р < 0,01), чем у интактных животных. Начиная с 15-х суток отмечалась тенденция к нормализации. Гепариновое время на 1-е сутки исследования укорачивалось на…
Р. С. Оганесян (1971) выявил укорочение времени свертывания крови у 70,6% и удлинение — у 3,9% обследованных. Нормальные показатели были у 25,5% больных. Не меньшее разнообразие данных выявляется и при исследовании свертывающей системы крови методом тромбоэластографии. По мнению некоторых авторов, в остром периоде инфаркта миокарда выраженные изменения свертываемости происходят в артериальной крови [Гаврилов О. К.,…
Параллельно проводимая регистрация скорости лимфооттока из дренированного грудного лимфатического протока после моделирования острого инфаркта миокарда свидетельствовала о ее замедлении через сутки на 61,3% (р < 0,01) по сравнению с исходной величиной, а на 3-й и 7-е сутки скорость лимфооттока была меньше, чем у интактных животных, соответственно на 53,9 (р < 0,01) и 33,5%. К концу…
Большинство авторов указывают на увеличение толерантности плазмы к гепарину в остром периоде инфаркта миокарда [Чураков Ю. А., Войтевич Е. Г., 1979; Мистрюков М. И., 1980; Голиков А. П., Королева С. А., 1981; Зверева Т. В., Хватов В. Б., 1982]. Однако имеются работы, указывающие и на снижение этого показателя в начальном периоде инфаркта миокарда с последующим…
Источник
Нарушения мозгового кровообращения. Москва. 1971г.

Семенистый М.Н. (слева) Профессор, Д.М.Н., Заслуженный Врач РФ, Круглов С.В. (справа)
Автор проекта: профессор, доктор медицинских наук, заслуженный врач РФ, Круглов Сергей Владимирович
Подробнее
Редактор страницы: Семенистый М.Н.
Подробнее
Ведущие специалисты в области нейрохирургии:

Балязин Виктор Александрович
Балязин Виктор Александрович, Профессор, Доктор Медицинских наук, Заслуженный врач РФ, Отличник Здравоохранения РФ, Врач-нейрохирург, Заведующий кафедрой нервных болезней и нейрохирургии
Подробнее

Молдованов Владимир Архипович
Молдованов Владимир Архипович, Кандидат Медицинских наук, Врач высшей квалификационной категории, 35 клинического стажа
Подробнее

Савченко Александр Федорович
Савченко Александр Федорович, Кандидат Медицинских наук, Врач высшей квалификационной категории, Заведующий нейрохирургическим отделением БСМП№2
Подробнее
П. Е. Лукомский (Москва)
Экспериментальные и клинические исследования, в том числе и наших сотрудников, показали, что типичными нарушениями гемодинамики при инфаркте миокарда являются уменьшение сердечного выброса, артериального давления и общего периферического сопротивления. Эти изменения особенно резко» выражены у больных с шоком. Однако между степенью уменьшения сердечного выброса и тяжестью нарушений циркуляции, в частности, возникновением шока, нет прямой зависимости. Все это заставило обратиться к изучению нарушений в системе микроциркуляции. Они оказались особенно резко выраженными при кардиогенном шоке. В патогенезе их большое значение имеет констрикция артериол вследствие повышенной активности симпатоадреналовой системы.

НАРУШЕНИЕ МИКРОЦИРКУЛЯЦИИ И ГЕМОСТАЗА У
БОЛЬНЫХ ИНФАРКТОМ МИОКАРДА
Для исхода заболевания, особенно кардиогенного шока, нарушения микроциркуляции, реологических свойств крови и свертываемости ее имеют решающее значение.
Это показывает, насколько важно клиницисту иметь возможность правильно оценить состояние микроциркуляции у больных инфарктом миокарда.
С этой целью наш сотрудник Ю. Ц. Зимин наблюдал и фотографировал микроциркуляцию в бульбарной конъюнктиве глаз. Этот метод дает ценные результаты, но применение его» у тяжелых больных, особенно с шоком, весьма затруднительно. Определялся период полувыведения J131 из внутрикожного депо. Этот период достоверно увеличивался у больных неосложненным инфарктом миокарда, еще в большей степени при явлениях застоя. Особенно же резко клиренс 7131 увеличивался при шоке у некоторых больных до 36-44 мин. вместо 7,2 в норме. Мы связываем замедление рассасывания из внутрикожного» депо с нарушением функции капилляров.
Большое значение в нарушении микроциркуляции и перфузии органов и тканей имеют изменения свертываемости крови, фибринолитической активности и функционального состояния пластинок. Эти факторы изучили наши сотрудники Ю. Б. Белоусов и В. А. Люсов. Особенно большое значение эти изменения имеют у больных инфарктом миокарда с шоком.
Была установлена определенная динамика в развитии этих нарушений в течение шока. В раннюю фазу шока при инфаркте миокарда имеется гиперкоагуляция, что видно по достоверному укорочению отрезков г и К тромбоэластограммы. Увеличена толерантность крови к гепарину, содержание фибриногена в плазме крови. Фибринолитическая активность понижается. Количество пластинок, адгезивность и агрегация их увеличиваются.
В поздней фазе шока наблюдаются явления гипокоагуляции. Отрезок г тромбоэластограммы достоверно увеличивается, активность факторов II, V, VII и протромбинового комплекса Quick уменьшается. Количество фибриногена также значительно достоверно уменьшается. Фибринолитическая активность повышается. Количество тромбоцитов, адгезивность и агрегация их: уменьшается также статистически достоверно.
Описанные фазовые изменения свертываемости крови и •функционального состояния пластинок имеют решающее значение для исхода шока. Гиперкоагуляция, увеличение адгезивности и агрегации пластинок в ранней фазе шока, развивающиеся на фоне нарушений микроциркуляции и реологических •свойств крови, способствуют возникновению диссеминированной внутрисосудистой коагуляции, описанной при других видах шока (геморрагическом, травматическом и др.). Диссеминированная внутрисосудистая коагуляция, в свою очередь, ведет к уменьшению содержания в крови фибриногена, активности плазменных факторов свертывания, уменьшению числа пластинок, их адгезивности и агрегации. Этот процесс может рассматриваться как коагулопатия потребления. Наступление диссеминированной внутрисосудистой коагуляции указыавает на необратимую фазу шока, так как сопровождается тяжелыми нарушениями перфузии органов и тканей, развитием аноксии, ацидоза, расстройством метаболизма, возникновением микронекрозов во внутренних органах.
Таким образом, шок при инфаркте миокарда возникает в связи с нарушениями сократительности сердца и падением сердечного выброса. Однако исход его зависит от процессов, развивающихся на периферии (нарушение микроциркуляции, реологии крови, возникновение диссеминированной внутрисосудистой коагуляции и коагулопатии потребления). В связи с этим в новом свете может представиться вопрос о применении антикоагулянтов и фибринолитических средств для профилактики и лечения кардиогенного шока.
Запись на прием к нейрохирургу
Уважаемые пациенты, Мы предоставляем возможность записаться напрямую на прием к доктору, к которому вы хотите попасть на консультацию. Позвоните по номеру ,указанному вверху сайта, вы получите ответы на все вопросы. Предварительно, рекомендуем Вам изучить раздел О Нас.
Как записаться на консультацию врача?
1) Позвонить по номеру 8-863-322-03-16.
1.1) Или воспользуйтесь звонком с сайта:
1.2) Или воспользуйтесь контактной формой:
2) Вам ответит дежурный врач.
3) Расскажите о том, что вас беспокоит. Будьте готовы, что доктор попросит Вас рассказать максимально подробно о своих жалобах с целью определения специалиста, требующегося для консультации. Под руками держите все имеющиеся анализы, особенно, недавно сделанные!
4) Вас свяжут с вашим будущим лечащим доктором (профессором, доктором, кандидатом медицинских наук). Далее, непосредственно с ним вы будете обговаривать место и дату консультации – с тем человеком, кто и будет Вас лечить.

Источник
Как ведет себя артериальное давление по отношению к инфаркту миокарда?
 Стабильность артериального давления поддерживается комплексом сложных регуляторных систем (гемодинамических и системы контроля).
Стабильность артериального давления поддерживается комплексом сложных регуляторных систем (гемодинамических и системы контроля).
Гемодинамические системы:
- СВ –сердечный выброс (объем крови, выталкиваемой в системный кровоток за 1 минуту);
- ПО – общее периферическое сопротивление артериальных сосудов;
Эти две величины взаимозависимы. Если в определенных условиях (ОИМ) сердечный выброс уменьшается, то периферическое сопротивление соответственно увеличивается для поддержания достаточного гемодинамического давления.
Система контроля:
- Система кратковременного действия:
- Барорецепторы и хеморецепторы дуги аорты и синокаротидных зон. Реагируют на резкое изменение АД импульсами в продолговатый мозг и ретикулярную формацию. Эфферентные сигналы регулируют просвет артериол, частоту и силу сердцебиения, емкость вен;
- Ренин-ангиотензин II-артериолы — в случае острой гипотензии увеличивается секреция ренина клетками юкстагломерулярного аппарата;
- Система длительного действия:
- Конечный эффект ангиотензина II;
- Альдостерон.
Острый инфаркт миокарда – заболевание в основе которого лежит ишемический некроз участка сердечной мышцы вследствие остро возникшей окклюзии сегмента коронарной артерии. В подавляющем большинстве случаев ОИМ развивается на фоне прогрессирования хронической сердечно-сосудистой патологии (атеросклероз, гипертоническая болезнь).
 Показатели артериального давления в динамике развития ОИМ зависят от:
Показатели артериального давления в динамике развития ОИМ зависят от:
- Величины АД до начала ОИМ;
- Площади некроза миокарда;
- Локализации некротического очага;
- Наличия осложнений ОИМ.
Перед эпизодом
Ангинозная симптоматика при ОИМ развивается через 30-40 минут после окклюзии участка сосуда. Поэтому первыми симптомами надвигающегося инфаркта могут быть изменения АД.
Вследствие «выключения» из работы большого участка миокарда понижается сердечный выброс, что сопровождается падением АД еще до развития болевого синдрома.
При развитии атипичной формы ОИМ (коллаптоидной, безболевой) бывает так, что гипотония является основным проявлением дисфункции миокарда.
В некоторых случаях инфаркт миокарда может развиваться как осложнение гипертонического криза, когда на фоне высокого АД (180-220/120-160 мм.рт.ст) присоединяются кинжальные боли в грудной клетке и характерные изменения на ЭКГ.
Во время коронарного синдрома
Начало болевого приступа может сопровождаться транзиторным повышением АД вследствие активации симпатоадреналовой системы, выброса в кровоток катехоламинов и прочих вазоконстрикторов (ренина, ангиотензина, альдостерона), которые вызывают системный спазм артериол и повышение общего периферического сопротивления. Транзиторная гипертония и тахикардия чаще встречается у мужчин. Данная реакция носит кратковременный характер и к концу первых суток давление снижается.
 Работа миокарда крайне зависима от кислорода (критическая ишемия провоцирует утрату сократительной функции уже через 1 минуту. В случае обширного трансмурального инфаркта миокарда (некроз 20-25% мышечной массы ЛЖ) прекращение функционирования может вызвать развитие острой сердечной недостаточности еще до гибели кардиомиоцитов. Вследствие некроза более 35% миокарда ЛЖ сердечный выброс становится экстремально низок, что проявляется развитием кардиогенного шока, отека легких, гемодинамического инсульта.
Работа миокарда крайне зависима от кислорода (критическая ишемия провоцирует утрату сократительной функции уже через 1 минуту. В случае обширного трансмурального инфаркта миокарда (некроз 20-25% мышечной массы ЛЖ) прекращение функционирования может вызвать развитие острой сердечной недостаточности еще до гибели кардиомиоцитов. Вследствие некроза более 35% миокарда ЛЖ сердечный выброс становится экстремально низок, что проявляется развитием кардиогенного шока, отека легких, гемодинамического инсульта.
Также падение АД наблюдается при нарушении ритма и проводимости (желудочковая аритмия, экстрасистолия, АВ блокада). Причиной служит неэффективные сокращения миокарда с снижение сердечного выброса.
В случае неосложненного течения ОИМ артериальное давление остается стабильно пониженным в остром периоде и постепенно повышается к концу стадии рубцевания, но доинфарктного уровня не достигает.
Проведение ПКВ (стентирования и баллонной ангиопластики) делает возможным достижение исходных гемодинамических показателей. Установленный стент возобновляет кровоток в коронарной артерии и ограничивает зону повреждения сердечной мышцы.
После инфаркта
Через 3 недели после ОИМ происходит формирование на месте некроза соединительнотканного рубца с компенсаторной перифокальной гипертрофией – т.н. ремоделирование миокарда. Неповрежденные участки берут на себя функцию некротизированного очага. Целью этого процесса является обеспечение достаточного уровня артериального давления.
В случае мелкоочагового ОИМ (субэндокардиального, субэпикардиального) ремоделированный миокард полностью восстанавливает доинфарктный уровень сердечного выброса и АД возвращается к прежним показателям. У пациентов страдающих гипертонической болезнью это чревато ускорением прогрессирования ИБС и увеличением риска развития повторного ОИМ. Для таких пациентов устанавливается уровень целевого систолического АД меньше 140 мм.рт.ст, диастолического – ниже 100 мм.рт.ст. Это достигается длительным приемом гипотензивных препаратов:
- Блокаторы бета рецепторов – Бисоролол, Небиволол, Пропранолол, Карведилол;
- иАПФ – Эналаприл, Лизиноприл, Периндоприл;
- Блокаторы рецепторов ангиотензина-II – Валсартан, Лозартан, Ирбесартан;
- Диуретики – при наличии сердечной недостаточности (Гидрохлортиазид, Фуросемид, Индапамид, Спиронолактон).
После перенесенного трансмурального ОИМ, особенно с поражением левого желудочка, жизнеспособный миокард не может поддерживать должную ФВ и достичь исходного АД. У таких пациентов сохраняется низкое давление после инфаркта, наблюдается хроническая тканевая гипоксия, формируется недостаточность кровообращения. В первую очередь страдают почки, головной мозг, собственно миокард и периферические ткани.
Как поднять давление?
 В остром периоде развития ОИМ гипотензию корригируют внутривенным введением инотропных средств:
В остром периоде развития ОИМ гипотензию корригируют внутривенным введением инотропных средств:
- Допамина – начальная доза 2-5 мкг/кг/мин с постепенным титрованием до 10 мкг/кг/мин;
- Добутамина – 2,5-10 мкг/кг/мин.
Для поддержания АД в домашних условиях показана длительная терапия сердечными гликозидами (Дигоксин, Дигитоксин), особенно в случае комбинации гипотонии с фибрилляцией предсердий. Дигоксин назначается в дозе 0,125-0,5 мг/сутки за 1-2 приема.
Также помощь в поддержании нормального АД оказывает модификация образа жизни, диета, режим сна, дозированные физические нагрузки, фитотерапия (препараты шиповника, экстракт элеутерококка, настойка женьшеня).
Выводы
Важно помнить, что у женщин признаки ОИМ часто выражены менее ярко в отличии от мужчин. Показатели ЧСС и артериального давления при инфаркте миокарда у них изменяются незначительно, а преобладают явления сердечной недостаточности. Поддержание целевого АД после перенесенного эпизода уменьшает риск развития отдаленных осложнений, повторных катастроф, увеличивает качество и продолжительность жизни пациента. Использование препаратов для повышения давления без консультации лечащего врача чреват прогрессированием сердечной недостаточности.
Источник
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
Общие сведения
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза. После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда.
Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности. Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. е. формирование постинфарктного рубца.
В клиническом течении инфаркта миокарда выделяют пять периодов:
- 1 период – предынфарктный (продромальный): учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель;
- 2 период – острейший: от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов;
- 3 период – острый: от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток;
- 4 период – подострый: начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4-8 недель;
- 5 период – постинфарктный: созревание рубца, адаптация миокарда к новым условиям функционирования.
Инфаркт миокарда
Причины инфаркта миокарда
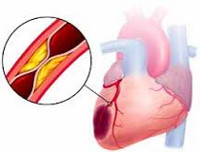
Инфаркт миокарда является острой формой ИБС. В 97—98% случаев основой для развития инфаркта миокарда служит атеросклеротическое поражение венечных артерий, вызывающее сужение их просвета. Нередко к атеросклерозу артерий присоединяется острый тромбоз пораженного участка сосуда, вызывающий полное или частичное прекращение кровоснабжения соответствующей области сердечной мышцы. Тромбообразованию способствует повышенная вязкость крови, наблюдаемая у пациентов с ИБС. В ряде случаев инфаркт миокарда возникает на фоне спазма ветвей венечных артерий.
Развитию инфаркта миокарда способствуют сахарный диабет, гипертоничесая болезнь, ожирение, нервно-психическое напряжение, увлечение алкоголем, курение. Резкое физическое или эмоциональное напряжение на фоне ИБС и стенокардии может спровоцировать развитие инфаркта миокарда. Чаще развивается инфаркт миокарда левого желудочка.
Классификация инфаркта миокарда
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда:
- крупноочаговый
- мелкоочаговый
На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов). В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией.
В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда:
- трансмуральный – с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый)
- интрамуральный – с некрозом в толще миокарда
- субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду
- субэпикардиальный – с некрозом миокарда в зоне прилегания к эпикарду
По изменениям, фиксируемым на ЭКГ, различают:
- «Q-инфаркт» – с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда)
- «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда)
По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на:
- правожелудочковый
- левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки
По кратности возникновения различают инфаркт миокарда:
- первичный
- рецидивирующий (развивается в срок 8 недель после первичного)
- повторный (развивается спустя 8 недель после предыдущего)
По развитию осложнений инфаркт миокарда подразделяется на:
- осложненный
- неосложненный
По наличию и локализации болевого синдрома выделяют формы инфаркта миокарда:
- типичную – с локализацией боли за грудиной или в прекардиальной области
- атипичные – с атипичными болевыми проявлениями:
- периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная)
- безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная
- малосимптомную (стертую)
- комбинированную
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
- стадию ишемии (острейший период)
- стадию некроза (острый период)
- стадию организации (подострый период)
- стадию рубцевания (постинфарктный период)
Симптомы инфаркта миокарда
Предынфарктный (продромальный) период
Около 43% пациентов отмечают внезапное развитие инфаркта миокарда, у большей же части больных наблюдается различный по продолжительности период нестабильной прогрессирующей стенокардии.
Острейший период
Типичные случаи инфаркта миокарда характеризуются чрезвычайно интенсивным болевым синдромом с локализацией болей в грудной клетке и иррадиацией в левое плечо, шею, зубы, ухо, ключицу, нижнюю челюсть, межлопаточную зону. Характер болей может быть сжимающим, распирающим, жгучим, давящим, острым («кинжальным»). Чем больше зона поражения миокарда, тем более выражена боль.
Болевой приступ протекает волнообразно (то усиливаясь, то ослабевая), продолжается от 30 минут до нескольких часов, а иногда и суток, не купируется повторным приемом нитроглицерина. Боль сопряжена с резкой слабостью, возбуждением, чувством страха, одышкой.
Возможно атипичное течение острейшего периода инфаркта миокарда.
У пациентов отмечается резкая бледность кожных покровов, липкий холодный пот, акроцианоз, беспокойство. Артериальное давление в период приступа повышено, затем умеренно или резко снижается по сравнению с исходным (систолическое < 80 рт. ст., пульсовое < 30 мм мм рт. ст.), отмечается тахикардия, аритмия.
В этот период может развиться острая левожелудочковая недостаточность (сердечная астма, отек легких).
Острый период
В остром периоде инфаркта миокарда болевой синдром, как правило, исчезает. Сохранение болей бывает вызвано выраженной степенью ишемии околоинфарктной зоны или присоединением перикардита.
В результате процессов некроза, миомаляции и перифокального воспаления развивается лихорадка (от 3-5 до 10 и более дней). Длительность и высота подъема температуры при лихорадке зависят от площади некроза. Артериальная гипотензия и признаки сердечной недостаточности сохраняются и нарастают.
Подострый период
Болевые ощущения отсутствуют, состояние пациента улучшается, нормализуется температура тела. Симптомы острой сердечной недостаточности становятся менее выраженными. Исчезает тахикардия, систолический шум.
Постинфарктный период
В постинфарктном периоде клинические проявления отсутствуют, лабораторные и физикальные данные практически без отклонений.
Атипичные формы инфаркта миокарда
Иногда встречается атипичное течение инфаркта миокарда с локализацией болей в нетипичных местах (в области горла, пальцах левой руки, в зоне левой лопатки или шейно-грудного отдела позвоночника, в эпигастрии, в нижней челюсти) или безболевые формы, ведущими симптомами которых могут быть кашель и тяжелое удушье, коллапс, отеки, аритмии, головокружение и помрачение сознания.
Атипичные формы инфаркта миокарда чаще встречаются у пожилых пациентов с выраженными признаками кардиосклероза, недостаточностью кровообращения, на фоне повторного инфаркта миокарда.
Однако атипично протекает обычно только острейший период, дальнейшее развитие инфаркта миокарда становится типичным.
Стертое течение инфаркта миокарда бывает безболевым и случайно обнаруживается на ЭКГ.
Осложнения
Нередко осложнения возникают уже в первые часы и дни инфаркта миокарда, утяжеляя его течение. У большинства пациентов в первые трое суток наблюдаются различные виды аритмий: экстрасистолия, синусовая или пароксизмальная тахикардия, мерцательная аритмия, полная внутрижелудочковая блокада. Наиболее опасно мерцание желудочков, которое может перейти в фибрилляцию и привести к гибели пациента.
Левожелудочковая сердечная недостаточность характеризуется застойными хрипами, явлениями сердечной астмы, отека легких и нередко развивается в острейший период инфаркта миокарда. Крайне тяжелой степенью левожелудочковой недостаточности является кардиогенный шок, развивающийся при обширном инфаркте и обычно приводящий к летальному исходу. Признаками кардиогенного шока служит падение систолического АД ниже 80 мм рт. ст., нарушение сознания, тахикардия, цианоз, уменьшение диуреза.
Разрыв мышечных волокон в зоне некроза может вызывать тампонаду сердца – кровоизлияние в полость перикарда. У 2-3% пациентов инфаркт миокарда осложняется тромбоэмболиями системы легочной артерии (могут стать причиной инфаркта легких или внезапной смерти) или большого круга кровообращения.
Пациенты с обширным трансмуральным инфарктом миокарда в первые 10 суток могут погибнуть от разрыва желудочка вследствие острого прекращения кровообращения. При обширном инфаркте миокарда может возникать несостоятельность рубцовой ткани, ее выбухание с развитием острой аневризмы сердца. Острая аневризма может трансформироваться в хроническую, приводящую к сердечной недостаточности.
Отложение фибрина на стенках эндокарда приводит к развитию пристеночного тромбоэндокардита, опасного возможностью эмболии сосудов легких, мозга, почек оторвавшимися тромботическими массами. В более позднем периоде может развиться постинфарктный синдром, проявляющийся перикардитом, плевритом, артралгиями, эозинофилией.
Диагностика инфаркта миокарда
Среди диагностических критериев инфаркта миокарда важнейшими являются анамнез заболевания, характерные изменения на ЭКГ, показатели активности ферментов сыворотки крови. Жалобы пациента при инфаркте миокарда зависят от формы (типичной или атипичной) заболевания и обширности поражение сердечной мышца. Инфаркт миокарда следует заподозрить при тяжелом и продолжительном (дольше 30-60 минут) приступе загрудинных болей, нарушении проводимости и ритма сердца, острой сердечной недостаточности.
К характерным изменениям ЭКГ относятся формирование отрицательного зубца Т (при мелкоочаговом субэндокардиальном или интрамуральном инфаркте миокарда), патологического комплекса QRS или зубца Q (при крупноочаговом трансмуральном инфаркте миокарда). При ЭхоКГ выявляется нарушение локально сократимости желудочка, истончение его стенки.
В первые 4-6 часов после болевого приступа в крови определяется повышение миоглобина – белка, осуществляющего транспорт кислорода внутрь клеток.Повышение активности креатинфосфокиназы (КФК) в крови более чем на 50% наблюдается спустя 8—10 ч от развития инфаркта миокарда и снижается до нормы через двое суток. Определение уровня КФК проводят через каждые 6-8 часов. Инфаркт миокарда исключается при трех отрицательных результатах.
Для диагностики инфаркта миокарда на более поздних сроках прибегают к определению фермента лактатдегидрогеназы (ЛДГ), активность которой повышается позже КФК – спустя 1-2 суток после формирования некроза и приходит к нормальным значениям через 7-14 дней. Высокоспецифичным для инфаркта миокарда является повышение изоформ миокардиального сократительного белка тропонина – тропонина-Т и тропонина-1, увеличивающихся также при нестабильной стенокардии. В крови определяется увеличение СОЭ, лейкоцитов, активности аспартатаминотрансферазы (АсАт) и аланинаминотрансферазы (АлАт).
Коронарная ангиография (коронарография) позволяет установить тромботическую окклюзию коронарной артерии и снижение желудочковой сократимости, а также оценить возможности проведения аортокоронарного шунтирования или ангиопластики – операций, способствующих восстановлению кровотока в сердце.
Лечение инфаркта миокарда
При инфаркте миокарда показана экстренная госпитализация в кардиологическую реанимацию. В остром периоде пациенту предписывается постельный режим и психический покой, дробное, ограниченное по объему и калорийности питание. В подостром периоде больной переводится из реанимации в отделение кардиологии, где продолжается лечение инфаркта миокарда и осуществляется постепенное расширение режима.
Купирование болевого синдрома проводится сочетанием наркотических анальгетиков (фентанила) с нейролептиками (дроперидолом), внутривенным введением нитроглицерина.
Терапия при инфаркте миокарда направлена на предупреждение и устранение аритмий, сердечной недостаточности, кардиогенного шока. Назначают антиаритмические средства (лидокаин), ß-адреноблокаторы (атенолол), тромболитики (гепарин, ацетилсалициловая к-та), антогонисты Са (верапамил), магнезию, нитраты, спазмолитики и т. д.
В первые 24 часа после развития инфаркта миокарда можно произвести восстановление перфузии путем тромболизиса или экстренной баллонной коронарной ангиопластики.
Прогноз при инфаркте миокарда
Инфаркт миокарда является тяжелым, сопряженным с опасными осложнениями заболеванием. Большая часть летальных исходов развивается в первые сутки после инфаркта миокарда. Насосная способность сердца связана с локализацией и объемом зоны инфаркта. При повреждении более 50% миокарда, как правило, сердце функционировать не может, что вызывает кардиогенный шок и гибель пациента. Даже при менее обширном повреждении сердце не всегда справляется нагрузками, в результате чего развивается сердечная нед
