Нарушение проводимости сердца при инфаркте
Нарушения ритма и проводимости при инфаркте миокарда. Желудочковая экстрасистолия при инфаркте миокарда.
Аритмии – самое частое осложнение инфаркта миокарда (встречаются в 90-95% случаев) и самая частая причина смерти на догоспитальном этапе. Половина смертных исходов при инфаркте миокарда происходит в первые 2 часа, и 50% из них абсолютно внезапны.
Синусовая тахикардия – имеется синусовый ритм, но частота сердечных сокращений не превышает 100 в мин. У больных ИМ это обычная рефлекторная реакция на сердечную недостаточность и гипотензию. И хотя сама по себе синусовая тахикардия не представляет опасности, прогноз может быть относительно неблагоприятным.
Синусовая брадикардия – имеется синусовый ритм с частотой сердечных сокращений меньше 60. Часто осложняет течение инфаркта миокарда диафрагмальной области стенки сердца.
Эта форма брадикардии может стать причиной сердечной недостаточности, гипотензии, а также очагов эктопического возбуждения в миокарде желудочков.

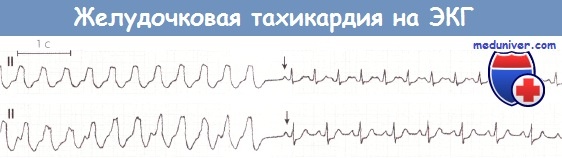
Желудочковая тахикардия после инфаркта миокарда (ИМ) передней локализации.
Начальная часть ЭКГ указывает на желудочковую тахикардию (частота сокращений желудочков 140 в минуту), которая после внутривенного введения аймалина (указано стрелкой вниз) внезапно перешла в синусовый ритм.
На нижней ЭКГ 2-й, 5-й, 8-й и 11-й комплексы сливные.
Желудочковая экстрасистолия при инфаркте миокарда
В настоящее время установлено, что сами по себе экстрасистолы безопасны (их даже называют «косметическими аритмиями»), не являются предвестниками фибрилляции желудочков. Поэтому лечение назначают только при очень частой, обычно групповой экстрасистолии, если они вызывают нарушения гемодинамики, или субъективно очень плохо переносятся. Эпизоды неустойчивой желудочковой тахикардии продолжительностью менее 30 сек, протекающие без нарушения гемодинамики, также требуют только наблюдения.
Устойчивая желудочковая тахикардия:
Без нарушения гемодинамики –
• назначение антиаритмических препаратов – кордарон, лидо-каин новокаинамид;
• кордарон – от 300 до 450 мг в/в, примерно за 20-30 мин. или 75-150 мг в течение 10-15 мин., затем 1мг/мин. в течение 6 часов, затем 0,5 мг/мин.;
• лидокаин – 1-1,5 мг/кг струйно, затем 20-50 мкг/кг/мин.;
• новокаинамид – 15 мг/кг в течение 20-30 мин., затем 1-4 мг/мин.
С нарушением гемодинамики
• Экстренная дефибрилляция несинхронизированным разрядом энергией 200-300 Дж, затем при неэффективности первого разряда – 300-360 Дж.
• Если три разряда неэффективны, вводят адреналин, 1 мг в/в или 10 мл раствора 1:10000 внутрисердечно, или амиодарон, 75150 мг в/в струйно, и повторяют дефибрилляцию (после введения каждого препарата – разряд).
Фибрилляция желудочков при инфаркте миокарда
Факторы риска – гипокалиемия (4,5 ммоль/л) и гипомагниемия (2 ммоль/л).
Первичная фибрилляция (не связанная с недостаточностью кровообращения) происходит в первые 4 часа в 60% случаев, 80% – в первые 12 часов. Эти данные служат предикторами для практикующего врача для готовности оказания помощи. Вторичная фибрилляция (после первых суток) в большинстве случаев возникает у больных с выраженным поражением миокарда, признаками сердечной недостаточности, нарушениями внутрижелудочковой проводимости. Единственным эффективным методом лечения фибрилляции желудочков является немедленное проведение электрической дефибрилляции.
В остром периоде инфаркта миокарда часто наблюдается фибрилляция (мерцание) предсердий – до 10-15%. Все остальные варианты наджелудочковых аритмий встречаются редко. Лечение стандартное.
Важное изменение в тактике лечения больных неосложненным инфарктом миокарда, происшедшее в последние годы, – отказ от профилактического применения лидокаина. Показано, что хотя в группе получавших препарат количество случаев первичной фибрилляции желудочков уменьшается, число смертельных исходов от всех причин имеет тенденцию к увеличению.
– Также рекомендуем “Нарушение проводимости при инфаркте миокарда. Тромбоэмболии при инфаркте миокарда. Синдром Дресслера.”
Оглавление темы “Неотложная помощь в при инфаркте миокарда.”:
1. Купирование ангинозного приступа. Неотложная помощь при болях в сердце.
2. Инфаркт миокарда. Пути развития инфаркта миокарда.
3. Клинические варианты инфаркта миокарда. Клиника инфаркта миокарда.
4. Церебральный вариант инфаркта миокарда. Безболевой вариант инфаркта миокарда. Аритмический, отечный вариант инфаркта миокарда.
5. Диагностика инфаркта миокарда. Резорбционно-некротический синдром инфаркта миокарда.
6. Осложнения инфаркта миокарда в остром периоде. Отек легких при инфаркте миокарда.
7. Кардиогенный шок. Гиповолемия при инфаркте миокарда.
8. Нарушения ритма и проводимости при инфаркте миокарда. Желудочковая экстрасистолия при инфаркте миокарда.
9. Нарушение проводимости при инфаркте миокарда. Тромбоэмболии при инфаркте миокарда. Синдром Дресслера.
10. Лечение инфаркта миокарда. Лечение болей при инфаркте миокарда.
Источник
Кардиогенный шок
является одним из самых тяжелых ранних осложнений острого инфаркта миокарда.
Патогенез
В патогенезе кардиогенного шока выделяют несколько звеньев: снижение насосной функции миокарда, снижение сосудистого тонуса, а при наличии аритмии (особенно при желудочковой пароксизмальной тахикардии) — дополнительное снижение сердечного выброса.
Тяжесть кардиогенного шока коррелирует с площадью очага некроза при инфаркте, т. е. зависит от уменьшения массы функционирующего миокарда левого желудочка. У больных повторным инфарктом миокарда на фоне уже имеющихся постинфарктных рубцов кардиогенный шок может возникать и при мелкоочаговой форме инфаркта.
В результате перечисленных патогенетических изменений возникают тяжелые нарушения микроциркуляции органов и тканей с формированием эритроцитарного стаза, повышением проницаемости стенок капилляров и развитием метаболического ацидоза.
В развитии кардиогенного шока имеет значение и исходное состояние больного, так как у лиц, страдающих гипертонической болезнью, кардиогенный шок может развиться при умеренном снижении артериального давления (до 130/80 мм рт. ст.).
1) его длительности;
2) реакции на прессорные амины;
3) выраженности олигурии;
4) степени выраженности ацидоза;
5) показателей артериального и пульсового давления. Наиболее тяжело протекает так называемый ареактивный шок, устойчивый к противошоковой терапии.
Клиника
Кадиогенный шок проявляется резким снижением артериального (особенно пульсового) давления, что сопровождается симптомами шока: бледностью, иногда цианозом кожи, холодным, липким потом. При этом черты лица заострены, пульс нитевидный, систолическое артериальное давление ниже 70 мм рт. ст., отмечаются нарушение сознания в различной степени, олигурия вплоть до анурии.
Сердечная астма. Отек легких
Развитие этих осложнений связано со слабостью сократительной функции миокарда левого желудочка при массивном некротическом поражении миокарда и резком повышении диастолического давления в левом желудочке. Левожелудочковая недостаточность возникает во время болевого приступа или сразу после его окончания.
Патогенез
В патогенезе левожелудочковой недостаточности имеют значение не только снижение насосной функции сердца, но и рефлекторный спазм легочных сосудов (рефлекс Катаева), повышение проницаемости капиллярной стенки в результате гипоксии и активизации симпатоадреналовой системы. В результате резко повышается давление в легочных венах и капиллярах, происходит выход жидкой части крови из их просвета вначале в ткань легких (интерстициальный отек), а затем в альвеолы (альвеолярный отек).
Клиника
Сердечная астма клинически проявляется в виде приступа удушья, который сопровождается бледностью кожных покровов, акроцианозом и появлением холодного пота.
Больной возбужден, чувствует страх смерти, принимает вынужденное положение-ортопноэ.
Аускультативно в легких (вначале только в нижних отделах, а затем над всей поверхностью) определяются влажные хрипы, нередко сочетающиеся с сухими свистящими хрипами, вызванными сопутствующим бронхоспазмом. При прогрессировании отека влажные хрипы усиливаются, дыхание становится клокочущим, появляется пенистая мокрота, часто с примесью крови.
Рентгенологически определяется картина «застойного легкого» с облаковидным прикорневым сгущением легочного рисунка, постепенно просветляющимся к периферии.
Клиника
Замирание сердца если выпадает один импульс. Головокружение, если выпадает несколько импульсов. Синдром Морганьи-Эдамса-Стокса (потеря сознания) — если выпадает 6-8 комплексов. На ЭКГ отсутствует весь сердечный комплекс, нет Р, Т, QRS, вместо них видна длительная пауза, которая бывает кратной какому-либо числу промежутков R-R.
Часто видны выскальзывающие, замещающие комплексы (во время длительной паузы на помощь выскакивает собственный импульс из атриовентрикулярного узла), при этом нет зубца Р. Аускультативно в это время может быть слышен громкий тон — сильное сокращение сердца. Этиология чаще всего функциональная, почти в половине случаев — органические изменения сердца, особенно часто ИБС. Врачебная тактика зависит от точного диагноза.
а) холинолитики (экстракт белладонны, платифиллин 0,05)
б) симпатолитики, но их назначать мало, с огромной осторожностью, так как они могут спровоцировать приступ грудной жабы (изадрин 0,05 под язык, для ингаляции 1% 25 мл).
2. Противоаритмическая терапия. Назначают очень мягкие средства — делагил 0,25 на ночь.
3. Антагонисты кальция — изоптин 0,04
При частой потере сознания больного переводят на постоянную электроимпульсную терапию, но чаще кардиостимуляцию приходится проводить «по требованию».
Синонимы — дисфункция синусового узла, Аррест-2-синус. Эта патология очень близка к синоаурикулярной блокаде6 но отличается тем6 что страдают Р клетки, вырабатывающие импульсы, а не Т клетки. В этом случае часто брадикардия, которая неуклонно возрастает и не поддается ваголитикам (атропину и его аналогам).
Затем6 по мере возрастания слабости синусового узла приходят в возбуждение гетеротопные очаги в предсердиях — возникают пароксизмальные нарушения ритма (пароксизмальная тахикардия, мерцание и трепетание предсердий). По выходе из тахикардии период асистолии в течение нескольких секунд, а затем снова возникает синусовая брадикардия.
Это патологияческое состояние связано с органическим поражением синусового узла (его Р клеток), оно изматывает больного, длительно затянувшееся может привести к смерти. Синдром Аррест-2-синус является показанием к постоянной электростимуляции, хирургическому вмешательству для размещения кардиостимулятора.
Часто связана с органическимм поражениями, нередко предвестник мерцательной аритмии. Может быть при резкой дилатации предсердий.
Этиология
Пороки сердца, ИБС, передозировка антиаритмических средств.
Клинических проявлений практически не дает. Единственный метод диагностики — по ЭКГ. Наблюдается уширение и расщепление зубца Р (в норме не более 0,10 секунды). Нередко зубец Р становится двуфазным — отрицательным и положительным. Может быть и более глубокое поражение — поражение пучка Бохмана — синдром парасистолии предсердий (правое предсердие работает в ритме синусового узла, а левое от собственных импульсов гетеротоных очагов возбуждения). Это приводитк к тяжелым нарушениям гемодинамики. Встречается редко.
1. Собственно атриовентрикулярный узел;
2. Пучок Гисса;
3. Ножки пучка Гисса.
1 степень. Замедление предсердно-желудочковой проводимости. До желудочков доходят все импульсы, но скорость их проведения понижена. Субъективных ощущений нет. диагностика только по ЭКГ: ритм правильный, но интервал PQ увеличен (в норме не более 0,20 секунд). Длительность интервала самая разная.
Этиология
а) Нередко функциональные нарушения(ваготония спортсменов).
б) Органические. Воспалительные процессы в миокарде, рубцовые измениния атриовентрикулярого узла.
в) Электролитные изменения.
Наиболее часто встречаются первая и вторая причины. При ваготонии спортсменов трудна дифференцировка, необходимо провести пробу с атропином. При ваготонии после его применения на ЭКГ исчезают характерные изменения.
1. Мобитц I. Периоды Венкенбаха-Самойлова. По мере проведения импульсов постепенно удлиняется интервал PQ, вплоть до полного выпадения пульсовой волны. Обычно при этом типе повреждение сравнительно высокое, поэтому QRS не изменен. Прогностически данный тип сравнительно благоприятен.
2. Мобитц II — с постоянным интервалом PQ, при этом не все импульсы доходят до желудочков — в одних случаях проводится каждый второй импульс, в других — каждый третий и т.д. Чем ниже импульсная проводимость, тем тяжелее тяжелее клиника. При этой патологии происходит низкое поражение — поэтому меняется комплекс QRS.
1. Прогрессирующая сердечная недостаточность, особенно при физической нагруузке, связанная с малой частотой сердечных сокращений.
2. Синдром Морганьи-Эдамса-Стокса. Часто возникает при переходе неполной блокады в полную при прогрессировании нарушений атриовентрикулярного проведения. При этом собственный автматизм еще не успел выработаться, кровь не поступает на периферию, чувствительный головной мозг отвечает потерей сознания.
Внезапная бледность, потеря сознания, пульс не определяется, тоны сердца не слышны. Затем больной синеет, появляются судороги. Может быть непроизвольное мочеиспускание и дефекация. Возможна смерть через 3-4 минуты, но часто приступ заканчивается на 1-2 минуте — включается идиовентрикулярный водитель ритма желудочков.
А. Постоянная форма.
Б. Эпизодическая (интермиттирующая). Чаще всего дает синдром Морганьи-Эдамса-Стокса. Прогностически является самой неблагоприятной формой. При этом блокада то полная, то неполная.
Нарушения ритма и проводимости
Нарушения ритма и проводимости возникают у подавляющего большинства больных инфарктом миокарда.
В связи с образованием очага некроза снижается порог возбудимости миокарда, возникают очаги патологической импульсации, создаются условия для механизма «re-entry», замедляется внутрисердечная проводимость. Нарушения ритма и проводимости при инфаркте миокарда часто носят транзиторный характер. Возникновение аритмии значительно изменяет гемодинамику.
Нарушения ритма, сопровождающиеся тахикардией со значительным снижением ударного и минутного выброса (тахисистолическая форма мерцательной аритмии, пароксизмальная желудочковая тахикардия), являются прогностически неблагоприятными. Они могут вызвать в дальнейшем развитие аритмогенного шока или острой сердечной недостаточности.
Некоторые аритмии могут предшествовать или провоцировать другие более тяжелые и прогностически неблагоприятные нарушения ритма. Полная атриовентрикулярная блокада может сопровождаться приступами Морганьи-Адамса-Стокса в виде кратковременной потери сознания с судорогами и вызывать развитие сердечной недостаточности.
Психические нарушения могут возникнуть на любой стадии заболевания. Они связаны с гипоксией, тромбозом или тромбоэмболией мелких сосудов мозга, чаще возникают у людей пожилого возраста.
В первые дни заболевания чаще регистрируется депрессивный или тревожно-депрессивный синдром, чередующийся с периодами эйфории.
Могут возникать кратковременные психотические состояния и даже делирий.
Истинные реактивные состояния возникают в течение первых 2 недель. В более поздние сроки могут сформироваться астенический синдром, ипохондрия.
При отсутствии адекватного лечения этих расстройств у больного могут на длительное время остаться астенизация, нарушение сна, тяжелые невротические реакции и фобии.
Разрыв сердца
Разрыв сердца является редким осложнением инфаркта миокарда, но приводит к почти 100%-ной летальности. Чаще возникает на 5—6-й день от начала инфаркта, но может наступить и в первые дни заболевания. Разрыв миокарда клинически проявляется резкой болью, которая не купируется приемом анальгетиков. При разрыве стенки миокарда быстро развиваются картина кардиогенного шока и остановка сердца, вызванная тампонадой сердца.
При обширном разрыве смерть наступает мгновенно, при небольшом — в течение нескольких минут или даже часов.
При маленьком («прикрытом») разрыве может формироваться ложная аневризма, что продлевает жизнь больных на несколько месяцев.
Разрыв межжелудочковой перегородки проявляется аускультативно грубым систолическим шумом в области нижней трети грудины и быстрым развитием тотальной недостаточности кровообращения.
Постинфарктный синдром
Абдоминальный синдром развивается в остром периоде инфаркта миокарда и может протекать в различных клинических формах: образования острых эрозий и язв слизистой оболочки желудочно-кишечного тракта, развития пареза желудка, кишечника, атонии мочевого пузыря.
Образование язв и эрозий связано с гипоксией слизистой оболочки на фоне гемодинамических нарушений, тромбозом мелких сосудов, действием медикаментозных препаратов (аспирина).
Формирование язв сопровождается болями, неустойчивым стулом, иногда кровотечением (возникают рвота кофейной гущей, мелена).
Парез кишечника проявляет себя вздутием живота, распирающими болями, задержкой отхождения стула и газов и может быть следствием повторного введения морфина и атропина, как и атония мочевого пузыря.
Постинфарктный синдром (синдром Дресслера) развивается на 2—6-й неделе инфаркта миокарда.
Развитие постинфарктного синдрома связано с образованием в некротизированном участке миокарда тканевых аутоантигенов, на которые в организме вырабатываются аутоантитела.
Клиническая картина синдрома Дресслера включает триаду признаков: перикардит, плеврит и пневмонии (синдром трех «П»).
Компоненты триады могут отмечаться у больного в виде монопоражения или сочетаться.
Кроме того, при постинфарктном синдроме могут развиться синовит, периартрит, нефрит, васкулит.
Это осложнение сопровождается повышением температуры тела, ускорением СОЭ и лейкоцитозом с сдвигом формулы влево, а также эозинофилией.
Поражение серозных оболочек носит фибринозный, серозный или геморрагический характер и часто характеризуется упорным рецидивирующим течением. В лечении эффективны глюкокортикоиды.
Аневризма сердца
Это ограниченное выпячивание стенки миокарда, обычно левого желудочка. Чаще аневризма формируется в острый, реже в подострый период инфаркта миокарда. Ее образование связано с давлением, которое оказывает кровь на поврежденный участок сердечной мышцы.
Чаще аневризма формируется в области передней стенки миокарда, реже — верхушки, задней стенки или межжелудочковой перегородки.
При пальпации больного определяется прекардиальная пульсация в области III-IV ребер слева от грудины. Левая граница сердца смещается влево до среднеаксиллярной линии. Аускультативно определяются глухость сердечных тонов, систолический, реже диастолический шум.
На ЭКГ длительное время сохраняется типичная для острого периода инфаркта монофазная кривая. Диагноз подтверждается данными эхокардиографии.
Аневризма может быть источником тромбоэмболии, разрываться на ранних стадиях формирования. Нередко у больных аневризмой развиваются нарушения ритма и проводимости.
Тромбоэндокардит
Это асептическое воспаление, развивающееся в тромботических массах на поверхности эндокарда в зоне инфаркта
Чаще тромбоэндокардит осложняет течение крупноочаговых и трансмуральных инфарктов, особенно с формированием постинфарктной аневризмысердца.
Отмечаются субфебрильная температура тела, слабость, тахикардия, повышенная потливость. У некоторых больных тромбоэндокардит никак себя не проявляет.
При эхокардиографии и вентрикулографии определяется внутрисердечный тромб.
Постинфарктный синдром
При выраженном атеросклерозе коронарных артерий, тенденции к стенозированию или активному тромбообразованию больной может переносить несколько инфарктов миокарда. Если новый инфаркт возникает в период, когда формирование рубца еще не закончилось (в течение 2—2,5 месяцев после острого приступа), говорят о рецидивирующем инфаркте, если в более поздние сроки — о повторном инфаркте миокарда.
Рецидивирующий инфаркт обычно проявляется типичным болевым приступом, воспалительно-резорбтивным синдромом (наблюдаются субфебрилитет, лейкоцитоз, ускорение СОЭ, повышение активности в крови ферментов — маркеров) и характерными изменениями ЭКГ.
Рецидивирующий инфаркт миокарда часто сопровождается развитием сердечной недостаточности, нарушениями ритма и проводимости, кардиогенным шоком.
Повторный инфаркт миокарда чаще возникает у лиц пожилого возраста. При этом болевой синдром может быть выражен незначительно или отсутствовать.
Иногда повторный инфаркт протекает по типу приступа сердечной астмы или эпизода острой аритмии. После него нередко развивается недостаточность кровообращения.
Диагностика повторного инфаркта осложняется наличием на ЭКГ постинфарктных изменений от предыдущих инфарктов.
Летальность при повторном инфаркте значительно выше, чем при первичном.
Источник
