Маски острого инфаркта миокарда
Классическая картина инфаркта миокарда – внезапная сильная режущая или давящая боль за грудиной, которая распространяется на всю грудную клетку, в подложечную область и в спину, в обе руки, челюсть, шею. “Как будто плиту положили”, – говорят некоторые больные. Резкая слабость, бледность, обильный пот сопровождают приступ.
С чего начинается диагностика инфаркта? С телефонного звонка 03. Повод для вызова скорой – затянувшийся приступ давящей боли за грудиной, которая не снимается нитропрепаратами. Параллельно возникают слабость, потоотделение, страх и даже потеря сознания.
От того, насколько быстро будет госпитализирован больной, зависит его жизнь. У многих пациентов, госпитализированных в специализированные отделения в первые 2 часа после начала инфаркта, удается не допустить развития обширного процесса благодаря применению тромболитиков – препаратов, растворяющих тромбы.
Пока врачи не приехали, можно дать больному нитроглицерин под язык. Но желательно сначала измерить артериальное давление: этот препарат резко снижает его, и если АД и без того пониженное, может ухудшить состояние.
ПЯТЬ МАСОК – ОДИН ИНФАРКТ
Но иногда инфаркт маскируется под другие недуги.
Коварен гастралгический вариант. Боль в животе, вздутие – налицо картина “острого живота” плюс слабость, падение артериального давления, тахикардия. Если у больного к тому же по случайности был черный стул (чернослива поел или черники), вырисовывается классическая картина желудочного кровотечения. Только своевременно сделанная электрокардиограмма способна внести ясность в ситуацию.
Астматический вариант протекает без сильной боли в сердце. Больной начинает задыхаться, ему дают препараты, облегчающие дыхание, но лучше от этого не становится – ведь причина приступа удушья совершенно в другом.
Церебральный вариант может напоминать инсульт: при нем возникает спутанность сознания, речи, сильные головные боли.
У больных сахарным диабетом бывает немой инфаркт – совершенно без боли. Сильная утомляемость и одышка после физических усилий, которые раньше давались без труда, могут быть единственными признаками сердечной катастрофы.
Стенокардия напряжения – еще одна маска инфаркта, под которой он прячется примерно у каждого 10-го больного. Боль у них проявляется только при ходьбе. Часто такие пациенты самостоятельно приходят в поликлинику, и уже на ЭКГ у них регистрируют инфаркт.
Однако как бы ни прятался недуг, обычно распознать его легко. Характерные признаки: сильная боль в области сердца, длящаяся больше получаса, которую не удается снять таблетками валидола и нитроглицерина, резкая слабость, в некоторых случаях – рвота.
Инфаркту часто предшествуют сильное физическое переутомление, особенно у людей, непривычных к физической работе, душевное потрясение, стресс.
ЛЕГЧЕ ПРЕДУПРЕДИТЬ
Среди факторов риска инфаркта миокарда есть такие, на которые мы повлиять не можем – так называемые немодифицируемые. Зато другая группа – модифицируемые это те, что полностью зависят от нашего образа жизни и могут быть исключены, стоит лишь захотеть и приложить усилия.
Немодифицируемые факторы риска
Пол: мужской. Мужчины подвержены этому заболеванию больше. Женщин до определенного возраста защищают половые гормоны.
Возраст: старше 65 лет. После 65 лет инфаркты встречаются чаще, чем в более молодом возрасте.
Модифицируемые факторы риска
Курение. Никотин ухудшает состояние сосудов. Чем больше вы курите, тем выше риск ишемической болезни сердца и инфаркта миокарда. Если не можете бросить, хотя бы снижайте количество выкуриваемых сигарет.
Повышенное артериальное давление. В каждом доме должен быть тонометр. Время от времени измеряйте АД себе и своим близким. А если имеется гипертоническая болезнь, после 40 лет надо делать это регулярно, как и принимать лекарства, назначенные врачом. Обязательно посоветуйтесь с доктором, в какое время лучше всего принимать препараты.
Повышенный уровень холестерина в крови. Знать свой уровень холестерина так же необходимо, как и артериальное давление. Если цифры превышают норму, сделайте развернутый анализ – липидограмму, чтобы определить, сколько процентов от общего холестерина приходится на липопротеиды низкой и высокой плотности. Это поможет врачу подобрать современные гиполипидемические средства.
Повышенный уровень глюкозы в крови. Он приводит к изменению эндотелия, выстилающего сосуды, что способствует образованию атеросклеротических бляшек.
Гиподинамия и лишний вес. О вреде первой уже говорилось, лишний вес же обычно сопутствует сидячему образу жизни. Чтобы узнать, в норме ли ваш вес, достаточно измерить окружность талии.
У мужчин ожирение отсутствует при окружности тали менее 94 см., от 94 – 101 см. – зона отклонений и если талия более 102 см. необходима квалификационная помощь.
У женщин ожирение отсутствует при окружности тали менее 80 см., от 80 – 87 см. – зона отклонений и если талия более 88 см. необходима квалификационная помощь.
МОЛОДОСТЬ – ОПАСНЫЙ ВОЗРАСТ?
Никого не удивишь историями о благополучно пережитых 2–3 инфарктах, а в кардиологических отделениях вам непременно расскажут о какой-нибудь старушке, перенесшей ни много ни мало – 8! Но от чего это зависит? Почему для одного человека первый инфаркт становится последним, а для другого – началом длинного списка?
Конечно, многое определяется тем, насколько обширен процесс, сколько коронарных сосудов в него вовлечено. Трансмуральных, то есть обширных инфарктов чаще всего удается пережить 1–2, микроинфарктов – гораздо больше. Парадоксально, но факт: у молодых людей инфаркт часто протекает тяжелее, чем у пожилых. Все дело в том, что у людей в возрасте, чье сердечко давно пошаливает, постепенно налаживается коллатеральное кровообращение: кровь находит обходные пути, минуя пораженный участок сосудов. У молодых этого преимущества нет.
Самое печальное, что при этом пациентов в самом расцвете лет – 30-летних, а то и моложе, становится все больше. Причин много. Во-первых, извечные спиртное и сигареты (и то, и другое ухудшают состояние сосудов). Во-вторых, многие сели за руль и стали ездить на машине даже в булочную. Вот вам еще один фактор риска – гиподинамия.
Молодости совершенно несвойственно беречь себя и экономить силы: просто не верится, что что-то может случиться.
Будьте здоровы! Берегите себя и близких!
Врач-кардиолог Данилова И.Ю.
Источник
Линчак Руслан Михайлович
Термин «инфаркт миокарда» появился в самом конце XIX века и был предложен французским клиницистом R. Marie. Уже в 1904 г. В.М. Керниг описал типичную клиническую картину этого заболевания, а еще через 5 лет на Первом съезде терапевтов В.П.Образцов и Н.Д. Стражеско первыми в мире дали описание status gastralgicus, status astmaticus, подчеркнув разнообразие клинических проявлений инфаркта миокарда (ИМ). В последующем отечественный невролог профессор Н.К. Боголепов обратил внимание на случаи ИМ, протекавшие с признаками нарушения мозгового кровообращения. В клинической практике нередки случаи дебюта ИМ с различных аритмий, зачастую заканчивающихся фатально, а также малосимптомного или бессимптомного течения заболевания. В то же время инфаркт миокарда и сам может являться «маской» целого ряда патологических состояний, иногда носящих ургентный хирургический характер, о чем свидетельствуют следующие клинические наблюдения.
НАБЛЮДЕНИЕ №1. Больной Л., 47 лет, поступил в ПИТ НМХЦ им. Н.И.Пирогова 02.04.07 с диагнозом направления «Инфаркт миокарда».
Анамнез заболевания: До 31.03.07 считал себя здоровым человеком. Утром 31.03.07 после физической нагрузки приступ давящих болей за грудиной без иррадиации длительностью до несколько часов. Госпитализирован в больницу г. Троицка, где на основании клинической картины заболевания, нестабильности гемодинамики (снижение АД до 70/40 мм рт. ст., впервые выявленный пароксизм мерцательной аритмии) состояние расценено как «Инфаркт миокарда» и проведен системный тромболизис проурокиназой с последующей терапией по программе данного заболевания. Вместе с тем, в связи с сохраняющимся дискомфортом за грудиной, появлением 01.04.07 эпизодов одышки 2.04.07 по желанию родных больной переведен для дальнейшего лечения в ЦКДК.
Статус при поступлении: сохранялся незначительной интенсивности болевой синдром за грудиной, перебои в работе сердца. При объективном обследовании – состояние средней тяжести. Гиперстеник. Кожные покровы и видимые слизистые физиологической окраски и влажности, теплые, гиперемия щек. Отеков нет. В легких дыхание везикулярное, проводится во все отделы, хрипов нет. ЧДД – 16 в мин. SаO2 96% без инсуффляции кислорода. Границы сердца расширены влево на 2 см. Тоны сердца звучные, интенсивный систоло-диастолический шум во всех точках аускультации с максимумом по левому краю грудины. ЧСС 130-145 в минуту, по монитору – фибрилляция предсердий. Дефицит пульса 65-70 в минуту. АД = 100/60 мм рт. ст. Варикозно расширенные вены нижних конечностей. Живот мягкий, безболезненный при пальпации во всех отделах. Печень не выступает из-под края реберной дуги. Больной в ясном сознании. Грубая очаговая и менингеальная симптоматика не выявляется.
Результаты лабораторно-инструментальных методов исследования:
- Клинический анализ крови – тромбоциты – 93*109/л, лейкоциты – 16,9*109/л, в остальном – без патологии;
- Биохимический анализ крови – незначительное повышение КФК до 201 ммоль/л, остальные показатели в норме;
- Анализ крови на тропонин – менее 0,1 (в норме менее 0,1), через 6 часов – 0,1; Д-димер – 0,93 (в норме менее 0,5);
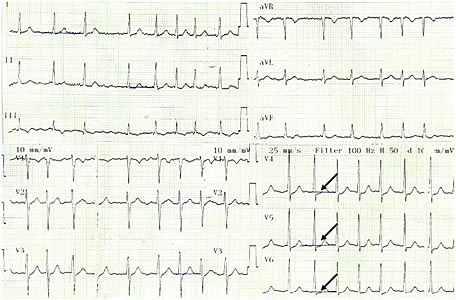
- Электрокардиография: фибрилляция предсердий с ЧСС 136 в минуту. ЭОС не отклонена. QRS 0,08, QT 0,34. Депрессия ST в V4-V6 до 1 мм (рис.1).
- Эхо-кардиография: расширение восходящего отдела аорты (максимально до 6,1 см), дополнительная подвижная линейная структура, делящая аорту на 2 канала (рис. 2.). Сепарация листков перикарда до 5 мм. Аортальная регургитация III ст.
- Консультация кардиохирурга – у больного расслаивающая аневризма аорты, показано экстренное оперативное вмешательство.
Проведенный комплекс обследований позволил верифицировать расслаивающую аневризму аорты, больной переведен в отделение кардиохирургии, где выполнена экстренная операция – резекция аневризмы восходящей аорты, устранение расслоения аорты, протезирование в условиях искусственного кровообращения. Через 3,5 недели от поступления больной выписан из стационара.

Рис. 1. ЭКГ больного Л, 47 лет. Стрелками показана депрессия ST в отведениях V4-V6.
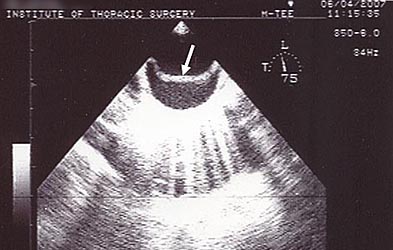
Рис. 2. Эхо-кардиография больного Л, 47 лет. Стрелкой показана диссекция интимы аорты.
НАБЛЮДЕНИЕ №2. Больной С., 38 лет, гражданин Голландии, поступил в ПИТ НМХЦ им. Н.И.Пирогова 10.07.07 с диагнозом направления «Инфаркт миокарда».
Анамнез заболевания: Заболел 10.07.07 в 05-00, проснулся от интенсивных болей в эпигастральной обл. опоясывающего характера. Был однократно стул обычной консистенции и цвета. Со временем интенсивность болей уменьшилась, однако окончательного купирования болевого синдрома не наступило, в связи с чем в 9-40 вызвал бригаду скорой МП, вводился нитроспрей – без существенного эффекта, кеторол с димедролом в/м, аспирин внутрь, госпитализирован с подозрением на инфаркт миокарда. Отец больного перенес инфаркт миокарда, ему выполнено коронарное стентирование.
Статус при поступлении: состояние средней тяжести. Кожные покровы и видимые слизистые физиологической окраски и влажности. Отеков нет. Со стороны легочной и сердечно-сосудистой систем – без особенностей. ЧСС 84 в минуту, АД = 120/60 мм рт. ст. Живот мягкий, умеренно болезненный при пальпации в правой подвздошной области. Симптомы раздражения брюшины отрицательные. Печень не выступает из-под края реберной дуги.
Результаты лабораторно-инструментальных методов исследования:
- Клинический анализ крови – лейкоциты – 14,1*109/л (через 4 часа 14,9*109/л) , количество тромбоцитов, эритроцитов в норме;
- Биохимический анализ крови – все оцениваемые показатели, в т.ч. амилаза (как и диастаза мочи) в норме;
- Анализ крови на тропонин – отрицательный;
- Электрокардиография: синусовый ритм, нормосистолия. ЭОС не отклонена. Одиночная мономорфная желудочковая экстрасистолия. Элевация ST в II, aVF, V5-V6 до 1 мм (рис.3). ЭКГ для сравнения не предоставлены.
- Эхо-кардиография, УЗИ органов брюшной полости и забрюшинного пространства – без патологии;
- Консультация хирурга – не исключено наличие острого аппендицита. Показана диагностическая лапароскопия.
Учитывая стабильность гемодинамических показателей в течение 5 часов наблюдения, отсутствие ЭКГ-динамики при ежечасной регистрации, нарастание лейкоцитоза позволили выполнить диагностическую лапароскопию, при которой диагностирован флегмонозный аппендицит, выполнена лапароскопическая аппендэктомия. Еще через 12 часов после повторного анализа крови на тропонин (результат отрицательный), регистрации ЭКГ (без динамики по сравнению с предыдущими) диагноз инфаркта миокарда был отвергнут окончательно. Через 6 дней после операции пациент выписан из стационара.
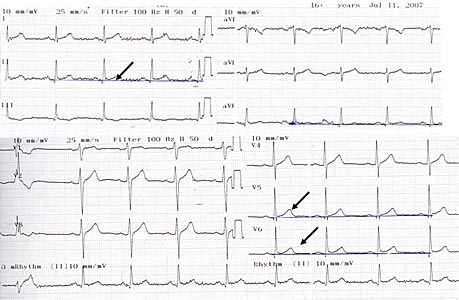
Рис. 3. ЭКГ больного C, 38 лет. Стрелками показана элевация ST в отведениях II, aVF, V5-V6
Таким образом, несмотря на наличие достаточно классических признаков ангинозного синдрома, изменений на ЭКГ и слабоположительного тропонинового теста, активный поиск причин, объясняющих систоло-диастолический шум при аускультации, позволил правильно и своевременно верифицировать расслаивающую аневризму аорты и выполнить оперативное вмешательство у пациента Л., 47 лет. Особенностью второго наблюдения стало наличие элевации сегмента ST в отведениях, характеризующих потенциалы нижне-боковой стенки левого желудочка. Как известно, именно для нижнего инфаркта миокарда характерен болевой синдром в эпигастральной области. Для окончательной верификации диагноза требовалось наблюдение за больным, его ЭКГ-картиной и кардиоспецифическими ферментами. И даже после того, как при лапароскопии был диагностирован флегмонозный аппендицит и выполнена аппендэктомия, диагноз инфаркта миокарда был отвергнут только через 12 часов после выполнения этих условий.
Вышеописанные наблюдения напоминают нам о важности проведения дифференциальной диагностики во всех случаях поступления в стационар каждого пациента, необходимости помнить о «масках» практически каждого заболевания, особенно тех, что требуют неотложных мероприятий по диагностике и лечению.
Другие клинические наблюдения
Источник
Содержание:
Инфаркт миокарда (ИМ) – самая серьезная клиническая форма ишемии сердца. Это острое, угрожающее жизни, состояние, обусловленное относительным либо абсолютным недостатком кровоснабжения определенной части миокарда вследствие тромбоза коронарной артерии, в результате чего формируется очаг некроза, т.е. область с отмершими клетками – кардиомиоцитами.
Инфаркт сердца – одна из ведущих причин смертности населения планеты. Его развитие напрямую зависит от возраста и пола человека. В связи с более поздним появлением атеросклероза у женщин инфаркты диагностируются у них в 3–5 раз реже, чем у мужчин. В группу риска попадают все представители мужского пола, начиная с 40-летнего возраста. У людей обоих полов, перешедших рубеж 55–65 лет, заболеваемость примерно одинакова. По статистике 30–35% всех случаев острого инфаркта сердечной мышцы заканчиваются летальным исходом. До 20% внезапных смертей вызваны этой патологией.
Причины инфаркта
Главные причины развития ИМ:
- Атеросклероз сосудов сердца, в частности коронарных артерий. В 97% случаев атеросклеротическое поражение стенок сосудов приводит к развитию ишемии миокарда с критическим сужением просвета артерий и длительным нарушением кровоснабжения миокарда.
- Тромбоз сосудов, к примеру, при коронарите различного генеза.Полное прекращение кровоснабжениямышцы происходит вследствиеобтурации (закупорки) артерий или мелких сосудов атеросклеротической бляшкой или тромбом.
- Эмболия венечных артерий, например, при септическом эндокардите, реже заканчивается образованием некротического очага, тем не менее являясь одной из причин формирования острой ишемии миокарда.
Нередко встречается сочетание вышеперечисленных факторов: тромб закупоривает спастически суженный просвет артерии, пораженной атеросклерозом или формируется в области атеросклеротической бляшки, выпяченной из-за произошедшего кровоизлияния в ее основание.
- Пороки сердца. Коронарные артерии могут отходит от аорты вследствие формирования органического поражения сердца.
- Хирургическая обтурация. Механическое вскрытие артерии или ее перевязка во время проведения ангиопластики.
Факторы риска инфаркта миокарда:
- Пол (у мужчин чаще).
- Возраст (после 40–65 лет).
- Стенокардия.
- Порок сердца.
- Ожирение.
- Сильный стресс или физическое перенапряжение при имеющейся ИБС и атеросклерозе.
- Сахарный диабет.
- Дислипопротеинемия, чаще гиперлипопротеинемия.
- Курение и прием алкоголя.
- Гиподинамия.
- Артериальная гипертония.
- Ревмокардит, эндокардит или другие воспалительные поражения сердца.
- Аномалии развития коронарных сосудов.
Механизм развития инфаркта миокарда
Течение болезни делится на 5 периодов:
- Прединфарктный (стенокардия).
- Острейший (острая ишемия сосудов сердца).
- Острый (некробиоз с формированием некротической области).
- Подострый (стадия организации).
- Постинфарктный (образование рубца в месте некроза).
Последовательность патогенетических изменений:
- Нарушение целостности атеросклеротического отложения.
- Тромбоз сосуда.
- Рефлекторный спазм поврежденного сосуда.
При атеросклерозе избыточный холестерин откладывается на стенках сосудов сердца, на которых образуются липидные бляшки. Они сужают просвет пораженного сосуда, замедляя кровоток по нему. Различные провоцирующие факторы, будь то гипертонический криз или эмоциональное перенапряжение, приводят к разрыву атеросклеротического отложения и повреждению сосудистой стенки. Нарушение целостности внутреннего слоя артерии активирует защитный механизм в виде свертывающей системы организма. К месту разрыва прилипают тромбоциты, из которых формируется тромб, закупоривающий просвет сосуда. Тромбоз сопровождается выработкой веществ, приводящих к спазмированию сосуда в области повреждения либо по всей его длине.
Клиническое значение имеет сужение артерии на 70% размера ее диаметра, при этом просвет спазмируется до такой степени, что кровоснабжение не может быть компенсировано. Это возникает вследствие атеросклеротических отложений на стенки сосудов и ангиоспазма. В результате нарушается гемодинамика области мышцы, получающей кровь через поврежденное сосудистое русло. При некробиозе страдают кардиомиоциты, недополучая кислород и питательные вещества. Нарушается метаболизм и функционирование сердечной мышцы, ее клетки начинают отмирать. Период некробиоза длится до 7 часов. При незамедлительно оказанной в этот промежуток времени медицинской помощи происходящие изменения в мышце могут быть обратимы.
При формировании некроза в пораженной области восстановить клетки и повернуть процесс вспять невозможно, повреждения приобретают необратимый характер. Страдает сократительная функция миокарда, т.к. некротизированная ткань не участвует в сокращении сердца. Чем обширнее область поражения, тем сильнее снижается сократимость миокарда.
Единичные кардиомиоциты или небольшие их группы гибнут спустя примерно 12 часов от начала острого заболевания. Через сутки микроскопически подтверждается массовое омертвление клеток сердца в зоне поражения. Замещение области некроза соединительной тканью начинается через 7–14 дней от начала инфаркта. Постинфарктный период продолжается 1,5–2 месяца, в течение которых окончательно формируется рубец.
Передняя стенка левого желудочка – наиболее частое место локализации некротической зоны, поэтому в большинстве случаев выявляется трансмуральный ИМ именно этой стенки. Реже поражается верхушечная область, задняя стенка или межжелудочковая перегородка. Инфаркты правого желудочка в кардиологической практике встречаются редко.
Классификация инфаркта миокарда
Относительно размера поражения ткани инфаркт миокарда бывает:
- Мелкоочаговый. Формируется один или несколько маленьких по размеру некротических участков. Диагностируется в 20% случаев от общего числа инфарктников. У 30% пациентов мелкоочаговый инфаркт трансформируется в крупноочаговый.
- Крупноочаговый (чаще трансмуральный). Образуется обширная область некроза.
По глубине некротического поражения различают:
- Трансмуральный. Некротическая область охватывает всю толщу миокарда.
- Субэпикардиальный. Участок с отмершими кардиомиоцитами прилегает к эпикарду.
- Субэндокардиальный. Некроз сердечной мышца в районе прилегания к эндокарду.
- Интрамуральный. Участок некроза находится в толще левого желудочка, но не доходит до эпикарда или эндокарда.
В зависимости от кратности возникновения:
- Первичный. Возникает первый раз.
- Повторный. Развивается через 2 месяца или позже после начала первичного.
- Рецидивирующий. Появляется на стадии формирования рубцовой ткани первичного инфаркта, т.е. в течение первых 2 мес. от первичного острого поражения миокарда.
Относительно локализации процесса:
- Левожелудочковый.
- Правожелудочковый.
- Септальный, или инфаркт межжелудочковой перегородки.
- Сочетанный, к примеру переднебоковой ИМ.
Отталкиваясь от электрокардиологических изменений, фиксируемых на кардиограмме:
- Q-инфаркт. Электрокардиограмма фиксирует сформировавшийся патологический з. Q или желудочковый комплекс QS. Изменения характерны для крупноочаговых ИМ.
- Не Q-инфаркт с инверсией з. Т и без патологии з. Q. Чаще встречается при мелкоочаговых инфарктах.
В зависимости от развития осложнений:
- Неосложненный.
- Осложненный.
Формы острого ИМ, относительно наличия и места расположения болей:
- Типичная. Боль сосредоточена в прекардиальной либо загрудинной области.
- Атипичная. Форма заболевания с атипичной локализацией болей:
Периоды заболевания:
- Острейший.
- Острый.
- Подострый.
- Постинфарктный.
Симптомы инфаркта миокарда
Интенсивность и характер болевых ощущений зависят от нескольких факторов: размера и локализации некротического очага, а также стадии и формы инфаркта. У каждого пациента клинические проявления различны в силу индивидуальных особенностей и состояния сосудистой системы.
Признаки типичной формы инфаркта миокарда
Яркая клиническая картина с типичным и выраженным болевым синдромом наблюдается при крупноочаговом (трансмуральном) инфаркте сердца. Течение болезни разделяю на определенные периоды:
- Прединфарктный, или продромальный период. У 43–45% инфарктников этот период отсутствует, т.к. болезнь начинается внезапно. Большинство пациентов перед инфарктом отмечают учащение приступов стенокардии, загрудинные боли становятся интенсивными и продолжительными. Изменяется общее состояние – снижается настроение, появляется разбитость и страх. Эффективность антиангинальных средств значительно снижается.
- Острейший период (от 30 мин до нескольких часов). При типичной форме острый инфаркт сопровождается нестерпимой загрудинной болью с иррадиацией в левую сторону туловища – руку, нижнюю челюсть, ключицу, предплечье, плечо, область между лопатками. Редко под лопатку или левое бедро. Боли могут быть жгучими, режущими, давящими. Некоторые ощущают распирание в груди или ломоту. В течение нескольких минут боль достигает своего максимума, после чего сохраняется до часа и дольше, то усиливаясь, то ослабевая.
- Острый период (до 2 суток, при рецидивирующем течении до 10 дней и дольше). У подавляющего большинства больных ангинозная боль проходит. Ее сохранение свидетельствует о присоединении эпистеноперикардиального перикардита либо о продолжительном течении ИМ. Нарушения проводимости и ритма сохраняются, также как и артериальная гипотензия.
- Подострый период (длительность – 1 мес). Общее состояние пациентов улучшается: температура нормализуется, проходит одышка. Полностью или частично восстанавливается сердечный ритм, проводимость, звучность тонов, но блокада сердца регрессу не поддается.
- Постинфарктный период – завершающий этап течения острого ИМ, длящийся до 6 месяцев. Некротическая ткань окончательно заменяется плотным рубцом. Сердечная недостаточность устраняется за счет компенсаторной гипертрофии сохранившегося миокарда, но при обширной площади поражения полная компенсация невозможна. В этом случае проявления сердечной недостаточности прогрессируют.
Начало боли сопровождается сильной слабостью, появлением обильного липкого (профузного) пота, чувством страха смерти, учащением сердцебиения. При физикальном обследовании выявляется бледность кожи, липкий пот, тахикардия и другие нарушения ритма (экстрасистолия, фибрилляция предсердий), возбуждение, одышка в покое. В первые минуты повышается артериальное давление, потом резко понижается, что свидетельствует о развивающейся недостаточности сердца и кардиогенном шоке.
При тяжелом течении развивается отек легких, иногда сердечная астма. Тоны сердца при аускультации приглушены. Появление ритма галопа говорит о левожелудочковой недостаточности, от степени выраженности которой зависит аускультативная картина легких. Жесткое дыхание, хрипы (влажные) подтверждают застой крови в легких.
Ангинозная боль в этом периоде нитратами не купируется.
В результате перифокального воспаления и некроза появляется лихорадка, сохраняющаяся на протяжении всего периода. Температура поднимается до 38,50 С, высота ее подъема зависит от размера некротического очага.
При мелкоочаговом инфаркте мышцы сердца симптоматика менее выражена, течение болезни не такое четкое. Редко развивается недостаточность сердца. Аритмия выражается в умеренной тахикардии, которая бывает не у всех больных.
Признаки атипичных форм инфаркта миокарда
Подобные формы характеризуются нетипичной локализацией болей, затрудняющей своевременную установку диагноза.
- Астматическая форма. Характерен кашель, приступы удушья, проливной холодный пот.
- Гастралгическая (абдоминальная) форма проявляется болями в эпигастральной области, рвотой, тошнотой.
- Отечная форма бывает при массивной очаге некроза, приводящем к тотальной сердечной недостаточности с отеками, одышкой.
- Церебральная форма характерна для пожилых пациентов с выраженным атеросклерозом не только сердечных, но и мозговых сосудов. Проявляется клиникой ишемии головного мозга с головокружениями, потерей сознания, шумом в ушах.
- Аритмическая форма. Единственным ее признаком может быть пароксизмальная тахикардия.
- Стертая форма отличается отсутствием жалоб.
- Периферическая форма. Боли могут быть только в руке, подвздошной ямке, нижней челюсти, под лопаткой. Иногда опоясывающая боль схожа с болями, возникающими при межреберной невралгии.
Осложнения и последствия инфаркта миокарда
- Тромбоз в желудочках.
- Острый эрозивный гастрит.
- Острый панкреатит либо колит.
- Парез кишечника.
- Желудочное кровотечение.
- Синдром Дресслера.
- Острая, а в дальнейшем хроническая прогрессирующая недостаточность сердца.
- Кардиогенный шок.
- Постинфарктный синдром.
- Эпистенокардиальный перикардит.
- Тромбоэмболии.
- Аневризма сердца.
- Отек легких.
- Разрыв сердца, приводящий к его тампонаде.
- Аритмии: пароксизмальная тахикардия, экстрасистолия, внутрижелудочковая блокада, фибрилляция желудочков и другие.
- Инфаркт легких.
- Пристеночный тромбоэндокардит.
- Психические и нервные расстройства.
Диагностика инфаркта миокарда
Анамнез болезни, электрокардиографические признаки (изменения на ЭКГ) и характерные сдвиги ферментативной активности в сыворотке крови являются основным критериями при диагностике острого ИМ.
Лабораторная диагностика
В первые 6 часов острого состояния в крови выявляется повышенный уровень белка – миоглобина, участвующего в транспортировке кислорода внутрь кардиомиоцитов. В течение 8–10 часов больше чем на 50% увеличивается креатинфосфокиназа, показатели активности которой нормализуются к концу 2 суток. Этот анализ повторяют каждые 8 часов. Если получают троекратный отрицательный результат, то инфаркт сердца не подтверждается.
На более позднем сроке необходим анализ на определение уровня лактатдегидрогеназы (ЛДГ). Активность этого фермента увеличивается спустя 1–2 суток от начала массового омертвления кардиомиоцитов, по прошествии 1–2 недель приходит в норму. Высокой специфичностью отличается повышение изоформ тропонина, увеличение уровня аминотрансфераз (АСТ, АЛТ). В общем анализе – повышение СОЭ, лейкоцитоз.
Инструментальная диагностика
ЭКГ фиксирует появление отрицательного з. Т либо его двухфазность в определенных отведениях (при мелкоочаговом ИМ), патологии комплекса QRS или з. Q (при крупноочаговом ИМ), а также различные нарушения проводимости, аритмии.
Электрокардиография помогает определить обширность и локализацию области омертвения, оценить сократительную способность сердечной мышцы, выявить осложнения. Рентгенологическое исследование малоинформативно. На поздних этапах проводят коронарографию, выявляющую место, степень сужения или непроходимости коронарной артерии.
Лечение инфаркта миокарда
При подозрении на инфаркт сердца срочно вызывают скорую помощь. До приезда медиков нужно помочь больному принять полусидячее положение с согнутыми в коленях ногами, ослабить галстук, расстегнуть одежду, чтобы она не стягивала грудь и шею. Открыть форточку или окно для доступа свежего воздуха. Под язык положить таблетку аспирина и нитроглицерина, которые предварительно измельчить или попросить больного их разжевать. Это необходимо для более быстрого всасывания действующего вещества и получения скорейшего эффекта. Если ангинозные боли не прошли от одной таблетки нитроглицерина, то его следует рассасывать через каждые 5 минут, но не больше 3 таблеток.
Больной с подозрением на инфаркт сердца подлежит незамедлительной госпитализации в кардиологическую реанимацию. Чем раньше реаниматологи начнут лечение, тем благоприятнее дальнейший прогноз: можно предупредить развитие ИМ, предотвратить появление осложнений, сократить площадь очага некроза.
Основные цели первоочередных лечебных мероприятий:
- снятие болевого синдрома;
- ограничение некротической зоны;
- предотвращение осложнений.
Купирование болевых ощущений – один из важнейших и неотложных этапов лечения ИМ. При неэффективности таблетированного нитроглицерина, его вводят в/в капельно либо наркотический анальгетик (например, морфин) + атропин в/в. В некоторых случаях проводят нейролептанальгезию – в/в нейролептик (дроперидол) + анальгетик (фентанил).
Тромболитическая и антикоагулянтная терапия направлена на сокращение зоны некроза. Впервые сутки от появления первых признаков инфаркта для рассасывания тромба и восстановления кровотока возможно проведение процедуры тромболизиса, но для предотвращения гибели кардиомиоцитов эффективнее ее делать в первые 1–3 часа. Назначают тромболитические препараты – фибринолитики (стрептокиназа, стрептаза), антиагреганты (тромбо-АСС), антикоагулянты (гепарин, варфарин).
Антиаритмическая терапия. Для устранения нарушений ритма, сердечной недостаточности, восстановления метаболизма в ткани сердца применяют антиаритмические препараты (бисопролол, лидокаин, верапамил, атенолол), анаболики (ретаболил), поляризующую смесь и т.д.
Для лечения острой недостаточности сердца используют сердечные гликозиды (коргликон, строфантин), диуретики (фуросемид).
Для устранения психомоторного возбуждения применяют нейролептики, транквилизаторы (седуксен), седативные средства.
Прогноз заболевания зависит от быстроты оказания первой квалифицированной помощи, своевременности проведения реанимационных мероприятий, размера и локализации очага поражения миокарда, наличия либо отсутствия осложнений, возраста пациента и имеющихся у него сопутствующих сердечно-сосудистых патологий.
Источник
