Как проверить риск инсульта

В России ежегодно фиксируется более 400 тысяч инсультов. При этом всё чаще от мозговых катастроф погибают молодые люди. С чем связана эта опасная тенденция? Почему инсульт не всегда удаётся распознать сразу и можно ли полностью восстановиться после удара?
Рассказывает замдиректора Научного центра неврологии, член-корреспондент РАН, профессор Маринэ Танашян.
Лидия Юдина, «АиФ»: Маринэ Мовсесовна, считается, что главная причина инсультов — слабые сосуды?
Маринэ Танашян: Слабые сосуды — не медицинский термин, хотя он довольно точно отражает суть проблемы. Ведь именно от состояния сосудистой стенки во многом зависит, разовьется ли у человека инсульт или нет, а выявление нарушений в сосудах — один из основных способов профилактики сосудистой катастрофы.
«Слабость» сосудов на бытовом уровне может проявляться повышенной склонностью к образованию кровоизлияний, синяков (иногда даже без провоцирующего фактора — удара, сильного сжатия и т. д.) или, наоборот, симптомами недостаточности кровоснабжения — головокружениями, предобморочными состояниями, транзиторными ишемическими атаками (что может быть вызвано сужением сосуда атеросклеротической бляшкой или дисфункцией эндотелия (внутренней выстилки сосуда).
Также нужно помнить, что большинство заболеваний сосудистой системы возраст-зависимы. Чем старше человек, тем, как правило, более изношены его сосуды и тем выше риск развития инсульта, инфаркта миокарда и других состояний, которые приводят к инвалидности.
Нажмите для увеличения
Найти и уничтожить
— Какие медицинские исследования помогают выявить изменения в сосудах?
— Самым результативным и эффективным методом оценки состояния сосудов считается дуплексное сканирование — ультразвуковое исследование, которое позволяет не только оценить степень изменения стенки сосуда (в том числе сужения — стеноза артерии), но и проанализировать структуру атеросклеротической бляшки.
— Если изменения выявлены, что можно предпринять для поддержания сосудов в рабочем состоянии?
— Основа медикаментозной терапии в ангионеврологии (которая и занимается патологией головного мозга из-за поражения питающих мозг сосудов) — препараты, влияющие на нормализацию баланса свёртывающей и противосвёртывающей систем крови. Если у пациента есть склонность к тромбообразованию — ему назначается антитромботическая терапия (антиагреганты, антикоагулянты). Помимо этого применяются средства, которые влияют на функцию сосудистой стенки. Однако стандартных схем лечения не существует. Это всегда комплексный подход с учётом индивидуальных особенностей конкретного пациента.
— Людей со слабыми или изношенными сосудами немало, но инсульт происходит не у каждого. Могут ли врачи предсказать, кому грозит мозговая катастрофа, а кого она минует?
— Врачи не занимаются предсказаниями. Мы оперируем данными крупных исследований, которые помогают довольно точно рассчитать риск инсульта у каждого конкретного пациента. Разработаны даже специальные инструменты оценки этого риска (например, рискометр инсульта, доступный на мобильных устройствах). Зная факторы риска, с ними можно бороться. Каждый пациент получает точные рекомендации — что нужно делать, чтобы избежать болезни. Одним следует отказаться от курения, другим — увеличить физическую активность, третьим — контролировать артериальное давление.
— Правила элементарные. Их соблюдение действительно помогает избежать инсульта?
— Диспансерное наблюдение позволяло ещё в советские годы выявлять патологические процессы на ранних стадиях и за счёт правильного ведения пациента снижать вероятность инсульта почти на 40% даже у людей с высоким риском. Сегодня появились более современные методы диагностики и эффективные лекарства (в частности, для гипертонической болезни). Благодаря этому острые неврологические состояния сейчас встречаются гораздо реже, но при этом увеличилось количество хронических нарушений мозгового кровообращения. Тем не менее
100%-ную гарантию от инсульта не может дать ни один врач — риск мозговой катастрофы есть даже у здорового человека, ведущего правильный образ, не имеющего вредных привычек, и пациента, соблюдающего все врачебные рекомендации.
Атеросклероз или тромбоз
— Инсульт молодеет. Как объясняют это врачи?
— В 40% случаев причина инсульта остаётся невыясненной, особенно если речь идёт о так называемом молодом инсульте. Однако известно, что в зрелом возрасте причиной ишемического инсульта обычно служит атеросклероз, а у молодых удар чаще происходит из-за различных форм повышения свёртываемости крови. Это провоцирует тромбоз и закупорку сосудов головного мозга. Изучением коагуляционных нарушений занимаются учёные всего мира, в том числе и нашего центра.
Нельзя не учитывать, что в последнее время появилось большое количество новых факторов риска, о которых раньше просто не знали.

— Чем раньше пациент с инсультом попадёт к врачу — тем больше у него шансов выжить и восстановиться. Правда ли, что инсульт часто имеет неочевидные признаки, из-за чего пациенты долго не обращаются за медицинской помощью?
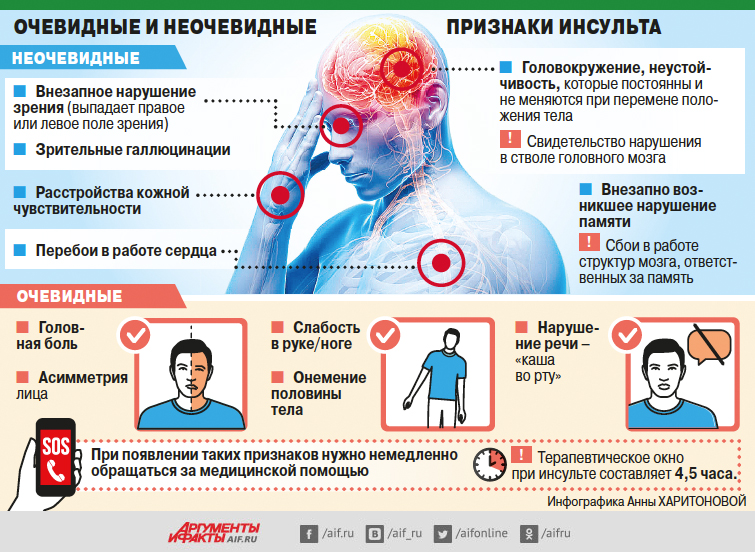
— Действительно, помимо очевидных симптомов инсульта (головная боль, слабость в руке/ноге, онемение половины тела, нарушение речи), существует и ряд необычных признаков удара — перебои в работе сердца, галлюцинации, внезапная потеря памяти, при которых распознать приближающуюся катастрофу довольно трудно.
На практике мы чаще сталкиваемся с другой ситуацией: даже при наличии чётких симптомов инсульта пациенты выжидают и, надеясь на авось, не обращаются за помощью, даже зная, что у врачей больше всего возможностей помочь пациенту в период «терапевтического окна», которое при инсульте составляет 4,5 часа.
Успеть за год
— Есть грустная шутка, что неврологи всё знают, но ничего не могут. Поэтому, если пациенту не удалось восстановиться за год после инсульта, он уже не восстановится никогда?
— К счастью, это не так. За последние 20 лет возможности неврологов вышли на принципиально новый уровень. Повсеместно внедрена в практику тромболитическая терапия, которая иногда позволяет полностью обратить заболевание — при условии, что пациент обратился за помощью на самых ранних стадиях инсульта.
Если раньше реабилитация после инсульта начиналась только после выписки пациента из больницы, то сейчас к восстановлению нарушенных функций приступают уже в первые дни, нередко ещё в реанимационном отделении. И это позволяет добиться результатов, о которых раньше нельзя было и мечтать. Наряду с традиционными, классическими методами (массажем, лечебной физкультурой и др.) применяются принципиально новые виртуальные и космические технологии (мозг-компьютер-интерфейс, различные методики стимуляции, виртуальная реальность и т. д.), помогающие ставить на ноги пациентов, у которых раньше было немного шансов на восстановление.
Имеются противопоказания. Обязательно проконсультируйтесь с врачом
Источник
Указанные ниже анализы крови, помогают определить риск развития ишемической болезни сердца, инсульта, периферических сосудов и при необходимости назначить лечение.
Липопротеин – А (Lp (а)) – белок крови, уровень которого указывает на повышенный риск развития сердечного приступа и инсульта.
Нормальное значение:
Желаемый уровень для взрослых: не более 30 мг / дл.
Подготовка к сдаче анализа:
Кровь берется для анализа после 12-часового голодания (за исключением употребления воды). Для получения более точных результатов, необходимо воздерживаться от проведения исследования, по крайней мере, в течение двух месяцев после перенесенного сердечного приступа, операции, инфекции, травмы или беременности.
Липопротеин А является липопротеидом низкой плотности (LDL), к которому присоединен белок называемый «апо». В настоящее время не полностью известно, какую функцию в организме выполняет липопротеин А, однако известно, что содержание в крови липопротеина А выше, чем 30 мг / дл, повышает риск развития инфаркта миокарда и инсульта. Кроме того, высокий уровень липопротеина А может привести к развитию жировой эмболии и повышает риск развития тромбов.
Особенно важно привести уровень ЛПНП (липопротеидов низкой плотности) к норме при повышенном содержании липопротеина А. Причинами высокого содержания липопротеина А являются заболевания почек и некоторые семейные (генетические) нарушения липидного обмена.
Аполипопротеин А1 (Аpо А1) – является основным белком ЛПВП (липопротеидов высокой плотности). Низкий уровень аполипопротеина А1 указывает на повышенный риск развития ранних сердечно-сосудистых заболеваний. Апо 1 чаще бывает снижен у пациентов страдающих гиподинамией, ожирением или употребляющих в пищу высокое количество жиров.
Нормальное значение:
Желаемый уровень для взрослого: более 123 мг / дл.
Подготовка к сдаче анализа:
Кровь должна быть забрана для анализа после 12-часового голодания (за исключением употребления воды). Для получения более точных результатов, необходимо воздерживаться от проведения исследования, по крайней мере, в течение двух месяцев после перенесенного сердечного приступа, операции, инфекции, травмы или беременности.
Аполипопротеин В (аpоВ) – основной белок, содержащийся в холестерине. Новое исследование предполагает, что ApoB является более лучшим общим маркером риска развития сердечно-сосудистых заболеваний, чем ЛПНП.
Нормальное значение:
Менее 100 мг / дл для лиц с низким / средним риском.
Менее 80 мг / дл для лиц с высоким риском, например, с сердечно-сосудистыми заболеваниями или сахарным диабетом.
Подготовка к сдаче анализа:
Кровь должна быть забрана для анализа после 12-часового голодания (за исключением употребления воды). Для получения более точных результатов, необходимо воздерживаться от проведения исследования, по крайней мере, в течение двух месяцев после перенесенного сердечного приступа, операции, инфекции, травмы или беременности.
Фибриноген – белок, содержащийся в крови и участвующий в системе свертывания крови. Однако, высокие уровни фибриногена могут повысить риск развития инфаркта миокарда и сосудистых заболеваний.
Нормальное значение:
Менее 300 мг / дл.
Подготовка к сдаче анализа:
Кровь должна быть забрана для анализа после 12-часового голодания (за исключением употребления воды). Для получения более точных результатов, необходимо воздерживаться от проведения исследования, по крайней мере, в течение двух месяцев после перенесенного сердечного приступа, операции, инфекции, травмы или беременности.
Повышенный уровень фибриногена чаще выявляется возрастных пациентов, у пациентов с повышенным артериальным давлением, массой тела и ЛПНП. С другой стороны, более низкий уровень фибриногена выявляется у пациентов употребляющих алкоголь и регулярно получающих физическую нагрузку. Рост уровня фибриногена наблюдается с менопаузой.
Высокочувствительный С-реактивный белок (протеин) (СRP) – белок, содержащийся в крови, который называют “маркером воспаления”, то есть его наличие указывает на воспалительный процесс в организме. Воспаление является нормальным ответом на многие физические состояния, включая лихорадку, травмы и инфекции. Но, воспалительный процесс, локализованный в стенке сосуда, играет важную роль в инициации и прогрессировании сердечно-сосудистых заболеваний. Воспаление (т.е. набухание и повреждение) внутренней стенки артерий является важным фактором риска развития таких сердечно-сосудистых заболеваний как, атеросклероз, инфаркт миокарда, внезапная смерть, инсульт, образование тромбов, а также заболеваний периферических артерий.
В Health Study Гарвардского Университета, в результате проведенных исследований, повышенный уровень CRP был более точным маркером развития коронарных заболеваний, чем уровень холестерина. В исследовании оценивались двенадцать различных маркеров воспаления у здоровых женщин в постменопаузе. После трех лет, С реактивный белок был самым сильным предиктором риска. Женщины в группе с самыми высокими уровнями CRP более чем в четыре раза чаще, умерли от ишемической болезни сердца, или пострадали от нефатального инфаркта или инсульта.
Совсем недавно, исследование JUPITER (Обоснование использования статинов для первичной профилактики) показало, что статины предотвращают болезни сердца и снижают риск инсульта, сердечного приступа, смерти у лиц с нормальным уровнем ЛПНП (плохой холестерин), но повышенным уровнем высокочувствительного С-реактивного белка (CRP).
В то время как повышенный уровень холестерина, ЛПНП и триглицеридов и низкий уровень ЛПВП являются независимыми факторами риска развития болезней сердца, высокочувствительный С – реактивный протеин предоставляет дополнительную информацию о воспалительном процессе в артериях, что невозможно определить по липидному спектру.
Нормальное значение:
Меньше, чем 1,0 мг / л = низкий риск развития сердечно-сосудистых заболеваний;
1,0 – 2,9 мг / л = промежуточный риск развития сердечно-сосудистых заболеваний;
более 3,0 мг / л = высокий риск развития сердечно-сосудистых заболеваний.
Иногда определяются уровни CRP 50 мг/л и выше, но обычно, уровень С – реактивного протеина выше 10 мг/л обусловлен иным воспалительным процессом, например, инфекцией, травмой, артритом, и т.д.
Таким образом, тестирование не должно происходить во время болезни или травмы. CRP должен быть исследован для оценки риска развития сердечно-сосудистых заболеваний у практически здоровых лиц, которые недавно не переносили то или иное инфекционное заболевание или другие серьезные заболевания. Те пациенты, у которых уровень CRP при исследовании, составил выше 10 мг/л, должны быть обследованы для выявления источника воспалительного процесса.
Подготовка к сдаче анализа:
Этот тест может быть выполнен в любое время дня, без какой бы то ни было подготовки. Единственным условием является – отсутствие острого воспаления.
Миелопероксидаза (МPО) – является маркером воспалительного процесса в артериях. В результате подобного процесса зачастую происходит разрушение атеросклеротических отложений в стенке сосуда, приводящее к тромбозу. Высокий уровень миелопероксидазы, в сочетании с другими факторами риска (CRP, ЛПНП, повышение артериального давления, лишний вес) является точным критерием повышенного риска развития сердечного приступа, инфаркта миокарда, внезапной смерти, инсульта или заболеваний периферических сосудов, в том числе у практически здоровых людей.
Нормальное значение:
Менее чем 400 мкм.
Подготовка к сдаче анализа:
Этот тест может быть выполнен в любое время дня и не требует голодания.
N-терминальный про-мозговой натрийуретический пептид (N-проМНП, NT-proBNT) – пептид, который продуцируется в предсердиях и желудочках сердца в ответ на повышение растяжимости кардиомиоцитов и увеличение давления в камерах сердца. Измеряя концентрацию NT-proBNP, можно судить о количестве синтезированного мозгового натрийуретического пептида. Уровень NT-proBNT тесно коррелирует с фракцией выброса левого желудочка и систолическим давлением в легочной артерии. Повышение уровня NT-proBNP указывает на высокую вероятность сердечной недостаточности и целесообразность соответствующего обследования для подтверждения диагноза.
Нормальное значение:
Менее чем в 125 пг / мл.
Подготовка к сдаче анализа:
Этот тест может проводиться в любое время в течение дня, голодание не требуется.
Уровень липопротеин – ассоциированной фосфолипазы (ЛП-ФЛА2, PLAC).
Высокие уровни липопротеин-ассоциированной секреторной фосфолипазы а2 (ЛП-ФЛА2) указывают на повышение риска развития сердечно-сосудистых заболеваний. Однако, в некоторых случаях, причиной повышенного уровня может быть не артериальная причина.
Нормальное значение:
Менее 200 нг / мл – относительно низкий риск развития сердечно-сосудистых заболеваний;
Между 200-235 нг / мл – средний риск развития сердечно-сосудистых заболеваний;
Более 235 нг / мл – высокий риск развития сердечно-сосудистых заболеваний.
Подготовка к сдаче анализа:
Кровь должна быть забрана для анализа после 12-часового голодания (за исключением употребления воды). Для получения более точных результатов, необходимо воздерживаться от проведения исследования, по крайней мере, в течение двух месяцев после перенесенного сердечного приступа, операции, инфекции, травмы или беременности.
Отношение альбумина к креатинину в моче. (Ualb / Cr). Появление альбумина в моче является признаком заболевания почек, сахарного диабета и сердечно-сосудистых осложнений.
Нормальное значение:
Более 30 мг / г указывает на повышенный риск сердечно-сосудистых заболеваний и диабетической нефропатии.
Более 300 мг / г указывает на клиническую нефропатию.
Подготовка к сдаче анализа:
Анализ мочи может быть проведен в любое время в течение дня и не требует поста.
Источник
К острым нарушениям мозгового кровообращения (ОНМК) принято относить ишемический инсульт (ИИ), геморрагический инсульт (ГИ) и транзиторные ишемические атаки (ТИА). Инсульт (И) – это гетерогенный клинический синдром повреждения головного мозга, связанный с острым нарушением центральной или церебральной гемодинамики. Проблема предупреждения инсульта (И) стала особенно острой в последние десятилетия, когда тенденция к росту заболеваемости и смертности от острых нарушений мозгового кровообращения (ОНМК) стала очевидной. В настоящее время в мире каждая 10-я смерть связана с инсультом – всего около шести миллионов случаев ежегодно [1]. Нагрузка от инсульта (комплекс медицинских, социальных и финансовых проблем) ложится непомерным бременем на системы здравоохранения и экономически развитых стран и стран с низким уровнем доходов. Лечение больного, пострадавшего от инсульта, обходится примерно в 10 раз дороже, чем лечение больного с инфарктом миокарда [2]. Профилактика инсульта, (как первичная, так и вторичная), требует значительных организационных усилий, новых методов диагностики, дорогостоящих лекарств. Это сказывается на доступности медицинской помощи и эффективности профилактически. В итоге, распространённость И в странах с низким и средним уровнем доходов примерно в 2 раза выше, чем в странах с развитой экономикой. Заболеваемость инсультом в Китае за последние 20 лет увеличилась на 50% и почти весь этот рост пришелся на период экономического развития страны [2]. Летальность от инсульта (отношение умерших к числу заболевших) зависит от состояния неотложной помощи и способности системы здравоохранения обеспечивать дальнейшее лечение больного и его реабилитацию. В последние годы в большинстве экономически развитых стран летальность в остром периоде инсульта заметно снизилась, но в течение года после ОНМК всё равно умирает почти 40% больных. Смертность (отношение числа умерших к населению) от инсульта тесно связана с заболеваемостью и эффективностью мер профилактики. В РФ смертность от инсульта на порядок выше, чем в США (251 и 32 на 100000 соответственно) [1]. В целом, смертность от заболеваний сердечно-сосудистой системы в РФ в 7 раз выше, чем в странах Европы при одинаковой распространённости заболеваний, ассоциированных с атеросклерозом [3].
Итак, число пострадавших от инсульта растёт вместе с заболеваемостью, а уменьшение летальности не снижает, а увеличивает нагрузку от инсульта. Ведь абсолютное число больных, требующих мер вторичной профилактики и дорогостоящей реабилитации становится больше. Единственный путь снижения остроты проблемы инсульта − уменьшение заболеваемости путём повышения эффективности профилактики. Но увеличение затрат на профилактическое программы (сегодня в большинстве стран мира они составляют около 3% средств, направляемых на здравоохранение) возможно в ограниченных пределах [3]. Расширения и углубления объема обследования до уровня, позволяющего определить явные и скрытые механизмы заболеваний системы кровообращения, не выдержит даже самая развитая экономика. В основе современной популяционной стратегии профилактики И лежит концепция факторов риска (ФР). Важнейшими факторами сердечно-сосудистого риска являются: ожирение, малоподвижный образ жизни, артериальная гипертензия, сахарный диабет, курение табака, злоупотребление алкоголем, нарушения жирового обмена – дислипидемия [4]. Управление этими факторами определяет успех профилактических программ. Насколько успешна эта стратегия в современном мире? Kim A.S., Johnston S.C. (2013) проанализировали динамику наиболее значимых кардиоваскулярных ФР (Таблица 1). Как видно из таблицы, более или менее эффективно удаётся контролировать только артериальную гипертензию: средний уровень АД снизился на 10 мм рт. ст в США и 8 мм рт. ст в Японии.
Таблица 1. Важнейшие кардиоваскулярные факторы риска (медиана). 25-летняя динамика в популяции США, Японии и Китая [2].
| Страны | Факторы риска | 1980 | 2005 | Тенденция |
| США | Холестерин (мг/дл) | 220 | 200 | ↓ |
| Индекс массы тела | 25 | 27 | ↑ | |
| Систолическое АД (мм рт ст) | 130 | 120 | ↓ | |
| Глюкоза (мг/дл) | 95 | 103 | ↑ | |
| Япония | Холестерин (мг/дл) | 185 | 200 | ↑ |
| Индекс массы тела | 22 | 23 | ↑ | |
| Систолическое АД (мм рт ст) | 135 | 127 | ↓ | |
| Глюкоза (мг/дл) | 89 | 97 | ↑ | |
| Китай | Холестерин (мг/дл) | 165 | 175 | ↑ |
| Индекс массы тела | 22 | 23 | ↑ | |
| Систолическое АД (мм рт ст) | 128 | 125 | ↓ | |
| Глюкоза (мг/дл) | 96 | 98 | ↑ |
Количество больных с избыточной массой тела и метаболическим синдромом в большинстве стран неуклонно увеличивается. Население развитых стран преимущественно избыточно питается и ведет малоподвижный образ жизни. По данным последнего доклада ВОЗ (2014), в Европе зарегистрирован самый высокий уровень употребления алкоголя на душу населения [5].
В условиях усложнения и удорожания диагностического процесса, недостаточной эффективности методов профилактики сосудистых катастроф, выбор стратегии высокого риска представляется наилучшим решением проблемы. Сущность идеи заключается в уменьшении количества пациентов, требующих сложных методов диагностики и лечения. На этот ограниченный круг больных должен быть направлен весь потенциал современных медицинских технологий. Больных с действительно высоким риском инсульта не так много, как можно было бы предположить. Предвидеть катастрофическое развитие событий, выделить из огромной массы больных относительно небольшую группу тех, кому действительно угрожает опасность, можно основываясь на методах оценки индивидуального риска. Распространённость в популяции заболеваний сердечно-сосудистой системы, приводящих к инсульту (атеросклероз, артериальная гипертония, ишемическая болезнь сердца) очень велика, а тяжелые осложнения возникают относительно редко – только у 1% больных [6]. Этот факт неизбежно приводит к выводу, что И у больного, страдающего «обычными возрастными» болезнями – это маловероятное событие, к которому приводят особые обстоятельства и фатальные изменения характера болезни, её поведения. Для того, чтобы выделить группы высокого риска, нужно опираться на точные знания, которые получают с помощью анализа результатов популяционных исследований, таких как Framingham Heart Study. Это многолетнее популяционное исследование показало связь важнейших ФР с заболеваемостью И [4]. Хорошо известно, например, что ежегодный риск И увеличивается с возрастом. Если в возрастной группе 45-54 лет он составляет 1 случай на 1000 человек, то в возрасте 75 – 84 лет – 1 случай на 50 человек. Подобные данные существуют и в отношении других ФР. Курение табака увеличивает риск И в 2 раза. Повышение АД на 10 мм рт ст по отношению к норме – в 2-3 раза. В последние годы популяционные риски уточняются не только для больных, но и для здоровых людей. Методами статистического анализа установлено, например, что 10-летний риск сердечно-сосудистых событий для некурящего белого мужчины 44 – 79 лет, не страдающего артериальной гипертонией (АГ), дислипидемией и сахарным диабетом составляет 5,3% (2,1% для белой женщины) [7]. Однако индивидуальное прогнозирование, построенное на относительных популяционных рисках методически некорректно и исключительно ненадёжно. Эти данные важны лишь для того, чтобы получить «нулевую», ориентировочную точку популяционного риска. Индивидуальный риск никогда не будет соответствовать этой точке и может весьма существенно отклоняться в связи с множеством особенностей и обстоятельств, присущих индивидууму.
Шкала EURO SCORE – общепринятая система оценки сердечно-сосудистого риска на основе результатов популяционных исследований [8].
По этой шкале степень 10-летнего риска фатальных сосудистых событий может достигать 20% в зависимости от влияния важнейших ФР, таких как АГ, курение, возраст и гиперхолестринемия (высокий риск). Наглядность и расстановка акцентов на коррегируемые ФР – несомненное достоинство этой шкалы, стимулирующее больных к изменению образа жизни. Но совпадение индивидуального прогноза с реальными событиями – маловероятно. Последние рекомендации по лечению АГ определяют умеренный риск серьёзных сосудистых событий как равный или превышающий 7,5% в течение 10 лет [9]. Таким образом, градации десятилетнего риска И, инфаркта миокарда или сосудистой смерти распределяются примерно так: низкий риск менее 7,5 %, средний: 7 – 15%, высокий – более 15%. Стратификация общего сердечно-сосудистого риска на категории низкого, среднего, высокого и очень высокого используется и в Рекомендациях ESH/ESC 2013 [9]. В основе этой прогностической системы лежит АГ – важнейший гемодинамический синдром, патогенетически связанный с большинством сосудистых событий.
Таблица 2. Стратификация общего сердечно-сосудистого риска ESH/ESC 2013
| Другие факторы риска, бессимптомное поражение органов-мишеней или ассоциированные заболевания | Артериальное давление (мм рт. ст.) | |||
| Высокое нормальное САД 130-139 Или ДАД 85-89 | АГ 1 степени САД 140-159 или ДАД 90-99 | АГ 2 степени САД 160-179 или ДАД 100-109 | АГ 3 степени САД >180 или ДАД >110 | |
| Других факторов риска нет | Низкий риск | Средний риск | Высокий риск | |
| 1-2 фактора риска | Низкий риск | Средний риск | Средний и высокий риск | Высокий риск |
| 3 и более факторов риска | Низкий и средний риск | Средний и высокий риск | Высокий риск | Высокий риск |
| Поражение органов-мишеней, ХБП 3 ст или диабет | Средний и высокий риск | Высокий риск | Высокий риск | Высокий и очень высокий риск |
| Клинически манифестные сердечно-сосудистые заболевания, ХБП >4 ст или диабет с поражением органов-мишеней или факторами риска | Очень высокий риск | Очень высокий риск | Очень высокий риск | Очень высокий риск |
АД – артериальное давление; АГ – артериальная гипертония; ХБП – хроническая болезнь почек; ДАД – диастолическое артериальное давление; САД – систолическое АД;
До 1994 значения АД были единственным критерием для оценки степени риска. В последующем было введено понятие суммарного риска, который учитывает негативное влияние и других факторов, которые в совокупности определяют более тяжелый прогноз. Однако оценка суммарного риска оказалась сложной задачей, поскольку зависимость сосудистых событий от ФР не является линейной. Многочисленные попытки уточнить прогноз с помощью математических формул не увенчались успехом – методики получались громоздкими и не увеличивали точность предсказаний [10]. Приходилось вводить всё новые и новые дополнения, которые в последних версиях рекомендаций и руководств охватывают более 30 ФР. В итоге эксперты констатируют, что «любой порог для определения высокого сердечно-сосудистого риска произволен» [9]. Прогностическая точность системы стратификации риска ESH/ESC невелика, но она позволяет на основании объективных критериев определить группу высокого риска. Недостаток этой шкалы – слишком широкий круг больных, который попадает в категорию высокого риска.
Чувствительность метода прогнозирования зависит от выбора ведущего синдрома, способного привести к И. Чем теснее патогенетические взаимоотношения анализируемых синдромов с сосудистыми событиями – тем точнее прогноз. Для больных с нарушениями ритма сердца более надёжной является шкала CHA2DS2VASc [11].
Таблица 3. Шкала CHA2DS2VASc
| Факторы риска | Баллы |
| Хроническая сердечная недостаточность | 1 |
| Артериальная гипертония | 1 |
| Возраст > 75 | 2 |
| Диабет | 1 |
| Ишемический инсульт, ТИА, системные эмболии | 2 |
Поражение артерий
| 1 |
| Возраст 65 – 74 года | 1 |
| Женский пол (за исключением женщин | 1 |
АКШ – аортокоронарное шунтирование; ТИА- транзиторные ишемические атаки.
Шкала предназначена для определения показаний к назначению антикоагулянтов у больных с фибрилляцией предсердий и её прогностическая ценность представляется значительной. Вместе с суммой баллов растет годовой риск И: 1-2 балла – 4.5%; 8-9 баллов – 18 – 24%. Вместе с тем, шкала учитывает и другие важные ФР (возраст, диабет), что, несомненно, уточняет прогноз. Введение баллов в структуру шкалы – методический приём, который позволяет ранжировать риски, придавая им разный вес [12]. Примером подобной прогностической системы может служить шкала оценки риска повторных сердечно-сосудистых оcложнений ESRS[13].
Таблица 4. Шкала ESRS
| Факторы риска | Баллы |
| Возраст менее 65 лет | |
| Возраст 65-75 лет | 1 |
| Возраст более 75 лет | 2 |
| Артериальная гипертония | 1 |
| Сахарный диабет | 1 |
| Инфаркт миокарда | 1 |
| Другие сердечнососудистые заболевания (ХСН, ИБС, желудочковые аритмии), за исключением ИМ и фибрилляции предсердий | 1 |
| Заболевания периферических артерий | 1 |
| Курение | 1 |
| Транзиторная ишемическая атака или ишемический инсульт в дополнение к оцениваемому событию | 1 |
ХСН – хроническая сердечная недостаточность; ИМ – инфаркт миокарда.
Сумма в 3 балла и более свидетельствует о 4% годовом риске серьезных осложнений и такой риск оценивается как высокий. Примечательно, что степень риска для повторных сосудистых событий возрастает на порядок в сравнении с 10-летним риском по шкале SCORE.
Новые прогностические системы всегда ориентированы на оценку годового риска и, как правило, связаны с «ответственными» за развитие инсульта клиническими, коагулопатическими, гемодинамическими синдромами. Многочисленные клинические исследования высокой степени достоверности продемонстрировали тесную связь репрезентативных синдромов с годовым риском И [6,14,15]. Величина этого риска для АГ составляет 4 – 7%, для аритмии – 2-12%, для гиперкоагуляционного синдрома – 5-7%, для стенозирующих атеросклеротических процессов магистральных артерий головного мозга – 4 – 12% [6,10]. Эти обобщения позволили нам предложить «пятипроцентную» шкалу риска И [6].
Таблица 5. Пятипроцентная шкала риска инсульта
| Репрезентативный синдром | Годовой риск инсульта |
| Артериальная гипертония | 5% |
| Гиперкоагуляционный синдром | 5% |
| Аритмия | 5% |
| Атеросклеротический стеноз магистральных артерий головного мозга (>50%) | 5% |
Шкала удобна для практических врачей и более точна в сравнении с системами, ориентированными на возрастные и нозологические критерии. Низкий риск определяется как 5% и менее (1 синдром), умеренный риск – 5 – 10% (2 синдрома), высокий риск 10 – 15% (три синдрома), очень высокий риск – 3 – 4 синдрома. Граница низкого и умеренного риска служит основанием для принятия решения о превентивном лечении (назначение антитромботических средств, статинов и других лекарств).
Современные системы оценки риска демонстрируют неплохую чувствительность, если они применяются для оценки вероятности повторных сосудистых событий. Это не удивительно, ведь более 30% больных, пострадавших от ОНМК, в течение 5 лет переносят ОНМК или ИМ, а транзиторные ишемические атаки (ТИА) у 20% больных в течение месяца приводят к инсульту [16,17].
Шкала ABCD (Age, Blood pressure, Clinical features, Duration of symptoms, Diabetes mellitus), которая используется для оценки вероятности развития инсульта у больных с ТИА, кроме основных ФР учитывает важные динамические характеристики болезни: продолжительность клинических проявлений.
Шкала оценки риска инсульта после ТИА – ABCD
- Возраст более 60 лет – 1 балл
- Артериальное давление при поступлении выше 140/90 мм рт ст – 1 балл
- Клинические симптомы: слабость конечностей с одной стороны – 2 балла, речевые расстройства без слабости в конечностях – 1 балл
- Длительность существования симптомов: 10-60 минут – 1 балл и более 60 минут – 2 балла
- Сахарный диабет – 1 балл
Специальное мультицентровое проспективное исследование показало, что граница низкого риска по этой шкале находится на уровне 3 баллов. Вероятность развития И у больных, перенесших ТИА и получивших больше 3 баллов по шкале ABCD в 7 раз выше [18].
Итог 0-3 балла: Низкий риск
Риск инсульта в течение 2 дней: 1.0%
Риск инсульта в течение 1 недели: 1.2%
Риск инсульта в течение 3 месяцев: 3.1%
Итог 4-5 баллов: Умеренный риск
Риск инсульта в течение 2 дней: 4.1%
Риск инсульта в течение 1 недели: 5.9%
Риск инсульта в течение 3 месяцев: 9.8%
Итог 6-7 баллов: Высокий риск
Риск инсульта в течение 2 дней: 8.1%
Риск инсульта в течение 1 недели: 11.7%
Риск инсульта в течение 3 месяцев: 17.8%
Таким образом, у больных с явными признаками декомпенсации мозгового кровообращения (ТИА) шкала ABCD довольно точно выводит на прогноз И.
Прогноз очень важен для обоснования объема обследования и выбора медикаментозного или хирургического лечения. Больные с низким риском И не нуждаются в углубленном обследовании с применением методов визуализации сердца, сосудов и головного мозга. Это позволяет правильно распределить ресурсы здравоохранения и оптимизировать рабочее время специалистов. С другой стороны, пациенты, относящиеся к категории высокого риска должны своевременно получить полноценное обследование.
В зависимости от степени риска изменяются и методы превентивного лечения. Например, антитромботическая терапия не показана пациентам с низким риском сердечно-сосудистых осложнений. Но больные с высокими градациями риска должны получать агрессивное комплексное лечение, включая статины, антикоагулянты, антигипертензивные средства, в зависимости ведущих синдромов, способных
