Ээг при ишемический инсульт
Современные представления о механизмах повреждающего действия острой церебральной ишемии связаны с пониманием сложных соотношений между сосудистым обеспечением и морфофункциональным состоянием тканей головного мозга. Изучение показателей биоэлектрической активности коры головного мозга в оценке функционального состояния центральной нервной системы больных с поражениями мозга различного генеза хорошо известно. Применение метода количественного анализа электроэнцефалограммы (ЭЭГ) позволяет разработать математические модели церебрального инсульта различных локализаций и генеза, изучить их изменение в связи с применением стандартной терапии. Цель исследования. Изучение возможности использования количественной электроэнцефалографии (КЭЭГ) в исследовании функционального состояния мозга больных, перенесших ишемический инсульт (ИИ), в сопоставлении с данными нейропсихологического исследования.
Методы. В исследование были включены 30 больных ИИ в бассейне средней мозговой артерии (СМА). Запись ЭЭГ проводилась продолжительностью 30 минут в первые сутки заболевания. Результаты. В результате проведенного исследования установлено, что постинсультные когнитивные и тревожно-депрессивные расстройства выявляются уже в острейшем и остром периодах ИИ. При математическом анализе ЭЭГ у пациентов с ИИ в бассейне СМА выявлено снижение уровня мощностей всех ритмов как в пораженном, так и в интактном полушарии, снижение показателей межполушарной когерентности, повышение интегрального индекса, наиболее показательное в височной и центральной областях в пораженном полушарии. Уровень когерентности во всех диапазонах частот в височной области на стороне поражения коррелирует с данными нейропсихологического исследования. Заключение. Данные нейропсихологического исследования сопоставимы с таковыми ЭЭГ, что позволяет высказать суждение о преимущественном поражении медиобазальных структур височной области.
Введение
Современные представления о механизмах повреждающего действия острой церебральной ишемии связаны с пониманием сложных соотношений между сосудистым обеспечением и морфофункциональным состоянием тканей головного мозга. Изучение показателей биоэлектрической активности коры головного мозга в оценке функционального состояния центральной нервной системы лиц с поражениями мозга различного генеза хорошо известно [1]. Применение метода количественного анализа электроэнцефалограммы (ЭЭГ) позволяет разработать математические модели церебрального инсульта различных локализаций и генеза, изучить их изменение в связи с применением медикаментозной терапии.
В работе Е.А. Жирмунской (1987) показано, что изменения ЭЭГ при инсульте неспецифичны и выражаются в дизритмии альфа-ритма, преобладании медленноволновой активности, острых волн в зоне поражения. Работ, посвященных анализу биоэлектрической активности мозга при ишемическом инсульте (ИИ) в бассейне средней мозговой артерии (СМА) в острейшем и остром периодах ИИ, недостаточно, а сопоставление данных математического анализа с нейропсихологическим исследованием практически не проводилось, что и послужило основанием выполнения данной работы.
Цель исследования: изучение возможности использования количественной электроэнцефалографии (КЭЭГ) в исследовании функционального состояния мозга больных, перенесших ИИ в бассейне СМА, в сопоставлении с данными нейропсихологического исследования.
Материал и методы
В региональном сосудистом центре ГБУЗ РБ «Больница скорой медицинской помощи» г. Уфы было проведено исследование 30 больных ИИ в бассейне СМА. Средний возраст больных обоих полов составил 61,63±1,9 года. По гендерному признаку преобладали мужчины – 19 (63,3%), женщин было 11 (36,7%). Соотношение мужчин и женщин составило 1,7:1. Всем пациентам осуществлено комплексное клинико-нейропсихологическое, инструментальное и лабораторные исследования. Запись ЭЭГ проведена продолжительностью 30 минут в первые сутки заболевания на 19-канальном безбумажном электроэнцефалографе фирмы «Nicolet» с локализацией электродов, установленных по международной схеме «10-20» с референтным ушным электродом. Всем пациентам наряду с изучением фоновой записи проведен анализ межполушарной когерентности и интегрального индекса. За норму мощностей ритмов ЭЭГ средних уровней межполушарной когерентности использованы данные В.С. Русинова [2]. Для оценки типов и ЭЭГ-паттернов использовали классификацию Е.А. Жирмунской (1991) и Г. Людерса (2000) [3, 4]. Также были тщательно проанализированы и изучены амбулаторные карты больных с целью выявления в преморбиде эмоциональных и когнитивных нарушений.
Для оценки двигательной и повседневной активности использованы показатели шкалы Рэнкина, индекса мобильности Ривермид, Бартела. С целью определения наличия когнитивных и тревожно-депрессивных расстройств проведено нейропсихологическое исследование с использованием следующих шкал: краткой шкалы исследования психических функций, или Mini-Mental State Examination (MMSE), Монреальской шкалы оценки когнитивных функций МоСА (Montreal Cognitive Assessment), шкалы реактивной и личностной тревожности Спилберга–Ханина, шкалы депрессии Бэка, госпитальной шкалы тревоги и депрессии HADS (Hospital Anxiety and Depression Scale). Для исследования вегетативной устойчивости и оценки степени выраженности вегетативных дисфункций применен опросник А.М. Вейна.
Статистическая обработка полученных результатов осуществлена с использованием программного обеспечения Excel Worksheet из пакета Microsoft Office (2013). Вычислены средняя арифметическая, стандартное отклонение и критерий достоверности (t), корреляция. За достоверные принимались различия на уровне значимости 95% при р
Результаты исследования
В структуре соматической патологии преобладали артериальная гипертензия у 27 (90%) больных, ишемическая болезнь сердца у 25 (83,3%), сахарный диабет у 8 (26,7%), дислипидемия у 7 (23,3%), фибрилляция предсердий у 6 (20%), метаболический синдром у 3 (10%). Аортокоронарное шунтирование присутствовало в анамнезе у 1 (3,3%) больного. По подтипам ИИ различали: неуточненный подтип – у 16 (53,3%) пациентов, лакунарный подтип – у 6 (20%), кардиоэмболический – у 5 (16,7%); атеротромботический – у 3 (10%). Преобладали больные с очагами инсульта в зоне СМА в левом полушарии – 18 (60%), у 12 (40%) очаг находился в правом полушарии. По данным ультразвукового дуплексного сканирования (УЗДС), у 20 (66,7%) больных выявлен стенозирующий атеросклероз магистральных артерий головы, причем у 3 (10%) – стеноз более 50%, у 1 (3,3%) – окклюзия, у 8 (26,6%) – нестенозирующий атеросклероз. Лишь у 2 (6,7%) больных данные УЗДС были в пределах нормы.
Неврологический дефицит по шкале NIHSS (National Institutes of Health Stroke Scale) у больных в среднем составил 5,1±0,2 балла. При поступлении средний балл индекса мобильности Ривермид составил 5,4±0,6; по шкале Рэнкина – 2,0±0,3; по шкале Бартела – 69,1±5,0; по опроснику Вейна – 34,2±4,3.
В неврологическом статусе преобладали двигательные расстройства у 19 (63,3%) больных в виде гемипареза различной степени выраженности: легкий гемипарез – у 12 (40%), неравномерный гемипарез – у 4 (13,3%), пирамидная недостаточность – у 2 (6,7%), глубокий – у 1 (3,3 %). Речевые нарушения представлены в виде моторной афазии у 5 (16,7%) больных, дизартрии – у 4 (13,3%), сочетание амнестической и сенсорной афазии – у 2 (6,6%), элементы сенсомоторной афазии – у 1 (3,3%).
Нарушения чувствительности по гемитипу были у 9 (30%) больных.
Анализ исследования интеллектуально-мнестической, эмоционально-аффективной сфер с применением шкал выявил наличие когнитивных, тревожно-депрессивных расстройств различной степени выраженности в острейшем и остром периодах ИИ. При поступлении средний балл по тесту MMSE составил 22,7±1,3, по тесту МоСА – 19,7±1,5, по шкале Бэка – 16,3±1,4, по шкале HADS (уровень депрессии) – 7,3±0,6, по шкале HADS (уровень тревожности) – 8,0±0,5, по шкале Спилберга–Ханина (уровень реактивной тревожности) – 33,1±3,5. Только у 4 (13,3%) больных определены показатели шкалы личностной тревожности Спилберга–Ханина, остальные 26 (86,7%) отказались, ссылаясь на плохое самочувствие и нежелание отвечать на вопросы данной шкалы. Когнитивные функции выявлены по шкале MMSE у 24 (80%) больных, из них деменция – у 2 (6,7%), по шкале МоСА – у 23 (76,7%), из них деменция – у 4 (13,3%). Депрессивные расстройства по шкале HADS (депрессия) определены у 19 (63,3%) больных, тяжелая депрессия – у 3 (10%), по шкале Бэка – у 26 (86,7%) и у 2 (6,7%) соответственно. Тревожные расстройства по шкале Спилберга–Ханина определены у 12 (40%) больных, из них выраженная тревога – у 3 (10%), по шкале HADS (тревога) – у 20 (66,7%), выраженная тревога – у 4 (13,3%).
При анализе ЭЭГ оценивались спектры мощности и частоты альфа-, бета1-, тета- и дельта-ритмов, что отражено в табл. 1–5.

Из приведенных данных видно, что по сравнению с контралатеральным полушарием в пораженном полушарии в центральном и затылочном отведениях выявляется тенденция к снижению мощности ритмов, не достигающая достоверности, в то время как в лобных и височных отведениях отмечается тенденция к повышению мощности в пораженном полушарии, вероятно, за счет преобладания медленной активности. Зональные различия распределения мощности сохранены. Наименьшая суммарная мощность определена в височных отведениях. Снижение общей мощности ритмов, видимо, можно объяснить ишемией головного мозга, особенно выраженной в пораженном полушарии.
Как видно из табл. 3, при сравнении с контралатеральным полушарием мощность альфа-ритма в пораженном полушарии достоверно снижена в височных отведениях, Также выявлена тенденция к снижению мощности альфа-ритма в центральном и лобном отведениях, более выраженная на стороне поражения.

Как видно из приведенных данных, отмечается снижение частоты альфа-ритма как в пораженном, так и в контралатеральном полушарии по сравнению с нормой. Наиболее пораженными оказались центральные и височные области пораженного полушария. Достоверно снижена частота альфа-ритма в центральном и височном отведениях. Наиболее выражена асимметрия частоты альфа-ритма между пораженным и контралатеральным полушарием в центральном и височных отведениях, т.к. эти отведения соответствуют зоне проекции прецентральной извилины.
Амплитуда альфа-ритма у пациентов с ИИ в каротидном бассейне оказалась достоверно сниженной: средняя амплитуда альф-ритма в затылочных отведениях составила 29,7±7,1 мкВ.
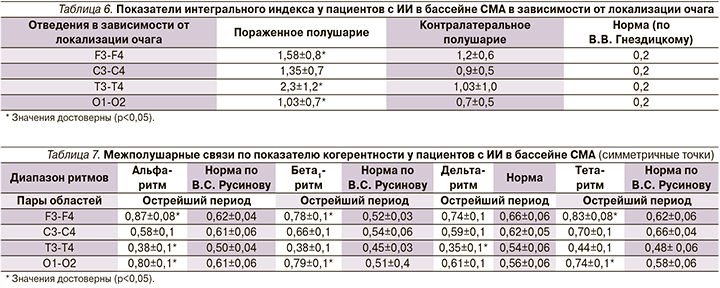
Для оценки степени изменений представительства спектральных составляющих в различных частотных диапазонах использованы полиспектральные индексы (отношение суммарных изменений в низкочастотной области ЭЭГ – тета+дельта к изменениям в высокочастотных областях – альфа+бета1), представленные в табл. 6, 7 (В.В. Гнездицкий, 2000) [4].
При анализе мощности бета1-ритма выявлена тенденция к снижению мощности данного ритма у пациентов по сравнению с нормой, не достигающая границ достоверности.
Мощность дельта-ритма оказалась сниженной во всех отведениях по сравнению с нормой. Выявилась асимметрия мощности дельта-ритма в пораженном и контралатеральном полушариях, особенно наглядная в лобных отведениях. С тяжестью инсульта коррелирует мощность дельта-волн на стороне очага. Выявлена умеренная обратная связь между мощностью дельта-волн и тяжестью инсульта (r=-0,29).
Из табл. 6 видно, что интегральный индекс повышен как в пораженном, так и в контралатеральном полушарии. Однако статистически значимые грубые нарушения выявляются в височных и центральном отведениях.
Межполушарные уровни когерентности характеризуются бóльшими значениями в лобных отделах коры, что свидетельствует о наиболее согласованной их деятельности по сравнению с другими корковыми зонами [5, 6]. Анализ межполушарных связей по показателю когерентности по различным диапазонам ритмов ЭЭГ у пациентов с ИИ в бассейне СМА представлены в табл. 7.
Как видно из представленной табл. 7, в острейшем периоде ИИ выявлено достоверное повышение межполушарной когерентности по альфа-, бета- и тета-диапазонам, в лобных и затылочных отведениях по альфа- и бета-диапазонам, в центральных отведениях тенденция к снижению межполушарной когерентности по всем диапазонам частот, достоверно снижена межполушарная когерентность по альфа- и тета-ритмам в височных отведениях. Отмечаются нарушения региональных различий у пациентов с ИИ: при достаточно высокой связи в лобных отведениях, выявлена также высокая связь по альфа-ритму и в затылочных отведениях (в норме когерентность в затылочных отведениях ниже). Общее снижение межполушарной когерентности в острейшем периоде ИИ и ее патологическое повышение в диапазоне низких частот (дельта и тета), вызывают нарушение функциональных связей электрических процессов коры головного мозга, обеспечивающих нормальную нервно-психическую деятельность человека [5, 6].
Обсуждение
Проведенный нами математический анализ ЭЭГ установил определенные корреляции между выраженностью нарушений электрогенеза коры и высшими мозговыми функциями. Выявлена умеренная прямая связь между когнитивной деятельностью и показателями частоты альфа-ритма: чем выше частота альфа-ритма, тем более выраженными были когнитивные нарушения (r=0,36). Выявлена умеренная обратная связь между амплитудой альфа-ритма и когнитивной деятельностью: чем ниже амплитуда альфа-ритма, тем более выраженными были когнитивные нарушения (r=-0,27). Установлена умеренная прямая связь между когнитивной деятельностью и показателями межполушарной когерентности по дельта-, тета- и альфа-ритмам в височных областях: чем ниже показатели межполушарной когерентности, тем более выраженными были когнитивные нарушения (r=0,27).
Заключение
Таким образом, в результате проведенного исследования установлено, что постинсультные когнитивные и тревожно-депрессивные расстройства выявляются уже в острейшем и остром периодах ИИ. Несомненно, депрессивные и когнитивные расстройства, влияющие на активную самостоятельную работу больных и их сотрудничество с членами мультидисциплинарной команды, негативно влияют на реабилитационный процесс. Кроме того, пациенты с легкими и умеренными когнитивными расстройствами имеют высокий риск развития деменции, что требует их диагностики и коррекции на раннем этапе заболевания.
При углубленном анализе ЭЭГ у пациентов с ИИ с локализацией очага в бассейне СМА выявлено, что наиболее выраженные изменения в виде преобладания медленноволновой активности, снижения уровня межполушарной когерентности регистрируются преимущественно в височных и центральной областях – на стороне поражения уже в острейшем периоде ИИ. Показатели межполушарной когерентности биоэлектрической активности мозга в височной области на стороне поражения коррелируют с данными нейропсихологического тестирования. Данные нейропсихологического исследования сопоставимы с таковыми ЭЭГ, что позволяет высказать суждение о преимущественном поражении медиобазальных структур височной области, играющих важную роль в мнестической деятельности, уже в остром периоде ИИ.
Определение полиспектральных индексов может быть рекомендовано для определения степени нарушения биоэлектрической активности мозга при мониторинге ЭЭГ-активности у больных с полушарным ИИ.
1. Зенков Л.Р. Клиническая электроэнцефалография. М., 2002. 368 с.
2. Русинов В.С. Биопотенциалы мозга человека. Математический анализ / Под ред. В.С. Русинова; АМН СССР. М., 1987. 256 с.
3. Жирмунская Е.А. Системы описания и классификация электроэнцефалограмм человека. М. 1984 г.
4. Luders H., Noachtar S., eds. Atlas and Classification of Electroencephalography. Philadelphia: WB Saunders. 2000.
5. Гнездицкий В.В. Обратная задача ЭЭГ и клиническая электроэнцефалография. Таганрог, 2000. 640 с.
6. Новикова Л.Б. Церебральные нарушения у больных геморрагической лихорадкой с почечным синдромом. Уфа. Здравоохранение Башкортостана. 2001. 251 с.
7. Новикова Л.Б., Сафина А.Г., Сафин Ш.М. Комплексная оценка состояния больного с черепно-мозговой травмой методом обобщения параметра. Уральский медицинский журнал. 2007;1(29):41–5.
Автор для связи: Л.Б. Новикова – д.м.н., проф., зав. кафедрой неврологии и нейрохирургии ИДПО Башкирского государственного медицинского университета, Уфа, Россия; тел. 8 (347) 255-10-38; e-mail: novicova@inbox.ru
Источник
В тех случаях, когда поражения церебральных сосудов не приводят к грубым деструктивным изменениям мозговой ткани и тяжелой, клинически проявляющейся ишемии мозга, изменения на электроэнцефалограмме, как правило, отсутствуют или носят пограничный с нормой характер. На ЭЭГ регистрируются дезорганизованный α-ритм, большое количество быстрых волн, иногда заостренные и медленные колебания, но количество их и амплитуда сохраняются в границах вариантов нормы. При дисциркуляторных расстройствах в вертебробазилярном русле без симптомов выпадения могут наблюдаться явления десинхронизации и уплощения ЭЭГ.
Признаки тромбоза и стеноза сосудов головного мозга на ЭЭГ
При тромбозах и стенозах с клиническими проявлениями в виде парезов, перемежающейся слепоты и афазии изменения на ЭЭГ проявляются медленными волнами θ- и δ-диапазона. Особый диагностический интерес представляет выявленная тесная корреляция между объемом кровотока в бассейне пораженного сосуда, измеренным ангиографически, и средней частотой ритмической активности в этой области. Это позволяет ориентировочно судить по данным ЭЭГ о состоянии кровотока и возможностях компенсации и реабилитации при ишемических нарушениях мозгового кровообращения. На этом же основании ЭЭГ используют для контроля мозговых функций во время операций каротидной эндартерэктомии. Обнаружение медленных волн на электроэнцефалограмме больных паркинсонизмом также рассматривается как показатель наличия циркуляторных изменений, что учитывается при проведении терапии.
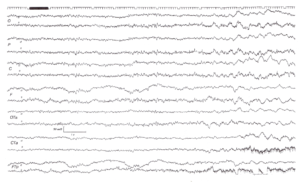
 Больной 60 лет с транзиторными ишемическими атаками со стенозом внутренних сонных артерий >75% слева и >50% справа
Больной 60 лет с транзиторными ишемическими атаками со стенозом внутренних сонных артерий >75% слева и >50% справа
Фоновая ЭЭГ — в пределах нормы. Пережатие правой сонной артерии не вызвало изменений в ЭЭГ. При пережатии левой внутренней сонной артерии (начало пережатия — черный прямоугольник на служебном канале в начале записи) появляются 5-волны частотой около 2 Гц до 100 мкВ амплитудой, сначала несколько преобладающие в левом полушарии, а затем диффузные двусторонние.
При ишемических нарушениях мозгового кровообращения электроэнцефалографические данные могут до определенной степени служить дифференциально-диагностическим целям. Так, при каротидном стенозе патологические ЭЭГ встречаются менее чем у 50% больных, при тромбозе сонной артерии — у 70%, а при тромбозе сильвиевой артерии — у 95% больных. Относительно меньший процент патологических ЭЭГ при стенозе сонной артерии объясняется, по-видимому, возможностями коллатерального кровообращения через систему артериального круга большого мозга (виллизиева круга). Дополнительные диагностические данные могут быть получены с помощью проб с пережатием сонной артерии. При полном тромбозе сонной артерии сжатие ее на стороне поражения не оказывает влияния на ЭЭГ, в то время как пережатие на здоровой стороне приводит к появлению двусторонних медленных волн. При стенозе сонной или тромбозе сильвиевой артерии может наблюдаться появление или увеличение количества и амплитуды медленных волн при сжатии сонной артерии на стороне поражения (рис.). Появление медленных волн ЭЭГ при пережатии сонной артерии независимо от стороны обычно наблюдается у стариков с глобальной церебральной сосудистой недостаточностью. Следует отметить, что оценку проб с пережатием сонных артерий надо проводить с учетом всего комплекса электроэнцефалографических и клинических данных. В частности, изменения ЭЭГ при пережатии сонной артерии могут обусловливаться рефлекторными синокаротидными эффектами. Дифференциации рефлекторных и органических гемодинамических эффектов могут помочь полиграфическая регистрация ЭЭГ и пульсации внутричерепных и наружных артерий головы реографическим или фотометрическим способом.
Ишемический инсульт
В острой фазе ишемического инсульта отмечаются изменения на ЭЭГ в виде локальных θ- и δ-волн соответственно зоне ишемии. При ишемических изменениях в бассейне вертебробазилярных сосудов наблюдается картина генерализованных билатерально-синхронных медленных волн или иногда явления десинхронизации с диффузной β-активностью, соответствующие поражению стволовых неспецифических ретикулярных систем мозга. Стойкость и выраженность патологических изменений на ЭЭГ в существенной мере зависят от возможностей коллатерального кровообращения и, естественно, тяжести поражения мозга. После острого периода в случае, если нет повторных инсультов, на электроэнцефалограмме наблюдается уменьшение выраженности патологических изменений, которое часто идет параллельно клиническому улучшению. В ряде случаев в достаточно отдаленном периоде перенесенного инсульта ЭЭГ полностью нормализуется даже в случае сохранения существенного клинического функционального дефицита.
Геморрагический инсульт
Определенное значение имеет электроэнцефалография в дифференциальной диагностике сосудистого инсульта. При геморрагических инсультах изменения на ЭЭГ значительно более грубые и стойкие, сопровождаются более выраженными общемозговыми изменениями, что соответствует более тяжелой клинической картине.
Церебрально-сосудистые аневризмы и мальформации
Церебрально-сосудистые аневризмы и мальформации, если они не сопровождаются кровоизлияниями, в большинстве случаев не вызывают существенных изменений на ЭЭГ. Наблюдаемые иногда изменения можно расценивать как пограничные между нормой и патологией. Они выражаются в виде диффузных нерегулярных θ-колебаний, не превышающих по амплитуде нормального α-ритма, и заостренных волн. Более грубые и иногда локальные изменения встречаются только при очень больших объемах артериовенозных мальформаций и обусловлены, очевидно, повреждающим воздействием на мозг сильных пульсаций патологического образования.
Признаки субарахноидальных кровоизлияний на ЭЭГ
При субарахноидальных кровоизлияниях если не происходит локального повреждения мозгового вещества в области прорыва аневризмы, изменения на ЭЭГ носят диффузный характер и нередко сопровождаются билатеральносинхронными разрядами, очевидно, обусловленными воздействием излившейся крови на медиобазальные неспецифические структуры мозга, а также гидроцефалией, связанной с временным затруднением ликворооттока. При благоприятном исходе изменения на ЭЭГ относительно быстро исчезают, и она возвращается к исходному состоянию.
Источник
