Эхокардиографическим признаком инфаркта миокарда
ЭхоКГ при ОИМ позволяет:
1) подтвердить или исключить ОИМ у больных с продолжительным болевым синдромом в груди и отсутствием диагностических ЭКГ-критериев;
2) оценить размер пораженного миокарда исходно и конечный размер ИМ после реперфузионной терапии;
3) выявить пациентов с нестабильной гемодинамикой и осложнениями ИМ;
4) оценить жизнеспособность миокарда;
Определить степень риска.
ЭхоКГ-признаки ОИМ:
★ локальное ухудшение работы миокарда (некротизированный участок не сокращается в обычном ритме);
★ в режиме допплер оценивается скорость кровотока, в том числе фракция выброса (что важно для диагностики сердечной недостаточности);
★ обнаружение формирующихся тромбов;
★ обнаружение формирующейся аневризмы сердца (в том числе ее формы, размеров, толщины стенок);
★ обнаружение признаков перикардита;
★ оценка работы сердечных клапанов;
★ оценка состояния основных сосудов;
★ обнаружение расширения полостей сердца и других структурных дефектов.
Принципы лечения инфаркта миокарда: цели и тактика. Помощь до приезда бригады службы «скорой медицинской помощи», на этапе «скорой помощи» и в стационаре. Методы обезболивания. Тромболитическая терапия: препараты, показания, абсолютные и относительные противопоказания, методы контроля, побочные эффекты, помощь при развитии кровотечения.
Основные принципы лечения
1) Купирование болевого синдрома (морфин, промидол, фентанил и дроперидол);
2) Тромболитическая терапия (неоднородная субстанция => возможно только уменьшить объем тромба и восстановить кровоток), используется 2 группы препаратов: стрептокиназа и альтеплаза – только в стационаре (!);
3) Антитромбическая и антиагрегантная терапия (Аспирин + Клопидогрел);
4) Оксигенотерапия (не эффективна);
Применение антиишемических препаратов
Ø Нитраты (нитроглицерин, молсидомин);
Ø Бета-АБ (бисопролол и с дополн. вазодилатирующим эффектом: небивилол и карведилол);
Ø Применение ингибиторов АПФ и АРА II (рамиприл и периндоприл);
Ø Антагонисты кальция (нефидипин, амлодипин, верапамил);
6) Антигиперлипидемическая терапия;
Ø Статины (по эффект: розувастатин, аторвастатин, симвастатин, ловастатин, правастатин, флувастатин) снижают уровень ЛННП и холестерина;
Ø Фибраты (фенофибрат) снижают уровень ТГ и повышают ЛПВП.
Принципы лечения
Терапия ИМ складывается из нескольких направлений:
I. Купирование болевого синдрома
Ø прием 0,5 мг нитроглицерина под язык или 0,4 мг препарата в виде аэрозоля; отсутствие эффекта =>
Ø введение наркотических анальгетиков, так как сохранение болевого синдрома активирует симпатическую нервную систему, что проявляется тахикардией, артериальной гипертензией, увеличением потребности миокарда в кислороде и может способствовать расширению зоны некроза. Морфина сульфат в/в струйно по 2 мг каждые 2-5 мин до купирования болей или появления побочных явлений. Общая доза препарата не должна превышать 20 мг. При развитии тошноты и рвоты показано в/в 10-20 мг метоклопрамида. Угнетение дыхания можно устранить введением 0,1-0,2 мг налоксона. Брадикардию ликвидируют внутривенным введением 0,5-1 мг атропина (М-ХБ). У лиц пожилого и старческого возраста возможна замена морфина на промедол в эквивалентной дозировке – 1:2. Если остается тревога, страх смерти, то дополнительно вводят 10 мг диазепама;
II. Восстановление кровотока в инфарктсвязанной артерии
Восстановление кровотока в тромбированной артерии в первые 12 ч инфаркта ограничивает зону некроза, уменьшает частоту развития аритмий, дисфункции и ремоделирования желудочков сердца, сердечной недостаточности и позволяет спасти от 30 до 50 жизней на 1000 больных.
Восстановление кровотока в окклюзированной артерии: тромболитик + ацетилсалициловая кислота + гепарин =>
Ø Тромболитик:
a) Стрептокиназа – в/в капельно в дозе 1,5 млн МЕ на 100 мл 0,9% физиологического раствора в течение 30-60 мин, половину дозы вводить в течение первых 10-15 мин;
b) Анистреплаза (комплекс стрептокиназы и плазминогена) в/в болюсом 30 ЕД в течение 2-5 мин + гепарин можно использовать по 12 500 ЕД подкожно 2 раза в сутки в течение 5-7 дней.
c) Тканевой активатор плазминогена (альтеплаза) болюсное/капельное введение препарата в суммарной дозе 100 мг + в/в капельно гепарин в течение 2 сут с таким расчетом, чтобы величина АЧТВ составляла 50-75 с;
d) Урокиназа (фермент из культуры клеток почек человека) в/в болюсно 2 000 000 ЕД или 1 500 000 ЕД струйно и 1 500 000 ЕД капельно в течение 60 мин, также 48 ч внутривенно назначается гепарин.
Ø Антитромбоцитарный препарат – АСК (аспирин) – 1 доза (75-150 мг/сут);
Ø Гепарин (не обязательно) – низкомолекулярный гепарин (эноксопарин) снижает риск смерти и повторного ИМ в первые 30 дней.
Источник
Эхокардиография при остром инфаркте миокарда. Механические осложнения инфаркта миокарда
ЭхоКГ при остром инфаркте миокарда позволяет: (а) подтвердить или исключить ОИМ у больных с продолжительным болевым синдромом в груди и отсутствием диагностических ЭКГ-критериев; (б) оценить размер пораженного миокарда исходно и конечный размер ИМ после реперфузионной терапии; (в) выявить пациентов с нестабильной гемодинамикой и осложнениями ИМ; (г) оценить жизнеспособность миокарда; (л) определить степень риска.
Анализ нарушений локальной сократимости в В-режиме полезен даже при ИМ с подъемом сегмента ST. У этих пациентов присутствует акинезия или дискинезия миокарда. После эффективной реперфузии в лечение соответствующего времени сократительная способность миокарда улучшается. Восстановление сократимости происходит в течение 24-48 ч и продолжается в течение нескольких дней и даже месяцев, поэтому двухмерная ЭхоКГ в динамике полезна для определения реперфузированных сегментов или расширения зоны ИМ.
Стойкая акинезия не всегда свидетельствует о недостаточной реперфузии. Для установления жизнеспособности акинетичного миокарда целесообразна ЭхоКГ, а также визуализация деформации после введения низких доз добутамина, контраста.
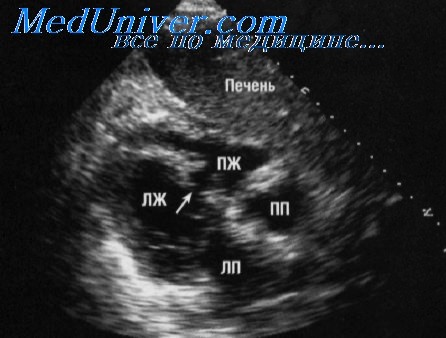
У больных после коронарной ангиопластики систолическая деформация была снижена, а постсистолическая — повышена, но отставала во время преходящей ишемии. Расслабление ишемизированных миокардиальных сегментов нарушается, и, следовательно, физиологические ранние диастолические истончение и удлинение замещаются постсистолическими утолщением и укорочением, поэтому локальную деформацию миокарла и ее скорость можно использовать как маркер острой ишемии.
С появлением эффективной реперфузионной терапии, проводимой во время ОИМ, частота распространения осложнений механического генеза снизилась, а также изменилось время их развития. Однако, поскольку осложнения могут угрожать жизни, достоверное определение времени связанных с инфарктом осложнений очень важно для оптимального ведения пациентов. Двухмерная ЭхоКГ и ДЭхоКГ с цветовым допплеровским картированием должны стать первыми методами исследования при подозрении на механические осложнения или у больных с нестабильной гемодинамикой.
Важным инструментом в самых сложных клинических ситуациях (в отделениях интенсивной терапии, у интубированных и послеоперационных больных, реанимированных после клинической смерти больных, тех, у кого по определенным причинам невозможна ТТЭхоКГ) стала ЧНЭхоКГ. При нормальной систолической функции у тяжелых и гемодинамически нестабильных больных следует подозревать механическое осложнение.
– Также рекомендуем “Появление систолического шума при инфаркте миокарда. Разрыв межжелудочковой перегородки, папиллярных мышц”
Оглавление темы “Эхокардиография при сердечной недостаточности и ишемической болезни сердца”:
1. Оценка диастолической функции. Оценка по ЭхоКГ диастолической функции сердца
2. Классификация диастолической дисфункции сердца. Нормальный тип диастолического наполнения
3. Легкая диастолическая дисфункция – 1-й степени. Умеренная диастолическая дисфункция – 2-й степени
4. Тяжелая диастолическая дисфункция – 3-й степени. Рестриктивное наполнение желудочка
5. Применение оценки диастолической функции. Значение ЭхоКГ диастолической функции миокарда
6. Эхокардиография при сердечной недостаточности. Объем левого желудочка
7. Эхокардиография при ишемической болезни сердца. Суммарный индекс подвижности стенок (WMSI)
8. Эхокардиография при остром инфаркте миокарда. Механические осложнения инфаркта миокарда
9. Появление систолического шума при инфаркте миокарда. Разрыв межжелудочковой перегородки, папиллярных мышц
10. Разрыв свободной стенки сердца – псевдоаневризма. Истинная аневризма и тромбоз левого желудочка
Источник
Эхокардиография при инфаркте миокарда. Диагностика осложнений инфаркта миокарда
Даже если при эхокардиографии удаётся обнаружить снижение регионарной сократимости левого желудочка, то оно может быть связано со “старым”, а не “свежим” инфарктом. К тому же, нарушение регионарной сократимости левого желудочка может наблюдаться при нестабильной стенокардии или при наличии так называемого миокарда в состоянии спячки на фоне хронически сниженного миокардиального кровотока без развития инфаркта миокарда.
Подтверждение диагноза ишемической болезни сердца (нарушение сократимости левого и/или правого желудочков)
Определение обширности поражения сердечной мышцы (прогноз, отбор больных для более “агрессивного55 лечения, в частности ангиопластики) Дифференциальная диагностика болевого синдрома в грудной клетке
• инфаркт миокарда
• расслаивающая аневризма аорты
• перикардит
• тромбоэмболия лёгочной артерии
Дифференциальная диагностика причин нарушения гемодинамики (гиповолемия, тампонада сердца, обширное поражение левого и, возможно, правого желудочка, разрыв сердца, разрыв межжелудочковой перегородки и т. д.) Диагностика ряда осложнений инфаркта миокарда
• аневризмы сердца
• псевдоаневризмы
• разрыва папиллярной мышцы (острой митральной недостаточности)
• разрыва межжелудочковой перегородки
• перикардита (возможность проведения перикардирцентеза под эхокардиографическим контролем)
• пристеночного тромба
Определение прогноза перед выпиской больного из стационара (либо на амбулаторном этапе реабилитации). Изучение процессов патологического ремоделирования (“перестройки”) левого желудочка (при наблюдении в динамике).
У больных с нестабильной гемодинамикой при подозрении на расслаивающую аневризму аорты, а также при плохом качестве изображения при трансторакальном сканировании предпочтительно проведение чреспищеводнои эхокардиографии (М. D. Cheitlin et al., 1997).
Диагностика нарушений регионарной сократимости — изюминка эхокардиографии. В исследовательских целях стенки левого желудочка делят на сегменты обычно от 12 до 16 сегментов). В частности, рекомендуемая Американским эхокардиографическим обществом схема предполагает разделение стенок левого желудочка на 16 сегментов (N. В. Schiller et al., 1989). На рисунке показан пример такого разделения миокарда левого желудочка на сегменты с использованием па-растернального (длинно- и короткоосевая проекции) и верхушечного (четырёх- и двухкамерная проекции) доступов. Для объективизации (полуколичественной оценки) сократимости миокарда левого желудочка движение его стенки в каждом из сегментов оценивают по специальной шкале. Например, норма — 1, гипокинез — 2, акинез — 3, дискинез — 4. Иногда выделяют также аневризматическое выпячивание — 5. Полученную сумму делят на число сегментов и получают усреднённый индекс сократимости стенок левого желудочка (В. А. Бобров и др., 1997). При нормальной сократимости во всех 16 сегментах левого желудочка усреднённый индекс его сократимости равняется единице (16:16=1).
– Также рекомендуем “Значение эхокардиографии. Практическая ценность эхокардиографии при инфаркте миокарда”
Оглавление темы “Диагностика и тактика при инфаркте миокарда”:
1. Тромбоз межжелудочковой ветви левой коронарной артерии. Инфаркт при тромбозе межжелудочковой ветви
2. Инфаркт при тромбозе левой огибающей артерии. Инфаркт при тромбозе правой коронарной артерии
3. Эхокардиография при инфаркте миокарда. Диагностика осложнений инфаркта миокарда
4. Значение эхокардиографии. Практическая ценность эхокардиографии при инфаркте миокарда
5. Эхокардиография при инфаркте правого желудочка. Значение эхокардиографии при патологии правого желудочка
6. Дифференциация инфаркта миокарда. Особенности инфаркта миокарда
7. Сердечно-легочная реанимация. Пути развития отечественной сердечно-легочной реанимации
8. Как проводить сердечно-легочную реанимацию? Техника сердечно-легочной реанимации
9. Отказ от искусственного дыхания при реанимации. Дефибрилляция сердца
10. Лечение инфаркта миокарда. Этапы терапии инфаркта миокарда
Источник
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
Общие сведения
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза. После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда.
Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности. Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. е. формирование постинфарктного рубца.
В клиническом течении инфаркта миокарда выделяют пять периодов:
- 1 период – предынфарктный (продромальный): учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель;
- 2 период – острейший: от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов;
- 3 период – острый: от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток;
- 4 период – подострый: начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4-8 недель;
- 5 период – постинфарктный: созревание рубца, адаптация миокарда к новым условиям функционирования.

Инфаркт миокарда
Причины инфаркта миокарда
Инфаркт миокарда является острой формой ИБС. В 97—98% случаев основой для развития инфаркта миокарда служит атеросклеротическое поражение венечных артерий, вызывающее сужение их просвета. Нередко к атеросклерозу артерий присоединяется острый тромбоз пораженного участка сосуда, вызывающий полное или частичное прекращение кровоснабжения соответствующей области сердечной мышцы. Тромбообразованию способствует повышенная вязкость крови, наблюдаемая у пациентов с ИБС. В ряде случаев инфаркт миокарда возникает на фоне спазма ветвей венечных артерий.
Развитию инфаркта миокарда способствуют сахарный диабет, гипертоничесая болезнь, ожирение, нервно-психическое напряжение, увлечение алкоголем, курение. Резкое физическое или эмоциональное напряжение на фоне ИБС и стенокардии может спровоцировать развитие инфаркта миокарда. Чаще развивается инфаркт миокарда левого желудочка.
Классификация инфаркта миокарда
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда:
- крупноочаговый
- мелкоочаговый
На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов). В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией.
В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда:
- трансмуральный – с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый)
- интрамуральный – с некрозом в толще миокарда
- субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду
- субэпикардиальный – с некрозом миокарда в зоне прилегания к эпикарду
По изменениям, фиксируемым на ЭКГ, различают:
- «Q-инфаркт» – с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда)
- «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда)
По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на:
- правожелудочковый
- левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки
По кратности возникновения различают инфаркт миокарда:
- первичный
- рецидивирующий (развивается в срок 8 недель после первичного)
- повторный (развивается спустя 8 недель после предыдущего)
По развитию осложнений инфаркт миокарда подразделяется на:
- осложненный
- неосложненный
По наличию и локализации болевого синдрома выделяют формы инфаркта миокарда:
- типичную – с локализацией боли за грудиной или в прекардиальной области
- атипичные – с атипичными болевыми проявлениями:
- периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная)
- безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная
- малосимптомную (стертую)
- комбинированную
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
- стадию ишемии (острейший период)
- стадию некроза (острый период)
- стадию организации (подострый период)
- стадию рубцевания (постинфарктный период)
Симптомы инфаркта миокарда
Предынфарктный (продромальный) период
Около 43% пациентов отмечают внезапное развитие инфаркта миокарда, у большей же части больных наблюдается различный по продолжительности период нестабильной прогрессирующей стенокардии.
Острейший период
Типичные случаи инфаркта миокарда характеризуются чрезвычайно интенсивным болевым синдромом с локализацией болей в грудной клетке и иррадиацией в левое плечо, шею, зубы, ухо, ключицу, нижнюю челюсть, межлопаточную зону. Характер болей может быть сжимающим, распирающим, жгучим, давящим, острым («кинжальным»). Чем больше зона поражения миокарда, тем более выражена боль.
Болевой приступ протекает волнообразно (то усиливаясь, то ослабевая), продолжается от 30 минут до нескольких часов, а иногда и суток, не купируется повторным приемом нитроглицерина. Боль сопряжена с резкой слабостью, возбуждением, чувством страха, одышкой.
Возможно атипичное течение острейшего периода инфаркта миокарда.
У пациентов отмечается резкая бледность кожных покровов, липкий холодный пот, акроцианоз, беспокойство. Артериальное давление в период приступа повышено, затем умеренно или резко снижается по сравнению с исходным (систолическое < 80 рт. ст., пульсовое < 30 мм мм рт. ст.), отмечается тахикардия, аритмия.
В этот период может развиться острая левожелудочковая недостаточность (сердечная астма, отек легких).
Острый период
В остром периоде инфаркта миокарда болевой синдром, как правило, исчезает. Сохранение болей бывает вызвано выраженной степенью ишемии околоинфарктной зоны или присоединением перикардита.
В результате процессов некроза, миомаляции и перифокального воспаления развивается лихорадка (от 3-5 до 10 и более дней). Длительность и высота подъема температуры при лихорадке зависят от площади некроза. Артериальная гипотензия и признаки сердечной недостаточности сохраняются и нарастают.
Подострый период
Болевые ощущения отсутствуют, состояние пациента улучшается, нормализуется температура тела. Симптомы острой сердечной недостаточности становятся менее выраженными. Исчезает тахикардия, систолический шум.
Постинфарктный период
В постинфарктном периоде клинические проявления отсутствуют, лабораторные и физикальные данные практически без отклонений.
Атипичные формы инфаркта миокарда
Иногда встречается атипичное течение инфаркта миокарда с локализацией болей в нетипичных местах (в области горла, пальцах левой руки, в зоне левой лопатки или шейно-грудного отдела позвоночника, в эпигастрии, в нижней челюсти) или безболевые формы, ведущими симптомами которых могут быть кашель и тяжелое удушье, коллапс, отеки, аритмии, головокружение и помрачение сознания.
Атипичные формы инфаркта миокарда чаще встречаются у пожилых пациентов с выраженными признаками кардиосклероза, недостаточностью кровообращения, на фоне повторного инфаркта миокарда.
Однако атипично протекает обычно только острейший период, дальнейшее развитие инфаркта миокарда становится типичным.
Стертое течение инфаркта миокарда бывает безболевым и случайно обнаруживается на ЭКГ.
Осложнения
Нередко осложнения возникают уже в первые часы и дни инфаркта миокарда, утяжеляя его течение. У большинства пациентов в первые трое суток наблюдаются различные виды аритмий: экстрасистолия, синусовая или пароксизмальная тахикардия, мерцательная аритмия, полная внутрижелудочковая блокада. Наиболее опасно мерцание желудочков, которое может перейти в фибрилляцию и привести к гибели пациента.
Левожелудочковая сердечная недостаточность характеризуется застойными хрипами, явлениями сердечной астмы, отека легких и нередко развивается в острейший период инфаркта миокарда. Крайне тяжелой степенью левожелудочковой недостаточности является кардиогенный шок, развивающийся при обширном инфаркте и обычно приводящий к летальному исходу. Признаками кардиогенного шока служит падение систолического АД ниже 80 мм рт. ст., нарушение сознания, тахикардия, цианоз, уменьшение диуреза.
Разрыв мышечных волокон в зоне некроза может вызывать тампонаду сердца – кровоизлияние в полость перикарда. У 2-3% пациентов инфаркт миокарда осложняется тромбоэмболиями системы легочной артерии (могут стать причиной инфаркта легких или внезапной смерти) или большого круга кровообращения.
Пациенты с обширным трансмуральным инфарктом миокарда в первые 10 суток могут погибнуть от разрыва желудочка вследствие острого прекращения кровообращения. При обширном инфаркте миокарда может возникать несостоятельность рубцовой ткани, ее выбухание с развитием острой аневризмы сердца. Острая аневризма может трансформироваться в хроническую, приводящую к сердечной недостаточности.
Отложение фибрина на стенках эндокарда приводит к развитию пристеночного тромбоэндокардита, опасного возможностью эмболии сосудов легких, мозга, почек оторвавшимися тромботическими массами. В более позднем периоде может развиться постинфарктный синдром, проявляющийся перикардитом, плевритом, артралгиями, эозинофилией.
Диагностика инфаркта миокарда
Среди диагностических критериев инфаркта миокарда важнейшими являются анамнез заболевания, характерные изменения на ЭКГ, показатели активности ферментов сыворотки крови. Жалобы пациента при инфаркте миокарда зависят от формы (типичной или атипичной) заболевания и обширности поражение сердечной мышца. Инфаркт миокарда следует заподозрить при тяжелом и продолжительном (дольше 30-60 минут) приступе загрудинных болей, нарушении проводимости и ритма сердца, острой сердечной недостаточности.
К характерным изменениям ЭКГ относятся формирование отрицательного зубца Т (при мелкоочаговом субэндокардиальном или интрамуральном инфаркте миокарда), патологического комплекса QRS или зубца Q (при крупноочаговом трансмуральном инфаркте миокарда). При ЭхоКГ выявляется нарушение локально сократимости желудочка, истончение его стенки.
В первые 4-6 часов после болевого приступа в крови определяется повышение миоглобина – белка, осуществляющего транспорт кислорода внутрь клеток.Повышение активности креатинфосфокиназы (КФК) в крови более чем на 50% наблюдается спустя 8—10 ч от развития инфаркта миокарда и снижается до нормы через двое суток. Определение уровня КФК проводят через каждые 6-8 часов. Инфаркт миокарда исключается при трех отрицательных результатах.
Для диагностики инфаркта миокарда на более поздних сроках прибегают к определению фермента лактатдегидрогеназы (ЛДГ), активность которой повышается позже КФК – спустя 1-2 суток после формирования некроза и приходит к нормальным значениям через 7-14 дней. Высокоспецифичным для инфаркта миокарда является повышение изоформ миокардиального сократительного белка тропонина – тропонина-Т и тропонина-1, увеличивающихся также при нестабильной стенокардии. В крови определяется увеличение СОЭ, лейкоцитов, активности аспартатаминотрансферазы (АсАт) и аланинаминотрансферазы (АлАт).
Коронарная ангиография (коронарография) позволяет установить тромботическую окклюзию коронарной артерии и снижение желудочковой сократимости, а также оценить возможности проведения аортокоронарного шунтирования или ангиопластики – операций, способствующих восстановлению кровотока в сердце.
Лечение инфаркта миокарда
При инфаркте миокарда показана экстренная госпитализация в кардиологическую реанимацию. В остром периоде пациенту предписывается постельный режим и психический покой, дробное, ограниченное по объему и калорийности питание. В подостром периоде больной переводится из реанимации в отделение кардиологии, где продолжается лечение инфаркта миокарда и осуществляется постепенное расширение режима.
Купирование болевого синдрома проводится сочетанием наркотических анальгетиков (фентанила) с нейролептиками (дроперидолом), внутривенным введением нитроглицерина.
Терапия при инфаркте миокарда направлена на предупреждение и устранение аритмий, сердечной недостаточности, кардиогенного шока. Назначают антиаритмические средства (лидокаин), ß-адреноблокаторы (атенолол), тромболитики (гепарин, ацетилсалициловая к-та), антогонисты Са (верапамил), магнезию, нитраты, спазмолитики и т. д.
В первые 24 часа после развития инфаркта миокарда можно произвести восстановление перфузии путем тромболизиса или экстренной баллонной коронарной ангиопластики.
Прогноз при инфаркте миокарда
Инфаркт миокарда является тяжелым, сопряженным с опасными осложнениями заболеванием. Большая часть летальных исходов развивается в первые сутки после инфаркта миокарда. Насосная способность сердца связана с локализацией и объемом зоны инфаркта. При повреждении более 50% миокарда, как правило, сердце функционировать не может, что вызывает кардиогенный шок и гибель пациента. Даже при менее обширном повреждении сердце не всегда справляется нагрузками, в результате чего развивается сердечная недостаточность.
По истечении острого периода прогноз на выздоровление хороший. Неблагоприятные перспективы у пациентов с осложненным течением инфаркта миокарда.
Профилактика инфаркта миокарда
Необходимыми условиями профилактики инфаркта миокарда являются ведение здорового и активного образа жизни, отказ от алкоголя и курения, сбалансированное питание, исключение физического и нервного перенапряжения, контроль АД и уровня холестерина крови.
Источник
