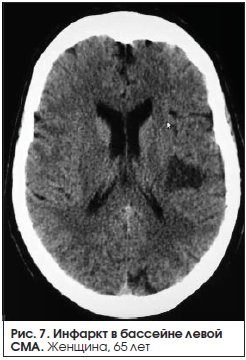
Ишемический инсульт в бассейне левой сма с геморрагической трансформацией
В статье рассматриваются варианты речевых нарушений и варианты изменений вещества головного мозга при инсульте в бассейне левой средней мозговой артерии
Введение
Для клиники левополушарных инсультов характерны речевые нарушения, среди которых наиболее значимой является афазия. Афазия, проявившаяся остро, указывает на нарушение кровообращения в бассейне средней мозговой артерии (СМА) [1].
Речевые процессы, как правило, обнаруживают значительную степень латерализации и у большинства людей зависят от ведущего (доминантного) полушария [2]. Необходимо учитывать, что в определении доминантного полушария, ответственного за речь, подход, связывающий доминантность только с праворукостью или леворукостью, является упрощенным. Профиль распределения функций между полушариями обычно многообразен [2, 3], что отражается на степени речевых нарушений и возможностях восстановления речи [4]. Многие люди проявляют лишь частичную и неодинаковую доминантность полушария в отношении разных функций [2]. Наряду с тем, что функция речи у правшей (≥90%) и большинства левшей (>50%) связана преимущественно с левым полушарием [1,4], существуют три исключения из этого правила:
1. Менее чем у 50% левшей функция речи связана с правым полушарием.
2. Аномическая (амнестическая) афазия может возникать при метаболических расстройствах и объемных процессах в головном мозге.
3. Афазия может быть связана с поражением левого таламуса [1].
Так называемую перекрестную афазию (афазию, вызванную ипсилатеральным к доминирующей руке церебральным поражением) в настоящее время относят только к правшам [4].
Область коры, ответственная за функцию речи, расположена вокруг Сильвиевой и Ролландовой борозд (бассейн СМА). Продукцию речи определяют четыре зоны этой области, тесно связанные между собой и расположенные последовательно вдоль заднепередней оси: зона Вернике (задняя часть верхней височной извилины), угловая извилина, дугообразный пучок (ДП) и зона Брока (задняя часть нижней лобной извилины) (рис. 1, 2) [1].


ДП представляет собой подкорковые волокна белого вещества, соединяющие зону Брока и зону Вернике. Есть сведения, что в левом полушарии ДП встречается в 100% случаев, тогда как в правом – только в 55% [5]. Ряд исследователей считают, что имеется несколько проводящих путей, участвующих в обеспечении речевой функции [6, 7]. Другие авторы получили достоверное подтверждение только роли ДП [8].
Патогенез дизартрических расстройств речи обусловливается различными по локализации очаговыми поражениями мозга. Нередко наблюдаются сложные формы дизартрии [9].
Цель исследования: изучить соотношение объема поражения головного мозга при инсульте в бассейне левой СМА и степени нарушения речи.
Материал и методы
В приемный покой КГБУЗ «Городская больница № 5» за 4-месячный период с подозрением на ОНМК поступили 356 человек. Все пациенты обследованы неврологом в приемном покое больницы, проведена оценка неврологического дефицита, отражено наличие/отсутствие нарушений речи. В дальнейшем, если состояние пациентов позволяло, им проводилось логопедическое исследование, в большинстве случаев – на следующий день после поступления в стационар.
В 124 случаях (каждый третий пациент) поставлен предварительный диагноз: ОНМК в бассейне левой средней мозговой артерии (ЛСМА). Данная локализация наиболее актуальна при изучении афазии у больных с ОНМК.
Всем пациентам при поступлении и большинству пациентов в динамике проводилась КТ головного мозга (томограф Bright Speed 16) с целью подтверждения/исключения очагового поражения головного мозга и уточнения объема поражения и локализации патологического участка.
По результатам КТ головного мозга у 32 (25,8%) человек из 124 выявлены типичные ишемические изменения в бассейне ЛСМА, из них у 7 при исследовании в динамике, т. е. при поступлении изменения еще не были явными (начальная стадия инсульта). В 5 (4,0%) случаях выявлены кровоизлияния: левосторонние медиальные гематомы и 1 случай субарахноидального кровоизлияния (САК). В 5 (4,0%) случаях из 124 выявлены инфаркты другой локализации (не в бассейне ЛСМА) (табл. 1).

В 22 (17,7%) случаях по данным КТ головного мозга не выявлено инфаркта в зоне интереса, но пациенты были госпитализированы в первичное неврологическое отделение для больных с ОНМК, т. к. у них выявлена значимая неврологическая симптоматика: явления атрофии вещества головного мозга, сосудистые очаговые изменения, сосудистый лейкоареоз, постинфарктные кисты. К этой группе отнесены также пациенты, у которых клиника была обусловлена транзиторной ишемической атакой.
В 60 (48,4%) случаях пациенты не были госпитализированы. В большинстве случаев ОНМК не подтвердилось (нет соответствующих изменений по данным КТ и в неврологическом статусе). В число не госпитализированных в отделение ОНМК вошли также пациенты с различными вариантами атрофии вещества головного мозга в сочетании со значимой неврологической симптоматикой, которые отказались от предложенной госпитализации. Единичные пациенты переведены в другие стационары, т. к. у них были выявлены травматические изменения черепа, головногомозга, новообразования. Часть пациентов переведена в дежурное отделение неврологии другого стационара, например, с диагнозом «остеохондроз».
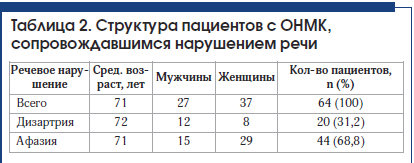
У 64 пациентов, госпитализированных в отделение ОНМК с инсультом, имелись нарушения речи (табл. 2). Детальный характер речевых нарушений определен логопедом. В 20 (31,2%) случаях у пациентов выявлены дизартрия и отсутствие афазии. В 2 случаях дизартрии сопутствовали дисфония и дисфагия. Выявлена афазия у 44 (68,8%) человек, из них в 7 случаях она регрессировала к моменту консультации логопедом на следующий день (в 2 случаях при регрессе афазии выявлены ишемические инфаркты). У 3 человек из группы с сенсомоторным вариантом афазии отмечалась выраженная дизартрия, у 9 человек – дисфагия. У 4 человек из группы с моторной афазией отмечались также явления дизартрии, в 1 случае – выраженная дизартрия.
Двум пациентам-левшам, у которых первоначально подозревался инсульт в бассейне левой СМА, с учетом результатов КТ головного мозга был поставлен диагноз: «Инсульт в бассейне правой СМА». В одном случае имелась афазия, которая регрессировала за 24 ч, в другом случае отмечена дизартрия.
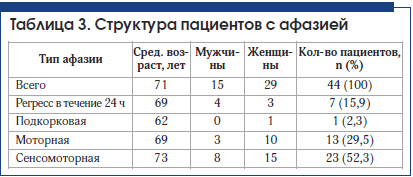
У пациентов с дизартрией без афазии выявлено 4 вида дизартрии: экстрапирамидная (3 случая), афферентная корковая (1 случай), бульбарная (1 случай), псевдобульбарная (8 случаев), в остальных случаях четко определить вид дизартрии было затруднительно, проявления были слабовыраженными (табл. 3).
В группах пациентов с дизартрией и регрессом афазии в течение 24 ч отмечается небольшое преобладание мужчин.
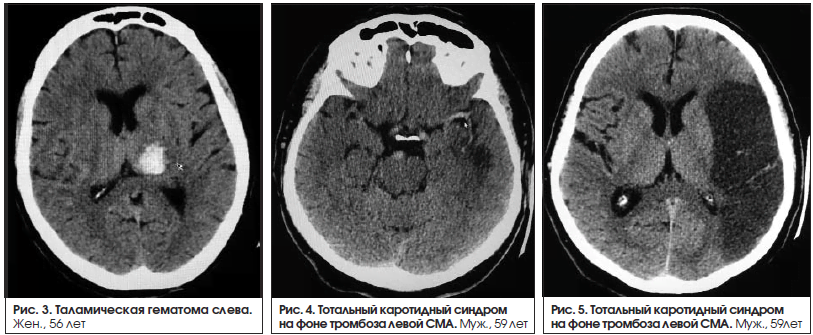
Афазии наблюдаются при поражениях коры головного мозга. В одном случае причиной афазии было поражение подкорковых структур левого полушария (медиальная внутримозговая гематома в таламусе (рис. 3). Нарушения речи в таких случаях не соответствуют ни одному из основных типов афазий. Поражение подкорковых структур можно заподозрить в тех случаях, когда амнестическая афазия сочетается с дизартрией или афазия – с гемипарезом. У данного пациента наблюдался правосторонний гемипарез 4 балла.
По классификации ишемических инсультов TOAST у госпитализированных пациентов с речевыми нарушениями выявлены следующие типы инсультов: в группе пациентов с сенсомоторной афазией наиболее частым был криптогенный вариант (47,6% случаев), на 2-м месте – кардиоэмболический (28,6%), на 3-м – атеротромботический (23,8%), отмечалась наибольшая частота повторных инсультов. В группе пациентов с моторной афазией также наиболее частым оказался криптогенный вариант, но в меньшем проценте случаев (41,7%), на 2-м месте – атеротромботический вариант (25,0%), на 3-м – кардиоэмболический (16,7%). В группе с дизартрией наиболее часто встречался лакунарный вариант (38,9% случаев), на 2-м месте – кардиоэмболический и криптогенный варианты (каждый по 22,2% случаев).
В группе больных с сенсомоторной афазией (23 человека) в 39,1% (9 человек) случаев у больных с сенсомоторной афазией был выявлен крупный инфаркт в бассейне ЛСМА доминантного полушария (рис. 4–6). В 47,8% (11 человек) случаев выявлен инфаркт малых размеров (рис. 7).


В 1 (4,3%) случае диагностировано САК вследствие разрыва аневризмы передней соединительной артерии, которое сочеталось с внутрижелудочковым кровоизлиянием. В 2 (8,7%) случаях КТ при поступлении и в динамике не выявила достоверного «свежего» участка инфаркта и постинфарктных изменений, у пациентов отмечены значительная атрофия вещества головного мозга, выраженный сосудистый лейкоареоз, клинический диагноз в обоих случаях: «Повторный ишемический инсульт в бассейне ЛСМА».
Основными группами сравнения стали 3 группы пациентов: с дизартрией (20 человек), моторной афазией (13 человек) и сенсомоторной афазией (23 человека). Критериями сравнения были объем и характер поражения, состояние сознания, сроки восстановления речи.
В таблице 4 в скобках указаны случаи соответствия локализации патологических изменений функционально-анатомическим зонам (при сенсомоторной афазии – обширной зоне вокруг Сильвиевой борозды; при моторной афазии – центру Брока; при дизартрии – локальным изменениям на уровне среднего мозга, подкорковых структур, коры).

Выявлены 3 медиальные гематомы слева, 2 из которых таламические (одна сопровождалась моторной афазией, другая – дизартрией), 1 – таламическая с распространением на внутреннюю капсулу (сопровождалась дизартрией). В одном случае в группе пациентов с дизартрией патологических изменений не выявлено, дизартрия регрессировала менее чем за 24 ч (табл. 5).

Случаев сопора и комы не было.
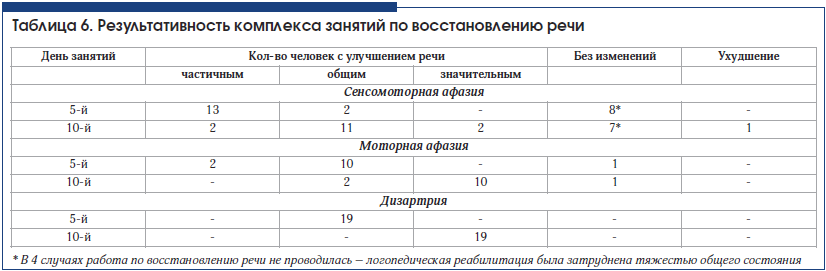
Достичь значительного улучшения речи у больных с сенсомоторной афазией в стационаре часто не удается (табл. 6). Поэтому логопед дает рекомендации каждому больному продолжать занятия в домашних условиях.
Результаты
Типичные «свежие» ишемические изменения, сопровождавшиеся афазией, по результатам КТ головного мозга выявлены у 30 человек. У половины из них диагностирована сенсомоторная афазия, и в свою очередь только у половины очаги поражения захватывали большую область вокруг Сильвиевой борозды. Не всегда локализация очагов поражения четко соответствовала локализации корковых речевых центров. Во всех 3 случаях медиальных гематом отмечены хорошая результативность восстановления речи (1 случай моторной афазии и 2 случая дизартрии), ее значительное улучшение.
Эти данные находят подтверждение в исследованиях афазического синдрома, проведенных во второй половине ХХ в., согласно которым у больных, переживших геморрагический инсульт, имеются возможности для восстановления речи, можно рассчитывать на благоприятный прогноз [10, 11]. В динамике степень нарушения речи, как правило, уменьшалась на фоне комплексного лечения, в т. ч. при сохранении гемодинамически значимого стеноза внутренней сонной артерии (по данным ультразвукового дуплексного сканирования), но при отсутствии рецидива инсульта или выраженной геморрагической трансформации.
Выводы
1. Сенсомоторная афазия при ишемическом инфаркте головного мозга может возникать как при поражении обширной области вокруг Сильвиевой борозды доминантного полушария, так и при локальном поражении в зоне одного из речевых корковых центров или зоне белого вещества между ними.
2. У больных с сенсомоторной афазией, вызванной инсультом, чаще, чем в других группах, отмечено оглушенное сознание, несмотря на то, что размер подтвержденного инфаркта более чем в половине случаев не был большим.
3. Фактические границы речевых центров индивидуально, по всей видимости, варьируют, поэтому не всегда обнаруживается совпадение точности предполагаемого анатомического поражения степени функциональных нарушений (афазии).
4. Полное соответствие объема выявленного инфаркта мозга объему речевых нарушений было отмечено в группе больных с сенсомоторной афазией, когда инфаркт был крупным.
5. Афазический синдром чаще встречается при криптогенном варианте ишемического инсульта, сенсомоторный вариант афазии часто возникает при повторных инсультах.
6. С учетом менее выраженной динамики восстановления речи в группе больных с сенсомоторной афазией этим больным следует продолжать логопедические занятия после выписки, чтобы достичь значительного/полного восстановления.
Источник
… в ряду внутричерепных кровоизлияний геморрагическая трансформация является наиболее частой формой.
Дефиниция. Термин «геморрагическая трансформация» (ГТ) отражает радиологические изменения, происходящие в инфаркте головного мозга, выявляемые при нейровизуализации – компьютерной (КТ) и магнитно-резонансной томографии (МРТ). ГТ инфаркта мозга расценивается большинством врачей как серьезное осложнение ишемического инсульта (ИИ), которое значительно ухудшает отсроченный прогноз и ограничивает возможности лечения и реабилитации (на неблагоприятный прогноз в случае развития ГТ указывают такие томографические признаки, как распространение геморрагии за пределы паренхимы мозга [интравентрикулярное и субарахноидальное кровоизлияния], а также наличие церебрального отека и масс-эффекта).
Чаще всего ГТ возникает при кардиоэмболическом подтипе ИИ, а также после проведения внутривенной тромболитической терапии (ТЛТ) и/или эндоваскулярного вмешательства у больных с острой окклюзией мозговых артерий, поэтому является одной из конечных точек безопасности в рандомизированных клинических исследованиях (РКИ). ГТ чаще возникает в сером веществе, особенно в коре головного мозга, из-за хорошо развитого коллатерального кровообращения (с которым связано увеличение реперфузионного повреждения).
Патогенез. По своей феноменологии ГТ является многофакторным патологическим процессом, который включает ишемию мозга, развитие коагулопатии, нарушение целостности ГЭБ и реперфузионное повреждение. Считается, что основным патофизиологическим механизмом развития ГТ является повышение проницаемости гематоэнцефалического барьера (ГЭБ). На экспериментальных моделях ИИ было показано, что снижение кровотока в питающей мозговой артерии и соответствующее уменьшение оксигенации тканей прежде всего влияют на микрососудистое русло. При этом наблюдаются повышение проницаемости и частичное разрушение ГЭБ, состоящего из эндотелиального слоя, базальной пластинки и периваскулярных астроцитов. В ответ на повреждение в микрососудистом эндотелии повышается экспрессия лейкоцитарных рецепторов адгезии, что сопровождается выбросом воспалительных цитокинов (интерлейкина 1β, фактора некроза опухоли α) и протеолитических ферментов (металлопротеиназ 1, 2, коллагеназы и эластазы). Это в свою очередь усугубляет дальнейшее повреждение базальной пластинки и приводит к образованию ее более крупных дефектов, что облегчает проникновение более крупных форменных элементов крови в мозговую ткань.
Введение тканевого активатора плазминогена замедляет процессы восстановления нормальной проницаемости за счет замедления образования комплексов тромбоциты-фибрин и прямого растворяющего действия на компоненты базальной пластинки гематоэнцефалического барьера. В связи с этим во всех крупных исследованиях системной тромболитической терапии (ECASS, NINDS, ATLANTIS) отмечалось повышение частоты геморрагической трансформации до 6,4% в сравнении с группой плацебо. Дополнительное влияние на целостность микрососудистого русла оказывают факторы, предрасполагающие к микроангиопатии: пожилой возраст, высокое артериальное давление (АД), сахарный диабет, церебральная амилоидная ангиопатия и непосредственно объем ишемического повреждения мозга.
Классификация. Основаниями для классификации ГТ служат [1] нейровизуализационные критерии и [2] сопутствующее неврологическое ухудшение. При нейровизуализации традиционно различают [1] геморрагические инфаркты (ГИ), которые представляют собой петехиальные геморрагии в зоне инфаркта, и [2] паренхиматозные гематомы (ПГ). Недостатки такого подхода – отсутствие однозначного разграничения между ПГ внутри и вне зоны инфаркта и четких критериев классификации субарахноидальных, субдуральных и внутрижелудочковых кровоизлияний. Для решения этих проблем была предложена расширенная гейдельбергская классификация, которая встретила всестороннее одобрение со стороны представителей ведущих РКИ по эндоваскулярным технологиям при ИИ:
Сопутствующее клиническое ухудшение позволяет подразделить ГТ на [1] асимптомную и [2] симптомную (сГТ). Связь ГТ с неврологическим ухудшением не всегда очевидна, т.к. существуют различные определения такого ухудшения и само ухудшение может произойти по причине, не имеющей отношения к ГТ. В РКИ по ТЛТ был предложен ряд дефиниций сГТ. Определения сГТ зависят от нейровизуализационных характеристик и степени неврологического ухудшения (подробнее в статье «Гемор-рагическая трансформация инфаркта мозга: классификация, патогенез, предикторы и влияние на функциональный исход» Д.Р. Хасанова, М.Н. Калинин, М.М. Ибатуллин, И.Ш. Рахимов, 2019 [см. «источники» в конце поста]). С учетом патогенеза ГТ также можно подразделить на [2] раннюю, возникающую в первые 18 – 24 ч от начала ИИ, и [2] отсроченную.
Факторы риска. За последние годы достоверно установлен ряд клинических предикторов ГТ у больных с ИИ. Тяжесть инсульта, объем инфаркта и время до реперфузии в значительной степеникоррелируют с ГТ. Как правило, клиническая тяжесть ИИ ассоциирована с объемом инфаркта. Время от начала ИИ до реперфузии является ключевым фактором, определяющим вероятность развития ГТ вне зависимости от применения ТЛТ. По экспериментальным и клиническим данным установлено, что реканализация, возникшая за пределами 6 ч от начала ишемии мозга, является независимым предиктором ГТ. К другим факторам риска ГТ относятся возраст, систолическое артериальное давление (АД), артериальная гипертензия, уровень гликемии и использование антиагрегантов. Метаанализ 55 клинических исследований показал, что ГТ после ТЛТ ассоциирована с пожилым возрастом, тяжелым инсультом, гипергликемией, фибрилляцией предсердий (ФП), застойной сердечной недостаточностью, почечной недостаточностью, предшествующим лечением антиагрегантами, лейкоареозом и острыми очагами ишемии при КТ до начала лечения. Эти клинические данные согласуются с экспериментальными моделями инсульта.
Диагностика. Для диагностики любой [формы] ГТ необходимо проводить нейровизуализацию в динамике. КТ и МРТ обладают одинаковой чувствительностью в выявлении ПГ. Однако ГИ чаще выявляются при высокопольной МРТ, [!!!] особенно с использованием градиентных режимов T2*-GRE и SWI/SWAN, поэтому частота обнаружения ГТ при МРТ в целом выше.
ГТ (КТ и МРТ) на radiopaedia.org [перейти]
Обратите внимание! Необходимо тщательно мониторировать пациентов с ИИ [в остром периоде] после ТЛТ и/или эндоваскулярного вмешательства, а также тех, у кого имеется высокий прогнозируемый риск ГТ (большинство сГТ при ИИ возникают в первые 24 ч и только около 10 – 15% – после 24 ч; несмотря на то, что любая ГТ может возникнуть через 7 суток и позже, большинство сГТ после ТЛТ возникают в течение первых 36 ч; связь сГТ с коагулопатией, обусловленной ТЛТ, за пределами 36 ч кажется маловероятной; спонтанная ГТ без применения ТЛТ является следствием ишемического повреждения ГЭБ и возникает, главным образом, в течение первых 2 недель после ИИ). Для раннего выявления ГТ необходимо проводить своевременную и регулярную нейровизуализацию в динамике. ПГ-2 чаще всего ассоциированы с высокой летальностью и неблагоприятным функциональным исходом.Подробнее о ГТ в следующих источниках:
статья «Геморрагическая трансформация инфаркта мозга: классификация, патогенез, предикторы и влияние на функциональ-ный исход» Д.Р. Хасанова, М.Н. Калинин, М.М. Ибатуллин, И.Ш. Рахимов; ФГБОУ ВО «Казанский государственный медицинский университет»; ГАУЗ «Межрегиональный клинико-диагностический центр», Казань; Елабужский институт (филиал) ФГАОУ ВО «Казанский (Приволжский) федеральный университет», г. Елабуга (журнал «Анналы клинической и экспериментальной неврологии» №2, 2019) [читать];
статья «Геморрагическая трансформация инфаркта мозга в постинсультном периоде (клиническое наблюдение)» В.В.Гудкова, Л.В.Губский, И.Л.Губский, Г.В.Панов, Н.Н.Волкова, А.К.Никогосова, Т.А.Логунова, А.Г.Гуцалюк, В.П.Подерина, Е.И.Кимельфельд, Е.В.Усанова; ГБОУ ВПО Российский национальный исследовательский медицинский университет им. Н.И. Пирогова МЗ РФ, Москва; ГБУ Госпиталь для ветеранов войн №3 ДЗМ, Москва; ГБОУ ДПО Российская медицинская академия последипломного образования МЗ РФ, Москва (журнал «Consilium Medicum» №2, 2016) [читать];
статья «Возможность прогнозирования развития геморрагической трансформации при реперфузионной терапии ишемического инсульта в популяции пациентов Свердловской области» Праздничкова Е.В., Алашеев А.М., Белкин А.А., Волкова Л.И.; «Свердловская областная клиническая больница №1», Екатеринбург; ГБОУ ВПО «Уральский государственный медицинский университет» МЗ РФ, Екатеринбург (журнал «Неврология, нейропсихиатрия, психосоматика» №1, 2015) [читать]
Источник
