Инфаркта миокарда 3 степени
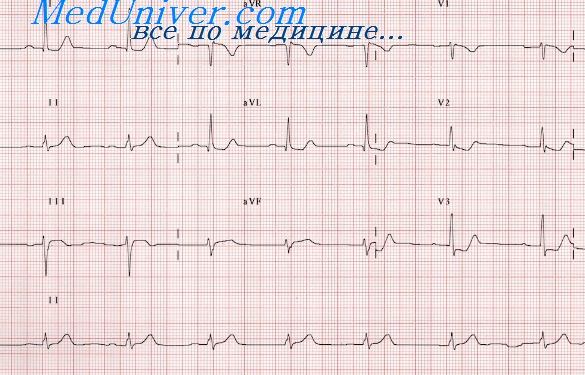
Выписной эпикриз
Больная ххх 69 лет (18.08.36), проживающая по адресу г. Сегежа ул. Комсомольская, поступила в хирургическое отделение Республиканской больницы г. Петрозаводска по направлению из Ладвигской больницы 09.09.2005 в 20.30
Клинический диагноз:
а) Основное заболевание — Язвенная болезнь, язва постбульбарного отдела двенадцатиперстной кишки, язва тела желудка, ассоциированные с Helicobacter pylori, впервые выявленные, осложнившиеся гастродуоденальным кровотечением
б) Осложнения основного заболевания — хроническая постгеморрагическая железодефицитная анемия, средней степени тяжести вследствие кровотечения из язвенного дефекта и алиментарной недостаточности.
в) Сопутствующие заболевания — Острая внутрибольничная правосторонняя нижнедолевая пневмония, бессимптомная парауретральная киста; полипы желчного пузыря.
На момент поступления: жалобы на общую слабость, разбитость, вялость; на ноющие, давящие, не иррадиирующие боли средней интенсивности в эпигастральной области, не связанные со временем суток и физической нагрузкой; после приема пищи (особенно молока) больная отмечала некоторое улучшение. Боли сопровождались изжогой (ощущением чувства жжения за грудиной), отрыжкой, легкой тошнотой, периодическими запорами; в течение последних четырех дней — черный стул. Также больная отмечает легкое похудание, снижение аппетита и нарушение сна (бессонница) в течение последних 1,5 лет.
Из анамнеза:
Подобные жалобы впервые появились в марте 2004 г; в середине марта 2004 г. внезапно добавились жалобы на общую слабость, разбитость, вялость, а также появление черного стула, что и заставило больную обратиться к врачу в апреле 2004 г. после чего она была госпитализирована в Ладвигскую больницу, где был поставлен диагноз анемии. Был проведен курс терапии энтеральными препаратами железа, с положительным эффектом.
В январе 2005 г. больная вновь поступила в то же медицинское учереждение в связи с аналогичными жалобами (кроме того, отмечалось легкое похудание, снижение аппетита и нарушение сна); был поставлен тот же диагноз и снова начата терапия препаратами железа для энтерального применения. В процессе лечения выявлена их непереносимость (появилась тошнота, периодическая рвота), поэтому больная переведена на терапию паренеральными препаратами железа (Феррум-лек), с положительным эффектом.
Текущее обострение с 04.09.2005, когда остро появились вышеперечисленные жалобы, в связи с чем больная срочно госпитализирована в хирургическое отделение Республиканской больницы.
Острый инфаркт миокарда, желудочковая экстрасистолия, кардиогенный шок, нестабильная стенокардия, артериальная гипертензия 3-й степени, атеросклероз аорты и коронарных артерий, кардиосклероз
Стенокардия 3-4 степени. Инфаркт миокарда
У пациентов со стабильной стенокардией уровни натрийуретических пептидов типа В повышены сообразно степени индуцированной ишемии миокарда и степени вовлечения венечных артерий. Однако BNP и NT-proBNP имеют недостаточную чувствительность и специфичность, чтобы использоваться для указания на ишемию миокарда. В результате они не являются полезными диагностическими маркерами в обычной клинической практике этой патологии. Было показано, что натрийуретические пептиды типа В служат важными прогностическими факторами смертности, не зависящей от функции ЛЖ, клинических признаков СН и традиционных факторов риска. Аналогично в результатах многочисленных клинических исследований сообщалось, что пациентам с симптомами ОКС и повышенными уровнями натрийуретических пептидов типа В присуща в 3-5 раз более высокая смертность по сравнению с такими же больными с более низкими уровнями NT-proBNP или BNP. В самом деле, связь повышения уровней натрийуретических пептидов типа В со смертностью остается сильной даже после компенсации по возрасту, классу СН по Киллип (Killip), ФВ ЛЖ, определенной по данным ЭхоКГ и установленному значению шкалы клинического риска, например TIMI.
Миокардиальный стресс. ведущий к нейрогуморальной активации со стороны сердца, может мониториро-ваться измерением системных уровней натрийуретических пептидов, секретируемых сердцем. Предсердные натрийуретические пептиды типа A (ANP) синтезируются преимущественно в предсердиях, в то время как натрийуретические пептиды типа В (BNP) синтезируются преимущественно в миокарде желудочков сердца. Оба типа пептидов синтезируются как прогормоны (proANP и proBNP), которые после секреции преобразуются в биологически активные пептиды (ANP и BNP) и N-терминальные фрагменты прогормона (NT-proANP и NT-proBNP). Натрийуретические пептиды высвобождаются в основном в ответ на увеличение степени растяжения или напряжения стенки и вовлекаются в регуляцию АД, объема крови и баланса натрия путем модуляции натрийуреза, вазодилатации и ингибирования РААС, так же как и симпатической нервной системы. В патологических состояниях уровни BNP и NT-proBNP пропорционально становятся выше, чем уровни ANP и NT-proANP, что привлекает больше интереса с точки зрения применения в клинической практике.
Выраженная СН — острая и хроническая
Расслоение аорты
Заболевания аортальных клапанов
Гипертрофическая кардиомиопатия
Тахиаритмия или мерцательная брадиаритмия, или блокада сердца
Синдром апикального вздутия
Острый некроз скелетных мышц с повреждением сердца
Легочная эмболия, тяжелая легочная гипертензия
ХПН
Острая неврологическая болезнь, включая инсульт или субарахноидальное кровоизлияние
Инфильтрирующие болезни, например амилоидоз, гемохроматоз, саркоидоз и склеродермия
Воспалительные заболевания, например миокардиты или эндо- и перикардиты, распространившиеся на миокард
Лекарственная токсичность или токсины
Серьезно больные пациенты, особенно с дыхательной недостаточностью или сепсисом
Ожоги, особенно если поражено больше 30% поверхности тела
Чрезмерные физические усилия
Повышение уровней сердечных тропонинов часто обнаруживается у пациентов с терминальным поражением почек в отсутствие нестабильной стенокардии.
Единственным препятствием, исходно стоявшем на пути общего признания определения уровня тропонинов «золотым стандартом» в диагностике поражений миокарда. стало наблюдение повышения концентрации тропонинов в редких случаях, обусловленных внесердечными причинами, чаще всего у пациентов с ХПН. Хотя измерение уровней сердечных тропонинов в целом расценивается как высокоспецифичное для повреждения миокарда, повышение уровня сердечного тропонина без повреждения миокарда было описано для ряда состояний, включая черепно-мозговые травмы, субарахноидальные кровоизлияния, эндокринные заболевания, полимиозит, дерматомиозит и онкогематологические заболевания, (табл. 16.9). Проведенные в отделениях интенсивной терапии исследования показали, что уровни тропонина повышены у септических больных. Важно, что концентрации тропонина у таких больных коррелировали с дисфункцией ЛЖ и наличием полиорганной недостаточности. Однако остается неизвестным, может ли подъем уровня тропонина повлиять на длительность госпитализации или выживаемость.
Клинической разницы между тропонином T и тропонином I не обнаружено. Разница в результатах исследований объясняется преимущественно различиями в критериях включения, составе выборки и применением наборов для анализа, имеющих разную диагностическую чувствительность. Диагностические значения должны быть основаны на результатах тщательно проведенных клинических испытаний для индивидуальных типов наборов для анализа на тропонин I; их генерализация для разных типов наборов для анализа на тропонин I недопустима
Подозрение на ОКС соответствует наличию потенциально угрожающего состояния, и экономия времени на этапе выбора схемы лечения и в ходе дальнейшего ведения пациента может стать решающей. В проспективных исследованиях было показано, что стратификация рисков, основанная на протоколах, предусматривающих немедленное проведение исследования тропонина при госпитализации больного по скорой, и повторное исследование спустя 6-12 ч являются, в целом, надежными. Одиночного исследования, проведенного при госпитализации больного, недостаточно для стратификации рисков, поскольку оно упускает до 10% больных с высокой степенью риска.
#35 дожим кисти #Tai-Chi Ch’uan (Martial Art) #armlock techniques уроки тай чи Болевые приемы
Источник
При поступлении больного в стационар я, как врач-кардиолог, всегда определяю, на каком этапе находится заболевание: провожу ЭКГ в динамике, оцениваю результаты анализа крови и общее состояние пациента. Это позволяет определиться с дальнейшими действиями по оказанию помощи. Давайте разберемся, какие выделяют стадии инфаркта миокарда по времени, чем они отличаются друг от друга и что происходит в каждый период с сердечной мышцей.
Инфаркт миокарда по стадиям
У большей части пациентов инфаркт миокарда развивается постепенно. Сначала у больного со стенокардией увеличивается частота и продолжительность сердечных приступов, снижается порог физической нагрузки, возникают боли в загрудинной области, которые не беспокоили уже много лет. А «Нитроглицерин» не купирует болевой синдром так быстро, как раньше.
После начала приступа и появления стойкой ишемии и некроза выделяется 4 стадии развития инфаркта, каждая имеет свои клинические симптомы и проявления на кардиограмме.
Острейшая стадия
Длительность — от 10–20 минут до нескольких часов. Нестабильная стенокардия перерастает в инфаркт:
- Резко возникшая боль уже не купируется нитратами и проходит после использования наркотических анальгетиков.
- Боль давящая, сжимающая, пекущая.
- При классическом проявлении определяется в груди слева, отдает под левую лопатку, ключицу, шею, нижнюю челюсть, половину головы.
При объективном осмотре:
- Бледные кожные покровы, холодный пот, синий носогубный треугольник.
- Аускультативно отмечается приглушение I тона в зоне верхушки.
- Частота пульса меняется. По данным статистики, нарушение ритма и проводимости, тахикардия или брадикардия, наблюдается у 90% больных.
- Давление сначала повышается, а потом падает.
- Появляется одышка, в некоторых случаях наблюдаются признаки легочной недостаточности.
- В анализе крови отмечается рост уровня тропонина и миоглобина.
На ЭКГ отмечается резкое снижение зубца R, значительный подъем ST выше изолинии и его слияние с T (монофазная кривая).
Морфология ткани изменяется. Очаг повреждения имеет отчетливые границы, миокард становится бледным, отечным. На вторые сутки область ишемии желтеет, у нее появляется демаркационная линия.
Подробнее о признаках инфаркта на ЭКГ можно прочесть здесь.
Острая
Продолжается до 10 дней. Ангинозная боль, характерная для острейшей стадии, проходит. Сохраняется пониженное давление, нарастают признаки сердечной недостаточности. Почти всегда прогрессируют нарушения ритма и проводимости. В первые двое суток на первое место выходит резорбционно-некротический синдром:
- Повышается температура, не выше 37,5 °C. Если показатель выше, то это свидетельствует о присоединении инфекции. Продолжается 5–7 дней.
- Увеличивается уровень лейкоцитов в крови, преимущественно нейтрофилов, увеличивается СОЭ.
- В крови определяются маркеры некроза сердечной мышцы (повышение миоглобина, АЛТ, АСТ, тропонина).
На кардиограмме острая стадия развившегося инфаркта миокарда проявляется четко, особенно при обширном поражении. В это время происходит формирование патологического зубца Q, T становится отрицательным, ST сохраняет позицию выше изолинии.

На гистологическом срезе хорошо виден участок повреждения с лизисом ядер и некротическим распадом клеток (стрелка вверху). Внизу указатель обозначает демаркационную область с инфильтрацией ткани лейкоцитами, образованием новых капилляров и отека. Она находится на границе области инфаркта и нормального миокарда.

Подострая
Подострая стадия инфаркта миокарда длится от 10 дней до 1–2 месяцев. Для этого периода характерными признаками являются:
- Полное прекращение боли в сердце.
- У многих больных — восстановление проводимости и ритма.
- Нормализация дыхания.
- Тоны сердца становятся громче или остаются приглушенными (в зависимости от степени повреждения).
- Температура и картина общего анализа крови приходит в норму.
- Давление нормализуется.
ЭКГ: Зубец Q переходит сразу в R, при крупноочаговом поражении R исчезает, желудочковый комплекс приобретает вид QS, ST возвращается к изоэлектрической линии, T становится отрицательным.
Если сделать срез в это время и рассмотреть микропрепарат, то на нем будет четко определяться область поражения серо-розового оттенка с красной каймой по периферии.
Рубцевание
Развивается на протяжении 2–6 месяцев от начала заболевания. В стадии рубцевания (формирования кардиосклероза) наблюдаются восстановительные процессы, миокард приспосабливается к работе в новых условиях:
- У многих пациентов развивается гипертрофия левого желудочка (компенсаторный механизм).
- Постепенно возвращается к исходным показаниям пороговая толерантность к физическим нагрузкам.
- Очень редко наблюдаются эпизоды нарушения ритма, у большей части больных ритм нормализуется.
- Возрастает вероятность появления истерий, фобий и других неврологических отклонений.
Кардиограмма показывает уменьшение патологического зубца Q, ST сохраняется на изолинии, снижается амплитуда отрицательного T или он переходит на изолинию. Это признак формирования рубца.
При гистологическом исследовании это выглядит как белое образование, немного западающее внутрь и состоящее из грануляций. Повторные инфаркты, стенокардия и гипертония приводят к развитию кардиосклероза там, где таких участков много и они не могут выполнять прежние функции. Морфогенез таких изменений хорошо виден на приложенном фото.

Ниже можно увидеть динамику изменения лабораторных показателей, в зависимости от времени развития некроза.
Клинический случай
В стационар поступил пациент с сильными загрудинными болями, которые отмечались на протяжении трех дней. Прием анальгетиков и «Нитроглицерина» не приносил облегчения. Ранее был поставлен диагноз стенокардии напряжения ФК II. За неделю до приступа испытал сильный стресс, состояние ухудшалось. На кардиограмме определился крупноочаговый инфаркт с локализацией в передней стенке, острая стадия. В крови — повышение миоглобина и тропонина.
Через месяц стационара пациент был выписан для лечения в амбулаторных условиях. ЭКГ показало рубцевание в области поражения, показатели крови пришли в норму.
Совет специалиста
При появлении первых признаков инфаркта меры следует принимать незамедлительно. Я советую сразу звонить в скорую помощь, и пока врач едет, обеспечить больному полный покой, усадить или уложить в такое положение, которое максимально облегчит состояние. Дать «Корвалол», «Нитроглицерин», «Аспирин», проветрить помещение.
Самым опасным является острейший период, который обычно проявляется очень сильной болью, одышкой, нарушениями ритма. От быстроты и правильности действий находящегося рядом человека зависит жизнь пациента. Лучше всего при вызове врача описать симптомы, чтобы могла приехать специализированная бригада, которая снимет ЭКГ, даст кислород и введет препараты для ограничения зоны некроза.
Источник
Третья стадия инфаркта миокарда. ЭКГ признаки подострой стадии инфаркта миокардаВ дальнейшем на ЭКГ отмечается медленное уменьшение глубины зубца Т (третья — «подострая стадия»). Обычно зубец Т остается максимально глубоким до 20 — 25-го дня, затем постепенно его глубина уменьшается до 40 — 50-го дня болезни, когда он либо становится положительным, либо изоэлектричным, либо остается отрицательным неглубоким на длительное время. Гистологическое исследование сердца 24 из 32 умерших в период повторной инверсии зубца Т (7 — 40-е сутки инфаркта) выявило наряду с признаками расплавления и организации очага некроза, в зоне организующихся повреждений и в непораженном миокарде на границе и вблизи инфарктного очага инфильтраты из лимфоидных и плазматических клеток, с отдельными эозинофильными клетками и гистиоцитами. Эту гистологическую картину миокарда в перифокальной зоне мы расценивали как проявление аутоаллергической (иммунной) реакции типа очагового миокардита (М. И. Кечкер, Т. А. Наддачина, 1970). В тех редких случаях (3 из 32 случаев в данном исследовании), где на ЭКГ и на 14 — 16-е сутки отсутствовала повторная инверсия зубца Т, при морфологическом исследовании определялось много фокусов ареактивных некрозов без лимфоцитарных и плазмоклеточных инфильтратов. Это свидетельствовало об отсутствии аутоиммунной реакции. Очаговый воспалительный процесс в миокарде может изменить потенциал мембраны пораженных клеток в период быстрой реполяризации и отклонить вектор Т, так же как и ишемия миокарда, в сторону, противоположную локализации процесса. Это ведет к регистрации на ЭКГ отрицательного симметричного зубца Т. Поэтому наличие локализованной, именно вокруг организующегося очага некроза, воспалительной аутоиммунной реакции в период 2 — 4-й недели инфаркта, вероятно, является причиной появления и нарастания глубины повторной инверсии зубца Т ЭКГ. Таким образом, в этих работах и следующих нами была сформулирована аутоиммунная гипотеза генеза повторной инверсии зубца Т ЭКГ на 2 — 3-й неделе острого периода инфаркта. В соответствии с выдвинутой аутоиммунной гипотезой мы описали полифазную динамику направления зубца Т ЭКГ в течении инфаркта миокарда, состоящую из 5 фаз: — I фаза — положительный высокий («гигантский») зубец Т, сливающийся с приподнятым сегментом RS – Т в первые часы инфаркта;
— III фаза — промежуточная фаза изменений зубца Т (начинается на 3 — 6-е сутки инфаркта), характеризуется уменьшением отрицательности, прекращением углубления или появлением вновь положительного (или сливающегося с сегментом RS – Т) зубца Т, связана с уменьшением ишемии и улучшением кровоснабжения пораженной области; — V фаза — постепенное уменьшение глубины зубца Т в течение подострой стадии инфаркта (4 — 7 недели) с превращением в части случаев в положительный зубец Т (уменьшение иммунной воспалительной реакции миокарда в процессе образования рубца). Такая же полифазная динамика реципрокных изменений зубца Т (но с прямо противоположным его направлением) наблюдается в отведениях с положительным полюсом с противоположной стороны от инфарктного очага. Учебное видео ЭКГ при инфаркте миокарда
– Также рекомендуем “Четвертая стадия инфаркта миокарда. Распространенный передний инфаркт миокарда” Оглавление темы “ЭКГ при инфаркте миокарда”: |
Источник

