Инфаркт почки и эндокардит

Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Симптомы инфекционного эндокардита обусловлены сочетанием симптомов инфекционного поражения клапанов сердца, тромбоэмболии из вегетации, бактериемии с метастатическими очагами в различных органах и иммунопатологических процессов.
- Инфекция на клапанах.
- Неспецифические симптомы инфекционного эндокардита: лихорадка, озноб, ночная потливость, слабость, анорексия, потеря массы тела, артралгии, миалгии, спленомегалия.
- Специфические симптомы инфекционного эндокардита и поражения клапанов: появление или изменение характера шумов в результате формирования клапанных пороков, перфорации створок, отрыва сухожильных хорд, разрыва клапана. Эти процессы более чем у 50% пациентов осложняются развитием недостаточности кровообращения.
- Артериальные эмболии фрагментами вегетации: тромбоэмболия сосудов головного мозга (острое нарушение мозгового кровообращения), инфаркт миокарда, ТЭЛА, окклюзия мезентериальных артерий с развитием картины «острого живота», инфаркт селезёнки, инфаркт почки, окклюзия крупных периферических артерий (гангрена конечности).
- Бактериемия с метастатическими очагами в органах: при высокой вирулентности возбудителя развиваются абсцессы почек, миокарда, головного мозга и др.
- Иммунопатологические проявления: гломерулонефрит, миокардит, полиартрит, кожный васкулит (сосудистая пурпура, узелки Ослера).
[1], [2], [3], [4], [5], [6], [7]
Поражение почек
Поражение почек при инфекционном эндокардите отличается многообразием и может быть связано как с самим заболеванием, так и с применяемыми для его лечения антибактериальными препаратами.
Поражение почек при инфекционном эндокардите
Характер иоражеиия | Причина поражения |
Инфаркт почки | Тромбоэмболия из вегетации (ветви почечной артерии) |
Иммунопатологические реакции (васкулит почечных сосудов) | |
Острый кортикальный некроз | Тромбоэмболия (ствол почечной артерии) |
Деструкция клапана с развитием острой сердечной недостаточности | |
Абсцессы почек | Бактериемия с метастатическими очагами в органах |
Гломерулонефрит | Иммунопатологические реакции |
Амилоидоз | Хроническое течение инфекционного эндокардита |
Лекарственная нефропатия (острый интерстициальный нефрит, острый канальцевый некроз) | Антибактериальные препараты |
Поражение почек осложняет течение инфекционного эндокардита у 50-80% пациентов, причём у 10% из них развивается хроническая почечная недостаточность. Наиболее частым вариантом поражения почек, в ряде случаев определяющим прогноз, является гломерулонефрит, который возникает при инфекционном эндокардите в 20-25% случаев. На связь между гломерулонефритом и инфекционным эндокардитом впервые обратил внимание М. Lohlein, описавший в 1910 г. фокальные гломерулярные изменения, которые он расценил как проявления «бактериальной эмболии», у умершего от инфекционного эндокардита пациента. Уже в 1932 г. A. Bell подверг сомнению эмболическую природу гломерулонефрита при инфекционном эндокардите и предположил ведущую роль иммунных механизмов в развитии поражения почек. В настоящее время иммунная природа гломерулярного поражения не вызывает сомнения и подтверждается развитием гломерулонефрита при эндокардите правых отделов сердца, когда исключена эмболия в сосуды почек, наличием гипокомплементемии, обнаружением у больных с инфекционным эндокардитом циркулирующих и фиксированных в клубочках иммунных комплексов, а также специфических бактериальных антигенов в их составе.
Основные симптомы гломерулонефрита при инфекционном эндокардите – гематурия, нередко достигающая степени макрогематурии, и протеинурия. Нефротический синдром развивается у 30-50% больных, артериальная гипертензия не характерна. У некоторых пациентов поражение почек манифестирует остронефритическим синдромом или нарастающей почечной недостаточности вследствие развития быстропрогрессирующего гломерулонефрита. В редких случаях симптомы поражения почек могут предшествовать развёрнутой клинической картине эндокардита («нефритическая» маска инфекционного эндокардита).
По спектру клинических проявлений и морфологической картине гломерулонерфрит при инфекционном эндокардите аналогичен «шунт-нефрит» – постинфекционный гломерулонерфрит, который развивается у больных с инфицированным вентрикулоатриальным шунтом (соединяет желудочек мозга с правым предсердием), установленным для устранения окклюзионной гидроцефалии. В 80% случаев возбудителем «шунт-инфекции» бывает эпидермальный стафилококк, колонизирующий дистальную (атриальную) часть шунтирующей системы либо в момент операции по её установке, либо, чаще, вследствие транзиторной бактериемии, аналогично тому, как это происходит с инфицированием эндокарда при инфекционном эндокардите. Почечной манифестации «шунт-нефрита», как правило, предшествует клиническая картина подострого сепсиса с эпизодами лихорадки, недомоганием, анемией, спленомегалией. У большинства больных отмечают симптомы внутричерепной гипертензии (головные боли, тошнота, рвота, сонливость) вследствие дисфункции шунта, связанной с его инфицированием. У пациентов с «шунт-инфекцией» развиваются также системные проявления (артриты, кожный некротизирующий васкулит). Самые частые почечные проявления «шунт-нефрита» – гематурия (макрогематурия у трети больных) и протеинурия. Нефротический синдром и артериальная гипертензия возникают примерно в половине случаев, нарушения функций почек – в 60%. В последние годы отмечена тенденция к трансформации как клинической, так и морфологической картины «шунт-нефрита»: всё чаще при биопсии почки выявляют экстракапиллярный гломерулонерфрит с полулуниями при преобладании клинических симптомов быстропрогресирующего гломерулонефрита. Основной причиной прогрессирования «шунт-нефрита» считают длительное персистирование инфекции, связанное главным образом с несвоевременно установленным диагнозом.
Источник
… клиника инфекционного эндокардита характеризуется широким спектром органных и системных проявлений.
Поражение почек от гломерулонефрита до абсцесса почки – считается классическим при инфекционном эндокардите и нередко является первым клиническим проявлением заболевания. В «доантибиотическую эру» гломерулонефрит встречался часто, почти в 75% случаев инфекционного эндокардита, являясь нередко и непосредственной причиной смерти больных. Во второй половине прошлого века отмечена тенденция к уменьшению частоты гломерулонефрита, которую большинство авторов оценивают в настоящее время, как 24-48% случаев.
Проявления почечной патологии практически однотипны: протеинурия, гематурия, нефритический синдром, реже нефротический синдром и артериальная гипертензия. Наиболее часто патология почек проявляется умеренным мочевым синдромом с широкой вариабельностью выраженности протеинурии, микрогематурии, цилиндурии.
По данным Н.С. Чипигиной, К.С. Озерецкого (РГМУ, Москва, 2003) изменения в анализах мочи наблюдались у 60% больных инфекционным эндокардитом, в том числе только изолированная умеренная протеинурия на фоне лихорадки у 26% больных. Стойкие изменения в анализах мочи, позволяющие диагностировать гломерулонефрит – сочетание микрогематурии с протеинурией и цилиндрурией отмечены в 33,1% всех наблюдений. Частота гломерулонефрита составила 34,1% среди 209 больных первичным инфекционным эндокардитом и 24% среди 108 со вторичным инфекционным эндокардитом. Гломерулонефрит чаще возникает при длительном течении заболевания.
«Почечные маски» – нефритический и нефротический синдромы, макрогематурия, азотемия в дебюте заболевания наблюдаются редко, но могут затруднять диагностику инфекционного эндокардита, так как ошибочно расцениваются как проявления хронического гломерулонефрита, хронического пиелонефрита, геморрагической лихорадки с почечным синдромом. О «почечной маске» можно говорить примерно в 4-5% случаев инфекционного эндокардита: макрогематурия наблюдается примерно в 4-9%, нефротический синдром – у 1-2% больных инфекционным эндокардитом.
Почечная недостаточность при инфекционном эндокардите обычно возникает вследствие иммунокомплексного диффузного гломерулонефрита, реже относится к проявлениям нарушенной гемодинамики или токсичности, связанной с антибиотикотерапией (интерстициальный нефрит или повреждение, индуцированное аминогликозидами).
Частота развития почечной недостаточности при инфекционном эндокардите оценивается довольно противоречиво – от 5% до 50% в разных группах больных. Риск почечной недостаточности выше у пожилых больных, при артериальной гипертензии в анамнезе, тромбоцитопении, стафилококковом инфекционном эндокардите, инфекционном эндокардите на искусственных клапанах; возраст и степень тромбоцитопении независимо связаны с повышенным риском развития почечной недостаточности. По данным S. Mouli и соавт., почечная недостаточность занимает второе по частоте место среди осложнений инфекционного эндокардита после сердечной недостаточности.
В большинстве исследований, анализирующих исходы инфекционного эндокардита, почечная недостаточность рассматривается, как один из предикторов неблагоприятного исхода и внутрибольничной летальности. наиболее высокая летальность от почечной недостаточности отмечается у больных с септическим синдромом или после сердечно-сосудистой хирургии.
Гломерулонефрит клинически при инфекционном эндокардите диагностируется реже, чем на секции. У умерших от инфекционного эндокардита, по наблюдениям Н.С. Чипигиной, К.С. Озерецкого (РГМУ, Москва, 2003), гломерулонефрит имел место в 38,4% вскрытий. Наиболее типичным гистологическим вариантом гломерулонефрита при инфекционном эндокардите является диффузный пролиферативный и экссудативный тип гломерулонефрита, реже наблюдался очаговый гломерулонефрит.
Гистологически диффузный гломерулонефрит характеризуется чаще всего картиной мезангиального, мезангиокапиллярного процесса, возможно вовлечение тубулоинтерстициальных компонентов. Редко болезнь может начаться с формирования экстракапиллярных эпителиальных полулуний с быстро нарастающим ухудшением функции почек. При диффузном пролиферативном гломерулонефрите степень протеинурии и цилиндрурии выше, чем при фокально-сегментарном пролиферативном гломерулонефрите, как и частота, и тяжесть развития почечной недостаточности.
Многие авторы подчеркивают иммунные механизмы развития гломерулонефрита при инфекционном эндокардите, обращают внимание на частое сочетание диффузного гломерулонефрита с геморрагическим васкулитом (у 32,3% больных, по наблюдениям В.Т. Комарова и соавт.), высоким уровнем циркулирующих иммунных комплексов, снижением активности С3-компонента комплемента, наличием ревматоидного фактора и криопреципитатов.
Течение нефрита при инфекционном эндокардите обычно благоприятное: лабораторные показатели подвергаются обратному развитию на фоне эффективной антибактериальной терапии и оперативного лечения. Азотемия, как результат гломерулонефрита, может прогрессировать или сохраняться в начале лечения, но обычно регрессирует при продолжительном назначении эффективных антибиотиков.
В редких случаях, несмотря на эффективное лечение инфекционного эндокардита антибиотиками, азотемия нарастает и может наступить смерть от быстропрогрессирующей почечной недостаточности. Анализируя морфологические данные в случае смерти от почечной недостаточности или результаты биопсии почек у больных инфекционным эндокардитом с быстропрогрессирующей почечной недостаточностью, представленные данные можно констатировать, что существенные нарушения функции почек при инфекционном эндокардите почти всегда обусловлены формированием экстракапиллярных сращений в большей части клубочков.
Экстракапиллярный пролиферативный гломерулонефрит является основной причиной развития тяжелой почечной недостаточности и может стать необратимым даже при излечении клапанной инфекции. В отличие от других вариантов гломерулонефрита, полностью обратимых при адекватной антибактериальной терапии инфекционного эндокардита, прогноз чаще неблагоприятный. Существуют единичные описания случаев разрешения экстракапиллярного гломерулонефрита, морфологически подтвержденного биопсией почки, при лечении антибиотиками и последующем протезировании клапанов сердца, успешного применения глюкокортикостероидов, цитостатиков или плазмафереза.
В этой связи можно согласиться с целесообразностью биопсии почек при инфекционном эндокардите в случаях с нарастающей почечной недостаточностью или выявлением антинейтрофильных цитоплазматических антител, рекомендуемой рядом авторов в 90-е годы, и поддержать высказывание группы французских авторов о том, что «хотя терапия глюкокортикостероидами в целом не рекомендуется при инфекционном эндокардите, она должна рассматриваться, если нарушение функции почек не проходит в течение 2-3 недель при адекватной антибактериальной терапии, особенно при большой длительности заболевания»; более широкое применение кортикостероидов, цитостатиков и дезагрегантов при гломерулонефрите у больных инфекционным эндокардитом недостаточно оправдано.
Вторичный амилоидоз почек – редкое осложнение современного инфекционного эндокардита – следует подозревать у больных с длительно текущим инфекционным эндокардитом c выраженной протеинурией, ухудшением функции почек, особенно в случаях увеличения размеров почек; для диагностики рекомендуется биопсия почек.
Лекарственные нефропатии, вызванные антибиотикотерапией, особенно аминогликозидами также могут наблюдаться у больных инфекционным эндокардитом. Антибактериальная терапия при инфекционном эндокардите с поражением очек предполагает исключение нефротоксических антибиотиков, а при почечной недостаточности – уменьшение доз и кратности их введения.
Эмболии почечных сосудов с развитием инфарктов почек, микотических аневризм почечных артерий, абсцессов почек довольно часто наблюдаются при инфекционном эндокардите. Тромбоэмболии артерий почек возникают у 5-17% больных. Внезапные односторонние боли в пояснице и животе, макрогематурия, болезненность при поколачивании по пояснице становятся нередко причиной ошибочного диагноза почечной колики или пиелонефрита при наличии лихорадки. Ультразвуковое исследование и компьютерная томография почек выявляют инфаркты почек.
По наблюдениям В.Е. Комарова и соавт., тромбоэмболии почечных артерий являлись неблагоприятным прогностическим фактором и в 95% случаев сочетались с другими эмболиями. Необычно высокая частота поражений почек за счет тромбоэмболий наблюдалась у инъекционных наркоманов с инфекционным эндокардитом клапанов левых камер сердца. Септический эмболический корковый инфаркт почик может осложниться почечным кровотечением и ретроперитонеальной гематомой. Vieira M.L. и соавт., подчеркивают в этой связи, что инфекционный эндокардит доложен всегда учитываться в дифференциальном диагнозе гематурии и болей в пояснице.
Поражение почек в настоящее время не является главной причиной смертности больных инфекционным эндокардитом, но имеет неблагоприятное прогностическое значение. Причиной уменьшения частоты поражения почек следует считать раннее антибактериальное лечение и сокращение вследствие этого длительности заболевания.
Источник
Инфаркт почки – это редкое нефрологическое заболевание, обусловленное эмболией артериальных сосудов органа с последующим некрозом его тканей и нарушением функциональной активности. Симптомы зависят от объема поражения, варьируются от полного отсутствия проявлений до резких болей в пояснице, гематурии, почечной недостаточности, увеличения уровня артериального давления. Диагностика производится на основании данных анамнеза, результатов анализов крови и мочи, УЗДГ сосудов почки, почечной ангиографии. Лечение преимущественно симптоматическое, также включает в себя применение антиагрегантных и антикоагулянтных средств, иногда показано хирургическое вмешательство.
Общие сведения
Инфаркт почки встречается намного реже других ишемических расстройств органов мочевыделительной системы. Данное состояние практически никогда не является изолированным нарушением, а выступает в качестве осложнений других, преимущественно сердечно-сосудистых патологий. Точные статистические данные относительно встречаемости болезни отсутствуют, поскольку определенная доля больных не обращается к специалистам из-за слабой выраженности симптомов.
Заболевание следует дифференцировать с мочекислым инфарктом почек у детей, являющимся одним из этапов адаптации мочевыделительной системы к внеутробному существованию. Из-за особенностей эпидемиологии болезней, способных осложняться инфарктом почки, патология чаще возникает у лиц старшего возраста, страдающих ожирением и обменными нарушениями.
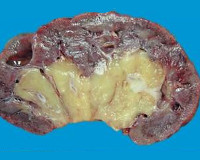
Инфаркт почки
Причины
В подавляющем большинстве случаев состояние имеет ишемический характер и вызывается эмболией магистральных почечных сосудов. Чаще всего эмбол представлен тромботическим сгустком, реже в таком качестве могут выступать фрагменты атеросклеротических бляшек, жировые массы. Картину, схожую с эмболией ветвей почечной артерии, иногда провоцируют артериовенозные фистулы или кровотечения. Таким образом, основной причиной заболевания является наличие в артериальной части большого круга кровообращения эмболов, которые могут образовываться при следующих патологиях:
- Эндокардит. Воспаление внутренней оболочки левого желудочка или предсердия часто осложняется формированием пристеночного тромба. Его фрагменты периодически попадают в большой круг кровообращения и могут закупоривать просвет артерий почек.
- Аритмии и пороки сердца. Различные нарушения сердечного ритма сопровождаются нарушениями гемодинамики внутри полостей сердца, что иногда приводит к тромбообразованию. Схожий механизм возникновения тромбов отмечается при недостаточности митрального клапана или пролапсе его створок.
- Атеросклеротическое поражение. Выраженный атеросклероз аорты или венечных артерий являются одной из наиболее частых причин инфаркта почки. Закупорка сосуда может быть обусловлена как фрагментом собственно атеросклеротической бляшки, так и тромбом, который образовался на ее поверхности. Атеросклероз почечных сосудов может приводить к расслоению их стенок, что также провоцирует закупорку просвета и острую ишемию.
- Узелковый периартериит. Данное состояние неясной этиологии в случае вовлечения в патологический процесс сосудистой сети почек может становиться причиной инфарктов.
- Медицинские манипуляции. Различные диагностические и лечебные манипуляции на органах мочевыделительной системы могут осложняться стенозом сосудов с развитием острой ишемии почечной ткани.
Косвенной причиной патологии иногда является наркотическая зависимость, связанная с частыми внутривенными вливаниями (опиоидная или эфедриновая наркомания). В случае использования нестерильного инструментария развивается специфический эндокардит с образованием многочисленных тромбов. Различные формы инфаркта почки обнаруживаются у 20-30% инъекционных наркоманов. Множественные очаги инфарктов в почечной ткани возникают и при диссеминированном внутрисосудистом свертывании крови (ДВС-синдроме).
Патогенез
Основополагающим звеном патогенеза более чем в 90% случаев инфаркта почки считается образование эмболов, которые вызывают закупорку сосудов органа. В результате нарушается снабжение участка почечной ткани кислородом и питательными веществами. По своей кислородной потребности почки уступают только нервной ткани и миокарду, из-за чего в результате ишемии довольно быстро возникают дистрофические изменения в клетках нефронов. Размер поражения зависит от калибра артериального сосуда, перекрытого эмболом – чем он больше, тем распространеннее зона инфаркта. Характерная форма зоны ишемии – клиновидная или треугольная с вершиной у ворот почки и обращенным к корковому веществу основанием. Это обусловлено особенностями распределения кровеносных сосудов в органе.
После прекращения поступления артериальной крови дистрофия клеток нефронов постепенно нарастает, сменяясь их гибелью и формированием участков некроза. Одновременно возникает раздражение юкстагломерулярного аппарата с образованием больших количеств гормона ангиотензина 2, что приводит к развитию вазоренальной гипертензии и каскаду связанных с этим нарушений (повышается риск инфаркта миокарда или инсульта). Продукты распада некротизированных тканей всасываются в системный кровоток и становятся причиной интоксикации организма, проявляющейся повышением температуры, головными болями, тошнотой. Исходом некроза становится разрастание фиброзной ткани и формирование рубца.
Симптомы инфаркта почки
Клиническая картина заболевания характеризуется различной выраженностью симптомов, которая, прежде всего, зависит от объема ишемизированной и некротизированной ткани почек. При незначительных инфарктах субъективные жалобы отсутствуют, патология выявляется случайно по измененным данным диагностических исследований. В случае более обширных поражений симптоматика становится выраженной, однако большинство проявлений неспецифичны – боль в пояснице, гематурия, уменьшение объема выделяемой мочи.
Болезненные ощущения, возникающие сначала с двух сторон, постепенно смещаются в сторону пораженной почки – двухсторонние инфаркты встречаются крайне редко. Интенсивность болевого синдрома иногда сопоставима с почечной коликой, боль устраняется только приемом сильных наркотических анальгетиков. Степень выраженности гематурии при инфаркте почки также может сильно варьироваться – от микроскопических количеств эритроцитов в моче до ее ярко алой окраски и профузного почечного кровотечения.
Иногда наблюдается реальная почечная колика, обусловленная прохождением кровяного сгустка или кусочка некротизированной ткани по мочевыводящим путям. Проявления почечной недостаточности обычно выражены слабо, особенно при сохраненной функциональной активности второй почки. При тотальном инфаркте возможно токсическое поражение парного органа, что проявляется развитием ОПН – анурией, запахом аммиака изо рта и от кожных покровов больного.
Общие симптомы заболевания сводятся к повышению температуры тела до 38 градусов, явлениям интоксикации (тошноте, рвоте, разбитому состоянию), ознобу. В некоторых случаях из-за нарушенного кровоснабжения почки возникает стимуляция юкстагломерулярного аппарата, провоцирующая рост артериального давления. Вышеперечисленные проявления обычно сочетаются с симптомами основной патологии, которая спровоцировала ишемию и инфаркт почечной ткани. Таковыми могут быть боли в области сердца, нарушения сердечного ритма, признаки циркуляторных расстройств при пороках клапанов (цианоз, повышение давления крови в малом круге кровообращения).
Осложнения
Ранним и наиболее тяжелым осложнением инфаркта почки является развитие острой почечной недостаточности. ОПН наблюдается достаточно редко, поскольку для этого необходимо наличие ряда условий – двухсторонний характер инфаркта либо наличие у больного только одной почки. При тотальной ишемии недостаточность может возникать из-за чрезмерной нагрузки на второй орган или по причине его токсического поражения. В отдаленной перспективе из-за формирования рубцов в пораженной почке снижается ее функциональная активность, что создает предпосылки для возникновения ХПН в будущем. У ряда больных после разрешения инфаркта сохраняется стойкое увеличение артериального давления, обусловленное нарушениями кровообращения в почках.
Диагностика
Определение инфаркта почки осложняется неспецифичностью симптомов, поскольку боли в пояснице, ухудшение общего состояния, гематурия характерны и для иных нефрологических заболеваний. Во многих случаях врачу-нефрологу или урологу требуется кооперация с другими медицинскими специалистами (например, с кардиологом) для уточнения диагноза. Особую важность имеет скорость определения болезни, так как от своевременности лечебных мер зависит ее исход, а при неправильном лечении повышается риск развития осложнений. В числе диагностических мероприятий выделяют следующие группы методов:
- Опрос и общий осмотр. При опросе акцентируют внимание на субъективных симптомах и жалобах больного. Имеет значение выраженность и локализация болезненных ощущений, наличие или отсутствие расстройств мочеиспускания. В анамнезе определяют наличие сердечно-сосудистых, гематологических или иных заболеваний, способных спровоцировать ишемию тканей почки.
- Лабораторные исследования. В общем анализе мочи практически всегда определяется наличие эритроцитов – от выраженной макрогематурии до микроскопических примесей крови, часто возникает протеинурия. При биохимическом исследовании мочи специфическим признаком инфаркта является увеличение уровня лактатдегидрогеназы (ЛДГ), аналогичное повышение наблюдается и в сыворотке крови. У большинства пациентов также обнаруживается незначительный лейкоцитоз, изменяются показатели коагулограммы – последняя выполняется для оценки необходимости использования антикоагулянтов.
- Инструментальные исследования. Обычно при подозрении на инфаркт почки производят ультразвуковую допплерографию (УЗДГ почечных артерий), позволяющую оценить показатели кровотока в основных сосудах органа. Еще больше информации дает селективная контрастная почечная ангиография, по результатам которой выявляется участок ишемизированной ткани, не накапливающей контраст. Как альтернативу последнему исследованию могут назначать МСКТ или МРТ с контрастом и последующим 3Д-моделированием почечной сосудистой сети.
- Эндоскопические исследования. Цистография при данном заболевании производится с целью дифференциальной диагностики. С помощью этого метода исключается вероятность кровотечения из мочевого пузыря (наблюдаемого при опухолях, травмах), уточняется односторонний характер поражения.
Дифференциальную диагностику инфаркта почки проводят с опухолевыми поражениями мочевыводящих путей (чашечно-лоханочной системы, мочеточников, мочевого пузыря и уретры) и кровотечениями из них. Иногда проявления заболевания создают ложную клиническую картину гломерулонефрита – он исключается при подтверждении одностороннего характера процесса и наличии ишемизированного участка тканей. При помощи дополнительных исследований инфаркт почки дифференцируют с почечной коликой при мочекаменной болезни и расслоением стенки брюшной аорты.
Лечение инфаркта почки
Основные цели терапии данного заболевания изменяются в зависимости от этапа патологического процесса. На начальных этапах первоочередной задачей является восстановление адекватного кровотока в органах выделения, что позволяет минимизировать негативные последствия ишемии. В дальнейшем на первый план выступает устранение кровотечения (макрогематурии), явлений общей интоксикации и сохранение функциональности оставшейся части органа. Зачастую для этих целей используют препараты с противоположным действием (например, антикоагулянты и гемостатики), поэтому от специалиста требуется особая осторожность при их назначении. Консервативная терапия инфаркта сводится к использованию следующих лекарственных средств:
- Обезболивающие препараты. Боли могут быть очень интенсивными, в ряде случаев болевой синдром устраняется только мощными наркотическими анальгетиками – морфином, фентанилом и другими.
- Тромболитические средства. К ним относят стрептокиназу и другие препараты данной группы, цель их применения – устранение тромба в сосуде, восстановления адекватного кровотока. Медикаменты используются только на первых этапах заболевания, до развития выраженной гематурии. После начала выделения крови с мочой назначение этих средств строго запрещено.
- Гемостатические препараты. Применяются при выраженной гематурии и профузном почечном кровотечении. Основным лекарственным средством данной группы является этамзилат натрия, введение которого позволяет минимизировать кровопотерю и улучшить прогноз заболевания.
- Антикоагулянты. На любом этапе патологии рекомендуется принимать меры по нормализации работы свертывающей системы крови, с этой целью назначаются антикоагулянты прямого действия (например, гепарин). Схема, дозировки и длительность применения строго индивидуальны, определяются после изучения коагулограммы больного.
- Антиагрегантные средства. Антиагреганты (например, ацетилсалициловая кислота) редко используются в остром периоде заболевания. Их назначают через 1-2 недели после исчезновения гематурии для снижения риска рецидива и отдаленных осложнений. Дозировка и длительность курса лечения определяется с учетом функциональной активности выделительной системы.
В тяжелых случаях (например, тотальный инфаркт почки) проводят хирургическое лечение, которое на начальных стадиях болезни сводится к восстановлению проходимости магистральных артерий и почечного кровотока. При поздней диагностике и развитии некротических изменений в почке по показаниям осуществляют оперативное удаление зоны инфаркта вплоть до нефрэктомии (при наличии у больного второго здорового органа). В числе вспомогательных лечебных мероприятий используют гемодиализ (при почечной недостаточности), назначают диуретические, гипотензивные и другие средства по показаниям.
Прогноз и профилактика
Прогноз инфаркта почки определяется объемом пораженных тканей – обычно страдает относительно небольшой фрагмент органа, после рубцевания это слабо отражается на работе выделительной системы. При ишемии значительной области органа возможно развитие острой или хронической почечной недостаточности, кровотечения и прочих жизнеугрожающих состояний. Существует риск рецидива, особенно при сохранении провоцирующего фактора (эндокардитов, пороков сердца, атеросклероза магистральных сосудов).
Поскольку заболевание часто является осложнением болезней сердечно-сосудистой системы, его профилактика заключается в правильном лечении основной патологии – использовании антиагрегантных средств, антибиотиков при эндокардитах, антихолестеринемических средств в случае атеросклероза.
Источник
