Инфаркт миокарда постинфарктное состояние

Постинфарктный синдром – это перикардит аутоиммунного генеза, развивающийся спустя несколько недель после острого инфаркта миокарда. Данное осложнение характеризуется классической триадой симптомов: боль в груди, шум трения листков перикарда, легочные проявления (хрипы, кашель, одышка). Для верификации диагноза выполняется общеклинический анализ крови, ЭКГ, рентген грудной клетки, УЗИ перикарда и плевральной полости. Лечение включает в себя симптоматическую, противовоспалительную и кардиотропную терапию. При осложненном течении проводится плевроцентез, перикардиоцентез или перикардэктомия.
Общие сведения
В клинической терминологии постинфарктным синдромом (ПС), или синдромом Дресслера, называется аутоиммунное поражение околосердечной сумки. Это осложнение, обусловленное неадекватной реакцией иммунной системы на деструктивно измененные белки миокарда, в 1955 году описал американский кардиолог В. Дресслер. В его честь болезнь получила свое второе название. Кроме того, в медицинской литературе встречаются такие термины, как поздний перикардит, посткардиотомический, посттравматический перикардиальный синдром и постинфарктный полисерозит. В целом распространенность ПС в популяции составляет 3-4%. Однако по данным различных авторитетных источников, с учетом атипичных и малосимптомных форм осложнение развивается у 15-30% пациентов, перенесших обширный, осложненный или повторный инфаркт миокарда (ИМ).
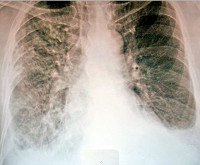
Постинфарктный синдром
Причины постинфарктного синдрома
Первопричиной заболевания является ишемическое повреждение структурных волокон миокарда, повлекшее за собой гибель кардиомиоцитов. Чаще всего оно возникает при крупноочаговом осложненном инфаркте. В процессе разрушения некротизированных тканей в кровоток поступают денатурированные белки, на которые иммунная система реагирует, как на чужеродные. В результате развивается аутоиммунная реакция, являющаяся причиной возникновения постинфарктного синдрома.
Определенную значимость в формировании симптомокомплекса играют антигены крови, проникающей в околосердечную оболочку при нарушении целостности сердечной мышцы. Поэтому, помимо острого ИМ, пусковым механизмом развития заболевания может стать гемоперикард (кровоизлияние в перикардиальную полость), обусловленное травмами грудной клетки, ранениями сердца или неадекватными кардиохирургическими вмешательствами. Также в группу риска входят постинфарктные пациенты с аутоиммунными патологиями. Некоторые авторы считают, что причиной воспалительного процесса является вирусная инфекция. Однако единодушия по поводу данного вопроса у специалистов в области кардиологии до сих пор нет.
Патогенез
Постинфарктный синдром представляет собой аутоиммунный процесс, возникающий вследствие интенсификации выработки антител к кардиальным антигенам. Острое нарушение кровоснабжения миокарда и гибель клеток влечет за собой резорбцию участков некроза и выход денатурированных компонентов в кровь. Это приводит к формированию иммунного ответа с образованием аутоантител, направленных против белков, входящих в состав серозных оболочек органов-мишеней.
Специфические антитела к кардиомиоцитам, в большом количестве присутствующие в плазме крови постинфарктных больных, формируют иммунные комплексы с клетками собственных тканей. Свободно циркулируя в кровяном русле, они накапливаются в перикардиальной, висцеральной плевре и во внутренних слоях суставных сумок, провоцируя асептическое воспаление. В дополнение повышается уровень Т-ЦТЛ (цитотоксических лимфоцитов), разрушающих поврежденные клетки собственного организма. Таким образом, изменяется состояние и клеточного, и гуморального иммунитета, что подтверждает аутоиммунный генез симптомокомплекса.
Классификация
Постинфарктный синдром подразделяется на 3 основные формы. В пределах каждой из них имеется несколько вариантов, классификация которых основана на локализации воспалительного процесса.
- Типичная. Клинические проявления типичной (развернутой) формы ПС связаны с воспалением перикарда, висцеральной плевры и тканей легкого. Она включает одиночные и комбинированные варианты постинфарктного аутоиммунного повреждения соединительной ткани:
- перикардиальный – воспаляется висцеральный и париетальный листок околосердечной сумки;
- плевральный – мишенью аутоантител становится плевра, на первый план выходят признаки гидроторакса;
- пневмонический – обнаруживаются инфильтративные изменения в легких, приводящие к развитию пневмонита;
- перикардиально-плевральный – присутствуют признаки сенсибилизации тканей серозной оболочки перикарда и плевры;
- перикардиально-пневмоничекий – выявляется поражение околосердечной оболочки и ткани легкого;
- перикардиально-плеврально-пневмонический – воспаление с сердечной сумки переходит на плевральные и легочные структуры.
- Атипичная. Для этой формы свойственны варианты, связанные с поражением антителами тканей сосудов и суставов. Она сопровождается воспалением крупных суставных сочленений или кожными реакциями: «синдромом плеча», пекталгией, дерматитом, узловой эритемой.
- Стертая (малосимптомная). При стертой форме со слабо выраженными основными симптомами наблюдается упорная артралгия, лихорадочное состояние и изменение количественного и качественного состава белой крови. При диагностике стертых и атипичных форм нередко возникают определенные трудности, обуславливающие актуальность более углубленного изучения данной проблемы.
Симптомы постинфарктного синдрома
Классический постинфарктный синдром формируется через 2-4 недели после ИМ. Иногда сроки могут увеличиваться или уменьшаться. К наиболее характерным симптомам заболевания относят лихорадочное состояние, болевые ощущения и тяжесть в груди, одышку, кашель. Патологический процесс чаще всего начинается остро, повышением температуры тела до субфебрильных или фебрильных отметок. Появляется слабость, головокружение, тошнота, учащается пульс и дыхание. Иногда температурные показатели остаются в пределах нормы.
Обязательным компонентом симптомокомплекса является перикардит. Для него типичны различные по интенсивности болевые ощущения в области сердца, отдающие в середину живота, под мечевидный отросток, в шею, лопатки, плечи и обе руки. Боли могут быть острыми, приступообразными, или тупыми, сжимающими. При кашле и глотании появляется чувство сдавленности в груди, болезненность усиливается. В положении стоя или лежа на животе боль ослабевает. Нередко наблюдается одышка, сердцебиение, частое поверхностное дыхание.
У 85% постинфарктных пациентов с самого первого дня появляется характерный шум трения перикардиальных листков. Он обнаруживается при аускультации, независимо от дыхания и сердечного цикла. Через несколько суток боли стихают, а шум исчезает после появления выпота. Типичное проявление плеврита – колющая односторонняя боль в верхней части туловища. Она усиливается при глубоких вдохах и наклонах в здоровую сторону. Вынужденное положение на больном боку облегчает состояние. При пальпации обнаруживается крепитация.
Для пневмонита характерно ослабленное жесткое дыхание, мелкопузырчатые хрипы, одышка, сухой или влажный кашель. Реже развивается резистентная к антибиотикам нижнедолевая пневмония. Заболевание сопровождается слабостью, усиленным потоотделением и лихорадкой. В мокроте могут обнаруживаться кровяные примеси, что существенно усложняет диагностику. При атипичных формах постинфарктного симптомокомплекса нарушаются функции различных суставов: плечевых, кистевых, грудинно-реберных. Болезнь может протекать по типу моно- и полиартритов.
Осложнения
При отсутствии своевременной диагностики и профессиональной врачебной помощи постинфарктный синдром способен привести к развитию геморрагического или констриктивного перикардита (появлению кровянистого экссудата или сдавливанию сердечных тканей), а в запущенных случаях стать причиной тяжелой тампонады сердца. Для заболевания свойственно рецидивирующее течение с обострениями и ремиссиями, возникающими в промежутках от 1-2 недель до 2-х месяцев. Как правило, под влиянием лечения наблюдается ослабление симптомов, а при отсутствии терапевтической коррекции болезнь атакует с новой силой.
Диагностика
При постановке диагноза учитываются жалобы больного, характерные клинические проявления и результаты комплексного лабораторного и инструментального обследования. К наиболее ценным диагностическим параметрам, позволяющим дать заключение о состоянии пациента на момент исследования и на дальнейшую перспективу, относят:
- Клинические критерии. Объективными признаками, подтверждающими высокую вероятность формирования постинфарктного полисерозита, является перикардит и фебрильная лихорадка. Характерной считается боль за грудиной, иррадиирующая в межлопаточную область и распространяющаяся вдоль трапециевидной мышцы, сухой кашель, различная по степени выраженности одышка.
- Лабораторные исследования. В общем анализе крови возможен лейкоцитоз, эозинофилия, увеличение СОЭ. Чтобы дифференцировать синдром Дресслера от повторного ИМ, проводится исследование крови на сывороточные маркеры повреждения миокарда. Увеличение содержания глобулярных белков – тропонина I и тропонина Т – позволяет подтвердить факт гибели клеток, случившийся в промежутке 4-48 часов. Титр противокардиальных антител остается таким же, как и при неосложненном ИМ.
- ЭКГ. На повторных электрокардиограммах наблюдается отрицательная динамика. Наиболее характерный признак – однонаправленное смещение сегмента ST в большинстве отведений (с максимальным зубцом желудочкового комплекса). По мере накопления в перикардиальной полости экссудата амплитуда комплекса ORS может снижаться.
- Рентгенография грудной клетки. При плеврите обнаруживается утолщение междолевой плевры, при перикардите расширяется сердечная тень, при пневмоните выявляются ограниченные затемнения в легких, усиливается диффузный рисунок в прикорневых зонах. В отдельных случаях на снимке четко видна кардиомегалия, ограничение подвижности левого купола диафрагмы.
- УЗИ перикарда и плевральной полости. Производится оценка эхографической картины, визуализируется утолщение листков перикарда, выявляется наличие и определяется количество жидкости в перикардиальной и плевральной полостях.
В неясных диагностических случаях для дифференциации болей и выявления жидкости в полостях или инфильтратов в легочной ткани назначается МРТ сердца и легких. При наличии признаков тампонады для уточнения характера выпота, скопившегося в околосердечной сумке, проводится диагностический перикардиоцентез с последующим лабораторным исследованием полученного материала.
Лечение постинфарктного синдрома
Лечение проходит в условиях специализированного стационара. Главная роль в перечне лечебных мероприятий принадлежит медикаментозной терапии. Она преследует несколько целей, и предполагает применение фармакопрепаратов разнонаправленного механизма действия:
- Противовоспалительные. При отсутствии противопоказаний препаратами выбора являются НПВП, которые назначаются с учетом профиля безопасности. В случае резистентности к нестероидным средствам проводятся короткие курсы глюкокортикоидов. При тяжелом течении болезни, рефрактерном к противовоспалительной терапии нестероидными средствами и гормонами, применяются ЛС других групп (колхицин, метотрексат).
- Кардиотропные. Для устранения сердечных нарушений назначаются препараты, использующиеся при лечении ишемической болезни сердца: антиангинальные средства, бета-блокаторы, блокаторы кальциевых каналов, нитраты, сердечные гликозиды. При назначении учитывается основной механизм фармакологического действия, возможные побочные эффекты и кардиотоксичность.
Антикоагулянты в связи с высоким риском развития гемоперикарда не применяются. При необходимости их использования назначаются субтерапевтические дозировки. В каждом конкретном случае лечение ПС подбирается индивидуально. При выраженных болях показаны внутримышечные инъекции анальгетиков. При большом скоплении выпота выполняется плевроцентез или пункция перикардиальной полости. При сердечной тампонаде проводится хирургическая операция – перикардэктомия.
Прогноз и профилактика
Постинфарктный синдром не является опасным для жизни состоянием, и даже при самом тяжелом течении прогноз относительно благоприятный. Методы первичной профилактики, направленной на устранение причин ПС, еще не разработаны. Для снижения частоты суставных проявлений пациентам, перенесшим острый ИМ, рекомендуется ранняя активизация. При заболеваниях с рецидивирующим течением назначается противорецидивная терапия, призванная предотвратить повторные обострения патологического процесса.
Источник
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
Общие сведения
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза. После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда.
Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности. Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. е. формирование постинфарктного рубца.
В клиническом течении инфаркта миокарда выделяют пять периодов:
- 1 период – предынфарктный (продромальный): учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель;
- 2 период – острейший: от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов;
- 3 период – острый: от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток;
- 4 период – подострый: начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4-8 недель;
- 5 период – постинфарктный: созревание рубца, адаптация миокарда к новым условиям функционирования.
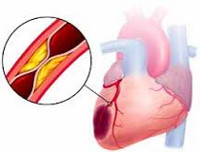
Инфаркт миокарда
Причины инфаркта миокарда
Инфаркт миокарда является острой формой ИБС. В 97—98% случаев основой для развития инфаркта миокарда служит атеросклеротическое поражение венечных артерий, вызывающее сужение их просвета. Нередко к атеросклерозу артерий присоединяется острый тромбоз пораженного участка сосуда, вызывающий полное или частичное прекращение кровоснабжения соответствующей области сердечной мышцы. Тромбообразованию способствует повышенная вязкость крови, наблюдаемая у пациентов с ИБС. В ряде случаев инфаркт миокарда возникает на фоне спазма ветвей венечных артерий.
Развитию инфаркта миокарда способствуют сахарный диабет, гипертоничесая болезнь, ожирение, нервно-психическое напряжение, увлечение алкоголем, курение. Резкое физическое или эмоциональное напряжение на фоне ИБС и стенокардии может спровоцировать развитие инфаркта миокарда. Чаще развивается инфаркт миокарда левого желудочка.
Классификация инфаркта миокарда
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда:
- крупноочаговый
- мелкоочаговый
На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов). В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией.
В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда:
- трансмуральный – с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый)
- интрамуральный – с некрозом в толще миокарда
- субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду
- субэпикардиальный – с некрозом миокарда в зоне прилегания к эпикарду
По изменениям, фиксируемым на ЭКГ, различают:
- «Q-инфаркт» – с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда)
- «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда)
По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на:
- правожелудочковый
- левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки
По кратности возникновения различают инфаркт миокарда:
- первичный
- рецидивирующий (развивается в срок 8 недель после первичного)
- повторный (развивается спустя 8 недель после предыдущего)
По развитию осложнений инфаркт миокарда подразделяется на:
- осложненный
- неосложненный
По наличию и локализации болевого синдрома выделяют формы инфаркта миокарда:
- типичную – с локализацией боли за грудиной или в прекардиальной области
- атипичные – с атипичными болевыми проявлениями:
- периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная)
- безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная
- малосимптомную (стертую)
- комбинированную
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
- стадию ишемии (острейший период)
- стадию некроза (острый период)
- стадию организации (подострый период)
- стадию рубцевания (постинфарктный период)
Симптомы инфаркта миокарда
Предынфарктный (продромальный) период
Около 43% пациентов отмечают внезапное развитие инфаркта миокарда, у большей же части больных наблюдается различный по продолжительности период нестабильной прогрессирующей стенокардии.
Острейший период
Типичные случаи инфаркта миокарда характеризуются чрезвычайно интенсивным болевым синдромом с локализацией болей в грудной клетке и иррадиацией в левое плечо, шею, зубы, ухо, ключицу, нижнюю челюсть, межлопаточную зону. Характер болей может быть сжимающим, распирающим, жгучим, давящим, острым («кинжальным»). Чем больше зона поражения миокарда, тем более выражена боль.
Болевой приступ протекает волнообразно (то усиливаясь, то ослабевая), продолжается от 30 минут до нескольких часов, а иногда и суток, не купируется повторным приемом нитроглицерина. Боль сопряжена с резкой слабостью, возбуждением, чувством страха, одышкой.
Возможно атипичное течение острейшего периода инфаркта миокарда.
У пациентов отмечается резкая бледность кожных покровов, липкий холодный пот, акроцианоз, беспокойство. Артериальное давление в период приступа повышено, затем умеренно или резко снижается по сравнению с исходным (систолическое < 80 рт. ст., пульсовое < 30 мм мм рт. ст.), отмечается тахикардия, аритмия.
В этот период может развиться острая левожелудочковая недостаточность (сердечная астма, отек легких).
Острый период
В остром периоде инфаркта миокарда болевой синдром, как правило, исчезает. Сохранение болей бывает вызвано выраженной степенью ишемии околоинфарктной зоны или присоединением перикардита.
В результате процессов некроза, миомаляции и перифокального воспаления развивается лихорадка (от 3-5 до 10 и более дней). Длительность и высота подъема температуры при лихорадке зависят от площади некроза. Артериальная гипотензия и признаки сердечной недостаточности сохраняются и нарастают.
Подострый период
Болевые ощущения отсутствуют, состояние пациента улучшается, нормализуется температура тела. Симптомы острой сердечной недостаточности становятся менее выраженными. Исчезает тахикардия, систолический шум.
Постинфарктный период
В постинфарктном периоде клинические проявления отсутствуют, лабораторные и физикальные данные практически без отклонений.
Атипичные формы инфаркта миокарда
Иногда встречается атипичное течение инфаркта миокарда с локализацией болей в нетипичных местах (в области горла, пальцах левой руки, в зоне левой лопатки или шейно-грудного отдела позвоночника, в эпигастрии, в нижней челюсти) или безболевые формы, ведущими симптомами которых могут быть кашель и тяжелое удушье, коллапс, отеки, аритмии, головокружение и помрачение сознания.
Атипичные формы инфаркта миокарда чаще встречаются у пожилых пациентов с выраженными признаками кардиосклероза, недостаточностью кровообращения, на фоне повторного инфаркта миокарда.
Однако атипично протекает обычно только острейший период, дальнейшее развитие инфаркта миокарда становится типичным.
Стертое течение инфаркта миокарда бывает безболевым и случайно обнаруживается на ЭКГ.
Осложнения
Нередко осложнения возникают уже в первые часы и дни инфаркта миокарда, утяжеляя его течение. У большинства пациентов в первые трое суток наблюдаются различные виды аритмий: экстрасистолия, синусовая или пароксизмальная тахикардия, мерцательная аритмия, полная внутрижелудочковая блокада. Наиболее опасно мерцание желудочков, которое может перейти в фибрилляцию и привести к гибели пациента.
Левожелудочковая сердечная недостаточность характеризуется застойными хрипами, явлениями сердечной астмы, отека легких и нередко развивается в острейший период инфаркта миокарда. Крайне тяжелой степенью левожелудочковой недостаточности является кардиогенный шок, развивающийся при обширном инфаркте и обычно приводящий к летальному исходу. Признаками кардиогенного шока служит падение систолического АД ниже 80 мм рт. ст., нарушение сознания, тахикардия, цианоз, уменьшение диуреза.
Разрыв мышечных волокон в зоне некроза может вызывать тампонаду сердца – кровоизлияние в полость перикарда. У 2-3% пациентов инфаркт миокарда осложняется тромбоэмболиями системы легочной артерии (могут стать причиной инфаркта легких или внезапной смерти) или большого круга кровообращения.
Пациенты с обширным трансмуральным инфарктом миокарда в первые 10 суток могут погибнуть от разрыва желудочка вследствие острого прекращения кровообращения. При обширном инфаркте миокарда может возникать несостоятельность рубцовой ткани, ее выбухание с развитием острой аневризмы сердца. Острая аневризма может трансформироваться в хроническую, приводящую к сердечной недостаточности.
Отложение фибрина на стенках эндокарда приводит к развитию пристеночного тромбоэндокардита, опасного возможностью эмболии сосудов легких, мозга, почек оторвавшимися тромботическими массами. В более позднем периоде может развиться постинфарктный синдром, проявляющийся перикардитом, плевритом, артралгиями, эозинофилией.
Диагностика инфаркта миокарда
Среди диагностических критериев инфаркта миокарда важнейшими являются анамнез заболевания, характерные изменения на ЭКГ, показатели активности ферментов сыворотки крови. Жалобы пациента при инфаркте миокарда зависят от формы (типичной или атипичной) заболевания и обширности поражение сердечной мышца. Инфаркт миокарда следует заподозрить при тяжелом и продолжительном (дольше 30-60 минут) приступе загрудинных болей, нарушении проводимости и ритма сердца, острой сердечной недостаточности.
К характерным изменениям ЭКГ относятся формирование отрицательного зубца Т (при мелкоочаговом субэндокардиальном или интрамуральном инфаркте миокарда), патологического комплекса QRS или зубца Q (при крупноочаговом трансмуральном инфаркте миокарда). При ЭхоКГ выявляется нарушение локально сократимости желудочка, истончение его стенки.
В первые 4-6 часов после болевого приступа в крови определяется повышение миоглобина – белка, осуществляющего транспорт кислорода внутрь клеток.Повышение активности креатинфосфокиназы (КФК) в крови более чем на 50% наблюдается спустя 8—10 ч от развития инфаркта миокарда и снижается до нормы через двое суток. Определение уровня КФК проводят через каждые 6-8 часов. Инфаркт миокарда исключается при трех отрицательных результатах.
Для диагностики инфаркта миокарда на более поздних сроках прибегают к определению фермента лактатдегидрогеназы (ЛДГ), активность которой повышается позже КФК – спустя 1-2 суток после формирования некроза и приходит к нормальным значениям через 7-14 дней. Высокоспецифичным для инфаркта миокарда является повышение изоформ миокардиального сократительного белка тропонина – тропонина-Т и тропонина-1, увеличивающихся также при нестабильной стенокардии. В крови определяется увеличение СОЭ, лейкоцитов, активности аспартатаминотрансферазы (АсАт) и аланинаминотрансферазы (АлАт).
Коронарная ангиография (коронарография) позволяет установить тромботическую окклюзию коронарной артерии и снижение желудочковой сократимости, а также оценить возможности проведения аортокоронарного шунтирования или ангиопластики – операций, способствующих восстановлению кровотока в сердце.
Лечение инфаркта миокарда
При инфаркте миокарда показана экстренная госпитализация в кардиологическую реанимацию. В остром периоде пациенту предписывается постельный режим и психический покой, дробное, ограниченное по объему и калорийности питание. В подостром периоде больной переводится из реанимации в отделение кардиологии, где продолжается лечение инфаркта миокарда и осуществляется постепенное расширение режима.
Купирование болевого синдрома проводится сочетанием наркотических анальгетиков (фентанила) с нейролептиками (дроперидолом), внутривенным введением нитроглицерина.
Терапия при инфаркте миокарда направлена на предупреждение и устранение аритмий, сердечной недостаточности, кардиогенного шока. Назначают антиаритмические средства (лидокаин), ß-адреноблокаторы (атенолол), тромболитики (гепарин, ацетилсалициловая к-та), антогонисты Са (верапамил), магнезию, нитраты, спазмолитики и т. д.
В первые 24 часа после развития инфаркта миокарда можно произвести восстановление перфузии путем тромболизиса или экстренной баллонной коронарной ангиопластики.
Прогноз при инфаркте миокарда
Инфаркт миокарда является тяжелым, сопряженным с опасными осложнениями заболеванием. Большая часть летальных исходов развивается в первые сутки после инфаркта миокарда. Насосная способность сердца связана с локализацией и объемом зоны инфаркта. При повреждении более 50% миокарда, как правило, сердце функционировать не может, что вызывает кардиогенный шок и гибель пациента. Даже при менее обширном повреждении сердце не всегда справляется нагрузками, в результате чего развивается сердечная недостаточность.
По истечении острого периода прогноз на выздоровление хороший. Неблагоприятные перспективы у пациентов с осложненным течением инфаркта миокарда.
Профилактика инфаркта миокарда
Необходимыми условиями профилактики инфаркта миокарда являются ведение здорового и активного образа жизни, отказ от алкоголя и курения, сбалансированное питание, исключение физического и нервного перенапряжения, контроль АД и уровня холестерина крови.
Источник
