Инфаркт левая коронарная артерия
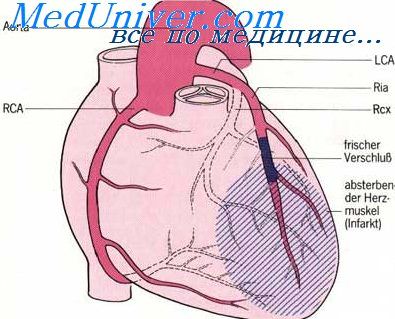
Инфаркт при тромбозе левой огибающей артерии. Инфаркт при тромбозе правой коронарной артерии
На данной коронарограмме, сделанной в левой передней косой проекции, хорошо видны ветви ЛКА. Передняя межжелудочковая (нисходящая) ветвь не изменена, тогда как огибающая ветвь ЛКА закупорена в проксимальной части.
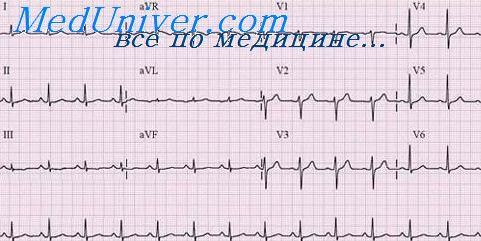
На ЭКГ видны подъём сегмента ST и формирование зубца QS в отведениях II, III, aVF, а также высокие зубцы R в сочетании с реципрокной депрессией сегмента ST в правых грудных отведениях (так называемая перевёрнутая инфарктная ЭКГ). Эти изменения на ЭКГ свидетельствуют о развитии обширного инфаркта миокарда задней стенки левого желудочка, как диафрагмальных, так и базальных её отделов.
Как уже отмечалось, 15 % всех случаев развития инфаркта миокарда в области задней стенки левого желудочка связано с тромбозом не ПКА, а огибающей ветви ЛКА, которая у этих больных обеспечивает кровоснабжение задней стенки левого желудочка. У данного больного как раз и отмечалась (неправо-) левовенечная форма кровоснабжения сердца.

Инфаркт при тромбозе правой коронарной артерии
На коронарограмме, сделанной в правой передней косой проекции хорошо виден проксимальный участок правой коронарной артерии. Этот крупный сосуд обтурирован тромбом в проксимальном отделе (выше места отхождения ветви к правому желудочку). Закупорка сосуда в этом отделе приводит к развитию обширного инфаркта задней стенки левого желудочка с вовлечением правого желудочка. Напомним, что задняя межжелудочковая (нисходящая) и задние левожелудочковые ветви доминирующей правой коронарной артерии обеспечивают кровоснабжение задней стенки левого желудочка приблизительно у 85 % случаев правовенечная форма кровоснабжения сердца).
На ЭКГ виден подъём сегмента ST в отведениях II, III, aVF с его реципрокной депрессией в грудных отведениях, а также I, aVL. Иногда депрессия сегмента ST у больных в остром периоде инфаркта задней стенки может быть связана также с сопутствующей ишемией передней стенки левого желудочка.
Независимо от причины развития у этих больных депрессии сегмента ST в передних грудных отведениях, это считается неблагоприятным признаком, свидетельствующем о повышенном риске развития таких осложнений, как атриовентрикулярная блокада, сердечная недостаточность, инфаркт правого желудочка. Напомним, что диагностировать инфаркт правого желудочка помогает запись отведений V3R, V4R, в которых можно выявить подьём сегмента ST и формирование патологического зубца Q.
В современных кардиологических клиниках метод эхокардиографии имеет существенное значение в диагностике инфаркта миокарда, его осложнений, выборе и оценке эффективности терапии, а также определении прогноза течения заболевания.
Когда в первые часы коронарной катастрофы ЭКГ неинформативна, а лабораторные маркеры поражения миокарда ещё “молчат”, эхокардиография может помочь в постановке диагноза инфаркта миокарда. Правда, реалии жизни таковы, что широко использовать этот метод в ранней диагностике инфаркта миокарда не удаётся по целому ряду причин. Прежде всего, не у всех больных можно получить приемлемое для “чтения” изображение. Кроме того, нужен опытный глаз, чтобы отличить глобальную дисфункцию у больных с кардиомиопатиями и болевым синдромом (пусть даже нетипичным) от нарушения регионарной сократимости левого желудочка при инфаркте миокарда.
– Также рекомендуем “Эхокардиография при инфаркте миокарда. Диагностика осложнений инфаркта миокарда”
Оглавление темы “Диагностика и тактика при инфаркте миокарда”:
1. Тромбоз межжелудочковой ветви левой коронарной артерии. Инфаркт при тромбозе межжелудочковой ветви
2. Инфаркт при тромбозе левой огибающей артерии. Инфаркт при тромбозе правой коронарной артерии
3. Эхокардиография при инфаркте миокарда. Диагностика осложнений инфаркта миокарда
4. Значение эхокардиографии. Практическая ценность эхокардиографии при инфаркте миокарда
5. Эхокардиография при инфаркте правого желудочка. Значение эхокардиографии при патологии правого желудочка
6. Дифференциация инфаркта миокарда. Особенности инфаркта миокарда
7. Сердечно-легочная реанимация. Пути развития отечественной сердечно-легочной реанимации
8. Как проводить сердечно-легочную реанимацию? Техника сердечно-легочной реанимации
9. Отказ от искусственного дыхания при реанимации. Дефибрилляция сердца
10. Лечение инфаркта миокарда. Этапы терапии инфаркта миокарда
Источник
Коронарное кровообращение. Левая коронарная артерия
Анатомия коронарного кровообращения весьма вариабельна. Особенности коронарного кровообращения каждого человека неповторимы, как отпечатки пальцев, поэтому и каждый инфаркт миокарда “индивидуален”. Глубина и распространённость инфаркта зависят от переплетения многих факторов, в частности от врождённых анатомических особенностей коронарного русла, степени развития коллатералей, выраженности атеросклеротического поражения, наличия “продромов” в виде стенокардии, впервые возникшей в течение предшествующих инфаркту суток (ишемическая “тренировка” миокарда), спонтанной либо ятрогенной реперфузии и др.
Как известно, сердце получает кровь из двух венечных (коронарных) артерий: правой венечной артерии [a. coronaria dextra — по-латыни или right coronary artery (RCA) — по-английски] и левой венечной артерии [соответственно a. coronaria sinistra и left coronary artery (LCA)]. Это первые ветви аорты, которые отходят от правого и левого её синусов.
Ствол ЛКА [по-английски — left main coronary artery (LMCA)] отходит от верхней части левого синуса аорты и идёт позади лёгочного ствола. Диаметр ствола ЛКА составляет от 3 до 6 мм, протяженность — до 10 мм. Обычно ствол ЛКА делится на две ветви: переднюю межжелудочковую ветвь (ПМВ) и огибающую (рис. 4.11). В 1/3 случаев ствол ЛКА делится не на два, а на три сосуда: переднюю межжелудочковую, огибающую и срединную (промежуточную) ветви. В этом случае срединная ветвь (ramus medianus) располагается между передней межжелудочковой и огибающей ветвями ЛКА.
Этот сосуд — аналог первой диагональной ветви (см. ниже) и обычно снабжает переднебоковые отделы левого желудочка.
Передняя межжелудочковая (нисходящая) ветвь ЛКА следует по передней межжелудочковой борозде (sulcus interventricularis anterior) в направлении верхушки сердца. В англоязычной литературе этот сосуд называют левой передней нисходящей артерией: left anterior descending artery (LAD). Мы будем придерживаться более точного анатомически (F. H. Netter, 1987) и принятого в отечественной литературе термина “передняя межжелудочковая ветвь” (О. В. Федотов и др., 1985; С. С. Михайлов, 1987). В то же время при описании коронарограмм лучше использовать термин “передняя межжелудочковая артерия”, чтобы упростить название её ветвей.
Главные ветви последней — перегородочные (проникающие, септальные) и диагональные. Перегородочные ветви отходят от ПМВ под прямым углом и углубляются в толщу межжелудочковой перегородки, где анастомозируют с аналогичными ветвями, отходящими снизу от задней межжелудочковой ветви правой коронарной артерии (ПКА). Эти ветви могут отличаться по количеству, длине, направлению. Иногда встречается крупная первая перегородочная ветвь (идущая либо вертикально, либо горизонтально — как бы параллельно ПМВ), от которой отходят веточки к перегородке. Отметим, что из всех областей сердца межжелудочковая перегородка сердца обладает самой густой сосудистой сетью. Диагональные ветви ПМВ проходят по переднебоковой поверхности сердца, которую и кровоснабжают. Таких ветвей бывает от одной до трёх.
В 3/4 случаев ПМВ не заканчивается в области верхушки, а, огибая последнюю справа, заворачивается на диафрагмальную поверхность задней стенки левого желудочка, кровоснабжая соответственно как верхушку, так и частично заднедиафрагмальные отделы левого желудочка. Именно этим объясняется появление на ЭКГ зубца Q в отведении aVF у больного с обширным передним инфарктом. В остальных же случаях, оканчиваясь на уровне или не доходя до верхушки сердца, ПМВ не играет существенной роли в её кровоснабжении. Тогда верхушка получает кровь от задней межжелудочковой ветви ПКА.
Проксимальным участком передней межжелудочковой ветви (ПМВ) ЛКА называют отрезок от устья этой ветви до отхождения первой перегородочной (проникающей, септальной) ветви или же до отхождения первой диагональной ветви (менее строгий критерий). Соответственно средний участок — это отрезок ПМВ от конца проксимального участка до отхождения второй либо третьей диагональной ветви. Далее располагается дистальный участок ПМВ. Когда есть только одна диагональная ветвь, границы среднего и дистального участков определяются приблизительно.
Учебное видео кровоснабжения сердца (анатомии артерий и вен)
При проблемах с просмотром скачайте видео со страницы Здесь
– Также рекомендуем “Огибающая ветвь левой коронарной артерии. Правая коронарная артерия”
Оглавление темы “Инфаркт миокарда на ЭКГ”:
1. Динамика тропонинов при инфаркте миокарда. Диагностика острого коронарного синдрома
2. ЭКГ признаки инфаркта миокарда. Волна Парди при инфаркте миокарда
3. Патологический зубец Q. Происхождение зубца Q
4. Трансмуральный инфаркт миокарда. Изменения ЭКГ при крупноочаговом инфаркте миокарда
5. Топическая диагностика инфаркта миокарда. Определение локализации инфаркта миокарда
6. Инфаркт миокарда с блокадой левой ножки пучка Гиса. Значение ЭКГ в диагностике инфаркта миокарда
7. Псевдоинфарктные изменения ЭКГ. Электрокардиокоронарографические изменения ЭКГ
8. Коронарное кровообращение. Левая коронарная артерия
9. Огибающая ветвь левой коронарной артерии. Правая коронарная артерия
10. Формы кровоснабжения сердца. Особенности кровотока в сердце
Источник
Коронарные артерии и локализация инфаркта миокарда
Ангиографические исследования, проведенные в самые ранние часы после ИМ↑ST, выявили в 90% случаев полную окклюзию инфаркт-связанной коронарной артерии (КА). Реканализация вследствие спонтанного тромболизиса, а также определенный уровень летальности среди пациентов с полной окклюзией приводят к тому, что процент ангиографически полной окклюзии в более поздние сроки меньше, чем сразу после ИМ. Фармакологический тромболизис и ЧКВ вскоре после ИМ↑ST значительно увеличивают количество пациентов с проходимыми инфаркт-связанными КА.
ИМ↑ST с трансмуральным некрозом обычно развивается дистальнее острой окклюзии КА при наложении тромба на поврежденную атеросклеротическую бляшку (АБ). Однако при такой постоянной полной окклюзии коронарной артерии (КА) не всегда возникает ИМ.
Коллатеральное кровообращение и другие факторы, например уровень метаболизма миокарда, наличие и локализация стенозов в других КА, скорость развития обструкции и объем миокарда, снабжаемого окклюзированным сосудом, влияют на жизнеспособность клеток миокарда, находящихся дистальнее сужения.
Во многих исследованиях при аутопсии или коронарной артериографии лишь у 5% пациентов с ИМ↑ST были нормальные коронарные сосуды. У таких пациентов ИМ могут вызывать лизированный эмбол, транзиторный окклюзи-рующий тромбоцитарный агрегат или длительный выраженный спазм коронарных артерий.
Исследования пациентов, у которых после недавней коронарной ангиографии (КАГ) все же развивался ИМ↑ST, помогли определить коронарную анатомию до инфаркта. И хотя стенозы высокой степени (если их выявляли) чаще, чем менее выраженные поражения, приводили к ИМ↑ST, в действительности большинство окклюзий происходило в сосудах с сужениями < 50%, выявленными ангиографически за месяц или даже за 1 год до события.
Эти данные свидетельствуют в пользу концепции развития ИМ↑ST в результате внезапной тромботической окклюзии в месте разрыва ранее необструктивной, но содержащей большое количество липидов атеросклеротической бляшки.
Когда коллатеральные сосуды перфузируют определенные зоны, ИМ может развиться на некотором расстоянии от места коронарного стеноза. Например, вследствие постепенной облитерации просвета ПКА нижняя стенка оставалась жизнеспособной только благодаря коллатеральным сосудам из левой передней нисходящей артерии. Позднее окклюзия этой артерии может привести к инфаркту диафрагмальной стенки.
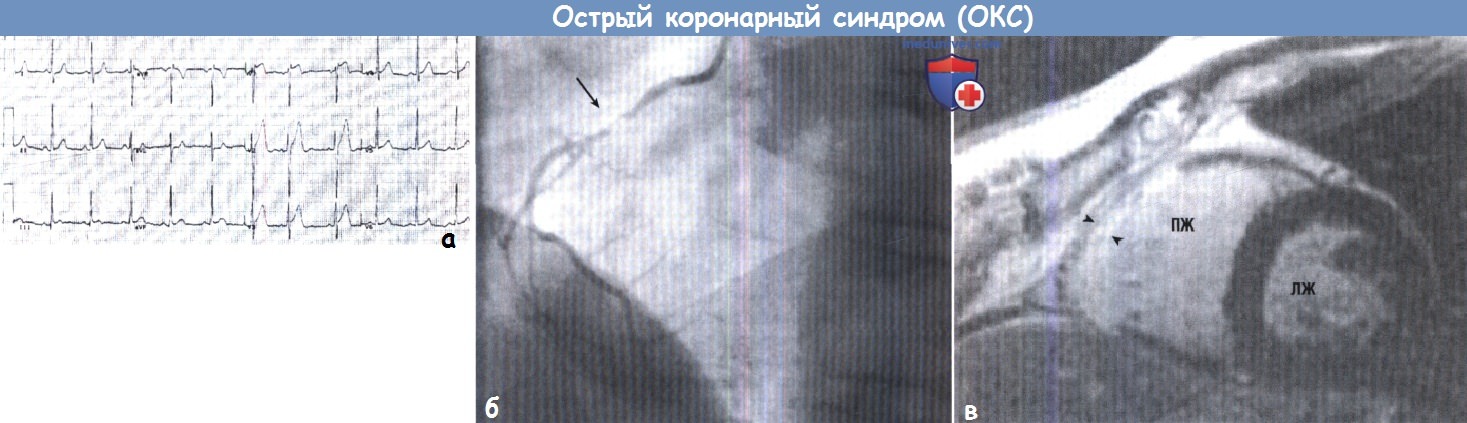
Пациент в возрасте 47 лет без заболевания сердца в анамнезе обратился в поликлинику с жалобами «на что-то в груди», сопряженными с двусторонней слабостью в руках.
(А) На первичной электрокардиограмме отмечается подъем сегмента ST в правых отведениях и в меньшей степени — в нижних.
Пациенту была назначена тромболитическая терапия и выдано направление на катетеризацию.
(Б) Ангиография выявила выраженный стеноз проксимальной части правой недоминирующей коронарной артерии (стрелка) без значительного поражения левой коронарной артерии.
(В) КМРТ с контрастным усилением демонстрирует отсроченное усиление, согласующееся с повреждением правого желудочка (ПЖ) и отчетливым вовлечением свободной стенки ПЖ (острия стрелок), не затрагивая левый желудочек (ЛЖ), а также верхушку ПЖ.
Пациент оставался гемодинамически стабильным все время нахождения в стационаре и выписан с улучшением состояния.
а) Инфаркт правого желудочка. У 50% пациентов с нижними ИМ поражение распространяется на ПЖ. Среди таких пациентов инфаркт ПЖ развивается только у тех, кто имеет трансмуральный ИМ нижнезадней стенки или задней части межжелудочковой перегородки (МЖП). Инфаркт ПЖ практически без исключений развивается совместно с инфарктом смежной МЖП и инфарктом нижней стенки ЛЖ, изолированный инфаркт ПЖ наблюдается лишь в 3-5% случаев, что подтверждается патоморфологически.
Инфаркт ПЖ происходит значительно реже, чем можно прогнозировать по частоте поражения ПКА. Это несоответствие, вероятно, объясняется более низкой потребностью ПЖ в кислороде. Инфаркты ПЖ чаще происходят в условиях повышенного потребления кислорода ПЖ, например при легочной гипертензии и гипертрофии ПЖ. Более того, коронарная система коллатералей ПЖ богаче, чем уЛЖ, а меньшая толщина стенок позволяет получать питательные вещества из крови, находящейся в полости.
В связи с этим ПЖ может переносить более длительные периоды ишемии и демонстрирует превосходное восстановление сократительной функции после реперфузии.
б) Инфаркт предсердий. Он наблюдается почти у 10% пациентов с ИМ↑ST, если смещение интервала PR использовать как критерий развития инфаркта предсердий. Несмотря на то что изолированный инфаркт предсердий по данным аутопсии встречается у 3,5% пациентов с ИМ↑ST, он часто развивается параллельно с ИМ желудочков и может вызвать разрыв стенки предсердия. Этот тип инфаркта более типичен для правых отделов сердца, чем для левых, чаще происходит в ушках предсердий, чем в боковой или задней стенке предсердия, и может быть результатом формирования тромба.
Различия в частоте развития между правым и левым предсердиями объясняются более высоким содержанием кислорода в крови, протекающей через левое предсердие. Инфаркты предсердий часто сопровождаются предсердными аритмиями. Также подтверждена связь со снижением секреции предсердного натрийуретического пептида и низким СВ при сопутствующем инфаркте ПЖ.
в) Коллатеральное кровоснабжение при остром инфаркте миокарда. Коронарная коллатеральная циркуляция хорошо развита у пациентов:
(1) с окклюзивным коронарным заболеванием, особенно при уменьшении просвета сосуда на > 75% в одном или нескольких основных сосудах;
(2) с хронической гипоксией, которая развивается при выраженной анемии, хронической обструктивной болезни легких и цианотических врожденных пороках сердца;
(3) с ГЛЖ.
Уровень коллатерального коронарного кровотока — это один из основных критериев размера ИМ. Действительно, пациенты с развитыми коллатералями могут иметь полностью окклюзированные КА без признаков ИМ при распределении крови от этой артерии. Таким образом, выживание миокарда дистальнее подобных окклюзий во многом зависит от коллатерального кровотока.
Даже если коллатеральная перфузия, присутствующая на момент коронарной окклюзии, не может предотвратить развитие ИМ, она может в дальнейшем дать положительный эффект в плане предотвращения развития аневризмы желудочка. Вполне вероятно, что наличие стеноза высокой степени (90%), возможно с периодами перемежающейся тотальной окклюзии, влияет на развитие коллатералей, которые остаются потенциальными коммуникантными сосудами до момента полной окклюзии или повторных ее эпизодов. Тотальная окклюзия приводит к тому, что эти сосуды становятся полностью функционирующими.

г) Неатеросклеротические причины острого инфаркта миокарда. Помимо атеросклероза приводить к ИМ↑ST могут разнообразные патологические процессы в КА. Например, окклюзии КА могут происходить в результате их эмболизации. Причины коронарной эмболии многочисленны: инфекционный эндокардит и небактериальный тромботический эндокардит, пристеночный тромб, протезы клапанов, неопластический процесс, воздух, попавший в процессе операции на сердце, и депозиты кальция при манипуляциях с кальцифицированными клапанами во время операций. Тромбоз КА in situ может происходить вторично после травмы грудной клетки.
За нарушения в КА могут отвечать некоторые воспалительные процессы, симулирующие атеросклеротическое заболевание и провоцирующие атеросклероз. Эпидемиологические исследования свидетельствуют, что иногда инфаркт миокарда могут вызывать вирусные инфекции, особенно вызванные вирусом Coxsackie В. Вирусные заболевания могут предшествовать ИМ у молодых пациентов, у которых впоследствии определяют неизмененные КА.
Сифилитический артериит может вызвать сужение или окклюзию обоих коронарных устий, а артериит Takaya.su — привести к обструкции КА. Некротизирующий артериит, узелковый полиартериит, кожнослизистый лимфатический синдром (болезнь Kawasaki), системная красная волчанка и гигантоклеточный артериит могут вызывать коронарную окклюзию. Терапевтическое облучение средостения может привести к коронарному артериосклерозу с последующим инфарктом. ИМ также может быть результатом поражения КА при амилоидозе, мукополисахаридозе I типа (болезнь Hurler), эластической псевдоксантоме и гомоцистинурии.
В связи с распространением кокаиновой зависимости сообщения о развитии НМ после употребления кокаина стали появляться все чащ. Кокаин может вызывать ИМ у пациентов с нормальными КА, с ИМ в анамнезе, при наличии коронарного заболевания или вследствие спазма коронарных артерий.
д) Инфаркт миокарда при ангиографически нормальных коронарных сосудах. Пациенты, перенесшие ИМ↑ST на фоне нормальных КА, обычно молодого возраста с относительно немногочисленными факторами коронарного риска, за исключением длительного курения. Обычно у них в анамнезе стенокардия не отмечается. Как правило, у таких пациентов не бывает продромальных состояний, тем не менее клинические, электрокардиографические признаки и лабораторные данные ИМ↑ST y них подобны таковым у большинства пациентов с ИМ↑ST, имеющих классическое обструктивное атеросклеротическое поражение КА.
После выздоровления у этих пациентов при ангиографии ЛЖ часто определяют зоны локальной дискинезии и гипокинезии. Причиной многих случаев является спазм КА и/или тромбоз, возможно при наличии исходной ЭД или небольших АБ, не выявленных при КАГ. Шарообразное расширение верхушки ЛЖ (кардиомиопатия takotsubo) характеризуется транзиторными нарушениями движения стенки верхушки и средней части ЛЖ. Этот синдром развивается при отсутствии обструктивного эпикардиального поражения КА и может имитировать ИМ↑ST. Обычно эпизоду КМП takotsubo предшествует психологический стресс.
Этиология не ясна, но специалисты считают, что важную роль в развитии играют индуцируемое катехоламинами станнирование миокарда и микрососудистая дисфункция.
Другими причинами могут быть:
(1) коронарные эмболы (возможно, при наличии небольших пристеночных тромбов, ПМК или миксомы);
(2) заболевания КА малого диаметра, которые невозможно визуализировать с помощью коронарной артериографии, или тромбоз КА с последующей реканализацией;
(3) большой спектр гематологических расстройств, вызывающих тромбоз in situ, при наличии нормальных КА (истинная полицитемия, врожденный порок сердца цианотичного типа с полицитемией, серповидно-клеточная анемия, синдром диссеминированного внутрисосудистого свертывания, тромбоцитоз и тромботическая тромбоцитопеническая пурпура);
(4) повышенная потребность в кислороде, например при тиреотоксикозе, употреблении амфетамина;
(5) гипотензия вследствие сепсиса, кровопотери или фармакологической терапии;
(6) анатомические особенности, например аномалии КА, коронарная артериовенозная фистула или миокардиальный мостик.
е) Прогноз. Долгосрочный прогноз для пациентов, перенесших ИМ↑ST на фоне ангиографически нормальных коронарных сосудов, более оптимистичный, чем после ИМ↑ST у пациентов, имеющих обструктивное поражение КА. После выздоровления повторные ИМ, СН или сердечная смерть для пациентов с нормальными КА нехарактерны. У большинства этих пациентов — отрицательная проба с физической нагрузкой, и лишь у немногих развивается стенокардия.
Учебное видео кровоснабжения сердца (анатомии артерий и вен)
При проблемах с просмотром скачайте видео со страницы Здесь
– Возврат в раздел сайта “кардиология”
Оглавление темы “Инфаркт миокарда (ИМ).”:
- Эффективность лечения инфаркта миокада (ИМ)
- Причины инфаркта миокарда без атеросклероза (острого коронарного синдрома, ОКС)
- Атеросклероз как причина острого коронарного синдрома (ОКС)
- Микроскопические изменения сердечной мышцы при инфаркте миокарда (ИМ)
- Световая микроскопия миокарда при инфаркте
- Варианты некроза миокарда при инфаркте
- Электронная микроскопия при инфаркте миокарда
- Апоптоз кардиомиоцитов при инфаркте миокарда
- Последствия реперфузии миокарда при инфаркте
- Коронарные артерии и локализация инфаркта миокарда
Источник
