Инфаркт это вид некроза сосудистого
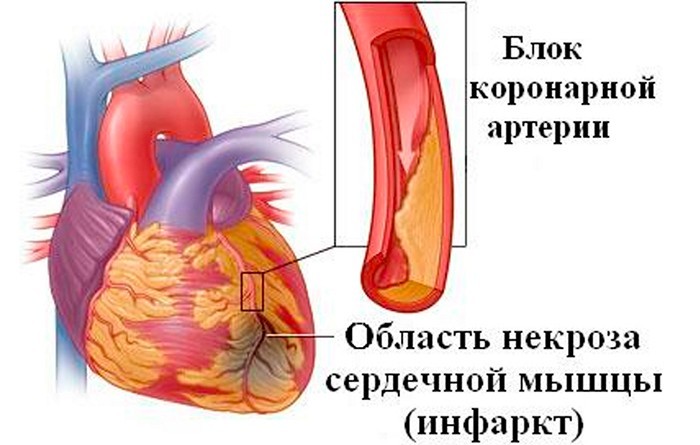
 Инфаркт миокарда. Виды, причины и лечение инфаркта миокарда. Кардиогенный шок.
Инфаркт миокарда. Виды, причины и лечение инфаркта миокарда. Кардиогенный шок.
Инфаркт Миокарда (ИМ) – это очаговый некроз (омертвение) сердечной мышцы (миокарда), обусловленный более или менее длительным прекращением доступа крови к миокарду.
В основе этого процесса лежит нарушение проходимости одной из коронарных (венечных) артерий сердца, пораженных атеросклерозом, которая приводит к коронарной недостаточности сердца. Атеросклероз — это длительный процесс, который постепенно ведет к сужению сосудов, замедлению тока крови.
Инфаркт – самое тяжелое проявление ишемической болезни сердца.
Нарушение проходимости коронарных артерий может произойти в результате закупорки артерии тромбом или из-за резкого его сужения — спазма.
Чаще всего в происхождении Инфаркта миокарда одновременно участвуют оба этих фактора.
Возникший в результате нервных влияний (переутомление, волнение, психическая травма и пр) длительный и сильный спазм коронарной артерии, замедлению тока крови в нем и образованию вследствие этого тромба.
В механизме возникновения инфаркта большое значение имеет нарушение процесса свертывания крови: увеличение в крови протромбина и других веществ, повышаюших свертывание крови, что и создает условия для образования тромба в артерии.
При инфарктах миокарда, в благоприятных случаях после расплавления омертвевшей ткани происходит ее рассасывание и замена молодой соединительной тканью (рубцевание). Прочный рубец формируется в течение 1,5 – 6 месяцев.
Реже, при неблагоприятном, тяжелом течении инфаркта, когда сердечная мышца подверглась омертвению на большую глубину, она резко истончается, и под влиянием внутрисердечного давления в этом месте образуется выбухание участка сердечной мышцы — аневризма сердца. На этом месте может произойти разрыв, что может привести к немедленной смерти, но это происходит довольно редко.
Причины инфаркта.
- Тромбоз, тромбоэмболия +атеросклероз.
- Атеросклероз + нервно-психическое напряжение, физическая нагрузка.
- Стресс.
В результате стресса происходит выброс катехоламинов, которые усиливают и учащают сердечные сокращения, вызывающих сужение сосудов, в результате возникает хроническая гипоксия тканей и органов. - Курение.
- Злоупотребление алкоголем.
Инфаркт чаще возникает у мужчин в возрасте 40-60 лет, а иногда и у более молодых. Заболевают чаще лица ведущие малоподвижный образ жизни, склонные к атеросклерозу, гипертонической болезни, ожирению, диабету и другим нарушениям обмена веществ. Около половины случаев инфаркт миокарда возникает на фоне стенокардии, и наоборот — у многих больных стенокардия наступает после перенесенного инфаркта.
Стенокардия и инфаркт миокарда представляют собой разные проявления одного и того же болезненного процесса.
Виды инфарктов миокарда.
Наиболее часто развиваются инфаркты в передней стенке левого желудочка, задней стенке левого желудочка, межжелудочковой перегородке и боковой стенке левого желудочка. Инфаркты правого желудочка встречаются очень редко.
По локализация очага некроза:
1. Инфаркт миокарда левого желудка (передний, боковой, нижний, задний),
2. Изолированный инфаркт миокарда верхушки сердца,
3. Инфаркт миокарда межжелудочковой перегородки,
4. Инфаркт миокарда правого желудочока,
5. Сочетанные локализации: задне-передний, передне-боковой, нижне-боковой и др.
По ширине поражения, определяется по ЭКГ:
1. Крупноочаговый (обширный) инфаркт миокарда (Q-инфаркт),
2. Мелкоочаговый инфаркт миокарда.
По глубине (в зависимости от того, какой слой сердца охвачен):
1. Субэндокардиальные,
2. Субэпикардиальные,
3. Интрамуральные
4. Трансмуральные (охватывает все слои сердца).
По течению:
1. Моноциклический ИМ
2. Затяжной ИМ
3. Рецидивирующий ИМ (развивается новый очаг некроза в течение 3-7 дней)
4. Повторный ИМ (новый очаг развивается через 1месяц)
Электрически немые зоны на ЭКГ– это инфаркт.
На ЭКГ лучше диагностируется трансмуральный инфаркт, инфаркт передней стенки. Трудно определить по ЭКГ инфаркт, который сочетается с аритмией, пароксизмальной тахикардией, блокадами и ЭКГ-негативные формы. По ЭКГ инфаркт определяется в 80% случаев.
Стадии развития инфаркта.
- Период предвестников, продромальный (от нескольких часов до нескольких дней).
Проявляется кратковременными болями в области сердца или за грудиной. В этот период уменьшается кровоснабжение сердца. - Острейший период, болевого приступа (от нескольких часов до 1 суток).
- Острый период, лихорадочный (8-10 дней).
Во 2-ой и 3-ий периоды происходит некроз и размягчение пораженного участка миокарда. - Подострый период (от 10 дней до 4-8 недель). Начинается период выздоровления.
- Период Рубцевания (от 1,5-2 мес. до 6 мес).
Клиника включает 2 синдрома:
1. Болевой синдром (условно)
2. Резапционно-некротический синдром (условно).
- Болевой синдром – это клиническое проявление развивающегося очага некроза. (1-ая стадия некроза).
- Типичный болевой с-м.
Это боль в области сердца, жгучая, давящая, иррадиирующая шире, чем при стенокардии в левую руку, правую, челюсть. Нет положения, успокаивающего боль. Боль нарастающая, больной бледный, появление липкого холодного пота, цвет кожных покровов серо-бледный, потом восковидный, может быть одутловатое лицо, аритмия. Систолическое давление падает, диастолическое остается на одном уровне или поднимается. Уменьшение расстояния АД между систолическим и диастолическим – признак инфаркта. Пульс слабый, нитевидный. Тоны глухие.
- Атипичный болевой с-м.
1-ая группа — Гастралгическая боль, изжога, слабость, рвота через 5-10 мин после еды, как правило сопровождается нарушением стула, вздутием живота.
2-ая группа — Безболевой синдром, по типу приступа сердечной астмы (status astmaticus), удушье, клокочущее дыхание. Но вводить эуфиллин при инфаркте, острой лево-желудочковой недостаточности нельзя.
Аритмическая форма- пока аритмия не купирована, больного надо лечить как при инфаркте.
Преходящие мозговые нарушения.- Бессимптомная форма– жалоб нет.
- Резапционно-некротический синдром – клинические проявления уже развившегося очага некроза, развившегося в очаге асептического воспаления. (2-ая стадия инфаркта).
- Резапционно-некротический синдром – это уже к концу первых суток и к началу вторых поднимается температура до 37,5—38,5 С. Температура должна в течение 7 дней нормализоваться. Но если длится более 7 дней , значит появились осложнения.
Лабораторные данные.
К концу первых суток появляется лейкоцитоз – 10-12000 (умеренно-нейтрофильный), стессовый – до 20000 лейкоцитов. В моче появляется белок, моча окрашена в красный цвет(миоглобинурия, миоглобин выходит). Миоглобин выходит при травмах мышц, в большом количестве может забить почечные фильтры и привести к почечной недостаточности. Ускорение СОЭ происходит в конце первых суток. А через 3-4 недели нормализуется.
К концу первых суток поднимается фибриноген А. В крови появляется патологический фибриноген В ( до ++++). Фибриноген В должен нормализоваться на 3-4 день. Фибриноген В повышается, если больному вводят фибринолитические вещества. С-реактивный белок появляется в острую стадию воспаления.
Повышение внутриклеточных трансаминаз при инфаркте описал Врублевский. Трансаминазы – это катализаторные ферменты в клетках. Клетки стареют, разрушаются, трансаминазы выходят в в кровь. Когда много клеток погибает, трансаминазы в большом количестве смываются кровью, миокард работает более активно — метаболическая гипертрофия. При инфаркте увеличивается количество трансаминаз АЛАТ, АСАТ, креатинфосфатазы, креатинфосфогеназы, лактатдегидрогеназы.
Увеличение ферментов — хороший метод диагностики, но только в острой фазе.
Эхокардиограмма — определяет очаги на любой стадии, но не определяет время развития инфаркта.
Лечение проводят в стационаре под мониторным наблюдением. Необходимо состояние покоя, небольшие движения, обязательное купирование боли.
- Можно грелку на сердце, теплый чай, подержать во рту водку или коньяк, анальгин, обезболивающие.
Морфий, Промедол и др. в/в с малыми дозами Атропина 0,3-0,5мл сочетать с Антигистаминными препаратами.
Таламанал 1 мл = 1мл Дроперидола + 1 мл Фентанал - Больной не должен спать, должен говорить. Нужно управлать дыханием (вдох — задержать — выдох).
Давать кислород через подушку, но через маску, давать увлажненный кислород через спирт.
Закись Азота 50% + Кислород 50%. Закись азота давать через наркозный аппарат. - Если есть тахикардия нужно давать в/в капельно поляризующую смесь ГИК (Глюкоза + Инсулин + Калий), KCl 1500–4500 + 5% Глюкозы + 4 ед. Инсулина на 200 мл. Затем 6 ед. Инсулина на 200 мл.
Нельзя вместо KCl давать NaCl. Диабетикам вместо глюкозы можно давать р-р Рингера или увеличить дозу Инсулина - Больному вводится 5-10 тыс. Гепарина, струйно, капельно, в эту же капельницу, что и смесь ГИК.
Лидокаин 1мл. струйно, затем капельно, B-блокаторы, Нитроглицерин в/в - Если развивается брадикардия, больному через каждые 2 часа вводится Атропин.
- При дефибрилляции желудочка — массаж сердца, дефибрилляторы.
- Если давление падает, в капельницу добавляем Кордиамин.
Лечение Кардиогенного Шока.
Применяют все методы, как при остром инфаркте + остальное. Обязательно обезболивание.
Кардиогенный шок связан с падением AD, с резким снижением сократительной способности миокарда.
- Даем Мезатон, если не помогает, то Адреналин, Норадреналин кап, в/в, если падает AD.
Норадреналин 0,2 п/к, в каждую руку. Допамин – кап, под контролем AD. - Можно давать Сердечные гликозиды в/в кап. Строфантин может дать остановку сердца. Корглюкон 0,06% до 2,0 мл – лучший сердечный гликозид, не кумулирует в организме.
- При кардиогенном шоке развивается ацидоз, можно давать капельно раствор Соды, Кокарбоксилаза – капельно можно до 200 мг (4 ампулы), в/м больше 50 мг нельзя.
- При кардиогенном шоке первое введение Гепарина – до 20 тыс. ед, суточная доза доходит до 100 тыс.ед.
В некоторых случаях применяют методы наружной и внутренней контрпульсации.
Резапционно-некротический – клинические проявления уже развившегося очага некроза, развившегося в очаге асептического воспаления. (2-ая стадия инфаркта).
КАТЕГОРИЯ:
Источник
Август 22, 2018
Нет комментариев
Некротические повреждения сердечной мышцы, т. е. гибель участков миокарда, бывают связаны или не связаны с нарушением коронарного кровообращения. В зависимости от этого они подразделяются на коронарогеннш и некоронарогенные некрозы.

Коронарогенные (ишемические) некрозы миокарда
Некроз миокарда, возникающий вследствие ухудшения коронарного кровотока (ишемии), называется инфарктом миокарда.
Некроз инфаркт миокарда
представляет собой одну из острых форм ИБС, при которой доставка к сердцу кислорода и питательных веществ не удовлетворяет потребности сердца в этих веществах.
Этиология
В этиологии инфаркта миокарда играют важную роль атеросклероз коронарных артерий, их тромбоз, спазм и (достаточно редко) эмболия коронарных артерий. К факторам риска инфаркта миокарда можно отнести все те, которые указаны как факторы риска ИБС (см. начало данного раздела). Сочетание двух или трех факторов риска увеличивает вероятность возникновения инфаркта миокарда.
Патогенез
Выделяют следующие последовательно развивающиеся стадии в патогенезе инфаркта миокарда.
1. Выключение дыхательной цепи митохондрий и активация гликолиза как следствие начавшейся ишемии. Накопление недоокисленных продуктов метаболизма (прежде всего молочной кислоты) обусловливает появление боли.
2. Ингибирование основных метаболических путей, подавление гликолиза (из-за слишком большого снижения pH в ткани миокарда) и цикла Кребса, вследствие чего развивается дефицит аденозинтрифосфата. Наблюдается накопление жирных кислот вследствие угнетения их р. окисления, а также нарушение ионного равновесия в кардиомиоцитах
3. Разрушение мембран кардиомиоцитов в результате включения в патогенез инфаркта так называемой липидной триады. В нее входят активация липаз и фосфолипаз, активация свободнорадикального перекисного окисления липидов и детергентное действие на миокард избытка жирных кислот. Все указанные изменения происходят в мембранах сарколеммы, лизосом, саркоплазматического ретикулума и митохондрий и приводят к их повреждению и повышению проницаемости. Следствием этого является выход аутолитических ферментов лизосом в клетки миокарда, а также накопление в них избытка свободного Са++. Избыток Са++ вызывает контрактуру миофибрилл и приводит к дальнейшей активации липаз и фосфолипаз.
4. Заключительная стадия необратимых повреждений кардиомио-цитов и некроз ишемического участка миокарда.
Клинические проявления
Основными клиническими симптомами инфаркта миокарда являются:
1. Локализующаяся за грудиной сильнейшая боль, иррадиирующая в левое плечо, левую руку и межлопаточную область. Эта боль может возникать в покое днем или в ночное время.
В отличие от приступа стенокардии болевой синдром при инфаркте миокарда длится дольше и не купируется повторным приемом нитроглицерина. Следует отметить, что в тех случаях, когда болевой приступ длится более 15 мин, а принимаемые меры неэффективны, необходимо немедленно вызвать бригаду скорой медицинской помощи.
Встречаются и атипичные формы инфаркта миокарда, при которых характерные симптомы, в частности болевой синдром, могут отсутствовать (безболевая форма инфаркта миокарда).
2. Ослабление сократительной способности миокарда вследствие выпадения из акта сокращения поврежденного участка миокарда ведет к уменьшению сердечного выброса. При этом в зоне некроза с помощью эхокардиографии могут выявляться различные нарушения движения стенки поврежденного желудочка: акинезия, гипокинезия, дискинезия (выбухание участка инфаркта в момент систолы). Последнее может свидетельствовать о формировании острой аневризмы сердца-
3. Аритмии. В связи с изменением в зоне инфаркта биоэлектрических свойств кардиомиоцитов возникают нарушения сердечного ритма (вплоть до развития фибрилляции сердца), что приводит к значительным расстройствам системной гемодинамики и усугубляет нарушение контрактильной функции сердца. Источником эктопической активности на ранних стадиях развития инфаркта служит, как правило, окржающая зону некроза так называемая паранекротическая зона.
4. Появление типичных изменений ЭКГ. К ним относятся смещение сегмента ST выше или ниже относительно изоэлектрической линии, появление патологического комплекса QS (свидетельствует о наличии в миокарде очага глубокой ишемии или некроза), а также появление гигантского зубца Т. Он может быть положительным или отрицательным. Если подобный зубец Т появляется в раннем периоде инфаркта миокарда, его трактуют (как и смещение сегмента ST) как проявление острой ишемии миокарда. Если же он появляется на поздних стадиях, его связывают с формированием в миокарде рубцовых изменений.
В зависимости от особенностей изменений ЭКГ различают следующие формы инфаркта миокарда:
• Q-образующий инфаркт, или Q-инфаркт (с формированием патологического глубокого зубца Q, что может свидетельствовать о крупноочаговом трансмуральном инфаркте);
• Q-необразующий инфаркт, или He-Q-инфаркт (сопровождается не появлением зубца Q, а появлением отрицательного зубца Т, что свидетельствует о мелкоочаговом инфаркте миокарда).
5. В крови повышается содержание так называемых маркеров инфаркта миокарда: миокардиальной фракции креатинфосфокиназы, миоглобина, а также тропонина-Т, который имеет на сегодняшний день наиболее важное значение в диагностике инфаркта миокарда.
6. Одно из важных проявлений инфаркта миокарда – ухудшение реологических свойств крови, что способствует тромбообразованию. При инфаркте миокарда венозный тромбоз диагностируется у 10-15 % больных.
7. Кроме описанных выше изменений могут наблюдаться расстройства мозгового кровообращения, нарушения функции желудочно-кишечного тракта. Через несколько часов от начала инфаркта миокарда развивается лейкоцитоз. Весьма характерно для инфаркта появление так называемого симптома перекреста между числом лейкоцитов в крови и СОЭ, когда в конце 1-й недели выраженность лейкоцитоза снижается, а СОЭ увеличивается.
Осложнения
К ранним осложнениям относят острую сердечную недостаточность, кардиогенный шок, отек легких, механические осложнения (разрыв папиллярных мышц, перегородки и стенок миокарда), тампонаду сердца, перикардит, тромбоэмболию легочной артерии, являющуюся одной из наиболее частых причин внезапной смерти.
К поздним осложнениям (возникают через 2-3 нед. и более от начала инфаркта) относят постинфарктный синдром Дресслера, хроническую недостаточность кровообращения, развитие аневризм сердца, тромбоэмболию легочной артерии и повторные инфаркты миокарда. Что касается синдрома Дресслера, то он возникает через 2-6 нед. от начала инфаркта и проявляется перикардитом, плевритом и пневмонией. В его патогенезе играет роль образование аутоантител к деструктивно измененным при инфаркте белкам миокарда — миокардиальным аутоантигенам.
Принципы патогенетической терапии
1. Ликвидация болевого приступа с помощью сильнодействующих анальгетиков и наркотических средств.
2. Использование антиагрегантов и тромболитических препаратов. В качестве доврачебной помощи рекомендуется использовать аспирин.
3. Уменьшение потребности сердца в кислороде, улучшение его доставки и снижение риска возникновения аритмий ф-адреноблокаторы).
Рекомендуется также использовать:
• ингибиторы ангиотензинпревращающего фермента;
• седативные и снотворные препараты;
• противоаритмические средства.
4. Важное значение имеют и хирургические методы лечения, в частности аортокоронарное шунтирование и баллонная ангиопластика со стентированием коронарных артерий.
Некоронарогенные (неишемические) некрозы миокарда
Поражения сердца этого типа возникают как результат нарушения метаболизма в сердечной мышце в связи с действием на сердце избытка электролитов, гормонов, токсических продуктов обмена, кардиальных аутоантител. Различают следующие виды некоронарогенных некрозов миокарда.
Электролитно-стероидные некрозы
Образование данного вида некрозов связано с патогенным действием на миокард избытка вводимых в организм гормонов коры надпочечников (прежде всего минералокортикоидов) в сочетании с солями натрия. Такое воздействие приводит к увеличению проницаемости мембран кардиомиоцитов для натрия и накоплению его в сердце. Развивающийся впоследствии отек и «осмотический взрыв» клеток миокарда сопровождается возникновением очагов некроза.
Катехоламиновые некрозы миокарда
Повреждающее действие избыточных концентраций катехоламинов на сердце объясняется следующими механизмами.
Во-первых, сами катехоламины, и прежде всего адреналин, обладают прямым повреждающим действием на миокард.
Во-вторых, несмотря на то что катехоламины расширяют коронарные сосуды, они в значительно большей степени увеличивают потребность сердца в кислороде, т. к. повышают частоту сердечных сокращений и артериальное давление. Поэтому при прохождении крови по венечным сосудам кислород утилизируется раньше, чем кровь достигнет прекапиллярного отдела микрососудистого русла. Это приводит к тому, что в миокарде появляются участки, получающие кровь, обедненную кислородом.
В-третьих, под влиянием избытка катехоламинов в миокарде происходит активация перекисного окисления липидов, продукты которого повреждают мембраны кардиомиоцитов.
Токсические и воспалительные некрозы миокарда
Данные виды некрозов возникают при интоксикации или поражении миокарда воспалительным процессом. Токсический миокардит может возникать вследствие воздействия некоторых химических соединений и фармакологических препаратов, например кокаина, лекарственных средств, применяемых при лечении злокачественных опухолей. Эти токсические вещества оказывают прямое повреждающее действие на миокард, приводя к развитию необратимой дистрофии и появлению мелкоочаговых некрозов.
Примером воспалительных некрозов миокарда служат различные миокардиты: ревматические и дифтерийные. При любом воспалительном процессе, как и в данном случае, наблюдается альтерация (повреждение) миофибрилл. Развивающийся воспалительный отек также способствует альтерации. Все это ведет к развитию микронекрозов миокарда.
Аутоиммунные некрозы
Одним из примеров аутоиммунных некрозов миокарда служит синдром Дресслера, о котором было сказано выше.
Поврежденные белки при инфаркте миокарда могут стать аутоантигенами, к которым в организме вырабатываются антитела. Повторное развитие некротического процесса обусловливает запуск реакции «антиген-антитело» во многих участках сердечной мышцы, что вызывает множественные микронекрозы.
Загрузка…
Источник
