Цитофлавин в профилактике инсульта

Комментарии
Опубликовано в журнале:
Журнал неврологии и психиатрии, 12, 2016
doi: 10.17116/jnevro201611612144-47
Ф.Х. Муратов1, Ф.К. Шермухамедова1, Б.В. Батоцыренов2, Т.В. Харитонова2
1 Ташкентская медицинская академия, Ташкент, Узбекистан; 2 ГБУ «Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе», Санкт-Петербург, Россия
Цель исследования. Оценка эффективности применения препарата цитофлавин у больных с острым ишемическим инсультом (ИИ) на фоне метаболического синдрома. Материал и методы. Обследованы 120 больных (60 пациентов — основная группа и 60 пациентов — группа сравнения). Всем больным проводилась стандартная базисная терапия, направленная на коррекцию гемодинамики, реологических свойств крови, профилактику осложнений инсульта. В основной группе дополнительно был назначен цитофлавин: первые 10 дней внутривенно капельно по 20 мл (на 200 мл 0,9% раствора NaCl) 2 раза в сутки, на 11—35-е сутки — по 2 таблетки 2 раза в день. Пациенты группы сравнения получали пирацетам: 10 дней внутривенно капельно по 30 мл (на 200 мл 0,9% раствора NaCl) 2 раза в день, на 11—35-е сутки — по 2 капсулы (800 мг) 2 раза в день. Проводилась оценка динамики восстановления функций по шкалам NIHSS, Рэнкина, Бартел, MMSE и данных компьютерной томографии очага ишемии. Результаты и заключение. Применение цитофлавина способствует уменьшению очага ишемического поражения головного мозга, улучшению неврологического статуса и когнитивных функций пациентов, что ведет к более раннему восстановлению способности к самообслуживанию больных с ИИ.
Ключевые слова: ишемический инсульт, метаболический синдром, цитофлавин.
Influence of multimodal effect of cytoflavin in the acute brain stroke in patients with metabolic syndrome
F.Kh. Muratov, F.K. Shermukhamedova, B.V. Batocyrenov, T.V. Haritonova
Tashkent Medical Academy, Tashkent, Uzbekistan; Dzhanelidze St. Petersburg Research Institute of Emergency Medicine, St. Petersburg, Russia
We present the results of a multicenter study on efficacy of cytoflavin in the treatment of patients with acute ischemic stroke. One hundred and twenty patients (60 of main group and 60 of control group) were enrolled in the study. All patients received basic therapy aimed at to improve systemic hemodynamics. Rheological blood properties and to prevent stroke complications. Patients of main group were treated with cytoflavin as follows: 1—10 days —20 ml (in200 ml of 0.9% NaCl solution) twice a day intravenously in groups: 11—35 days —850 mg twice a day. We assessed dynamics of restoration of lost functions (NIHSS, Rankin scale, Barthel index) and volume of ischemic lesion (KT, diffusion-weighted image). We reveled a trend towards effect of cytoflavin on the preservations of brain mater in acute phase of stroke. Cytoflavin reduced neurological deficit and improved activities of daily living in patients that may be explained by less brain damage.
Keywords: metabolic syndrome, cytoflavin, an ischemic stroke.
Метаболический синдром (МС) является в настоящее время одной из важных проблем медицины. Диагностика МС имеет большое значение, поскольку это состояние лежит в основе таких заболеваний, как сахарный диабет 2-го типа, эссенциальная гипертензия, атеросклероз и др., т.е. заболеваний, которые являются основными причинами смертности во всем мире. По данным литературы [1—4], в западных странах распространенность МС составляет в среднем 25—35%. С возрастом частота развития МС увеличивается, составляя 42—43,5% у лиц старше 60 лет. В США от МС страдают примерно 47 млн граждан. Наличие МС увеличивает в 3 раза риск развития сердечно-сосудистых заболеваний и их осложнений [5—7].
Вопрос о существовании данного синдрома и необходимости установления его диагноза активно обсуждается в научной литературе. Вместе с тем в современной литературе недостаточно четко описаны подходы к профилактике инсульта у пациентов с МС. Следует подчеркнуть, что в крупном исследовании [7], проведенном в Швеции и Финляндии, установлено: распространенность инсульта у пациентов с проявлениями МС составляет 4,8%, в то время как у лиц без МС — 1,4%.
Метаболические, функциональные и морфологические особенности нервной системы, многофакторность патогенеза, зональность и этапность ишемического повреждения головного мозга при инсульте создают чрезвычайно сложные условия для успешного использования препаратов нейропротективного действия. Однако поиск оптимального нейропротективного препарата (или комбинации препаратов) является одной из наиболее актуальных задач клинической и экспериментальной ангионеврологии [8—10].
Анализ работ, посвященных прогнозу исходов консервативного лечения сосудистых осложнений МС, показал отсутствие единого подхода к тактике ведения таких больных. На сегодняшний день общепризнанным консервативным методом лечения считаются коррекция артериального давления, сахарного диабета и другие виды симптоматической терапии [10].
В то же время теоретические представления о значимости прогрессирования вторичной ишемии и дизрегуляции оксидантных и антиоксидантных систем, расширения перифокальной зоны в патогенезе ишемического инсульта (ИИ) создают предпосылки для изучения и внедрения новых эффективных методов лечения, в том числе базирующихся на коррекции свободнорадикальных процессов.
В последние годы широко изучается действие янтарной кислоты (сукцинат), ее солей и эфиров, представляющих собой универсальные внутриклеточные метаболиты. Янтарная кислота, содержащаяся во всех тканях и органах, является продуктом 5-й и субстратом 6-й реакции цикла трикарбоновых кислот. Окисление янтарной кислоты в 6-й реакции осуществляется с помощью сукцинатдегидрогеназы. Выполняя каталитическую функцию в цикле Кребса, янтарная кислота снижает в крови концентрацию других продуктов цикла — лактата, пирувата, цитрата, продуцируемых и накапливающихся на ранних стадиях гипоксии. Феномен быстрого окисления янтарной кислоты сукцинатдегидрогеназой, сопровождающийся АТФ-зависимым восстановлением пула пиримидиновых динуклеотидов, называется «монополизацией дыхательной цепи», биологическое значение данного феномена заключается в быстром ресинтезе АТФ [8]. В нервной ткани функционирует цикл Робертса, или так называемый γ-аминобутиратный шунт, в ходе которого из γ-аминомасляной кислоты (ГАМК) через промежуточную стадию янтарного альдегида образуется янтарная кислота. Образование янтарной кислоты возможно также в условиях гипоксии и окислительного стресса в реакции окислительного дезаминирования α-кетоглутаровой кислоты в печени. Янтарная кислота нормализует содержание медиаторов воспаления, гистамина и серотонина, улучшает микроциркуляцию в органах и тканях, прежде всего в мозге, не оказывая влияние на артериальное давление и показатели работы сердца. Антигипоксантный эффект янтарной кислоты связан с активацией сукцинатдегидрогеназного окисления и с восстановлением активности цитохромоксидазы — ключевого окислительно-восстановительного фермента дыхательной митохондриальной цепи [8].
Цель настоящего исследования — оценка эффективности применения препарата цитофлавин (ООО «НТФФ «ПОЛИСАН», Санкт-Петербург, Россия) у больных с острым ИИ на фоне МС.
Материал и методы
Объективное неврологическое исследование было проведено у 120 пациентов с ИИ полушарной локализации, развившемся на фоне МС. В исследование были включены больные с острым ИИ (МКБ-10: I63.0—I63.9.), соответствующие критериям: возраст от 40 до 80 лет; срок поступления до 72 ч от момента заболевания (если точное время начала инсульта неизвестно, то принималось среднее время между тем, когда пациента видели последний раз в нормальном состоянии, и временем, когда у него обнаружили симптомы инсульта); ИИ полушарной локализации с объемом поражения не более двух смежных бассейнов мозговых артерий в одном полушарии; начало терапии в стационаре в первые 72 ч от момента заболевания; оценка по шкале комы Глазго от 15 до 10 баллов; легкая и средняя тяжесть инсульта по шкале NIHSS (до 21 балла включительно); диагноз инсульта, верифицированный с помощью КТ, проведенной в течение 72 ч от начала заболевания; состояние до инсульта — функционально независимый амбулаторный больной (не более 2 баллов по модифицированной шкале Рэнкина); впервые возникший инсульт или повторный инсульт по данным анамнеза и данным медицинской документации с восстановлением по шкале Рэнкина до 2 баллов; количество лейкоцитов: лейкопения не менее 2500/мм³, лейкоцитоз не более 10500/мм³; количество эритроцитов — свыше 3 500 000 мм³; уровень образования: не менее 5 лет (до настоящего заболевания пациент умел читать, писать); пациенты, которые смогут, по мнению исследователя, соблюдать протокол в течение необходимого времени (комплаентные больные).
Лечение больных проводили в отделении интенсивной неврологии и реанимационном отделении 1-й клиники Ташкентской медицинской академии.
Все больные были рандомизированы на две группы, по 60 пациентов в каждой. Все они получали стандартную базисную терапию. Пациентам 1-й (основной) группы назначали цитофлавин по схеме: первые 10 дней внутривенно капельно по 20 мл (на 200 мл 0,9% раствора NaCl) 2 раза в сутки, на 11—35-е сутки — перорально по 2 таблетки 2 раза в день. Пациенты 2-й группы (сравнения) получали пирацетам по схеме: 10 дней внутривенно капельно по 30 мл (на 200 мл 0,9% раствора NaCl) 2 раза в день, на 11—35-е сутки — по 2 капсулы (800 мг) 2 раза в день.
Средний возраст всех обследованных пациентов составил 61,39±5,2 года. Средний возраст больных, получавших цитофлавин, составил 61,0±4,9 года, принимавших пирацетам — 62,2±5,3 года. Из 120 обследованных пациентов — 68 (56,7%) мужчин, 52 (43,3%) женщины. Половой состав в обеих группах был практически идентичным.
У 52 (43,33%) пациентов ишемические очаги поражения локализовались в правом полушарии, у 68 (56,67%) — в левом полушарии головного мозга.
Проводилась оценка динамики восстановления функций по шкалам NIHSS (Американская шкала инсульта), Рэнкина, Бартел, MMSE (краткая шкала оценки психического статуса) и данных КТ.
Статическая обработка полученных результатов с оценкой достоверности межгрупповых различий осуществлялась параметрическими (критерий Стьюдента) и непараметрическими (критерий Манна—Уитни) методами с использованием программы Microsoft Office Excel (2003).
Результаты и обсуждение
Все больные поступили в клинику в остром периоде заболевания, среди них в ясном сознании — 104 (86,66%) пациента. Нарушение сознания различной степени выраженности отмечались у 16 (13,3%) больных. Из них, согласно оценке степени нарушения сознания по шкале комы Глазго, у 10 (8,3%) больных определялось оглушение, у 6 (5,0%) больных — сопор. Средний балл по шкале Глазго при поступлении в основной группе составил 14,60±0,14 балла, в группе сравнения — 14,53±0,14 балла.
Для объективизации состояния и динамического обследования больных и сравнения эффективности терапии в двух группах пациентов проведена оценка тяжести неврологического дефицита по шкале NIHSS (табл. 1).
Таблица 1. Оценка неврологического статуса у больных с острым ИИ по шкале NIHSS
| Группа обследования | Средний балл по шкале NIHSS | ||
| 1-е сутки | 10-е сутки | 35-е сутки | |
| Основная (n=60) | 12,63±0,75 | 6,45±0,46 * *** | 2,33±0,27* ** *** |
| Сравнения (n=60) | 12,40±0,42 | 7,72±0,52* | 2,99±0,18* ** |
Примечание. Здесь и в табл. 2 и 3: * — p<0,001 — достоверность по отношению к 1-м суткам лечения; ** — p>0,001 — достоверность к 10-м суткам лечения; *** — p<0,05 — достоверность по отношению к группе сравнения.
Положительная динамика неврологического статуса с высокой статистической достоверностью (р<0,001) наблюдалась уже в первые 10 дней заболевания как в группе леченных цитофлавином, так и в группе сравнения. К 35-му дню заболевания у пациентов, принимавших цитофлавин, суммарный клинический балл по шкале NIHSS уменьшился до 2,33±0,27, у пациентов, получавших пирацетам, — до 2,99±0,18, что и в том и в другом случае свидетельствует об уменьшении неврологического дефицита и благоприятном прогнозе заболевания. Однако исследование клинической эффективности лечения цитофлавином и пирацетамом показало, что согласно шкале NIHSS к 10 и 35 дням заболевания имеется статистически значимая (р<0,05) положительная динамика неврологического дефицита у больных, леченных цитофлавином, по сравнению с больными, леченными пирацетамом. Статистическое сравнение регресса неврологического дефицита выявило не только достоверную разницу между выраженностью неврологического дефицита по шкале NIHSS, но и опережение темпа восстановления нарушенных функций у больных на фоне лечения цитофлавином.
Следующим этапом нашего исследования была оценка общей функциональной независимости по шкале Бартел и оценка степени инвалидизации по модифицированной шкале Рэнкина (табл. 2).
Таблица 2. Динамика среднего суммарного балла по шкале Бартел и модифицированной шкале Рэнкина
| Сутки обследования | Основная группа (n=60) | Группа сравнения (n=60) | ||
| средний балл по шкале Бартел | средний балл по шкале Рэнкина | средний балл по шкале Бартел | средний балл по шкале Рэнкина | |
| 1-е | 31,00±2,01 | 3,77±0,10 | 33,83±2,02 | 3,50±0,14 |
| 10-е | 58,86±2,17* *** | 2,43±0,12* *** | 52,83±2,05* *** | 2,10±0,11* *** |
| 35-е | 77,80±2,27* ** *** | 1,33±0,09* ** *** | 71,50±2,04* ** *** | 1,60±0,10* ** *** |
Функциональные возможности больных, оцениваемые по шкале Бартел в обеих группах, соответствовали дезадаптации средней степени выраженности. Анализ функционального исхода лечения показал, что как на 10-е, так и на 35-е сутки заболевания у больных, принимавших цитофлавин, отмечался более выраженный прирост возможностей самообслуживания. На фоне лечения балл по модифицированной шкале Рэнкина статистически значимо уменьшался у больных основной группы и группы сравнения, при этом восстановление нарушенных функций было более значимым на фоне терапии цитофлавином (р<0,05).
Таким образом, проведенный анализ свидетельствует о снижении выраженности неврологических нарушений, улучшении общего клинического состояния, повышении повседневной активности, уменьшении степени инвалидизации и более высоком уровне функциональных возможностей в группе, где применялся цитофлавин, чем в группе сравнения на 10-е и 35-е сутки заболевания.
Для оценки влияния исследуемого препарата на динамику когнитивного статуса было проведено обследование по шкале MMSE (табл. 3). Результаты исследования свидетельствуют об улучшении когнитивных способностей в обеих группах на 10-е и 35-й дни заболевания. Улучшение когнитивных функций больных с ИИ, получавших цитофлавин, статистически значимо превышало таковое у больных, получавших пирацетам.
Таблица 3. Оценка когнитивных функций у больных с острым ИИ по шкале MMSE
| Группа обследования | Средний балл по шкале MMSE | ||
| 1-е сутки | 10-е сутки | 35-е сутки | |
| Основная (n=60) | 15,97±0,93 | 23,57±0,72* *** | 27,43±0,52* ** *** p1<0,001 p3<0,05 |
| Сравнения (n=60) | 16,73±1,04 | 21,20±0,84* p1<0,001 | 25,91±0,49* ** |
Для объективизации полученных результатов проведено изучение состояния ишемического очага (размер) в динамике заболевания у обследованных групп. По данным КТ-исследований 91,в 1-е сутки средний размер ишемического очага у больных, лечившихся цитофлавином, составил 4,83±0,16 см², а у больных, получавших пирацетам, — 4,32±0,16 см². На 10-е сутки лечения зона ишемического очага у больных основной группы уменьшилась на 23,4% (3,70±0,14 см²), у больных группы сравнения — на 18,2% (3,53±0,14 см²), к 35-му дню средние размеры ишемического очага статистически значимо уменьшились и составили соответственно 2,17±0,14 и 2,35±0,14 см² (р<0,05).
Таким образом, терапия цитофлавином статистически значимо уменьшает размеры ишемического поражения головного мозга при ИИ полушарной локализации, развившемся на фоне МС. При этом уменьшение морфологических изменений мозга (по данным КТ) коррелирует с клиническим уменьшением неврологического дефицита и тяжести ИИ (по результатам оценки неврологического статуса по шкале NIHSS).
Применение ступенчатой терапии цитофлавином у больных с ИИ на фоне МС способствует восстановлению когнитивных функций и уменьшению степени инвалидизации. Это, безусловно, положительно влияет на уровень самообслуживания у пациентов, перенесших ИИ.
Литература
- Eckel RH, Grundy SM, Zimmet PZ. The metabolic syndrome. Lancet. 2005;365:1415-1428.
doi: 10.1016/S0140-6736(05)66378-7 - Hanley AJ, Karter AJ, Williams K, Festa A, D’Agostino RB Jr, Wagenknecht LE, Haffner SM. Prediction of type 2 diabetes mellitus with alternative definitions of the metabolic syndrome: the Insulin Resistance Atherosclerosis Study. Circulation. 2005;112:3713-3721.
doi: 10.1161/CIRCULATIONAHA.105.559633 - Arenillas JF, Moro MA, Dávalos A. The Metabolic Syndrome and Stroke. Stroke. 2007;38:2196-2203.
doi: 10.1161/STROKEAHA.106.480004 - Grundy SM, Brewer HB Jr, Cleeman JI, Smith SC Jr, Lenfant C; American Heart Association; National Heart, Lung, and Blood Institute. Definition of Metabolic Syndrome: Report of the National Heart, Lung, and Blood Institute/American Heart Association Conference on Scientific Issues Related to Definition. Circulation. 2004;109:433-438.
doi: 10.1161/01.CIR.0000111245.75752.C6 - Negrato CA, Tambascia M, Calderon IM, Pauletti TA, Rudge MV. Current Diagnostic Criteria of the Metabolic Syndrome. Femina. 2007;35:623-629.
- Alberti KG, Zimmet P, Shaw J. IDF Epidemiology Task Force Consensus Group. The metabolic syndrome — a new worldwide definition. Lancet. 2005;366(9491):1059-1062.
doi: 10.1016/S0140-6736(05)67402-8 - Isomaa B, Almgren P, Tuomi T, Forsén B, Lahti K, Nissén M, Taskinen MR, Groop L. Cardiovascular morbidity and mortality associated with the metabolic syndrome. Diabetes Care. 2001;24(4):683-689.
- Федин А.И., Румянцева С.А. Современные подходы к энергокорригирующей терапии гипоксических поражений мозга. Consilium Medicum. 2007;9:8:104-105.
- Гусев Е.И., Скворцова В.И. Ишемия головного мозга. M.: Медицина; 2001.
- Орлов С.В., Домашенко М.А., Танашян М.М. Особенности лечения больных с ишемическим инсультом на фоне метаболического синдрома. Атмосфера. Нервные болезни. 2008;4:2-5.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник
Комментарии
Опубликовано в журнале:
Амбулаторный прием / Т. 2. № 3 (6), 201 6
А. Л. Вёрткин, Г. Ю. Кнорринг
Московский государственный медико-стоматологический университет имени А. И. Евдокимова
В последние годы заметно растет интерес к исследованиям головного мозга и разработке новых способов коррекции различных нарушений мозговой деятельности. Нейропротекторная терапия относится к наиболее бурно развивающимся направлениям лечения заболеваний и нарушений функций головного мозга.
Появление нейропротекторной терапии во второй половине XX в. обусловлено существенным ростом числа работ, посвященных исследованию нервной системы. Тем не менее головной мозг остается самым малоизученным органом человеческого организма — не столько с точки зрения анатомии, сколько с позиций функциональной организации самой сложной из систем, благодаря которой, собственно, написаны и прочитаны эти строки.
Головной мозг вызывает особый интерес исследователей уже на протяжении многих веков и, конечно, последних десятилетий. Нельзя не отметить, что именно работы российских ученых (Сеченова И. М., Павлова И. П., Лурии А. Р.) сыграли большую роль в формировании представлений о высшей нервной деятельности, когнитивных функциях и памяти (рис. 1).

Рис. 1. Родоначальники учения о когнитивных функциях и их нарушениях
Новые методики, разработанные уже в XXI в., позволили не только точнее распознать анатомические особенности, но и изучить электрическую активность головного мозга, увидеть возбуждение его отдельных структур при разных видах мозговой деятельности (рис. 2).
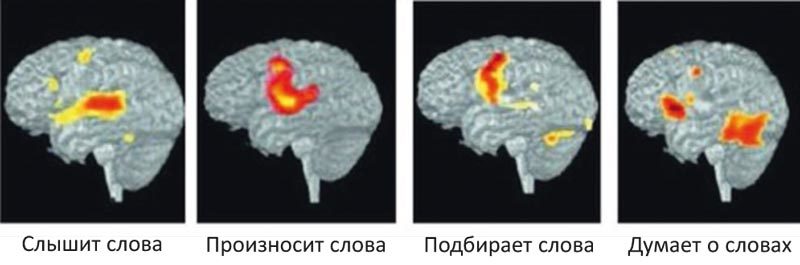
Рис. 2. Позитронно-эмиссионная томограмма при различных видах мозговой деятельности (A. C. Revkin. Fostering Insights by Engaging the Whole Brain)
Как известно, для деятельности головного мозга необходимо больше энергии, чем для работы любого другого органа: мозг является «лидером» по энергопотреблению в организме. Несмотря на относительно небольшую массу (отношение массы головного мозга к общей массе тела составляет всего 2%), на мозг «работает» 15% сердца, причем он потребляет более 20% кислорода и 80% глюкозы. Интенсивность потребления кислорода нейронами в десятки раз превышает потребности других клеток и тканей, составляя 350–50 мкл О2/г в минуту, в то время как для сердца необходимо 70–90 мкл/г в минуту, для скелетных мышц соответствующий показатель составляет 1,6–2,4 мкл/г, для фагоцитирующих лейкоцитов — 9–24 мкл/г [2].
Мозг в состоянии бодрствования вырабатывает от 10 до 23 ватт электроэнергии (этого хватит, чтобы зажечь лампочку!). Общая длина кровеносных сосудов в мозге превышает 100000 км, а скорость проведения импульсов в нервной системе человека достигает 288 км/ч, и лишь к старости снижается до 220 км/час.
При такой мощной метаболической активности и ювелирности протекающих процессов нервная ткань оказывается достаточно чувствительна к нарушениям кровообращения, гипоксии и иным электролитным, метаболическим и свободнорадикальным сдвигам. Средства антиишемического и антирадикального действия, изначально предложенные для терапии инсультов и получившие название «нейропротекторы», при последующем изучении оказались полезны и при менее значимых нарушениях функций мозга, черепно-мозговых травмах, астенических состояниях, а также в детской практике [2]. Многообразие патофизиологических изменений при заболеваниях мозга стимулировало исследования более чем 1000 субстанций, предположительно, способных повлиять на выживаемость нейронов в условиях недостатка глюкозы и кислорода [12]. Большую часть этих препаратов обычно отбраковывают еще на экспериментальном этапе разработки.
Проведено более 160 клинических исследований нейропротекторов, однако на долю крупных исследований с участием более 200 пациентов приходится только около четверти [11]. На сегодняшний день не удалось продемонстрировать убедительное преимущество подавляющего большинства препаратов при лечении ишемического инсульта, что связано с неудовлетворительным дизайном доклинических исследований, малыми выборками пациентов, невозможностью использовать адекватные дозы препаратов в исследованиях у людей и другими аспектами [10–11].
Нейропротекция — общемировой тренд, объединяющий и неврологию, и терапию, и психиатрию: по мнению многих ученых, именно за нейропротекторами — будущее человечества, все более погружающегося в глубины собственного разума (рис. 3).

Рис. 3. Нейропротекция — общемировой тренд
Один из хорошо изученных комплексных препаратов с доказанной эффективностью — Цитофлавин производства российской научно-технологической компании «Полисан». Состав Цитофлавина представлен комбинацией хорошо изученных веществ, апробированных на практике (табл. 1).
Таблица 1. Состав препарата Цитофлавин
| Основные компоненты, мг | Ампулы | Таблетки |
| Янтарная кислота | 1000 | 300 |
| Никотинамид | 100 | 25 |
| Рибофлавин мононуклеотид | 20 | 5 |
| Рибоксин | 200 | 50 |
| Вспомогательные вещества, мг | ||
| N-метилглюкамин | 1650 | – |
Цитофлавин обладает комплексным действием: способствует компенсации дефицита энергетических субстратов и коррекции нарушений метаболизма, проявляет антирадикальный и антигипоксантный эффекты. Все компоненты препарата являются естественными метаболитами человеческого организма, тропными к нервной ткани.
Янтарная кислота — энергокорректор + антигипоксант — эндогенный универсальный внутриклеточный метаболит, выполняющий в цикле Кребса каталитическую функцию. Янтарная кислота повышает скорость реакций цикла; стимулирует образование АТФ, необходимой для жизнедеятельности. Антигипоксическое действие реализовано вследствие увеличения концентрации ГАМК в мозговой ткани.
Рибофлавин — энергокорректор — флавиновый кофермент (ФАД), активирующий окислительно-восстановительные реакции цикла Кребса.
Никотинамид — антигипоксант + антиоксидант — влияет на окислительно-восстановительные процессы (кофермент НАД). Замедляет развитие энцефалопатии и снижает выраженность ее проявлений.
Инозин — энергокорректор — производное пурина, предшественник АТФ (метаболит). Обладает способностью активировать некоторые ферменты цикла Кребса, стимулируя синтез ключевых веществ. Защищает клетки от действия повреждающих факторов.
Фармакологическое действие
Фармакологические эффекты Цитофлавина обусловлены комплексным действием его компонентов. Препарат стимулирует дыхание и энергообразование в клетках, улучшает процессы утилизации кислорода тканями, восстанавливает активность ферментов антиоксидантной защиты. Он активирует синтез белка, способствует утилизации глюкозы и жирных кислот, а также ресинтезу ГАМК в нейронах.
Цитофлавин улучшает коронарный и мозговой кровоток, активирует метаболические процессы в ЦНС, восстанавливает сознание и интеллектуально-мнестические функции мозга, способствует коррекции рефлекторных нарушений и расстройств чувствительности. Благодаря сбалансированному составу препарат оказывает метаботропное, энергокорригирующее действие, активирует сукцинатгидразное окисление, увеличивает содержание ГАМК в головном мозге через шунт Робертса, восстанавливает как НАД-, так и ФАД-зависимые звенья цикла Кребса, ингибирует реакции окислительного стресса. Все это в конечном итоге приводит к оптимизации цикла трикарбоновых кислот, способствуя быстрому ресинтезу АТФ и предотвращая прогрессирование постишемического энергодефицита; таким образом, Цитофлавин оказывает противоишемическое действие, улучшает кровоток, ограничивает зону некроза и апоптоза, обладая выраженными нейропротекторными свойствами (рис. 4).
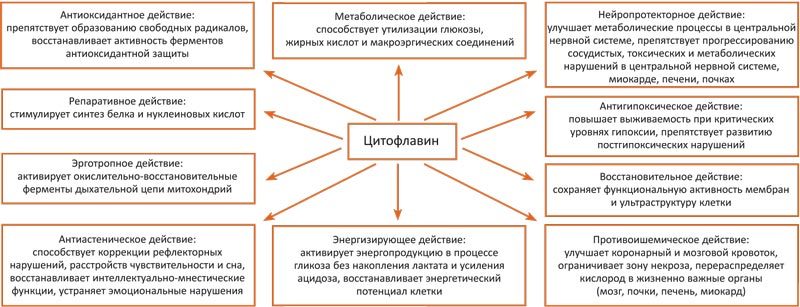
Рис. 4. Основные фармакологические эффекты и механизмы действия Цитофлавина
Применение Цитофлавина подтвердило его высокую эффективность у пациентов с разными формами цереброваскулярной недостаточности (от острых и острейших проявлений до отдаленных последствий ишемических повреждений головного мозга) [3, 5, 7–9]. Клинический результат при такой широте патологических состояний подчеркивает универсальный характер действия Цитофлавина при разных заболеваниях мозга, что объясняется разносторонним метаболическим действием основных компонентов препарата.
Например, в многоцентровом рандомизированном исследовании (2005; 8 клинических баз) показана эффективность Цитофлавина у больных с острым ишемическим инсультом (n = 300), причем наблюдение за пациентами вели в течение 120 дней [1]. Доказано, что применение Цитофлавина в раннем восстановительном периоде обеспечивает высокую клиническую эффективность (89,4%), положительную динамику неврологического статуса хотя бы по одному симптому (94%), статистически значимое увеличение показателей двигательной активности и речевой функции. Препарат положительно влияет на когнитивно-мнестические функции, улучшая концентрацию внимания и запоминание, увеличивает скорость сенсомоторных реакций, достоверно повышая объем краткосрочной и долговременной памяти, улучшает социальную адаптацию и качество жизни пациентов, положительно влияет на биоэлектрическую активность головного мозга у этой очень сложной в курации категории больных.
Продемонстрирована эффективность Цитофлавина в составе комплексной стандартной консервативной терапии геморрагического инсульта (n = 120) [4]. Результаты лечения заключались в снижении госпитальной летальности; более быстрой активации сознания, опережающей группу сравнения; уменьшении выраженности неврологических симптомов и улучшении функционального исхода к моменту выписки больных из стационара. Кроме того, результаты данного исследования доказали присутствие у больных с внутримозговыми кровоизлияниями окислительного стресса, выраженность которого в острейшем периоде превосходит таковую при инфаркте мозга. В ходе исследования продемонстрировано положительное влияние раннего (с первых 3 суток заболевания) включения Цитофлавина в комплексную терапию не только на клиническую картину заболевания, но и на различные показатели свободнорадикальных процессов кислородного и перекисно-липидного звена [4].
По результатам многоцентрового рандомизированного двойного слепого плацебо-контролируемого исследования, проведенного на базе 12 ведущих неврологических школ России, доказана высокая клиническая эффективность приема Цитофлавина внутрь у больных с хронической ишемией головного мозга I, II и III стадии [6]. В исследование включено 600 пациентов (средний возраст 51,3 ± 9,4 года), динамично обследованных в течение 60 дней. Цитофлавин (n = 320) или плацебо (n = 280) назначали по 2 таблетки 2 раза в сутки в течение 25 дней на фоне базисной терапии, включающей антиагреганты (100 мг ацетилсалициловой кислоты ежедневно) и антигипертензивные средства.
Установлено, что у пациентов, получавших Цитофлавин, статистически значимо уменьшилась частота жалоб на головную боль, головокружение, снижение памяти, эмоциональную лабильность и снижение работоспособности. Как показало исследование качества сна по шкале Sleep Quality Scale, к концу терапии в группе Цитофлавина на 26,8% увеличилось число пациентов с нормализацией сна, что сохранилось и на 60-е сутки, тогда как после курса плацебо улучшения удалось достичь у 9,9% пациентов (p < 0,05). Положительная динамика неврологического статуса на 30-е сутки установлена у 79% пациентов, получавших Цитофлавин, и у 27% пациентов, получавших плацебо (p < 0,05).
Для оценки астенического синдрома в динамике на 1-е, 30-е и 55-е сутки применяли валидизированные специализированные опросники: шкалу астенизации, госпитальную шкалу тревоги и депрессии, шкалу качества сна, а также опросники по оценке когнитивных функций (по тестам концептуализации интеллекта, беглости речи, «пятый лишний», запоминания 10 слов, Мюнстерберга). В ходе исследования выявлено положительное влияние Цитофлавина на клинические проявления и течение астеноневротического синдрома у больных с хронической цереброваскулярной недостаточностью. Отмечали мягкое стимулирующее действие препарата на ЦНС, отсутствие дневной сонливости. К 30-м суткам большинство пациентов меньше жаловались на быструю утомляемость, раздражительность, плохой сон, эмоциональную неустойчивость, плохую память и недостаточное внимание.
В группе получавших Цитофлавин число пациентов без астении увеличилось с 43,5% до 56,9%, а число больных с исходно выявленной астенией легкой степени — с 29,0% до 35,9% соответственно. В то же время значительно уменьшилось число больных с выраженными и умеренными проявлениями астении (до 1,9% и 5,3% соответственно). В группе больных, получавших плацебо-терапию, отмечена только статистически незначимая тенденция к улучшению.
Положительная динамика зарегистрирована по показателям субшкал «тревога» и «депрессия» (табл. 2).
Таблица 2. Динамика среднего балла субшкал астенизации, тревоги и депрессии
| Субшкалы | Больные, получавшие Цитофлавин | Больные, получавшие плацебо | ||
| 1-е сутки | 30-е сутки | 1-е сутки | 30-е сутки | |
| Астенизация | 77,9 ± 21,3 | 61,3 ± 15,4* | 71,2 ± 19,3 | 68,9 ± 17,6 |
| Тревога | 13,4 ± 3,2 | 9,6 ± 2,7* | 12,9 ± 4,1 | 12,6 ± 3,9 |
| Депрессия | 11,1 ± 2,5 | 8,4 ± 2,9* | 10,7 ± 3,1 | 9,9 ± 2,6 |
Под влиянием Цитофлавина улучшались и когнитивные функции. Препарат увеличивал объем непосредственного запоминания, улучшал внимание, память, мышление, под действием Цитофлавина наблюдали повышение трудоспособности и улучшение социальной адаптации. Так, в Московском областном научно-исследовательском клиническом институте им. М. Ф. Владимирского при выполнении теста Мюнстерберга (теста на внимание) на 30-е сутки эксперимента больным, принимавшим Цитофлавин, требовалось меньше времени для выполнения задания, они делали меньше ошибок, что существенно сказывалось на результате. Показатели в группе плацебо были лучше исходных, но уступали таковым в группе Цитофлавина.
У больных с хронической цереброваскулярной недостаточностью курсовая терапия Цитофлавином (100 таблеток в течение 25 дней) приводит к статистически значимому уменьшению выраженности как астенического, так и невротического синдрома. Применение Цитофлавина характеризуется быстрым наступлением клинического эффекта и отсутствием синдрома привыкания. Основное действие препарата заключается в улучшении когнитивно-мнестических функций, показателей качества жизни и сна пациентов. Это позволяет считать, что с помощью Цитофлавина можно купировать как отдельные симптомы астеноневротического синдрома, так и синдром в целом.
Заключение
Приведенные подтверждения положительных эффектов Цитофлавина при острой и хронической цереброваскулярной патологии служат доказательством того, что антиоксидантная энергокоррекция — универсальный механизм защиты нервной ткани. Противогипоксическое и антиоксидантное действие препарата проявляется более выражено в условиях ишемии, так как Цитофлавин препятствует резкому снижению уровня АТФ. Это также потенцирует антиоксидантное действие препарата. В клинической практике результатом стало улучшение неврологических и когнитивных функций, регресс астении, то есть улучшение качества жизни пациентов с различными формами цереброваскулярной болезни и астенией разного генеза.
Для достижения максимального и наиболее продолжительного эффекта терапии Цитофлавин следует назначать курсами (10 мл препарата на 200 мл 5%-ного раствора глюкозы или 0,9% раствора NaCl внутривенно капельно в течение 10 дней, затем в рамках ступенчатой терапии продолжить прием в течение 25 дней по 2 таблетки 2 раза в сутки) с перерывом 25–30 дней в течение 6–12 мес. Рекомендованные схемы применения при различных нозологических формах приведены в таблице 3.
Таблица 3. Показания, схемы и сроки применения Цитофлавина в клинической практике
| Показания | Период заболевания | Схема приема | Курс |
| Острое нарушение мозгового кровообращения | Острая фаза | По 10 мл 2 раза в сутки, в/в капельно на 200 мл 5% р-ра глюкозы или 0,9% р-ра натрия хлорида | 10 дней |
| Ранний восстановитель-ный период | По 10 мл 1 раз в сутки, в/в капельно на 200 мл 5% р-ра глюкозы или 0,9% р-ра натрия хлорида | 10 дней | |
| Хроническая ишемия мозга | Декомпенсация | По 10 мл 2 раза в сутки, в/в капельно на 200 мл 5% р-ра глюкозы или 0,9% р-ра натрия хлорида | 10 дней |
| Субкомпенсация | По 10 мл 1 раз в сутки, в/в капельно на 200 мл 5% р-ра глюкозы или 0,9% р-ра натрия хлорида | 10 дней | |
| Поддерживающая терапия | 2 таблетки 2 раза в день | 25 дней | |
| Гипоксическая энцефалопатия | Декомпенсация | По 10 мл 2 раза в сутки, в/в капельно на 200 мл 5% р-ра глюкозы или 0,9% р-ра натрия хлорида | 5 дней |
| Субкомпенсация | По 10 мл 1 раз в сутки, в/в капельно на 200 мл 5% р-ра глюкозы или 0,9% р-ра натрия хлорида | 5 дней | |
| Поддерживающая терапия | По 2 таблетки 2 раза в день | 25 дней | |
| Астенический синдром | – | По 2 таблетки 2 раза в день | 25 дней |
| Последствия легкой черепно-мозговой травмы | – | По 2 таблетки 2 раза в день | 25 дней |
Литература
- Агафьина А. И., Коваленко А. Л., Румянцева С. А., Скоромец А. А. и др. Эффективность нейрометаболического протектора Цитофлавина у больных, перенесших ишемический инсульт, в раннем восстановительном периоде (многоцентровое рандомизированное исследование) // Врач. 2006. № 1. С. 62–68.
- Джумагазиев А. А., Рахимова Л. Р. Применение метаболических препаратов для реабилитации новорожденных с церебральной ишемией // Доктор.Ру. 2015. № 5 (106) — № 6 (107). С. 63–66.
- Силина Е. В., Румянцева С. А., Орлова А. С. Нарушения памяти и астения. Москва: Тактик-Студио, 2014. 180 с.
- Скоромец А. А., Румянцева С. А., Федин А. И., Пирадов М. А. и др. Эффективность нейрометаболического протектора Цитофлавина при инфарктах мозга (многоцентровое рандомизированное исследование) // Вестник СПб ГМА им. И. И. Мечникова. 2005. № 1. С. 13–19.
- Су
