Большая медицинская энциклопедия инфаркт миокарда
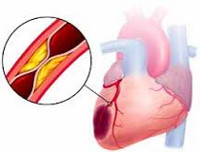
ИНФАРКТ (лат. infarctus от infarcire набивать, наполнять, втискивать; син. дисциркуляторный некроз) — очаговый некроз органа, являющийся следствием внезапного нарушения местного кровообращения.
Термин «инфаркт» был предложен Р. Вирховом для обозначения омертвевшего участка ткани, инфильтрированного («инфарцированного») эритроцитами.
Непосредственной причиной развития И. является препятствие кровотоку, внезапно возникающее в соответствующем отрезке артерии. Предполагали, что И. развивается лишь в органах с так наз. концевыми артериями, не имеющими анастомозов. Однако в дальнейшем было установлено, что анастомозы между конечными ветвлениями артерий имеются во всех органах, хотя степень их выраженности неодинакова. Малый калибр сосудов, индивидуальные варианты ветвления и аномалии развития их, недостаточное количество сосудистых анастомозов, свойственные данному органу, являются предпосылками для возникновения И. в условиях общих расстройств кровообращения. Только закупорка крупных магистральных артерий может привести к омертвению ткани органа без предшествующих общих гемодинамических расстройств.
При неполном закрытии просвета сосуда причиной развития И. является несоответствие потребности в питании функционально отягощенного органа и недостаточного кровоснабжения данного участка. Такое несоответствие может наблюдаться, напр., при гипертонической болезни, пороках сердца и обусловлено не столько сужением сосудов, сколько потерей ими эластичности и их неспособностью к адаптационному расширению. Ишемия (см.) определенного участка органа с минимальным кровотоком может возникать также при резком падении АД. Развитие И. в этом случае является показателем недостаточности общего кровообращения (И. мозга, миокарда). Для развития И. сердечной мышцы продолжительность ишемии, по экспериментальным данным, составляет 20 мин., для образования И. мозговой ткани — достаточно 5 — 6 мин. Макроскопически и микроскопически некроз ткани в зоне И. миокарда четко выявляется на 2-е сут. На более ранней стадии (так наз. донекротический период) удается выявить нарушения микроциркуляции, очаги контрактурного сокращения сосудистых миоцитов или их лизис. Большое значение в механизме развития тканевых изменений при И. принадлежит гипоксии (см.). Нарушение окислительно-восстановительных процессов в тканях в связи с расстройством кровообращения ведет к накоплению недоокисленных продуктов обмена, которые оказывают влияние на коллоиды тканей, стенки сосудов и приводят к их некрозу (см.).
Большое значение в развитии И. имеет внезапное сужение или закрытие сосудистого просвета, поэтому наиболее частой причиной И. является тромбоз (см.) и эмболия (см.), реже спазм (см.). В этих условиях коллатерали оказываются недостаточными, легко возникают дистонические явления и закупорка сосуда приводит к И.
И. чаще встречаются в сердце (см.), почках (см.), селезенке (см.), легких (см.), головном мозге (см.), сетчатке (см.), кишечнике (см.). И. в почках, селезенке, легких имеет клиновидную форму, что связано с их ангиоархитектоникой (магистральный тип сосудов, направляющихся от ворот к периферии), захватывает центральную часть ишемизированной области; при этом острие клина направлено в сторону препятствия кровотоку (места закупорки или резкого сужения сосуда), а широкая часть (основание) обращена на периферию органа. В мышце сердца И. имеет неправильную форму, захватывая послойно различные зоны миокарда, начиная от подэндокардиальных слоев, что обусловлено рассыпным типом ветвления сосудов; в кишечнике И. резко отграничен, протяженность его зависит от калибра закупоренной артерии.
На фоне общих и местных расстройств кровообращения в разных органах могут возникать небольшие, иногда микроскопических размеров, очаги некроза — микроинфаркты, характерные для миокарда и головного мозга. В возникновении их определенную роль могут играть перепады давления в мелких сосудах, а также несоответствие между повышенной потребностью в питании ткани и недостаточным кровотоком в условиях эмоциональной или физ. нагрузки, а также метаболические нарушения, обусловленные гипоксией или ишемией.
Различают три вида И.: белый (ишемический, анемический), красный (геморрагический), белый с геморрагическим поясом.

Рис. 1.Разрез селезенки: стрелками указаны белые (ишемические) инфаркты.

Рис. 3. Продольный разрез почки: стрелками указаны белые инфаркты; справа внизу микропрепарат (нижней стрелкой указан участок белого инфаркта, верхней — геморрагический пояс по периферии).
Белые (ишемические) И. наблюдаются в почках, селезенке, головном мозге, миокарде (цветн. рис. 1 и 3). Они треугольной формы, желтовато-белого цвета (отсюда название «белый»), довольно резко отграничены от окружающей ткани, плотной консистенции. Возникают в связи с полным прекращением тока крови в данном сосуде и его разветвлениях. Некроз в таких случаях всегда вначале носит характер сухого коагуляционного.

Рис. 2. Продольный разрез легкого с участками красного (геморрагического) инфаркта (указаны стрелками); справа внизу микропрепарат (стрелками указан пораженный участок, пропитанный кровью).
Красные (геморрагические) И. наблюдаются в легких (цветн. рис. 2), в кишечнике, иногда в селезенке и головном мозге; возникают, как правило, в условиях декомпенсации кровообращения и венозного застоя: в легких — при сердечной недостаточности различного происхождения, в селезенке — при тромбозе ее вены, в головном мозге — при тромбозе яремных вен или синусов твердой мозговой оболочки. При этом имеет место обратный ток венозной крови в зону И., паралитическое расширение сосудов, повышение их проницаемости и пропитывание зоны И. кровью. Геморрагический И. треугольной формы, на разрезе темно-красного цвета, что определяет его название, довольно резко отграничен от окружающей ткани. Со временем И. бледнеет вследствие гемолиза эритроцитов.
Белый И. с геморрагическим поясом — белого или светло-серого цвета с темно-красным ободком — наблюдается в сердце и селезенке, иногда в почках. Зона кровоизлияния возникает в связи с тем, что рефлекторный спазм по периферии И. быстро сменяется паралитическим расширением и переполнением кровью капилляров с развитием явлений престаза, стаза (см.) и диапедезного кровоизлияния (см. Диапедез).
В отдельную группу следует выделить близкие к геморрагическим так наз. застойные, или венозные, И., обусловленные закрытием просвета и прекращением оттока крови по сравнительно крупным венозным стволам или тромбозом большого количества мелких вен. Застой крови, отек и массивные кровоизлияния создают условия, не совместимые с жизнедеятельностью тканей,— возникает инфаркт. Такие венозные застойные И. наблюдаются в кишечнике при тромбозе брыжеечных вен, в почках при нарастающем тромбозе почечных вен, в селезенке при закупорке просвета селезеночной вены.
Одновременно или последовательно в различных органах могут возникать множественные И. разной локализации, формы и размеров. Можно также наблюдать образование свежих очагов некроза по периферии более старых, организующихся И., а также появление свежих некрозов в сохранившихся участках паренхимы в толще И. Это может быть обусловлено прогрессированием нарушения кровообращения с захватом новых сосудистых ветвей, напр, при распространении в их просвет тромба, ухудшением кровообращения в связи с падением кровяного давления или, как это бывает при инфаркте миокарда (см.), с внезапной неадекватной физ. или эмоциональной нагрузкой. Этому предшествуют изменения на уровне внутриклеточных органелл и макромолекул — набухание и разрушение крист митохондрий, изменения ультраструктуры саркоплазматического ретикулума, накопление липопротеидных комплексов.
Гистохимически в зоне И. определяется снижение и исчезновение гликогена (в миокарде, печени, почках), снижение активности окислительно-восстановительных ферментов, уменьшение содержания ДНК и РНК, накопление нейтральных мукополисахаридов типа сиаловых к-т, нарушение ионного равновесия. После кратковременного рефлекторного сужения сосуды в зоне И. паралитически расширяются; по существу, в этой области (в сердце, легких) имеется не малокровие, а венозный застой с картиной стаза и мелкими кровоизлияниями. Некроз носит коагуляционный характер (почки, селезенка, миокард) или с самого начала принимает характер влажного, колликвационного (в мозге). При микроскопическом исследовании И. структура органа нарушена, ядра не окрашиваются и все структурные элементы сливаются в однородную гомогенную массу (см. Некроз). По периферии И. всегда существует зона некробиоза, дистрофических изменений и реактивного воспаления. По клеточному составу воспалительной инфильтрации и пролиферативным реакциям стромы на границе И. можно судить о давности процесса. Небольшие И. (микроинфаркты) в течение 3—4 дней замещаются молодой соединительной тканью. В обширных И. некротические массы в центре очага могут сохраняться в течение недель и даже месяцев.
Исход И. зависит от условий его образования, локализации и размеров. При благоприятных условиях И. замещается грануляционной, а затем рубцовой тканью. В мозге на месте влажного некроза развивается киста. В некротические массы возможно отложение извести — петрификация И. При наличии микробов И. может подвергнуться гнойному расплавлению. В рубцах на месте геморрагического И. обнаруживается пигмент гемосидерин.
Значение И. для организма в конечном итоге зависит от его локализации, размеров, функциональной значимости пораженных участков, регенераторных и адаптационных возможностей органа и тканей. И. миокарда и вещества мозга могут явиться причиной смерти или вызывать тяжелые нарушения функций пораженного органа. Обширные И. вызывают интоксикацию организма продуктами тканевого распада: отмечаются повышение температуры, лихорадочное состояние, дистрофические изменения внутренних органов. Всасывание денатурированных белков из очага поражения обусловливает аутоиммунную реакцию с образованием органоспецифических антител и плазматизацией лимфоидных образований.
Термином «инфаркт» обозначают также некрозы, развивающиеся в почках при пропитывании их мочекислыми солями (см. Мочекислый инфаркт) или желчными к-тами и гемоглобиногенными пигментами (см. Билирубиновый инфаркт).
Библиография: Анброх Я. М. К вопросу об инфаркте печени, Хирургия, № 1, с. 114, 1965; Вопросы морфологии и патогенеза инфаркта (Миокард, легкие, почки, селезенка), под ред. А. И. Струко-ва, М., 1959, библиогр.; Давыдовский И. В. Общая патология человека, М., 1969; Многотомное руководство по патологической анатомии, под ред. А. И. Струкова, т. 1—9, М., 1956—1964; Delarue J. et Laumonier R. Anatomie pathologique, t. 1—3, P., 1969; General pathology, ed. by H. W. Florey, L., 1970, bibliogr.; Handbuch der allgemeinen Pathologie, hrsg. v. H. W. Altmann u. a., Bd 1-3, B. u. a., 1955-1972; K e t t-1 e r L.-H. Lehrbuch der speziellen Pathologie, Stuttgart, 1976, Bibliogr.; L e p a d a t P. Infarctul intestinal, Bu-cure§ti, 1973, bibliogr.; O g i 1 v i e R.F. Histopathology, Baltimore, 1962; Systemic pathology, ed. by G. P. Wright a. W. Sym-mers, L., 1966; Zollinger H.U. Pa-thologische Anatomie, Bd 1—2, Stuttgart, 1969.
С. А. Виноградов.
Источник
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
Общие сведения
Инфаркт миокарда – очаг ишемического некроза сердечной мышцы, развивающийся в результате острого нарушения коронарного кровообращения. Клинически проявляется жгущими, давящими или сжимающими болями за грудиной, отдающими в левую руку, ключицу, лопатку, челюсть, одышкой, чувством страха, холодным потом. Развившийся инфаркт миокарда служит показанием к экстренной госпитализации в кардиологическую реанимацию. При неоказании своевременной помощи возможен летальный исход.
В возрасте 40-60 лет инфаркт миокарда в 3–5 раз чаще наблюдается у мужчин в связи с более ранним (на 10 лет раньше, чем у женщин) развитием атеросклероза. После 55-60 лет заболеваемость среди лиц обоего пола приблизительно одинакова. Показатель летальности при инфаркте миокарда составляет 30—35%. Статистически 15—20% внезапных смертей обусловлены инфарктом миокарда.
Нарушение кровоснабжения миокарда на 15-20 и более минут приводит к развитию необратимых изменений в сердечной мышце и расстройству сердечной деятельности. Острая ишемия вызывает гибель части функциональных мышечных клеток (некроз) и последующее их замещение волокнами соединительной ткани, т. е. формирование постинфарктного рубца.
В клиническом течении инфаркта миокарда выделяют пять периодов:
- 1 период – предынфарктный (продромальный): учащение и усиление приступов стенокардии, может продолжаться несколько часов, суток, недель;
- 2 период – острейший: от развития ишемии до появления некроза миокарда, продолжается от 20 минут до 2 часов;
- 3 период – острый: от образования некроза до миомаляции (ферментативного расплавления некротизированной мышечной ткани), длительность от 2 до 14 суток;
- 4 период – подострый: начальные процессы организации рубца, развитие грануляционной ткани на месте некротической, продолжительность 4-8 недель;
- 5 период – постинфарктный: созревание рубца, адаптация миокарда к новым условиям функционирования.

Инфаркт миокарда
Причины инфаркта миокарда
Инфаркт миокарда является острой формой ИБС. В 97—98% случаев основой для развития инфаркта миокарда служит атеросклеротическое поражение венечных артерий, вызывающее сужение их просвета. Нередко к атеросклерозу артерий присоединяется острый тромбоз пораженного участка сосуда, вызывающий полное или частичное прекращение кровоснабжения соответствующей области сердечной мышцы. Тромбообразованию способствует повышенная вязкость крови, наблюдаемая у пациентов с ИБС. В ряде случаев инфаркт миокарда возникает на фоне спазма ветвей венечных артерий.
Развитию инфаркта миокарда способствуют сахарный диабет, гипертоничесая болезнь, ожирение, нервно-психическое напряжение, увлечение алкоголем, курение. Резкое физическое или эмоциональное напряжение на фоне ИБС и стенокардии может спровоцировать развитие инфаркта миокарда. Чаще развивается инфаркт миокарда левого желудочка.
Классификация инфаркта миокарда
В соответствии с размерами очагового поражения сердечной мышцы выделяют инфаркт миокарда:
- крупноочаговый
- мелкоочаговый
На долю мелкоочаговых инфарктов миокарда приходится около 20% клинических случаев, однако нередко мелкие очаги некроза в сердечной мышце могут трансформироваться в крупноочаговый инфаркт миокарда (у 30% пациентов). В отличие от крупноочаговых, при мелкоочаговых инфарктах не возникают аневризма и разрыв сердца, течение последних реже осложняется сердечной недостаточностью, фибрилляцией желудочков, тромбоэмболией.
В зависимости от глубины некротического поражения сердечной мышцы выделяют инфаркт миокарда:
- трансмуральный – с некрозом всей толщи мышечной стенки сердца (чаще крупноочаговый)
- интрамуральный – с некрозом в толще миокарда
- субэндокардиальный – с некрозом миокарда в зоне прилегания к эндокарду
- субэпикардиальный – с некрозом миокарда в зоне прилегания к эпикарду
По изменениям, фиксируемым на ЭКГ, различают:
- «Q-инфаркт» – с формированием патологического зубца Q, иногда желудочкового комплекса QS (чаще крупноочаговый трансмуральный инфаркт миокарда)
- «не Q-инфаркт» – не сопровождается появлением зубца Q, проявляется отрицательными Т-зубцами (чаще мелкоочаговый инфаркт миокарда)
По топографии и в зависимости от поражения определенных ветвей коронарных артерий инфаркт миокарда делится на:
- правожелудочковый
- левожелудочковый: передней, боковой и задней стенок, межжелудочковой перегородки
По кратности возникновения различают инфаркт миокарда:
- первичный
- рецидивирующий (развивается в срок 8 недель после первичного)
- повторный (развивается спустя 8 недель после предыдущего)
По развитию осложнений инфаркт миокарда подразделяется на:
- осложненный
- неосложненный
По наличию и локализации болевого синдрома выделяют формы инфаркта миокарда:
- типичную – с локализацией боли за грудиной или в прекардиальной области
- атипичные – с атипичными болевыми проявлениями:
- периферические: леволопаточная, леворучная, гортанно-глоточная, нижнечелюстная, верхнепозвоночная, гастралгическая (абдоминальная)
- безболевые: коллаптоидная, астматическая, отечная, аритмическая, церебральная
- малосимптомную (стертую)
- комбинированную
В соответствии с периодом и динамикой развития инфаркта миокарда выделяют:
- стадию ишемии (острейший период)
- стадию некроза (острый период)
- стадию организации (подострый период)
- стадию рубцевания (постинфарктный период)
Симптомы инфаркта миокарда
Предынфарктный (продромальный) период
Около 43% пациентов отмечают внезапное развитие инфаркта миокарда, у большей же части больных наблюдается различный по продолжительности период нестабильной прогрессирующей стенокардии.
Острейший период
Типичные случаи инфаркта миокарда характеризуются чрезвычайно интенсивным болевым синдромом с локализацией болей в грудной клетке и иррадиацией в левое плечо, шею, зубы, ухо, ключицу, нижнюю челюсть, межлопаточную зону. Характер болей может быть сжимающим, распирающим, жгучим, давящим, острым («кинжальным»). Чем больше зона поражения миокарда, тем более выражена боль.
Болевой приступ протекает волнообразно (то усиливаясь, то ослабевая), продолжается от 30 минут до нескольких часов, а иногда и суток, не купируется повторным приемом нитроглицерина. Боль сопряжена с резкой слабостью, возбуждением, чувством страха, одышкой.
Возможно атипичное течение острейшего периода инфаркта миокарда.
У пациентов отмечается резкая бледность кожных покровов, липкий холодный пот, акроцианоз, беспокойство. Артериальное давление в период приступа повышено, затем умеренно или резко снижается по сравнению с исходным (систолическое < 80 рт. ст., пульсовое < 30 мм мм рт. ст.), отмечается тахикардия, аритмия.
В этот период может развиться острая левожелудочковая недостаточность (сердечная астма, отек легких).
Острый период
В остром периоде инфаркта миокарда болевой синдром, как правило, исчезает. Сохранение болей бывает вызвано выраженной степенью ишемии околоинфарктной зоны или присоединением перикардита.
В результате процессов некроза, миомаляции и перифокального воспаления развивается лихорадка (от 3-5 до 10 и более дней). Длительность и высота подъема температуры при лихорадке зависят от площади некроза. Артериальная гипотензия и признаки сердечной недостаточности сохраняются и нарастают.
Подострый период
Болевые ощущения отсутствуют, состояние пациента улучшается, нормализуется температура тела. Симптомы острой сердечной недостаточности становятся менее выраженными. Исчезает тахикардия, систолический шум.
Постинфарктный период
В постинфарктном периоде клинические проявления отсутствуют, лабораторные и физикальные данные практически без отклонений.
Атипичные формы инфаркта миокарда
Иногда встречается атипичное течение инфаркта миокарда с локализацией болей в нетипичных местах (в области горла, пальцах левой руки, в зоне левой лопатки или шейно-грудного отдела позвоночника, в эпигастрии, в нижней челюсти) или безболевые формы, ведущими симптомами которых могут быть кашель и тяжелое удушье, коллапс, отеки, аритмии, головокружение и помрачение сознания.
Атипичные формы инфаркта миокарда чаще встречаются у пожилых пациентов с выраженными признаками кардиосклероза, недостаточностью кровообращения, на фоне повторного инфаркта миокарда.
Однако атипично протекает обычно только острейший период, дальнейшее развитие инфаркта миокарда становится типичным.
Стертое течение инфаркта миокарда бывает безболевым и случайно обнаруживается на ЭКГ.
Осложнения
Нередко осложнения возникают уже в первые часы и дни инфаркта миокарда, утяжеляя его течение. У большинства пациентов в первые трое суток наблюдаются различные виды аритмий: экстрасистолия, синусовая или пароксизмальная тахикардия, мерцательная аритмия, полная внутрижелудочковая блокада. Наиболее опасно мерцание желудочков, которое может перейти в фибрилляцию и привести к гибели пациента.
Левожелудочковая сердечная недостаточность характеризуется застойными хрипами, явлениями сердечной астмы, отека легких и нередко развивается в острейший период инфаркта миокарда. Крайне тяжелой степенью левожелудочковой недостаточности является кардиогенный шок, развивающийся при обширном инфаркте и обычно приводящий к летальному исходу. Признаками кардиогенного шока служит падение систолического АД ниже 80 мм рт. ст., нарушение сознания, тахикардия, цианоз, уменьшение диуреза.
Разрыв мышечных волокон в зоне некроза может вызывать тампонаду сердца – кровоизлияние в полость перикарда. У 2-3% пациентов инфаркт миокарда осложняется тромбоэмболиями системы легочной артерии (могут стать причиной инфаркта легких или внезапной смерти) или большого круга кровообращения.
Пациенты с обширным трансмуральным инфарктом миокарда в первые 10 суток могут погибнуть от разрыва желудочка вследствие острого прекращения кровообращения. При обширном инфаркте миокарда может возникать несостоятельность рубцовой ткани, ее выбухание с развитием острой аневризмы сердца. Острая аневризма может трансформироваться в хроническую, приводящую к сердечной недостаточности.
Отложение фибрина на стенках эндокарда приводит к развитию пристеночного тромбоэндокардита, опасного возможностью эмболии сосудов легких, мозга, почек оторвавшимися тромботическими массами. В более позднем периоде может развиться постинфарктный синдром, проявляющийся перикардитом, плевритом, артралгиями, эозинофилией.
Диагностика инфаркта миокарда
Среди диагностических критериев инфаркта миокарда важнейшими являются анамнез заболевания, характерные изменения на ЭКГ, показатели активности ферментов сыворотки крови. Жалобы пациента при инфаркте миокарда зависят от формы (типичной или атипичной) заболевания и обширности поражение сердечной мышца. Инфаркт миокарда следует заподозрить при тяжелом и продолжительном (дольше 30-60 минут) приступе загрудинных болей, нарушении проводимости и ритма сердца, острой сердечной недостаточности.
К характерным изменениям ЭКГ относятся формирование отрицательного зубца Т (при мелкоочаговом субэндокардиальном или интрамуральном инфаркте миокарда), патологического комплекса QRS или зубца Q (при крупноочаговом трансмуральном инфаркте миокарда). При ЭхоКГ выявляется нарушение локально сократимости желудочка, истончение его стенки.
В первые 4-6 часов после болевого приступа в крови определяется повышение миоглобина – белка, осуществляющего транспорт кислорода внутрь клеток.Повышение активности креатинфосфокиназы (КФК) в крови более чем на 50% наблюдается спустя 8—10 ч от развития инфаркта миокарда и снижается до нормы через двое суток. Определение уровня КФК проводят через каждые 6-8 часов. Инфаркт миокарда исключается при трех отрицательных результатах.
Для диагностики инфаркта миокарда на более поздних сроках прибегают к определению фермента лактатдегидрогеназы (ЛДГ), активность которой повышается позже КФК – спустя 1-2 суток после формирования некроза и приходит к нормальным значениям через 7-14 дней. Высокоспецифичным для инфаркта миокарда является повышение изоформ миокардиального сократительного белка тропонина – тропонина-Т и тропонина-1, увеличивающихся также при нестабильной стенокардии. В крови определяется увеличение СОЭ, лейкоцитов, активности аспартатаминотрансферазы (АсАт) и аланинаминотрансферазы (АлАт).
Коронарная ангиография (коронарография) позволяет установить тромботическую окклюзию коронарной артерии и снижение желудочковой сократимости, а также оценить возможности проведения аортокоронарного шунтирования или ангиопластики – операций, способствующих восстановлению кровотока в сердце.
Лечение инфаркта миокарда
При инфаркте миокарда показана экстренная госпитализация в кардиологическую реанимацию. В остром периоде пациенту предписывается постельный режим и психический покой, дробное, ограниченное по объему и калорийности питание. В подостром периоде больной переводится из реанимации в отделение кардиологии, где продолжается лечение инфаркта миокарда и осуществляется постепенное расширение режима.
Купирование болевого синдрома проводится сочетанием наркотических анальгетиков (фентанила) с нейролептиками (дроперидолом), внутривенным введением нитроглицерина.
Терапия при инфаркте миокарда направлена на предупреждение и устранение аритмий, сердечной недостаточности, кардиогенного шока. Назначают антиаритмические средства (лидокаин), ß-адреноблокаторы (атенолол), тромболитики (гепарин, ацетилсалициловая к-та), антогонисты Са (верапамил), магнезию, нитраты, спазмолитики и т. д.
В первые 24 часа после развития инфаркта миокарда можно произвести восстановление перфузии путем тромболизиса или экстренной баллонной коронарной ангиопластики.
Прогноз при инфаркте миокарда
Инфаркт миокарда является тяжелым, сопряженным с опасными осложнениями заболеванием. Большая часть летальных исходов развивается в первые сутки после инфаркта миокарда. Насосная способность сердца связана с локализацией и объемом зоны инфаркта. При повреждении более 50% миокарда, как правило, сердце функционировать не может, что вызывает кардиогенный шок и гибель пациента. Даже при менее обширном повреждении сердце не всегда справляется нагрузками, в результате чего развивается сердечная недостаточность.
По истечении острого периода прогноз на выздоровление хороший. Неблагоприятные перспективы у пациентов с осложненным течением инфаркта миокарда.
Профилактика инфаркта миокарда
Необходимыми условиями профилактики инфаркта миокарда являются ведение здорового и активного образа жизни, отказ от алкоголя и курения, сбалансированное питание, исключение физического и нервного перенапряжения, контроль АД и уровня холестерина крови.
Источник
