Биохимические показатели инфаркта миокарда
Измерение уровней кардиомаркеров ускоряет и уточняет такого мероприятия, как диагностика инфаркта миокарда, а также возможность предсказать его дальнейшее развитие. Основные биохимические маркеры, которые использует диагностика инфаркта миокарда — миоглобин, тропонин I, тропонин Т, креатин-фосфокиназа и лактатдегидрогеназа.
Миоглобин
Миоглобин — кислородсвязывающий белок поперечно-полосатых скелетных мышц и миокарда. Его молекула содержит железо, структурно похожа на молекулу гемоглобина и отвечает за транспорт 02 в скелетных мышцах. Миоглобин является одним из самых первых маркеров повреждения миокарда, так как повышение его уровня в крови определяется уже через 2-4 часа после возникновения острого инфаркта миокарда. Пик концентрации достигается в срок до 12 часов, а затем в течение 1-2 суток снижается до нормы. В связи с тем, что выход свободного миоглобина в кровь может быть обусловлен рядом другим патологических состояний, для точной постановки диагноза инфаркта миокарда лишь одного этого маркера недостаточно.
Тропонины
Наиболее специфичные и надежные маркеры некроза миокарда — кардиальные тропонины Т и I (позволяют выявить даже самые незначительные повреждения миокарда).
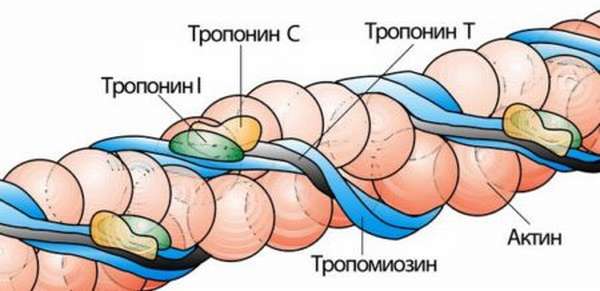
Тропонины представляют собой белки, участвующие в процессе регуляции мышечного сокращения. Тропонин-I и тропонин-Т миокарда и скелетных мышц имеют структурные различия, что позволяет изолированно выделять их кардиоспецифичные формы методами иммуноанализа. Приблизительно 5% тропонина-I находится в свободном виде в цитоплазме кардиомиоцитов. Именно за счет этой фракции тропонин-I обнаруживается в плазме крови уже через 3-6 часов после повреждения сердечной мышцы. Большая же часть тропонина-I в клетке находится в связанном состоянии и при повреждении миокарда освобождается медленно. В результате увеличенная концентрация тропонина в крови сохраняется в течение 1 −2 недель. Обычно пик концентрации тропонина-I наблюдается на 14-20 часах после появления болей в груди. Приблизительно у 95% пациентов через 7 часов после развития острого инфаркта миокарда определяется увеличение концентрации тропонина-I.
Небольшой подъем уровня сердечного тропонина-I должен интерпретироваться со значительной осторожностью, так как это может быть обусловлено разными патологическими состояниями, вызывающими повреждение клеток миокарда. То есть увеличенный уровень тропонина изолированно не может служить основанием для постановки диагноза инфаркта миокарда.
Если у больного с подозрением на острый коронарный синдром без подъема сегмента ST повышен уровень тропонина Т и/или тропонина I, то такое состояние следует расценивать как инфаркт миокарда и проводить соответствующую терапию.
Определение тропонинов позволяет обнаружить повреждение миокарда примерно у трети больных, не имеющих повышения МВ-КФК. Для выявления или исключения повреждения миокарда необходимы повторные взятия крови и измерения в течение 6- 12 часов после поступления и после любого эпизода сильной боли в грудной клетке.
Креатинфосфокиназа (креатинкиназа)
Креатинфосфокиназа (креатинкиназа) — фермент, содержащийся в миокарде и скелетных мышцах (в небольшом количестве содержится в гладких мышцах матки, желудочно-кишечного тракта и головном мозге). В мозге и в почках содержится преимущественно изоэнзим ВВ (brain), в скелетных мышцах — ММ (muscle) и в сердце MB энзим. Наибольшей специфичностью обладает именно креатинкиназа MB. Имеется высокая корреляция между уровнем ее активности и массой некроза. При повреждении миокарда и скелетных мышц наблюдается выход фермента из клеток, приводящий к повышению активности креатинкиназы в крови. Через 2-4 часа после ангинозного приступа уровень креатинкиназы MB в крови значительно повышается, в связи с чем определение креатинфосфокиназы и креатинкиназы MB в крови широко применяется в ранней диагностике инфаркта миокарда.
Нормальный уровень креатинкиназы в крови у мужчин < 190 Ед/л и < 167 Ед/л у женщин. Нормальным содержанием креатинкиназы-МВ в крови считается 0-24 Ед/л. Креатинфосфокиназа (КФК) и ее изофермент MB КФК недостаточно специфичны, так как возможны ложноположительные результаты при травме скелетных мышц. Кроме того, имеет место значительное перекрывание между нормальными и патологическими сывороточными концентрациями указанных ферментов.
Лактатдегидрогеназа (ЛДГ)
Лактатдегидрогеназа (ЛДГ) — фермент, участвующий в процессе окисления глюкозы и образовании молочной кислоты. Она содержится практически во всех органах и тканях человека. Больше всего ее содержится в мышцах. Лактат в норме образуется в клетках в процессе дыхания и, при полноценном снабжении кислородом, в крови не накапливается. Происходит его разрушение до нейтральных продуктов, после чего он выводится из организма. При гипоксических состояниях лактат накапливается, вызывая чувство мышечной усталости и нарушая тканевое дыхание.
Более специфично исследование изоэнзимов этого фермента ЛДГ1-5. Наибольшей специфичностью обладает ЛДГ1. При инфаркте миокарда специфично превышение соотношения ЛДГ1 и ЛДГ2 более 1 (в норме ЛДП/ЛДГ2 < 1). Норма лактатдегидрогеназы для взрослых составляет 250 Ед/л.
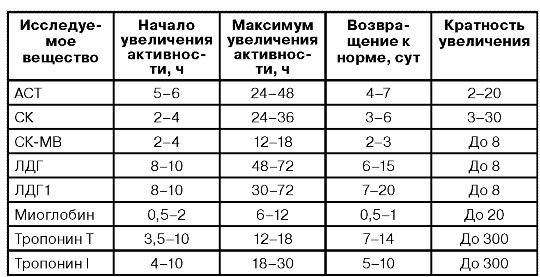
При некрозе миокарда повышение концентрации этих маркеров в сыворотке крови происходит не одновременно. Наиболее ранний маркер — миоглобин. Увеличение концентрации MB КФК и тропонина происходит несколько позже. Следует учитывать, что при пограничных уровнях кардиомаркеров существует следующая тенденция:
- чем ниже их уровень, тем больше ложноположительных диагнозов;
- чем выше, тем больше ложноотрицательных диагнозов.
Определение тропонина и кардиомаркеров
Экспресс диагностика инфаркта миокарда легко осуществима в любое время с помощью различных качественных тест-систем для определения «Тропонина Т». Результат определяется через 15 минут после нанесения крови на тест-полоску. Если тест положительный и появилась вторая полоса, то уровень тропонина превышает 0,2 нг/мл. Следовательно, инфаркт есть. Чувствительность и специфичность этого теста более 90%.
Изменения других лабораторных показателей
Повышение уровня АсАТ отмечается у 97-98% больных с крупноочаговым инфарктом миокарда. Повышение определяется через 6-12 часов, достигая максимума через 2 суток. Показатель обычно нормализуется на 4-7 день от начала заболевания.
При развитии инфаркта миокарда отмечается увеличение числа лейкоцитов в крови, повышение скорости оседания эритроцитов (СОЭ), возрастание уровня гамма-глобулинов, снижение уровня альбумина, положительная проба на С-реактивный белок.
Лейкоцитоз наблюдается приблизительно у 90% больных. Выраженность его в определенной степени зависит от обширности инфаркта (в среднем 12- 15×109/л). Лейкоцитоз появляется через несколько часов от начала болевого приступа, достигая максимума на 2-4 день и, в неосложненных случаях, постепенно снижаясь до нормы в течение недели. Лейкоцитоз преимущественно обусловлен увеличением числа нейтрофилов.
При инфаркте миокарда СОЭ начинает увеличиваться на 2-3-й день, достигая максимума на 2-й неделе. Возвращение к исходному уровню происходит в течение 3-4 недель. В целом эти изменения свидетельствуют о существовании воспаления или некроза в организме и лишены какой-либо органоспецифичности.
Эхокардиография при инфаркте миокарда
Эхокардиография — неинвазивный метод, с помощью которого можно поручить достоверную информацию о состоянии регионарной и общей сократительной функции миокарда, изучить движение крови в полостях сердца, а также изучить структуру и функции его клапанного аппарата. С помощью эхокардиографии возможно получение сведений о таких показателях, как сердечный выброс, конечно-систолический и конечно-диастолический объемы левого желудочка, фракция выброса и др.
Эхокардиография, применительно к диагностике острых коронарных синдромов, позволяет:
- исключить или подтвердить диагноз острого инфаркта миокарда;
- идентифицировать не ишемические состояния, вызывающие боль в грудной клетке;
- оценить кратковременный и долгосрочный прогноз;
- идентифицировать осложнения острого инфаркта.
Инфаркт миокарда вызывает нарушения локальной сократимости левого желудочка разной степени выраженности. Структура ткани в области с нарушенной сократимостью может указать на давность инфаркта. Нередко на границе с нормальными сегментами видна резкая демаркационная линия. Граница между акинетичным и нормальным миокардом иногда хорошо визуализируется.
Для появления сегментарного нарушения сократимости миокарда, определимого при помощи эхокардиографии, необходимо повреждение более 20% толщины стенки желудочка. Могут быть определены локализация и распространенность инфаркта миокарда.
Эхокардиография особенно полезна в ранние сроки. Легко идентифицируются дисфункция митрального клапана, протяженность инфаркта, пристеночный тромб и механические осложнения инфаркта миокарда. Во время эпизода ишемии миокарда могут быть обнаружены локальная гипокинезия или акинезия стенки левого желудочка. После исчезновения ишемии может отмечаться восстановление нормальной сократимости.
Количество вовлеченных сегментов, полученное при оценке сократительной способности стенки сердца, как мера остаточной функции левого желудочка имеет раннее и позднее прогностическое значение при предсказании возможности осложнений и выживаемости. Истончение стенки левого желудочка указывает на ранее перенесенный инфаркт миокарда. При хорошей визуализации, когда виден весь эндокард, нормальная сократимость левого желудочка почти исключает инфаркт миокарда.
Источник
При
инфаркте миокарда (ИМ) в результате
некроза клеток сердечной мышцы в
кровеносное русло попадают содержащиеся
в них ферменты и белки. По их наличию,
времени появления и концентрации в
плазме крови можно оценить ущерб,
нанесенный сердечной мышце. Эти сведения
дополняют данные ЭКГ и помогают в
ранней диагностике ИМ, что позволяет
своевременно избрать правильную тактику
лечения.
Идеальный
биохимический маркер должен обладать
наивысшей специфичностью и чувствительностью
в отношении некроза миокарда, в течение
короткого времени после начала симптомов
ИМ достигать в крови диагностически
значимого уровня, этот уровень должен
сохраняться в течение многих дней. В
настоящее время маркера, полностью
отвечающего всем этим требованиям, не
существует, поэтому для диагностики ИМ
рекомендуется параллельно использовать
два маркера — “ранний” и “поздний”.
Содержание “раннего” маркера при
ИМ диагностически значимо повышается
в крови в первые часы заболевания,
“поздний” —достигает диагностически
значимого уровня только через 6—9 ч, но
обладает высокой специфичностью в
отношении некроза миокарда.
Ранние
маркеры некроза миокарда:
Миоглобин
МВ-КФК
(сердечная форма креатинфосфокиназы
— КФК)Сердечная
форма белка, связывающего жирные кислоты
(сБСЖК)
Поздние
маркеры некроза миокарда:
Лактатдегидрогеназа
(ЛДГ)Аспартатаминотрансфераза
(АсАТ)Сердечные
тропонины I и Т
Среди
множества биохимических маркеров,
которые могут менять свою концентрацию
в плазме крови при ИМ, наиболее
кардиоспецифическими являются тропонины,
МВ-фракция креатенинфосфокиназы
(КФК-МВ) и миоглобулин, которые и
представляют наибольшую диагностическую
ценность.
Тропонин
– является ферментом «быстрого
реагирования», поскольку попадает в
периферический кровоток из зоны некроза
уже в первые часы повреждения миокарда.
Тропонины Т и I присутствуют только в
клетках миокарда, поэтому повышение
их концентрации в крови является
достоверным признаком ИМ и показателем
его распространенности. Отрицательный
тропониновый тест вначале сердечного
приступа и через 12 часов позволяет
исключить у больного ИМ и диагностировать
нестабильную стенокардию. Даже
незначительное повышение уровня
тропонинов в периферической крови через
6-12 часов после болевого приступа
расценивается как признак ишемии
миокарда ведущей к некрозу и позволяет
выявить ИМ без явных клинических
симптомов и ЭКГ-признаков заболевания.
МВ-фракция
креатенинфосфокиназы (МВ-КФК)
содержится преимущественно в клетках
миокарда, но в небольшом количестве
присутствует и в скелетных мышцах,
поэтому активность этого фермента в
крови может повышаться при повреждении
не только сердечной мышцы, но и других
мышечных групп. Судить о повреждении
миокарда на фоне сердечного приступа
позволяет нарастание активности МВ-КФК
в динамике. Для диагностики ИМ в первые
сутки от начала сердечного приступа ее
определяют 2-3 раза каждые 8 часов. Три
отрицательных результата позволяют
исключить ИМ, а нарастание концентрации
этого фермента в крови с высокой долей
вероятности свидетельствует об ИМ.
Уровень активности MB – КФК позволяет
определить величину инфаркта миокарда
и тяжесть заболевания.
Миоглобин
— очень ранний и чувствительный, но
менее специфичный маркер ИМ, поскольку
содержание этого мышечного белка в
крови может увеличиваться и по другим
причинам. Миоглобин при сердечном
приступе появляется в крови еще до
формирования очага некроза, на стадии
выраженного ишемического повреждения
сердечной мышцы. Повышение уровня
миоглобина в 10 раз и больше указывает
на некроз мышечных клеток.
Лактатдегидрогеназа
(ЛДГ)
—
фермент, принимающий участие в реакциях
гликолиза, катализируя превращение
лактата в пируват, при этом образуется
NADH. ЛДГ имеет пять изо-энзимов. В сердечной
мышце содержится преимущественно
изоэнзим ЛДГ-1. При ИМ концентрация ЛДГ
начинает превышать нормальный уровень
через 14—48 ч после начала симптомов,
достигает максимального значения на
3—6-е сутки заболевания и возвращается
к норме на 7—14-е сутки болезни. ЛДГ-1 была
обнаружена также в эритроцитах, почках,
мозге, желудке, повышение концентрации
этого белка в крови больных далеко не
всегда связано с некрозом миокарда.
Отношение ЛДГ-1/ЛДГ-2, превышающее 0,76,
обладает 90% специфичностью при выявлении
некроза миокарда. Это соотношение может
увеличиваться и в случае отсутствия
ИМ, если у больного имеются массивный
гемолиз, мегалобластическая анемия,
распространенное повреждение скелетных
мышц, тяжелое заболевание печени. Из-за
позднего повышения концентрации ЛДГ в
сыворотке крови этот маркер не применяется
для ранней диагностики ИМ и суждения
об успехе тромболитической терапии,
однако ЛДГ длительно использовалась
для диагностики ИМ в поздние сроки
заболевания.
Аспартатаминотрансфераза
(АсАТ)
– фермент, который катализирует
преобращение оксалоацетата в аспартат,
перенося NH3 на первую молекулу. Вторым
продуктом реакции является α-кетоглутарат.
Реакция играет важную роль в высвобождении
NH3 из аминокислот, который затем
перерабатывается в цикле мочевины, так
как аспартат, полученный в процессе
реакции, нужен для образования
аргининосукцината. У больных ИМ уровень
АсАТ превышает норму через 8—12 ч после
начала боли, достигает максимального
значения к 24—З6-му часу и возвращается
к норме за 3—4 дня. Большое количество
этого фермента содержится в тканях
печени, что сильно снижает его специфичность
в отношении некроза миокарда. АсАТ
неудобна как для ранней, так и для поздней
диагностики ИМ, она используется только
в сочетании с более чувствительными и
специфичными маркерами. Низкая
специфичность в отношении некроза
миокарда послужила причиной того, что
использование этого маркера, как и ЛДГ,
для диагностики ИМ в настоящее время
также признано нецелесообразным..
Повышение
АСТ, превышающее повышение АЛТ, характерно
для повреждения сердечной
мышцы;
если же показатель АЛТ выше, чем АСТ, то
это, как правило, свидетельствует о
разрушении клеток печени.
Неспецифическая
реакция
на повреждение миокарда включает
нейтрофильный лейкоцитоз
(появляется через несколько часов после
окклюзии и длится 3-7 сут, число лейкоцитов
достигает 12000-15000 в мкл). СОЭ
повышается медленнее, достигает пика
в 1-ю неделю и часто остается повышенной
в течение 1-2 нед.
сБСЖК
по последовательности аминокислот
идентичен БСЖК, содержащемуся в
поперечнополосатой мышечной ткани
скелетных мышц, однако представлен в
скелетной мускулатуре в минимальном
количестве. Максимальное количество
сБСЖК находится в ткани миокарда — 0,5
мг/г. Единственная мышца, в которой
имеется относительно большое количество
сБСЖК, — это диафрагма (примерно 25% от
содержания в ткани миокарда). Некоторое
количество сБСЖК содержится в тканях
аорты, и можно предположить, что содержание
его повышается, в крови при расслаивающей
аневризме аорты. Так как сБСЖК в основном
свободно расположен в цитоплазме клеток,
в случае повреждения клеточной мембраны
кардиомиоцита он быстро попадает в
кровоток. В крови здоровых людей
циркулирует небольшое количество сБСЖК.
Соседние файлы в предмете Лабораторная диагностика
- #
- #
- #
- #
- #
- #
- #
Источник
При приступе инфаркта миокарда в крови больного происходят биохимические изменения. Потому для подтверждения диагноза и выявления срока давности недуга проводят анализ крови. При инфаркте миокарда он позволяет уточнить диагноз и дополняет другие методы исследования. Ниже представляется перечень информации об изменениях в крови.

Биохимические изменения
Внимание! При инфаркте миокарда в кровь выбрасывается определенное количество специфических белков (тропонин, миоглобин), которые позволяю диагностировать приступ.
При приступе некроза кардиомиоциты выделяют огромное количество белка тропонина. Чтобы поставить диагноз, необходимо выявить уровень данного белка к моменту восстановления перфузии. Поскольку определяется уровень белка прикроватно, это позволяет облегчить диагностику, которая может быть осложнена при сомнительном результате ЭКГ.
После того как с момента приступа прошло около 4-6 часов, возрастает уровень некоторых специфичных ферментов. К ним относится КФК (креатинфосфокиназа). Пик активности КФК достигается после суток с момента приступа. Нормализуется содержание данного фермента после 2-3 суток. Пика КФК может достичь и через 12 часов на фоне тромболизиса.
Однако повышение КФК не может служить единственным и точным показателем инфаркта миокарда, так как оно наблюдается и при повреждении скелетных мышц или при гипотиреозе.
Более специфичным показателем служит активность МВ-фракций КФК. Например, если активность КФК при повреждении скелетных мышц наблюдается, то МВ-фракция не так активна. Это связано с тем, что она имеется в большей степени именно в сердечных тканях.
Если сравнивать динамику всей КФК и отдельной МВ-фракции, то вторая быстрее достигает своей максимальной точки. Нормализация, следовательно, тоже достигается раньше (через 1,5 суток).
Повышенная активность МВ-фракций наблюдается и при миокардите, после хирургических вмешательств на сердечной мышце или гипотиреозе, но в данных случаях динамика не такая, как при инфаркте. В этом случае уровень МВ-фракции выше КФК на 2,5 процента. Выявление активности МВ-фракций и общего КФК проводится через 12 и 24 часа после приступа.
Вышеописанная МВ-фракция присутствует в МВ1 и МВ2 изоформе. Для диагностирования инфаркта миокарда применяют анализ отношения МВ2 к МВ1. К примеру, более чем у 90% пациентов уже через 4-6 часов с момента приступа данное соотношение превышает коэффициент 1,5.
Высокоспецифичный признак инфаркта миокарда – уровень сердечных тропонинов T и I. Распознать произошедший инфаркт по ним можно уже после 3 часов с момента приступа, так как уровень этих белков начинает повышаться и сохраняется на несколько суток. Это позволяет выявить некроз сердечной мышцы даже при поступлении больных через 48 часов после появления ангинозных неприятных ощущений в груди.
Более того, данный метод диагностирования весьма информативен потому, что позволяет прогнозировать течение недуга. Согласно проведенным исследованиям, чем выше уровень тропонина I и чем раньше анализ на тропонин T дает положительный результат, тем хуже прогноз.
После некроза коронарной артерии уже через 2 часа в кровь поступает белок миоглобин. Но из-за того что почки очень быстро выводит его из организма, специфичной важности данный показатель не представляет.
Спустя через 1-2 сутки с момента приступа активизируется фермент ЛДГ (лактатдигидрогеназа). Пик ее приходится на 3-5 сутки и нормализуется ЛДГ к 8-10 суткам.
Внимание! Раньше использовали метод выявления уровня ЛДГ у больных, поступивших через 2-3 суток, когда КФК уже приходит в норму. В последнее время для постановки диагноза определяют уровень тропонина.
Показатели крови при инфаркте миокарда
Делая краткий вывод, можно отметить биохимические изменения в крови после приступа инфаркта.
Ферменты
Для диагностирования используют показатели следующих ферментов:
- АСТ. Повышение уровня данного фермента проходит в 1-2 сутки и нормализуется к 3-4 суткам.
- КФК. Повышение данного фермента начинается уже после 4-8 часов с момента некроза сердечной мышцы и достигает пика через сутки. Нормализация КФК проходит в последующие 2-3 суток.
- ЛДГ. Активизируется ЛДГ через 2-3 суток и достигает максимального уровня через 4-6 суток. Вызвать повышение могут и иные патологии, которые не связаны с инфарктом миокарда, повышение ЛДГ не считается 100% показателем некроза сердечной мышцы.
Как видно, каждый из ферментов имеет свои особенности, которые позволяют установить диагноз инфаркт миокарда в различное время после появления первых ощущений.
Лейкоцитоз
При инфаркте миокарда данный показатель может возрасти до 12-15 тыс. кубическом миллиметре. В некоторых случаях пик может быть больше, а нормализация данного показателя происходит через несколько недель после приступа инфаркта миокарда. Количество лейкоцитов увеличивается большей частью за счет молодых нейтрофилов, поэтому происходит нейтрофильный сдвиг лейкоцитарной формулы влево, что становится диагностически значимым признаком.
Скорость оседания эритроцитов
Повышение СОЭ происходит спустя несколько суток после некроза сердечной мышцы, высокий уровень сохраняется несколько недель.
Сердечно-сосудистые заболевания часто сопровождаются повышенным содержанием тяжелых металлов в крови. Повышенное содержание кадмия или алюминия оказывает токсичное воздействие. А уровень некоторых важных для жизнедеятельности микроэлементов снижается – хром, медь, марганец.
Ниже рассмотрены несколько тяжелых металлов и их негативное воздействие на организм при избыточном содержании:
- Свинец. Вызывает разрушение эндокринной системы. Помимо сердца и сосудов, поражается печень. Следствием повышенного уровня свинца становится артериальная гипертензия и атеросклероз. У пациентов появляются следующие осложнения:
- аритмия,
- тахикардия,
- синусовая брадикардия,
- васкулит.
- Кадмий. При избытке данного тяжелого металла может возникнуть отравление печени, развиться кардиопатия и нарушиться регуляция гипофиза. Повышенное содержание кадмия вызывает развитие повторных атеросклеротических бляшек, артериальной гипертензии.
- Мышьяк. Из-за большого количества мышьяка в организме сосуды теряют способность пропускать кровь. Утолщение сосудов ведет к развитию кардиогенного шока.
Изменения в содержании тяжелых металлов происходит из-за приступа инфаркта миокарда, а они, в свою очередь, могут развить осложнения.
Полная диагностика

Сложность диагностирования инфаркта миокарда заключается в том, что многие его симптомы способны маскироваться под другие заблевания. Например, нестабильная стенокардия протекает с теми же ангинозными болями в загрудинной области. Иногда боль при приступе стенокардии тоже отдается в руки или спину.
Но стенокардию можно отличить от инфаркта. Если после успокоения человека болевые ощущения не проходят, то это не стенокардия, а инфаркт миокарда. Даже 3-4 дозы нитроглицерина не погасят дискомфорт и жжение при инфаркте, как при стенокардии.
Чтобы правильно диагностировать патологию, пациенту придется принять непосредственное участие в этом процессе. У больного врач собирает анамнез, в котором требуется ответить на следующие вопросы:
- Время начала приступа и продолжительность.
- Был ли эффект от принятия обычных медикаментов.
- Сколько раз приступ повторялся, и с какой периодичностью.
- Изменялись ли ощущения при успокоении или при изменении положения тела.
Внимание! Анамнез становится важной частью диагностики. Опытный врач отталкивается от него при слабовыраженных симптомах.
При сахарном диабете нередко приступ инфаркта миокарда имеет смазанные симптомы, что связано с поражением нервных окончаний. При появлении подозрений на инфаркт миокарда следует срочно обратиться за медицинской помощью, даже если ощущения не ярко выраженные.
Для постановки диагноза используют не только биохимический анализ крови. Вот перечень обследований, которые проходит пациент:
- Электрокардиография. Данное обследование позволяет врачу получить полную картину о функционировании сердечной мышцы. Квалифицированный врач сможет точно определить факт некроза клеток сердечной мышцы по нескольким показателям. Оценивается высота остроконечного зубца T, появление зубца Q, изменение сегмента ST. Для лучшей оценки состояния ЭКГ проводят периодично с получасовым перерывом. При каждом снятии данных проводится оценка динамики некроза.
- Биохимия. После полученных результатов ЭКГ подтверждением диагноза становится анализ крови. Как уже отмечено, при поступлении больного сразу после приступа инфаркта миокарда у него наблюдается увеличенное СОЭ. В крови обнаруживаются маркеры, подтверждающие некроз сердечной мышцы. Другой специфичный показатель – белок тропонин, который появляется при приступе инфаркта миокарда, а в нормальном состоянии не наблюдается.
- Эхокардиография. В качестве дополнительного обследования проводят эхокардиографию, если полученные результаты ЭКГ не позволяют выстроить ясную картину. К тому же это обследование позволяет определить наличие иных недугов, например, ишемической болезни. С другой стороны, эхокардиография может отменить диагноз инфаркта.
- Рентгенография. В некоторых случаях пациенту с жалобами на ангинозные ощущения в груди могут назначить рентгенографическое исследование, на котором специалист сможет определить, имеется ли застой в легких – признак инфаркта миокарда.
Как и у анализа крови, у других методов диагностирования есть свои особенности, которые позволяют определить приблизительное время начала некроза. Если после обследования поставлен диагноз инфаркт миокарда, больного определяют на стационарное лечение. Только стационарно можно предотвратить дальнейшее развитие некроза и спасти жизнь пациенту.
Читайте также: Тропониновый тест при инфаркте миокарда – правила проведения, расшифровка результатов
Загрузка…
Источник
