Антидепрессант при сердечной недостаточности
Чаще всего кардиологам приходится применять антидепрессанты при различных депрессивных состояниях. По данным зарубежных авторов, частота депрессивных расстройств среди госпитализированных терапевтических больных составляет 15-36%, среди больных ишемической болезнью сердца (ИБС) — 16-23%. В постинфарктном периоде, при рецидивах стенокардии, а также в связи с аортокоронарным шунтированием часто возникают тревога, кардиофобия, а в дальнейшем нередко формируется вторичная депрессия.
Депрессия (независимо от ее происхождения), развившаяся на фоне тяжелого соматического заболевания, значительно отягощает его течение и реабилитацию больного. В ряде исследований установлено, что симптомы депрессии являются достоверными прогностическими показателями смертности от сердечно-сосудистых заболеваний после перенесенного инфаркта миокарда. По данным N. Frasure-Smith и соавт. (1991, 1993), депрессивная симптоматика, выявленная после инфаркта миокарда, достоверно повышает риск смерти или повторного инфаркта миокарда, даже если принять во внимание другие факторы риска (в частности, дисфункцию левого желудочка, наличие инфарктов миокарда в анамнезе, частоту желудочковых экстрасистол).
С другой стороны, иногда при депрессии соматические жалобы и функциональные симптомы настолько превалируют в клинической картине, что врач-интернист даже не предполагает наличия у больного психического расстройства. По данным ВОЗ, более половины больных депрессиями лечатся у врачей общей практики и не попадают в поле зрения психиатров. Такие депрессии, называемые ларвированными или соматизированными, протекают под видом разнообразной соматовегетативной симптоматики, а собственно проявления депрессии оказываются атипичными. Это нередко приводит к ошибкам в диагностике, а изнурительные дополнительные обследования и длительное неэффективное лечение разочаровывают и больного, и врача. Эти соматовегетативные эквиваленты крайне разнообразны и включают в себя различные болевые синдромы (кардиалгии, головные боли, невралгии и т. д.), нередко имитирующие серьезную патологию; снижение или увеличение аппетита и, соответственно, потерю или прибавку в весе, расстройства сна, вегетативные пароксизмы и ряд других расстройств.
К основным признакам депрессии относят пониженное настроение, отсутствие интересов или чувства удовлетворения, повышенную утомляемость; к дополнительным — снижение способности к концентрации внимания, заниженную самооценку и неуверенность в себе, чувство вины, самоуничижение, мрачное пессимистическое видение будущего, суицидальные мысли или действия, нарушения сна (чаще ранние пробуждения), аппетита. При длительных хронических заболеваниях, этиологию которых не удается выявить, протекающих с периодическими спонтанными обострениями, врачу всегда следует подумать о наличии замаскированной депрессии.
Среди состояний, требующих применения психотропных средств, в частности антидепрессантов, необходимо выделить вегетативные кризы (панические атаки). В практике врача-терапевта и кардиолога часто встречаются пароксизмальные состояния, сопровождающиеся тревогой, страхом смерти, кардиалгией, сердцебиением, чувством нехватки воздуха, другими психическими и соматическими проявлениями. Такие пациенты нередко госпитализируются в кардиологические отделения стационаров с ошибочным диагнозом «стенокардия напряжения». Прежде всего необходимо четко установить, имеется ли у больного заболевание внутренних органов с тенденцией к пароксизмальным проявлениям (например, пароксизмальная тахикардия, мерцательная аритмия, феохромоцитома, бронхиальная астма и др.) или речь идет о приступах паники с разнообразными соматическими симптомами, связанными с повышенной активностью вегетативной нервной системы. При исключении органической патологии следует думать, что у больного имеется расстройство психического характера, проявляющееся в виде панических приступов. Такие приступы изредка протекают изолированно, тогда они рассматриваются в рамках панического расстройства. Значительно чаще они возникают на фоне депрессии, сочетаются с различными фобиями — выраженными и устойчивыми или немотивированными страхами, например боязнью открытых (агорафобия) или закрытых (клаустрофобия) пространств, страхом социальных ситуаций, публичных выступлений (социофобия) и др.
Наконец, антидепрессанты применяются при некоторых нарушениях сна. Традиционно сложилось так, что время сна (примерно треть жизни пациента) не попадает в сферу анализа и диагностики врача. Вместе с тем сон — это не просто состояние пониженной активности: он играет уникальную роль в поддержании жизнедеятельности живого организма. А. И. Бардер (1975) в ходе специальных исследований выявил группу заболеваний, включающую стенокардию, инфаркты миокарда, артериальную гипертензию, инсульты и некоторые другие заболевания, достоверно связанные с расстройствами сна. По данным Mittlmen и соавт. (1999), 20% случаев инфаркта миокарда и 15% случаев внезапной смерти приходится на период сна (между полуночью и 6 часами утра). Кроме того, ночные инфаркты миокарда имеют более тяжелое течение и чаще заканчиваются летальным исходом.
С другой стороны, приступы стенокардии также часто возникают в ночной период и в свою очередь вызывают нарушение сна. В работах О. Масагtur и соавт. (1995) продемонстрировано, что эмоциональное напряжение у пациентов с ишемической болезнью сердца заметно нарастает в вечерние и ночные часы из-за боязни повторения ангинозного приступа и смерти во время сна.
Кроме того, по данным Hung и соавт. (1993), у 5-9% населения работоспособного возраста встречается полное прекращение дыхания во сне продолжительностью 10 секунд и более — обструктивное сонное апноэ. Эти приступы играют определенную роль в развитии инфаркта миокарда и внезапной смерти при ИБС, поскольку возникающая при этом гипоксемия способна провоцировать ишемию миокарда. Убедительные доказательства этого были получены исследователями Стэнфордской группы. Стенокардия и изменения сегмента QТ совпадают по времени с периодами тяжелого обструктивного сонного апноэ, сопровождавшимися эпизодами десатурации крови. Все это неблагоприятно влияет на процесс реабилитации пациентов с инфарктом миокарда.
Таким образом, основными показаниями к применению антидепрессантов в кардиологической практике являются депрессивные расстройства, а также вегетативные кризы (панические атаки) и расстройства сна.
Необходимость лечения неглубоких депрессий врачами общей практики обусловлена, с одной стороны, большой распространенностью этих заболеваний, а с другой — упорным нежеланием многих больных обращаться в психоневрологические учреждения. При решении вопроса о самостоятельной курации больного с депрессией врач общей практики должен исключить следующие состояния, требующие обязательной специализированной психиатрической помощи: суицидальные мысли, которые могут активно не высказываться больными, однако при расспросе они обнаруживаются в активной или пассивной форме (например, «лучше бы попасть под машину и отмучиться»); бредовые идеи (чаще вины, ипохондрические или обвинения), галлюцинации; указания на наличие психического заболевания в прошлом; тяжелое соматическое состояние, требующее особой осторожности при подборе психотропной терапии; беременность.
После исчерпывающего соматического обследования врач должен тщательно проанализировать психопатологические особенности состояния, чтобы выбрать наиболее адекватную терапию. Лечение депрессии в общемедицинской сети осуществляется в основном с помощью лекарственных препаратов, однако простая разъяснительная беседа позволяет не только успокоить больного, но и обеспечить его приверженность рекомендованной терапии.
Противопоказаниями для назначения антидепрессантов являются острые заболевания печени и почек (с учетом их биотрансформации и выведения), кроветворных органов, нарушения мозгового кровообращения, декомпенсированные пороки сердца, судорожные припадки и некоторые другие тяжелые соматические заболевания.
Безопасность терапии
В настоящее время уже существует огромный выбор различных антидепрессантов, и их спектр продолжает неуклонно расширяться. Сегодня имеется достаточно много разнообразных классификаций антидепрессантов. В основе этих классификаций лежат особенности химической структуры, метаболизма, механизмов действия на нейромедиаторную систему и др. В самом общем виде антидепрессанты можно условно разделить на две группы: антидепрессанты классические (амитриптилин, лудиомил, мелипрамин и др.) и современные (прозак, коаксил, леривон и др).
Классические антидепрессанты (трициклические, четырехциклические) обладают наибольшим терапевтическим эффектом, но при этом имеют наиболее широкий и выраженный спектр побочных действий (связанных преимущественно с холинолитическим эффектом). В связи с этим часто приходится отказываться от терапии, у многих больных невозможно достичь достаточной терапевтической дозы. В связи с выраженным холинолитическим действием трициклические антидепрессанты могут вызывать запоры, затруднения мочеиспускания, ухудшение зрения (расстройства аккомодации). При использовании этих средств у больных сердечно-сосудистыми заболеваниями следует учитывать, что трициклические антидепрессанты имеют свойство накапливаться в сердечной мышце, где их концентрация оказывается более чем в 100 раз выше, чем в плазме крови. С передозировкой трициклических антидепрессантов связывают увеличение смертности от сердечно-сосудистых расстройств, в терапевтических дозах они могут вызывать удлинение интервалов PQ, QRS, QT, что объясняется их хинидиноподобной активностью.
Необратимые ингибиторы МАО (ниаламид) в настоящее время используются крайне редко ввиду высокого риска лекарственных взаимодействий, тираминовых, или «сырных», реакций и развития серьезных осложнений.
Современные антидепрессанты сравнимы с традиционными по эффективности, однако обладают значительно меньшими побочными эффектами, они гораздо безопаснее и проще в применении. К ним относят селективные ингибиторы обратного захвата серотонина (СИОЗС) — флуоксетин (прозак), циталопрам (ципрамил), флувоксамин (феварин), сертралин (золофт), пароксетин (паксил), а также препараты другого механизма действия — тианептин (коаксил), миансерин (леривон), моклобемид (аурорикс), бупропион и др. При терапии серотонинергическими антидепрессантами наиболее серьезным осложнением, особенно в случае использования высоких доз, является развитие серотонинового синдрома. Начальные проявления синдрома затрагивают главным образом желудочно-кишечный тракт и нервную систему. Характерно бурление и колики в животе, диарея, тошнота и другие диспептические жалобы. Неврологические симптомы включают тремор, дизартрию, мышечный гипертонус и миоклонические подергивания. Основная симптоматика является обратимой и быстро исчезает после снижения дозы или отмены антидепрессантов.
В кардиологической практике применение СИОЗС безусловно предпочтительнее в связи с их большей селективностью и лучшей переносимостью. Однако и здесь существуют некоторые различия в переносимости этих препаратов, обусловленные прежде всего избирательностью основного действия. В этой подгруппе наивысшей селективностью обладает циталопрам (ципрамил), представляющий собой наиболее безопасный в применении препарат. Так, например, действие циталопрама на сердечную проводимость и реполяризацию оценивалось в ходе рандомизированного двойного слепого плацебо-контролируемого исследования, в котором приняли участие 23 человека. Кроме того, Soren L.R. и соавт. (1999) дали ретроспективную оценку более чем 6000 ЭКГ, сделанным 1460 пациентам в период с 1978 по 1996 год, во время проведения трех рандомизированных двойных слепых исследований; из них 1789 ЭКГ снято на фоне терапии циталопрамом. Результаты проведенных исследований показали, что воздействие циталопрама на электрокардиографические параметры проявлялось лишь в виде небольшого снижения частоты сердечных сокращений (менее 8 ударов в минуту). Значимого влияния препарата на продолжительность интервалов PQ, QRS и QT выявлено не было, то есть циталопрам не оказывает заметного воздействия на сердечную проводимость и процессы реполяризации.
Другим важным преимуществом современных антидепрессантов является их минимальное взаимодействие с другими лекарственными средствами, в том числе применяемыми при лечении сердечно-сосудистых заболеваний. Важнейшую роль при этом играет цитохром Р450, участвующий в метаболизме различных лекарственных средств (табл. 1).
Препараты, которые ингибируют более чем один изомер цитохрома Р450, в большей степени взаимодействуют с другими лекарственными средствами. Влияние СИОЗС на различные изомеры цитохрома Р450 представлено в табл. 2. Исходя из этих данных можно утверждать, что наименьшая вероятность возникновения лекарственных взаимодействий отмечается при использовании циталопрама.
Основные принципы антидепрессивной терапии справедливы как для классических, так и для новых современных антидепрессантов
- Необходимо использовать адекватные терапевтические дозы, которые для классических (трициклических, четырехциклических) антидепрессантов составляют до 150-300 мг в сутки. Лечение этими антидепрессантами начинают с малых доз (25-50 мг в сутки), при хорошей переносимости дозу постепенно наращивают до появления положительного или возникновения побочного эффекта. В общесоматической практике не рекомендуется применять дозу свыше 75-100 мг в сутки, так как с последующим увеличением дозы возрастает риск различных осложнений — как соматических, так и психоневрологических (например, опасность холинолитического делирия у лиц пожилого возраста). При неэффективности лечения указанной дозой необходима консультация психиатра. Для современных антидепрессантов дозы, как правило, фиксированы и различаются в зависимости от вида препарата.
- Эффект антидепрессивной терапии проявляется не сразу, а в течение 1-3 недель от начала лечения.
- Если к четвертой неделе лечения эффект от проводимой терапии отсутствует, в первую очередь необходимо убедиться, что достигнута терапевтическая доза. Только в этом случае можно считать, что препарат неэффективен и, следовательно, должен быть заменен на другой (в данном случае необходима консультация психиатра).
- Лечение депрессии должно осуществляться длительно, от 4-6 месяцев до нескольких лет, в зависимости от особенностей течения заболевания; ранняя отмена препарата даже на фоне клинического благополучия может привести к рецидиву болезни. Доза препарата при этом должна сохраняться на прежнем уровне и только в случае необходимости (побочные действия) может быть уменьшена, но не более чем на 25-30%.
Препаратами выбора для лечения депрессий с соматическими симптомами являются лекарственные средства, обладающие наименьшей выраженностью побочных действий. К таким препаратам можно отнести селективные ингибиторы обратного захвата серотонина, в частности циталопрам (ципрамил) в дозе 20 мг в сутки, сертралин (золофт) в дозе 50-100 мг в сутки, а также препараты иной химической структуры: коаксил в дозе 25-37,5 мг в сутки, миансерин (леривон) в дозе до 100 мг в сутки и доксепин (синекван) в дозе до 150 мг в сутки.
При тревожной депрессии используются препараты, обладающие седативным или анксиолитическим эффектом: амитриптилин в дозе до 75-100 мг в сутки, циталопрам (ципрамил) в дозе 20 мг в сутки, коаксил в дозе 37,5 мг в сутки, миансерин (леривон) в дозе до 100 мг в сутки; или сбалансированные препараты: лудиомил в дозе до 100 мг в сутки, феварин в дозе 50-100 мг в сутки, золофт в дозе 50-100 мг в сутки, паксил в дозе 20 мг в сутки.
Если депрессия сопровождается тревогой, раздражительностью, вегетативными пароксизмами (паническими атаками), антидепрессанты целесообразно сочетать с транквилизаторами или использовать комбинированные препараты, например амиксид (амитриптилин+хлордиазепоксид). Транквилизаторы не назначаются при наличии у больного суицидальных мыслей, так как это облегчает проведение суицида.
В случае преобладания в структуре депрессии апатии, анергии целесообразно использовать препараты с активирующим действием: мелипрамин в дозе до 100 мг в сутки, прозак в дозе 20 мг в сутки, моклобемид (аурорикс) в дозе 300 мг в сутки. При апатоадинамических депрессиях с признаками астении, трудностями концентрации внимания и мышления целесообразно присоединение ноотропов.
В лечении панических приступов, особенно если они развиваются на фоне депрессии, в сочетании с фобиями, применению антидепрессантов также придается большое значение. Лечение этих расстройств осуществляется длительно. Наиболее эффективным является применение антидепрессантов в сочетании с психотерапией. Для выбора правильной терапевтической тактики необходима консультация психиатра. В такой ситуации целесообразно применение ципрамила, имипрамина, анафранила, золофта, феварина, флуоксетина и других препаратов; транквилизаторам же отводится вспомогательная роль. Наличие у ципрамила отчетливого анксиолитического действия делает его наиболее эффективным при панических атаках.
Ципрамил входит в число препаратов, с помощью которых можно корректировать нарушения сна у пациентов с инфарктом миокарда, особенно в среднем возрасте. К его достоинствам следует отнести отсутствие отрицательного воздействия на дыхание пациента, что представляется важным в связи с возможностью обструктивного апноэ сна. Более того, как показано в некоторых исследованиях, антидепрессанты — ингибиторы обратного захвата серотонина способны несколько уменьшать индекс апноэ сна. Ципрамил обладает способностью нормализовать структуру сна, повышать его эффективность и сокращать время засыпания, что делает этот препарат весьма перспективным для медикаментозной коррекции нарушений сна при инфаркте миокарда.
А. Л. Верткин, доктор медицинских наук, профессор
А. В. Тополянский
О. В. Любшина
Источник
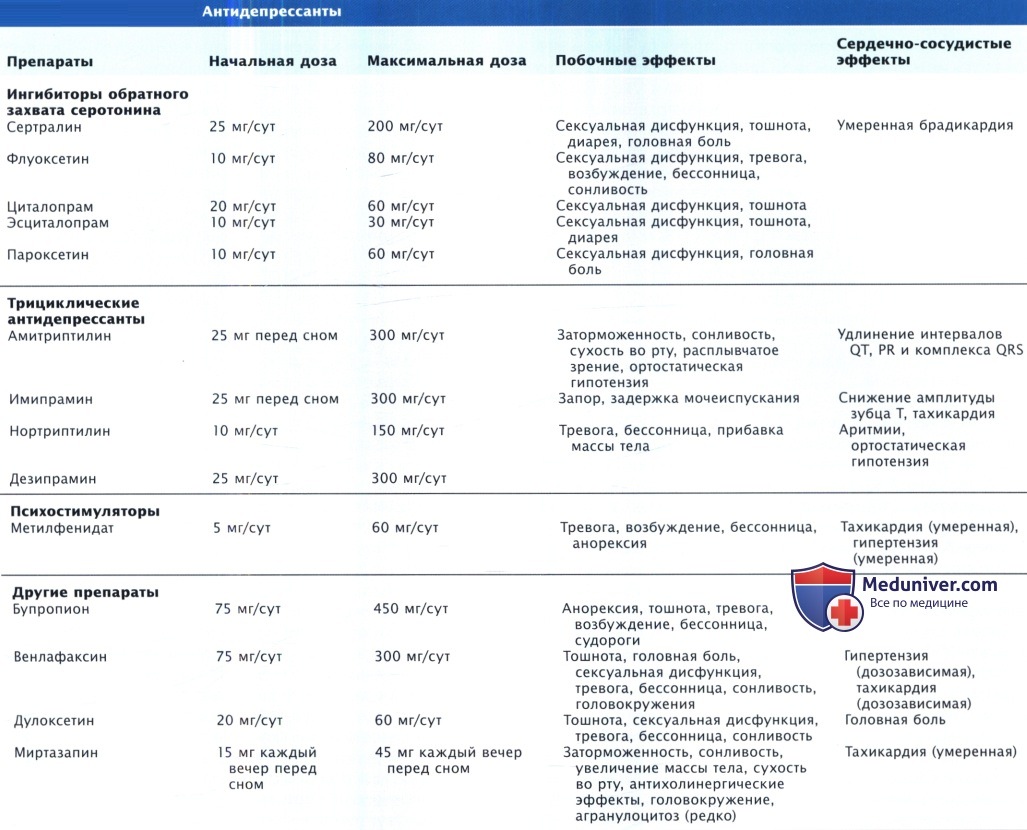
а) Селективные ингибиторы обратного захвата серотонина (СИОЗС). Селективные ингибиторы обратного захвата серотонина (СИОЗС) заменили трициклические антидепрессанты (ТЦА) и стали препаратами первой линии терапии кардиологических пациентов с большим депрессивным расстройством. Эффективность СИОЗС сопоставима с эффективностью ТЦА, но СИОЗС лучше переносятся, оказывают меньшее негативное фармакологическое воздействие на сердечно-сосудистую систему, а передозировка их менее опасна.
В настоящее время показано, что СИОЗС минимально влияют на сердечно-сосудистую систему и имеют широкие границы безопасности при лечении пациентов даже с тяжелыми заболеваниями сердца. СИОЗС обладают незначительной антихолинергической, антигистаминной и норадренергической активностью и, по всей видимости, ингибируют агрегацию тромбоцитов.
У здоровых людей СИОЗС не оказывают отрицательного влияния на сократимость и проводимость миокарда, доказательства их кардиотоксичности при передозировке отсутствуют. У кардиологических пациентов СИОЗС не вызывают существенных изменений на ЭКГ и не влияют на АД, хотя могут замедлить сердечный ритм. В редких случаях они вызывают клинически значимую синусовую брадикардию. Поскольку СИОЗС нарушают агрегацию тромбоцитов, они способны увеличить время кровотечения. СИОЗС могут взаимодействовать со многими лекарственными препаратами, применяемыми у кардиологических больных.
СИОЗС ингибируют изоферменты цитохрома Р450 в печени, вовлеченные в окислительный метаболизм препаратов, включая липофильные β-блокаторы (например, метопролол, пропранолол); блокаторы кальциевых каналов, антиаритмические средства класса 1C, ИАПФ, антиконвульсанты, антигистаминные препараты; бензодиазепины, ТЦА, кодеин и варфарин. Вследствие этого СИОЗС могут повышать уровень перечисленных препаратов в крови при совместном назначении, поэтому необходимо соблюдать меры предосторожности при назначении СИОЗС пациентам, принимающим перечисленные препараты, и особенно тщательно контролировать протромбиновое время, если больной принимает одновременно и СИОЗС, и варфарин.
СИОЗС — это препараты, активно связывающиеся с белками, поэтому СИОЗС могут замещать (при совместном назначении) другие связывающиеся с белками лекарственные средства, тем самым повышая их биодоступность. Такое взаимодействие может наблюдаться при назначении СИОЗС совместно с варфарином и дигоксином, однако это взаимодействие не представляется клинически значимым.
Поскольку и депрессия, и ИМ активируют тромбоциты, период постинфарктной депрессии характеризуется повышенным риском развития тромботических осложнений. В одном из последних контролируемых исследований, включившем 281 больного с ОКС, у пациентов с ОКС в сочетании с депрессией выявлены значительно более высокие уровни тромбоцитарного фактора 4, β-тромбоглобулина, молекул тромбоцитарно-эндотелиальной клеточной адгезии 1 (РЕСАМ-1) по сравнению с пациентами без депрессии или здоровыми людьми (контрольная группа). У пациентов с ИБС и ХСН, принимающих аспирин, назначение для лечения депрессии СИОЗС оказывает дополнительный антитромбоцитарный эффект.
Следовательно, при использовании СИОЗС может понадобиться изменение дозы аспирина или других антитромбоцитарных препаратов либо переоценка показаний к их назначению.

б) Трициклические антидепрессанты (ТЦА). Раньше ТЦА были основой фармакотерапии депрессий, в настоящее время ТЦА продолжают широко использовать. Однако их многочисленные сердечно-сосудистые побочные эффекты и вероятность летального исхода при передозировке ограничивают круг их использования у кардиологических пациентов. ТЦА действуют на адренергические и серотонинергические нейроны ЦНС и проявляют антихолинергические свойства на периферии. Кроме того, ТЦА обладают хинидинподобным действием и блокируют а-адренергические рецепторы. ТЦА влияют на ЧСС, АД, ритм, проводимость и сократимость миокарда, поэтому ТЦА обычно не используют при нарушениях ритма и проводимости сердца, тяжелой ХСН и в течение 4-6 нед после ИМ.
Среди ТЦА третичные амины (например, имипрамин, амитриптилин] ассоциируются с большим количеством побочных эффектов, поэтому в кардиологической практике предпочтительнее вторичные амины (например, нортриптилин).
ТЦА, являясь ангиаритмическими препаратами класса IA, угнетают проводимость миокарда, снижают возбудимость желудочков и подавляют эктопическую активность. ТЦА замедляют деполяризацию предсердий и желудочков, удлиняют интервалы QT, PR и комплекс QRS, уменьшают амплитуду зубца Т. При отсутствии в анамнезе нарушений проводимости сердца эти эффекты чаще бывают клинически незначимыми, если используют терапевтические дозы препаратов. Однако АВ-блокада II степени, синдром слабости синусового узла, блокада ножек пучка Тиса, удлинение интервала QT и сопутствующий прием антиаритмических препаратов являются противопоказаниями к применению ТЦА.
Помимо антиаритмического эффекта ТЦА могут обладать аритмогенным действием, возможно из-за их способности удлинять интервал QT и/или увеличивать концентрацию норадреналина в миокарде вследствие ингибирования его обратного захвата на периферии. Наиболее часто ТЦА провоцируют такие аритмии, как предсердная и желудочковая экстрасистолии, но могут развиться и более опасные желудочковые аритмии. Токсические проаритмогенные эффекты проявляются в первую очередь при передозировке ТЦА и более вероятны у пациентов с ИБС, с удлиненным интервалом QT, электрической нестабильностью миокарда или недавно перенесенным ИМ. ТЦА также повышают ЧСС на 5-20 уд/мин в результате антихолинергической блокады. Хотя это не является проблемой для относительно здоровых людей, но должно учитываться у больных с сердечной патологией.
ТЦА провоцируют ортостатическую гипотензию у 20% пациентов. У пожилых людей ортостатическая гипотензия может вызывать гипоперфузию головного мозга и привести к падениям и переломам, поэтому такой побочный эффект ТЦА становится критическим. У пациентов, принимающих ТЦА, особенно в начале терапии и при повышении дозы, необходимо следить за уровнем АД и ЧСС для своевременного выявления признаков ортостатической гипотензии. Пожилым пациентам нужно советовать медленно вставать после длительного пребывания в положении лежа или сидя. Выраженность ортостатической гипотензии, связанной с приемом ТЦА, зависит от степени ее выраженности до начала лечения и, вероятно, клинически будет более значима у пациентов с ХСН, снижением функции ЛЖ, гиповолемией или получающих антигипертензивные препараты.
С осторожностью следует назначать ТЦА пациентам со сниженной ФВ, т.к. в экспериментах на животных была отмечена способность ТЦА угнетать сократимость миокарда. У людей этот эффект отмечается только при передозировке и ТЦА редко усугубляют течение ХСН.
в) Другие антидепрессанты. Бупропион избирательно действует на допаминовые и норадреналиновые рецепторы, приводит к менее выраженной гипотензии, чем ТЦА, и не влияет на проводимость и сократимость миокарда. Использование бупропиона у пациентов с заболеваниями сердца безопасно. У больных с желудочковыми аритмиями и нарушениями проводимости этот препарат не усугубляет их тяжесть. Дополнительное преимущество применения бупропиона у кардиологических пациентов состоит в том, что он, по всей видимости, способствует отказу от курения. При использовании высоких доз бупропиона могут наблюдаться судороги, иногда возможно повышение АД и ЧСС, хотя редко до клинически значимого уровня. Поскольку бупропион блокирует изоферменты цитохрома Р450, возможно повышение концентрации β-блокаторов и антиаритмических препаратов класса 1C при комплексном применении.
Венлафаксин воздействует на обратный захват и серотонина, и норадреналина, обладает небольшим влиянием на работу сердечно-сосудистой системы и не изменяет ЭКГ. В больших дозах венлафаксин может повышать АД и пульс. В отличие от СИОЗС не блокирует изоферменты цитохрома Р450 и слабо связывается с белками плазмы, поэтому венлафаксин можно назначать пациентам, получающим кардиотропную терапию.
Дулоксетин — самый новый ингибитор обратного захвата серотонина и норадреналина, использование которого у пациентов с сердечно-сосудистой патологией не изучено. Сейчас мы можем только предполагать, что препарат можно применять так же, как и венлафаксин, но с одной существенной разницей: в отличие от венлафаксина высокие дозы дулоксетина не повышают АД.
Тразодон — производное триазолопиридина, которое часто используют в малых дозах как снотворное средство. Сердечно-сосудистые осложнения при приеме тразодона редки. Препарат имеет незначительные (если имеет) антиаритмические свойства, есть единичные наблюдения его связи с блокадами сердца и желудочковыми аритмиями. Из-за слабого α-адреноблокирующего действия может вызвать ортостатическую гипотензию.
Нефазодон — близкий к тразодону препарат. Нефазодон ингибирует изоферменты цитохрома Р450, поэтому может повышать уровень блокаторов кальциевых каналов, хинидина и лидокаина при совместном использовании. В редких случаях нефазодон может вызывать ортостатическую гипотензию.
Миртазапин является тетрациклическим антидепрессантом со сложным механизмом действия. Применение миртазапина у пациентов с ССЗ не изучено, однако известно, что у пациентов с некардиальной патологией он не влияет на АД и проводящую систему сердца. Миртазапин не обладает антихолинергической активностью, но может немного повышать ЧСС.
Такие психостимуляторы, как декстроамфетамин и метилфенидат, используют для лечения депрессии в случае жизнеугрожающего состояния и у пожилых пациентов. Эти препараты назначают, когда лечение депрессии жизненно важно и быстрый терапевтический ответ имеет решающее значение (эти препараты обладают быстрым началом действия), а также при депрессиях с выраженной апатией и резким снижением (вплоть до отсутствия) психической, двигательной и речевой активности. Хотя существует значительный опыт клинического применения этих психостимуляторов, эмпирических доказательств их длительной и устойчивой эффективности недостаточно.
Такие значимые сердечно-сосудистые побочные эффекты, как тахикардия, гипертензия, аритмия, относительно редки, но следует проявлять осторожность при назначении этих препаратов пациентам с тяжелой гипертензией, тахикардией или желудочковой экстра-систолией. В процессе лечения необходим тщательный контроль АД и ЧСС.
– Читать “Применение нейролептиков при сердечно-сосудистых заболеваниях (ССЗ)”
Редактор: Искандер Милевски. Дата публикации: 26.3.2019
Источник
