Адреналиновая модель инфаркта миокарда
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Большов П.С.
1
Чижмак А.О.
1
Мульский С.В.
1
Куликова С.Г.
1
1 ГБОУ ВПО Кубанский государственный медицинский университет Министерства здравоохранения Российской Федерации
Одним из наиболее грозных заболеваний сердечно-сосудистой системы является инфаркт миокарда. Новым подходом в терапии инфаркта миокарда может стать стимуляция процессов органотипической репаративной регенерации, что требует проведения исследований, в том числе и на in vivo моделях инфаркта миокарда. В связи с этим, целью нашей работы является разработка модели инфаркта миокарда у крыс пригодной для хронического эксперимента. В результате проведенного исследования было показано, что модель инфаркта миокарда пригодная для хронического эксперимента в области исследования процессов органотипической регенерации миокарда должна быть максимально малоинвазивной, так как даже применение щадящей межреберной торакотомии сопряжено с формированием большого числа интраоперационных осложнений в основном связанных с дефектами операционной техники и герметизации грудной полости.
инфаркт миокарда
крыса
хроническая модель
эксперимент
1. Галенко-Ярошевский А.П., Туровая А.Ю., Городжая Г.Г. Влияние РУ-353 на содержание биогенных аминов, ацетилхолина и активность ацетилхолинэстеразы в миокарде и различных отделах головного мозга крыс // Бюллетень экспериментальной биологии и медицины. – 2002. – П. 2. – С. 58–62.
2. Джиджихия К.М. Лабораторный синтез экспериментальной модели инфаркта миокарда у крыс / К.М. Джиджихия, А.Х. Каде, С.А. Занин [и соавт.] // Фундаментальные исследования. – 2013. – № 12. – Ч. 3. – С. 461–465.
3. Джиджихия К.М. Получение модели крупноочагового инфаркта миокарда в остром эксперименте на крысах / Джиджихия К.М., Каде А.Х., Занин С.А., Самоследова Д.А., Джиджихия З.М. // Фундаментальные исследования. – 2012. – № 4–2. – С. 270–273.
4. Трофименко А.И. Влияние ТЭС-терапии на исходы острого адреналинового повреждения сердца у крыс / А.И. Трофименко, А.Х. Каде, В.П. Лебедев [и соавт.] // Кубанский научный медицинский вестник. – 2013. – № 5 (140). – С. 174–180.
5. Трофименко А.И. Гистологическая картина миокарда при адреналиновом повреждении сердца у крыс / А.И. Трофименко, А.Х. Каде, С.А. Занин [и соавт.] // Международный журнал прикладных и фундаментальных исследований. – 2013. – № 7. – С. 135–138.
6. Трофименко А.И. Особенности электрокардиограммы у крыс с моделью церебральной ишемии, вызванной посредством коагуляции правой средней мозговой артерии // А.И. Трофименко, А.Х. Каде, В.П. Лебедев [и соавт.] // Кубанский научный медицинский вестник. – 2012. – № 2 (131). – С. 175–179.
7. Трофименко А.И. Моделирование церебральной ишемии посредством коагуляции средней мозговой артерии у крыс / А.И. Трофименко, А.Х. Каде, В.П. Лебедев [и соавт.] // Фундаментальные исследования. – 2012. – № 2. – Ч. 1. – С. 215–218.
8. Трофименко А.И. Влияние ТЭС-терапии и агонистов пурин-эргической стресс-лимитирующей системы на течение адреналиновой кардиомиопатии у крыс в эксперименте / А.И. Трофименко, А.Х. Каде, С.А. Занин, Ю.В. Дынько // Вестник МУЗ ГБ № 2. – 2013. – № 5 (29); URL: http: //vestnik.kmldo.ru/pdf/13/05/02.pdf (дата обращения: 03.11.2013).
9. Трофименко А.И. Гистологическая картина миокарда у крыс с моделью церебральной ишемии, вызванной коагуляцией правой средней мозговой артерии / А.И. Трофименко, А.Х. Каде, С.А. Занин, Ю.В. Дынько // Вестник МУЗ ГБ № 2. – 2012. – № 5 (23); URL: https://vestnik.kmldo.ru/pdf/12/05/02.pdf (дата обращения: 08.10.2012).
10. Туровая А.Ю., Кигурадзе М.И., Галенко-Ярошевский П.А., Каде А.Х., Уваров А.В., Татулашвили Д.Р., Сукоян Г.В. Cостояние симпатико-адреналовой системы и соотношения нейроактивных аминокислот в продолговатом мозге крыс под влиянием неселективных β-адреноблокаторов // Бюллетень экспериментальной биологии и медицины. – 2005. – Т. 139, № 5. – С. 525–527.
Заболевания сердечно-сосудистой системы являются ведущей причиной инвалидизации и смертности в Российской Федерации. Одним из наиболее грозных проявлений патологии сердечно-сосудистой системы является инфаркт миокарда [2, 3]. Новым подходом в терапии инфаркта миокарда может стать стимуляция процессов органотипической репаративной регенерации, что требует проведения исследований, в том числе и на in vivo моделях инфаркта миокарда [1, 10].
Цель работы – разработка модели инфаркта миокарда у крыс пригодной для хронического эксперимента.
Материалы и методы исследования
Исследование проведено в лаборатории кафедры общей и клинической патофизиологии ГБОУ ВПО КубГМУ. Эксперименты проведены на 10 белых нелинейных крысах средней массой – 280 ± 30 гр. Содержание животных и постановка экспериментов проводилась в соответствии с требованиями приказов № 1179 МЗ СССР от 11.10.1983 года и № 267 МЗ РФ от 19.06.2003 года, а также международными правилами «Guide for the Care and Use of Laboratory Animals». Все потенциально болезненные сопровождались использованием золетил-ксилазинового наркоза по следующей схеме: золетил 0,3 мг в/м («Virbac» Франция), ксиланит 0,8 мг в/м (ЗАО «НИТА-ФАРМ, Россия, г. Саратов), атропина сульфат 0,1 % раствор – 0,01 мл п/к из расчета на 100 гр. массы тела животного [7]. Наркоз верифицировали по исчезновению реакции на болевые раздражители (укол лапы) и угнетению роговичного рефлекса. Регистрацию электрокардиограмм у крыс проводили на электрокардиографе ЭК 1Т- 1/3- 07 «АКСИОН» в стандартных отведениях I, II, III (двухполюсные отведения от конечностей): I – левая и правая передние конечности, II – левая задняя и правая передняя конечности, III – левая задняя и левая передняя конечности) в положении на спине, с использованием игольчатых электродов помещаемых подкожно на конечности [6].
Операция проходила с помощью искусственной вентиляции легких через трахеостому с использованием аппарата «ВИТА-1» (СССР). Доступ к сердцу осуществлялся за счет межреберной торакотомии. Предварительно в связи с относительно высокой частотой декстрокардии у крыс проводили пальпаторное определение локализации верхушечного толчка. Торакотомия выполнялась в 6 межреберье. При ревизии плевральной полости вскрывался перикард, с помощью надавливания на грудную клетку сердце пролабировало в рану, с помощью ватных палочек осуществляли разворот сердца. Под левую венечную артерию подведена игла атравмат (шелк 7/0), произведена перевязка артерии. Выполнялся прокол грудной клетки в 8 межреберье противоположной стороны, установлен плевральный дренаж. В дальнейшем проводилось послойное ушивание торакотомной раны непрерывными швами. С помощью шприца через дренаж аспирирован воздух из плевральной полости, после чего плевральный дренаж удален. П-образным швом ушита трахея. После удаления дыхательной трубки шов затянут, проведено послойное ушивание раны непрерывным швом. Проводилась послеоперационная антибиотикотерапия с использование бициллина-5 из расчета 30 тыс. ЕД на 100 гр. веса тела животного. У крыс переживших создание модели проводилась эвтаназия на 14 сутки с забором сердца.
Сердце разрезалось по длиннику вдоль полостей, быстро промывалось в холодном растворе 0,9 % натрия хлорида и подвергалось фиксации в 10 % нейтральном забуференном фосфатами формалине. Выполнялась проводка образцов через изопропанол-минеральное масло, с последующей заливкой в парафин. В дальнейшем изготавливались парафиновые блоки, проводилась их нарезка на микротоме МПС-2 (СССР) на срезы толщиной 10 мкм. Проводилось монтирование срезов на предметные стекла с адгезивным покрытием. Микропрепараты окрашивались гематоксилином-эозином и по Маллори [4, 5, 8, 9]. Заключение под покровное стекло проводилось в пихтовый бальзам. Полученные микропрепараты фотографировали с помощью окулярной камеры «Levenhuk 230» (США) на микроскопе Микромед-6 (Россия).
Результаты исследования и их обсуждение
При анализе причин смерти животных выяснено, что 4 крысы погибли интраоперационно ввиду повреждения крупных магистральных сосудов и кровотечения. У всех крыс начиная с момента перевязки левой венечной артерии определялись электрокардиографические признаки ишемии миокарда, в виде появления и подъема сегмента ST [4]. Причиной гибели 3-х крыс послужили дефекты установки трахеостомической трубки и ушивания трахеи. У двух крыс летальный исход развился на 1 и 3 сутки соответственно, при этом как клинически, так и секционно выявлена картина тяжелой сердечной недостаточности. При исследовании микропрепаратов сердца видна картина глыбчатого распада кардиомиоцитов с исчезновением поперечной исчерченности, ядра прокрашивались плохо данные явления могут быть объяснены процессами аутолиза, так как забор сердца у погибшего животного выполнялся после обнаружения трупа в клетке.
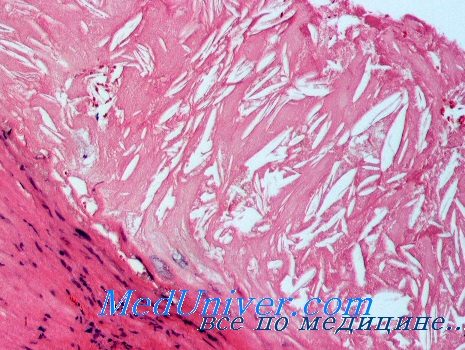
Только одна крыса нормально перенесла оперативное вмешательство по созданию модели инфаркта миокарда, ее эвтаназия с забором гистоматериала была проведена на 14 сутки от начала эксперимента. В миокарде при окрашивании четко выявляется зона свежей соединительной ткани в области кровоснабжения левой венечной артерии.
Выводы
В результате проведенного исследования было показано, что модель инфаркта миокарда пригодная для хронического эксперимента в области исследования процессов органотипической регенерации миокарда должна быть максимально малоинвазивной, так как даже применение межреберной торакотомии сопряжено с формированием большого числа интраоперационных осложнений в основном связанных с дефектами операционной техники и герметизации грудной полости.
Библиографическая ссылка
Большов П.С., Чижмак А.О., Мульский С.В., Куликова С.Г. РАЗРАБОТКА МОДЕЛИ ИНФАРКТА МИОКАРДА В ХРОНИЧЕСКОМ ЭКСПЕРИМЕНТЕ У КРЫС // Международный журнал прикладных и фундаментальных исследований. – 2015. – № 5-1. – С. 52-53;
URL: https://applied-research.ru/ru/article/view?id=6758 (дата обращения: 17.09.2020).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник
Инфаркт миокарда – очень грозное заболевание, как не крути. Даже малосимптомные проявления, которые практически не беспокоили, дадут о себе знать в будущем. Поэтому так много сил и времени уделяется максимально ранней диагностике этого недуга.
Источник картинки: pixabay.com
Инфаркт миокарда – это острый коронарный синдром, который возникает из-за внезапного и полного прекращения кровотока в коронарной артерии в связи с тромбозом и с последующим развитием очагов ишемического некроза в сердечной стенке.
В США показатель догоспитальной смертности составляет около 50% всех случаев острого ИМ, а практически все случаи первичной фибрилляции желудочков происходят в первые 4 часа после начала инфаркта миокарда. Думаю вы и сами понимаете, насколько это опасное заболевание и насколько важно быстро его диагностировать.
Диагностические методы
Чтобы врачу определить, что перед ним именно инфаркт миокарда, нужно сопоставить три важных показателя: клиническую картину, изменения на ЭКГ, повышение маркеров в крови.
Если говорить о клинической картине (затяжная, более 20 минут, ангиозная боль, которая не снимается нитроглицерином), то её трактовка достаточно субьективна, и некоторые врачи могут не обратить на неё внимание, либо не иметь достаточных знаний чтобы распознать, к примеру, атипичные клинические проявления.
Типы боли при инфаркте миокарда. Источник: Внутренняя медицина за Неттером.
Всё вышесказанное можно отнести и к ЭКГ (электрокардиография), которая, хоть и способна показать изменения, обладает довольно существенным минусом – необходимостью в интерпретации, из-за чего субьективность расшифровки, а, следовательно, возможная неквалифицированность медика сыграет злую шутку с больным.
Вид инфаркта на ЭКГ. Отчётливо видна элевация сегмента ST в отведенияз V1-V5, avR, avL. Если хотите понять, что видно на ленте – добро пожаловать в мою статью про ЭКГ на канале.. Источник картинки – Я.Картинки
Вот тут мы и подходим к третьему пункту диагностики инфаркта и, по совместительству, темой нашего сегодняшнего разговора – сердечным маркерам. Давайте разбираться, что это.
Маркеры инфаркта миокарда
Что же такое биохимические маркеры заболевания? Это специфические вещества, наличие в крови которых в норме минимально, либо отсутствует вовсе. Их повышение сигнализирует о том, что в организме случился сбой, и повредился именно тот орган, с которым конкретный маркер ассоциирован. Для всего организма существуют самые различные маркеры (тот же альфа-фетопротеин как онкомаркер рака печени, аминотрансферазы как маркеры повреждения почек, печени, поджелудочной железы, сердца(в меньшей степени). Все они повышаются при тех или иных патологиях.
Конкретно для сердца существуют четыре основных маркера: миоглобин, сердечные тропонины, КФК-МВ, ЛДГ. Остановимся на каждом из них.
Миоглобин
Миоглобин – это белок, который транспортирует кислород в скелетные мышцы и миокард. При повреждении мышечной ткани концентрация этого белка в крови повышается в 5-10 раз. Поскольку миоглобин содержится не только в сердечных мышцах, он не является специфическим маркером, однако реагирует он одним из первых: уже через час концентрация его в крови значительно вырастает.
Кроме ИМ, миоглобин выявляется при синдроме длительного сдавливания, травмах мышц, после хирургических операций.
Сердечные тропонины
Сердечные тропонины – тропонин I и тропонин Т – обнаруживаются только в сердечной мышце. Это белки, которые так же, как и миоглобин, в норме не обнаруживаются в крови, и высвобождаются при повреждении сердца. Повышение значений происходит несколько позже, чем у миоглобина – через 4-5 часа, и держится повышенным до 10-14 дней.
Креатинфосфокиназа-МВ
Креатинфосфокиназа-МВ (КФК-МВ) – даный маркер повышается в крови спустя 4-8 часов, что немного уступает по скорости тому же миоглобину. Однако он обладает значительным преимуществом перед коллегами – его уровень снижается уже на 3 сутки (вышеописанный тропонин начинает снижаться только с 8-10 дня), что даёт возможность определить повторный инфаркт миокарда в случае его возникновения.
Лактатдегидрогеназа
Лактатдегидрогеназа 1 и 2 (ЛДГ) – это ферменты гликолиза, которые преобладают в сердце (Другие изоформы ЛДГ преобладают в лёгких, поджелудочной железе). Не является специфическим показателем инфаркта, так как изоформы 1 и 2 также находятся в других органах, хоть и в меньшей мере. Имеет самый длительный период выхода в кровь (выявляется только спустя 8-10 часов), и не имеет первоочередную ценность в диагностике инфаркта миокарда, однако в сумме с остальными маркерами всё же используется.
Источник картинки: Передерий, Ткач. Основы внутренней медицины, 2009г.
Суммируя всё вышесказанное, стоит сказать, что ни один из маркеров не лишён недостатков, однако в комплексной диагностике они дают чёткую картину развития инфаркта миокарда.
Спасибо, что читали статью! Подписывайтесь, чтобы получать новую дозу интересных и познавательных статей из мира медицины!
Источник
Адренергические причины стенокардии и инфаркта миокарда. Влияние адреналина на коагуляциюГормональные влияния могут проявляться и в отношении таких осложнений атеросклероза, как стенокардия и инфаркт миокарда. Многие авторы находят повышение адренергических веществ в крови у больных со стенокардией (А. А. Дубинский и А. Е. Пащенко, 1958). Raab высказал предположение, что приступы стенокардии, вызванные физическим напряжением, действием холода или эмоциональным возбуждением, обусловлены внезапным повышением выделения адреналина, который оказывает гипоксическое действие на сердечную мышцу. Это предположение базировалось на наблюдениях автора, установившего значительное повышение содержания катехоламинов в крови при приступах стенокардии напряжения, что может привести даже к тромбированию сосудов. Выраженный спазм сосудов повреждает эндотелий сосудистой стенки в связи с ишемией, что способствует прилипанию тромбоцитов к поврежденной поверхности и их агглютинации. Усиление процесса свертывания крови под влиянием адреналина было установлено также Adelson с соавт. (1961). Спазм коронарных артерий, несомненно, играет главенствующую роль при их тромбозе, так как, помимо сужения просвета сосуда и замедления вследствие этого тока крови, спазм сосудов провоцирует также и рефлекторные изменения в свертывающей и антисвертывающей системе крови, а также в функциональном состоянии тромбоцитов. Как показали наблюдения, проведенные в пашей клинике ассистентом Л. П. Ермиловым (1960), у больных с частыми приступами стенокардии наблюдается повышение содержания в крови прокоагулянтов и понижение антикоагулянтов. Такое состояние свертывающей системы крови можно расценивать как угрожающее в отношении тромбообразования.
Эти данные были подтверждены также и в работе аспиранта Л. Л. Гущиной (1966), которая изучала функциональные свойства тромбоцитов у больных с приступами стенокардии и нашла повышение коагулябилыюсти пластинок непосредственно после болевого приступа — повышение агглютинабильности, адгезивности пластинок, их вязкого метаморфоза. Наблюдения Л. А. Гущиной стоят в соответствии с интересными данными McKay (1965), который установил влияние адреналина на функциональное состояние тромбоцитов. Приведенные им наблюдения с меченными по Р32 тромбоцитами показали, что под влиянием адреналина срок жизни этих клеток сокращается и резко повышается их разрушаемость, что свидетельствует о состоянии гиперкоагулябильности. Адренергическим воздействиям придается большое значение и в развитии инфаркта миокарда, который, согласно теории Селье, представляет собой пример тяжелой стрессовой ситуации, в особенности в первый период реакции «бедствия». Forssman (1954) и многие другие авторы считают, что эта реакция обусловлена внезапным поступлением в кровь больших количеств катехоламипов. Проявлениями этой гиперадреналемии считаются гипергликемия, глюкозурия, повышенный лейкоцитоз и анэозинемия. За последние годы появилось много описаний случаев развития некроза миокарда не в результате тромбоза коронарных артерий, а вследствие повреждения миокарда с развитием его некроза. Считается, что примерно в 15—20% случаев погибших от инфаркта миокарда на секции не находят тромбоза коронарных артерий. Возможно, что повреждающим фактором в этих случаях являются катехоламины, вызывающие гипоксию сердечной мышцы. – Также рекомендуем “Пример инфаркта миокарда без тромбоза коронарных артерий. Катехоламины при инфаркте миокарда” Оглавление темы “Жировой обмен и атеросклероз под влиянием гормонов”:
|
Источник
